苝分子低聚体的形成及其光谱性质
2012-12-21刘丽敏张先付
刘丽敏 张先付,2,*
(1河北科技师范学院理化学院,河北秦皇岛,066004;2MPC Technologies,Hamilton,ON,Canada L8S 3H4)
苝分子低聚体的形成及其光谱性质
刘丽敏1张先付1,2,*
(1河北科技师范学院理化学院,河北秦皇岛,066004;2MPC Technologies,Hamilton,ON,Canada L8S 3H4)
探讨了苝分子低聚体的形成条件和影响因素,这些低聚体与晶核形成紧密相关.用荧光光谱和吸收光谱法研究了不同的水含量和苝浓度对聚集的影响,低聚体属于具有光活性的J型,能发红光.计算得到低聚体的聚集数为9,平衡常数数量级较大.
苝;聚集;晶核;聚集数;平衡常数;荧光
1 引言
共轭芳香分子间普遍存在非化学键力如π-π相互作用、疏水相互作用、静电相互作用等所致的聚集行为,1,2形成的低聚体或纳米级多聚体将呈现许多单分子所不具有的性质,3并且在紫外、核磁等光谱上都有不同表现.4,5在过去几十年中许多科学家都对聚集行为进行了深入研究.激子耦合理论已可对聚集体的光谱做出较满意解释,而有关聚集作用对各种功能分子性质的影响尚在研究中.6苝是一类重要的功能染料,有关苝纳米晶体的制备及光学性质最近有较多报道,7-9但纳米晶的形成机理尚未见报道.本文报道了无取代苝低聚体的形成,这一低聚体的形成与纳米晶体的成核步骤紧密相关.我们定量计算了聚集数和聚集常数,研究了聚集对苝光谱性质的影响.
苝是一种由五个苯环组成的芳香分子(其结构如图1(a)所示),存在于自然界的煤焦油中.1910年Scholl等10首次发现并合成了苝,他用无水氯化铝氧化两个萘分子的对位得到苝.苝具有很高的荧光量子产率(>99.0%)11和化学稳定性,具有多方面的应用价值,如可用作颜料、还原染料、药物和生物分子的标记试剂,尤其是在有机发光二极管、有机场效应管、有机太阳能电池器件等领域具有广泛的应用前景.12苝由于其紧密的分子堆积而具有良好的光物理和光化学特性,而苝的堆积形式很大程度上依赖于分子结构凹陷处邻近位置的取代基和溶剂的极性.3,13-16苝分子可通过π-π相互作用、氢键等非化学键力形成聚集体,同时苝的聚集行为是影响其光物理性质的重要因素之一.根据聚集体中分子偶极的相对方向可将聚集体分为偶极平行的H聚集体(图1(b)),头尾相连的J聚集体(图1(c))以及非典型的H,J聚集体的形式,即当0°<θ<54.7°时为H聚集体;当54.7°<θ<90°时为J聚集体(图1(d)),其中θ指分子中心线与极化偶极轴间的角.17,18
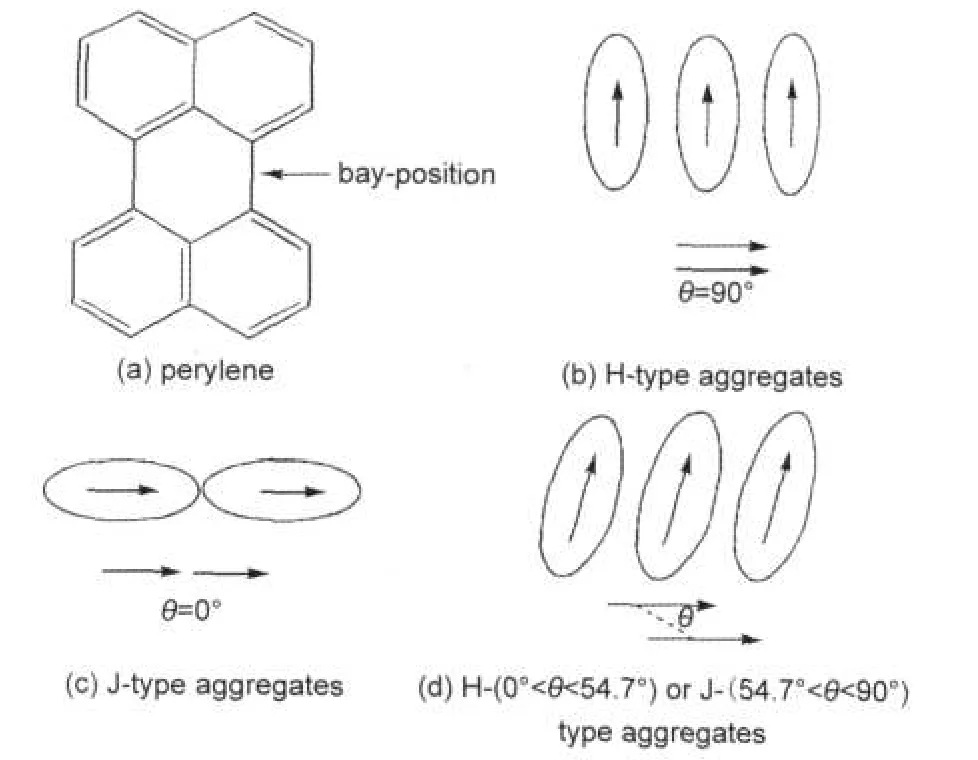
图1 Fig.1 Chemical structure of perylene and the orientation of molecules in an aggregate
文献中关于苝的报道主要集中在苝聚集形成的多聚纳米晶体及纳米晶体的光学性质.1992年,日本的Nakanishi小组19,20首次报道了利用再沉淀法制备有机纳米晶体的研究,并且发现这些纳米晶体具有特殊的光学性质,如光谱的尺寸依赖性以及非线性光学性质.谢锐敏等9,21报道了苝纳米晶体的形成、荧光光谱及荧光寿命等,但是其纳米晶的形成机理尚无报道.纳米晶体也是由二聚等低聚体生长形成,22,23因此研究苝分子的低聚行为及有关参数在揭示苝纳晶的形成机理等方面也很重要.据此我们研究低浓度下,苝分子的聚集行为及其对光物理性质的影响,其中的方法是对本课题组之前对酞菁和呫吨染料聚集行为研究的进一步发展.24苝聚集态具有独特的光学性能,有文献曾报道了苝聚集体成膜后可用于场效应晶体管,非线性光学材料和光伏材料等领域.25-28
2 实验部分
2.1 试剂和仪器
苝购自阿法埃莎公司,丙酮购自天津市佳兴化工仪器有限公司,均为分析纯.所用水为超纯水,初始苝丙酮溶液浓度为7.00×10-4mol·L-1.荧光光谱用FLS920稳态、瞬态荧光光谱仪测定,英国爱丁堡仪器公司.吸收光谱用美国StenarNet公司光纤光谱仪测定.
2.2 低聚集体系的建立
取16个容量瓶,分别标号,各加入0.200 mL 7.00×10-4mol·L-1的苝丙酮溶液,然后依次加入0.00、1.00、2.00、2.50、2.63、2.65、2.69、2.71、2.75、2.90、3.00、3.10、3.20、3.30、3.50、4.00 mL超纯水,再用丙酮定容至5 mL,使溶剂丙酮-水中水的体积分数(φwater)分别为0%、20.0%、40.0%、50.0%、52.5%、53.8%、54.2%、55.0%、58.0%、60.0%、62.0%、64.0%、66.0%、68.0%、70.0%、80.0%,配成苝浓度为28.0 μmol·L-1的溶液.29,30
2.3 配制丙酮-水的不同苝浓度的溶液
配制不同浓度的苝丙酮溶液.取9支5 mL的容量瓶依次编号,加入初始溶液(7.00×10-4mol·L-1)的体积分别为5.00、10.0、20.0、30.0、50.0、60.0、70.0、100、200 μL,用丙酮定容至5 mL,配成所需浓度的溶液.
以丙酮-水(φwater=50.0%)为例,配制丙酮-水(φwater=50.0%)的不同苝浓度的溶液.取7支容量瓶分别编号,依次加入2.50 mL水和下列体积的初始溶液:0.10、0.20、0.30、0.40、0.50、0.60、0.70 mL,初始溶液浓度为7.00×10-4mol·L-1,后用丙酮定容至5 mL,配成所需浓度的溶液.
3 结果及讨论
3.1 疏水作用导致的苝分子聚集及其在吸收光谱
上的表现
苝在丙酮中易溶,溶解后以单分子状态存在,而在水中完全不溶.另一方面,丙酮和水互溶.因此在苝的丙酮溶液中加入水,并逐渐提高水的比例,苝的溶解度会逐渐降低并形成聚集体,31-33文献9,34中将微量体积的苝丙酮溶液注射入水(φwater>99.9%),来制备苝的纳米晶体.晶体的形成通常包括两步: (1)形成晶核;(2)晶核进一步长大成晶体.通常形成晶核是关键步骤.很明显,这里的晶核是一种含有少数苝分子的低聚体.而低聚体的形成条件主要有苝分子的数量(聚集数)和聚集平衡常数(决定成核能力),它们是本研究关心的内容,这些条件主要由苝的浓度和水的含量(φwater)决定.
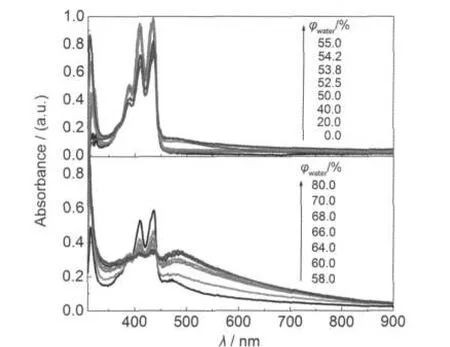
图2 丙酮-水溶剂中苝的紫外-可见吸收光谱随水含量的变化Fig.2 UV-Vis absorption spectra of perylene in acetone-water mixed solvent with different watervolume fractionscperylene=28.0 μmol·L-1
当φwater过大,低聚体快速生长成纳米级多聚体,给研究低聚体(晶核形成)带来困难,因此需要选择合适的水含量.图2是溶剂中φwater逐渐增大对苝分子紫外-可见吸收光谱的影响.在丙酮溶液中,苝呈现单分子的吸收谱,最大吸收在436 nm处.9对于28.0 μmol·L-1的苝,水含量小于52.5%,没有明显的新吸收峰,增加到53.8%后,在470 nm处出现明显新吸收峰,相对于单体发生了较大红移,区别于苝在丙酮溶液中单分子的吸收.8而对于56.0 μmol·L-1的苝,水含量大于40.0%,470 nm处就开始有新峰出现.很明显浓度越大,J聚集体形成需要的水含量就越低.图2显示,随着水含量的增加,单分子吸收逐渐降低,而470 nm左右的新吸收峰同步上升(这表明新吸收峰代表的物种来自于苝单分子),当丙酮-水中φwater=50.0%时,吸收光谱中有等吸光点在443 nm处出现(表明新吸收峰代表的物种与苝单分子之间存在一个转化平衡),而水含量大于60.0%时,则偏离等吸光点(有多聚体形成或晶体沉淀析出),且吸收峰变宽,峰位红移.红移的新吸收峰说明苝分子在混合溶剂中形成的是J聚集体,35,36而且经历了由低聚向多聚的变化,与在文献中J聚集体形成的表现类似.37-39随着水含量的增加,即聚集程度的增大,在600 nm以后出现拖尾现象,这说明形成的聚集体不是只有简单的二聚体,下面的计算也证明了这点.
3.2 浓度对苝分子聚集的影响
3.2.1 单分子苝在丙酮中的吸收光谱与浓度的关系
纯丙酮中苝的紫外-可见吸收光谱随浓度的变化如图3所示.在0.700-28.0 μmol·L-1的浓度范围内,苝的光谱峰形和位置都不随浓度变化,且吸光度与浓度成正比(图3(b)),符合朗伯-比尔定律.这表明苝在丙酮中以单一的物种-单分子形式存在.由吸光度对浓度作图,计算得到苝单分子的摩尔消光系数,在408和434 nm处的摩尔消光系数分别为30811和41087 L·mol-1·cm-1.
3.2.2 聚集体大小和聚集平衡常数的计算
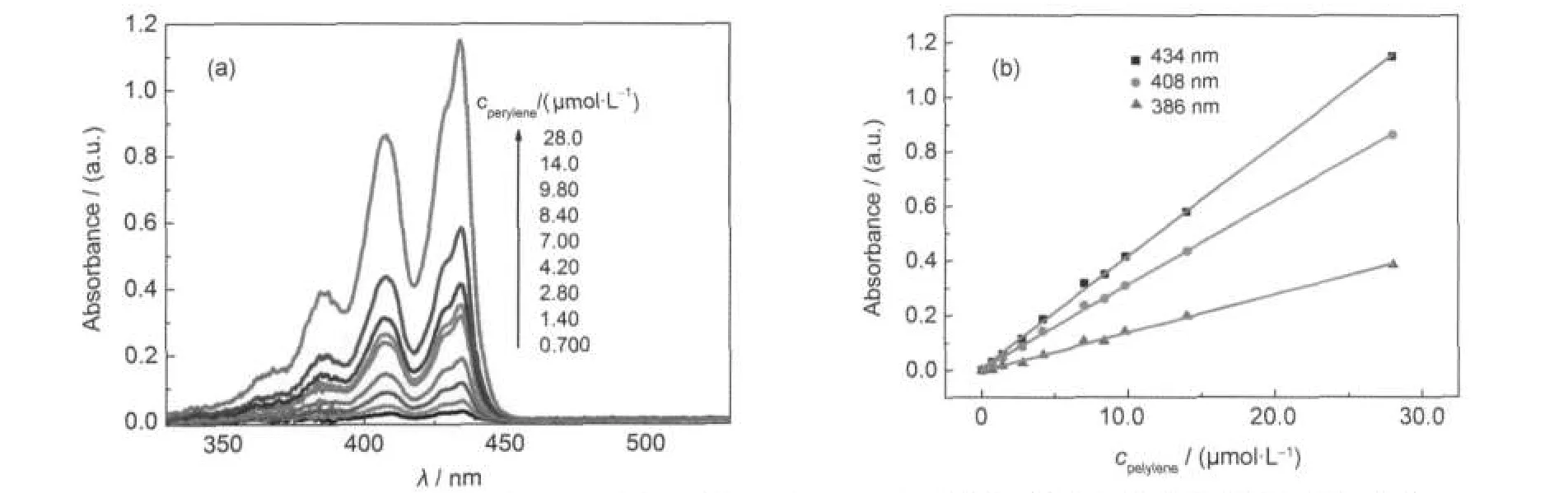
图3 (a)丙酮中苝的UV-Vis吸收光谱随苝浓度的变化及(b)不同波长下苝的吸光度随苝的浓度的变化Fig.3 (a)Concentration-dependent UV-Vis absorption spectra of perylene in acetone and(b)plots of absorbance against ploylene concentration at different wavelengths
水的含量过大时,苝浓度较低就析出部分晶体,给定量研究低聚体或晶核形成造成困难,故选择丙酮-水中φwater=50.0%附近以消除这一困扰.混合溶剂中苝的紫外-可见吸收光谱(这里是摩尔消光系数对波长作图)随浓度的变化,如图4所示.随着溶液中苝浓度的增大,在386-434 nm区间单分子的三个吸收峰虽有升高,但吸光度与浓度的关系负偏离了朗伯-比尔定律(见插图).同时在486-641 nm间出现新的代表聚集体的宽峰(在苝的丙酮溶液中并没有出现此峰),并且随着苝浓度的增大,此处的吸收也不断增大,而吸光度与浓度的关系正偏离了朗伯-比尔定律(见图4(b)),说明形成了苝分子的聚集体.与图3相比,图4在317 nm处新出现一窄而尖的吸收峰,也是聚集体的吸收峰.这样在386和434 nm处的单分子吸收峰都与两边聚集体吸收峰有较大重叠,而408 nm处的单分子吸收峰离聚集体吸收峰较远,故选择此处代表单分子的吸收来计算苝的聚集常数和平衡常数可以明显地消除干扰.

图4 (a)丙酮-水(φwater=50.0%)中苝紫外-可见吸收光谱随浓度的变化及(b)不同波长下苝的吸光度随苝的浓度的变化Fig.4 (a)Concentration-dependent UV-Vis absorption spectra of perylene in acetone-water(φwater=50.0%)mixed solvent and (b)plots of absorbance against perylene concentration at different wavelengths
在丙酮-水(φwater=50.0%)混合溶剂中,苝分子的吸光度随浓度的变化分两个阶段,如图4(b)所示,浓度低于35.0 μmol·L-1时,为线性区,符合朗伯-比尔定律,表明苝以单分子形式存在,浓度更高时,吸光度明显偏离线性,表明有聚集体形成.后者很可能对应于晶体形成的第一个阶段,即晶核形成期.40为了得到聚集数,本研究曾尝试将Baxter41和Zhao42等提出的等键模型以及我们以前4,43,44提出的二聚体平衡常数的计算方法应用于苝聚集的计算,但非线性拟合都不收敛,说明这里苝的聚集需用不同的模型.而利用下列方法,可计算苝的聚集数和平衡常数.

图5 lgA与lgAʹ分段线性拟合Fig.5 lgAand lgAʹpiecewise linear fit

设初始浓度为[M]0,平衡后聚集体的浓度为[Mn],单体浓度为[M].其中A和Aʹ分别为聚集体和单体在选定波长408 nm处的吸光度,ε和εʹ分别为聚集体和单体的摩尔消光系数.式(1)中lgA与lgAʹ线性相关,n、K、ε为常数, εʹ已知.用线性拟合法将lgA对lgAʹ作图(如图5所示),可求得斜率为n.结合对图4进行高斯分峰可求得ε,因而从图5截距可得到平衡常数K.选择408 nm处的数据,不同浓度范围内的计算结果列于表1中.φwater为50.0%时,在苝浓度小于42.0 μmol·L-1时,苝分子为单体;当苝浓度在42.0-98.0 μmol·L-1范围内,形成多聚体,聚集数为9,平衡常数较大.这一聚集数为9的低聚体可以认为是晶核.当水含量为60.0%,在浓度小于14.0 μmol·L-1时,苝分子为单体;而苝浓度在14.0-140 μmol·L-1区间时,形成多聚体,聚集数为7,平衡常数同样较大.考虑到实验和计算误差,可以认为聚集数和平衡常数受水含量影响不大.因水含量小于48.0%聚集很弱,而水含量大于60.0%时出现沉淀,因此计算未在此范围进行.

表1 苝的聚集平衡常数(K)、聚集数(n)和聚集体摩尔消光系数(ε)Table 1 Equilibrium constant(K),aggregation number (n)and molar extinction coefficients(ε)of perylene oligomers
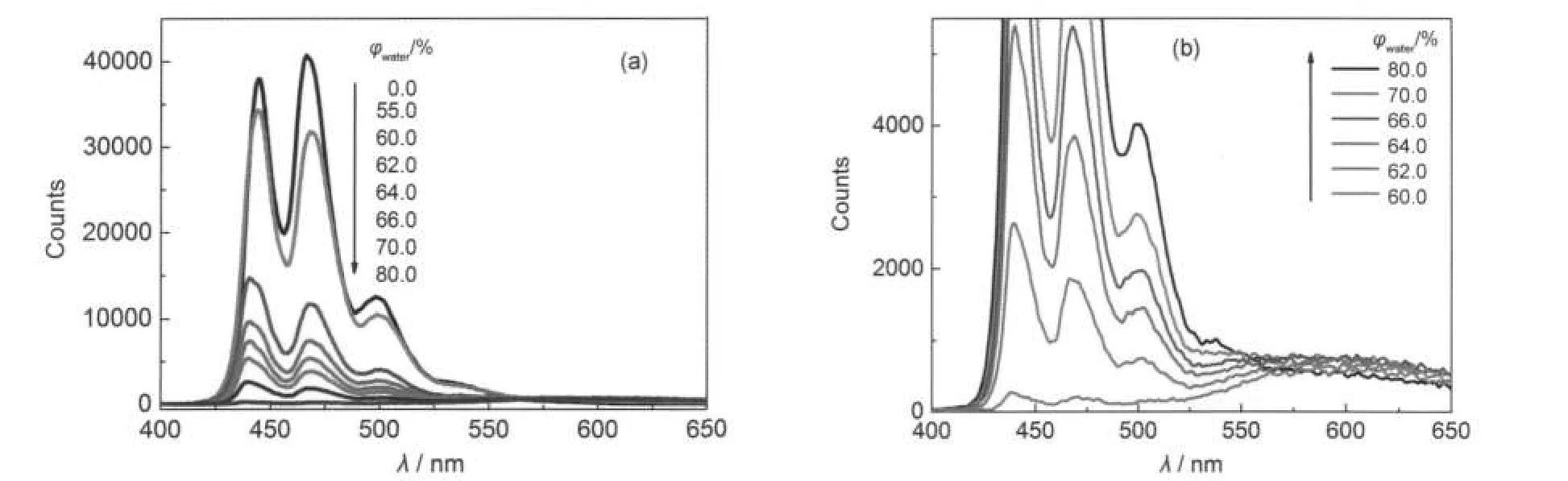
图6 溶剂丙酮-水体积比不同时苝的发射光谱Fig.6 Fluorescence spectra of perylene in acetone-water mixed solvent with different volume ratios cperylene=28.0 μmol·L-1;λex=385 nm
3.3 苝聚集作用与荧光光谱
3.3.1 苝分子聚集体的发射光谱
图6是苝的荧光发射光谱随溶剂中φwater的变化,荧光激发波长为385 nm,苝浓度恒定为28.0 μmol·L-1,水的体积分数从0%逐渐增加到80.0%.苝在纯丙酮溶液中,呈现单分子的发射谱.当溶剂中水的体积分数达到55.0%以上时,在520-650 nm间出现一弱的新发射峰,峰位和宽度明显区别于苝单分子的发射谱.随着水含量的增加,单分子发射峰降低,新谱峰同时增强(见图6(b)),这一变化规律与吸收光谱相同,说明新发射峰代表的物种由苝单分子转化形成.新峰与文献37中苝酰亚胺类聚集体的发射峰相类似,因此归属为苝分子J聚集体的发射峰;由于苝单分子的发射光谱减小的强度比相应形成的J聚集体光谱增大的强度大很多,说明J聚集体的荧光量子效率要比单分子荧光效率低得多.

图7 溶剂丙酮-水体积比不同时苝的激发光谱Fig.7 Excitation spectra of perylene in acetone-water mixed solvent with different volume ratios cperylene=47.0 μmol·L-1;λem=500 nm
3.3.2 苝分子聚集体的激发光谱
图7是发射波长固定为500 nm时,苝的荧光激发光谱随溶剂中φwater的变化.图8是溶剂中φwater为70.0%,发射波长分别为500和600 nm时苝的激发光谱对比.由图8可知,选择不同的发射波长激发光谱有很大不同.500 nm处为苝单分子的发射,因此激发光谱与苝丙酮/水溶液的单分子吸收光谱位置和形状很相似.600 nm处主要为苝J聚集体的发射,因而图8中的激发谱峰形状明显区别于图7,但对比后可发现,除了单分子的贡献,470、330和340 nm处为聚集体激发峰.
3.4 浓度与苝J聚体的发射光谱
图9是激发波长为465 nm时,苝在丙酮-水(φwater= 50.0%)溶液中的发射光谱随苝浓度的变化.苝聚集体在500-700 nm间的宽峰随着苝浓度的增加发射峰强度不断增大.当苝浓度为14.0 μmol·L-1时,几乎看不到苝的发射峰,当苝浓度大于42.0 μmol·L-1时,可以看到明显的发射峰,且随浓度的增加而增大.
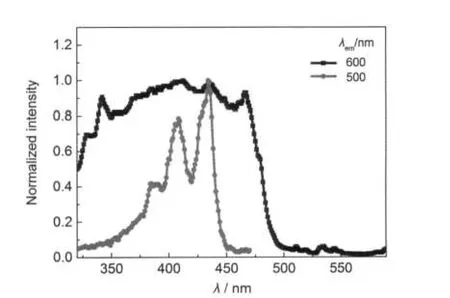
图8 溶剂丙酮-水中苝归一化的激发光谱Fig.8 Normalized excitation spectra of perylene in acetone-water mixed solvent cperylene=28.0 μmol·L-1;φwater=70.0%
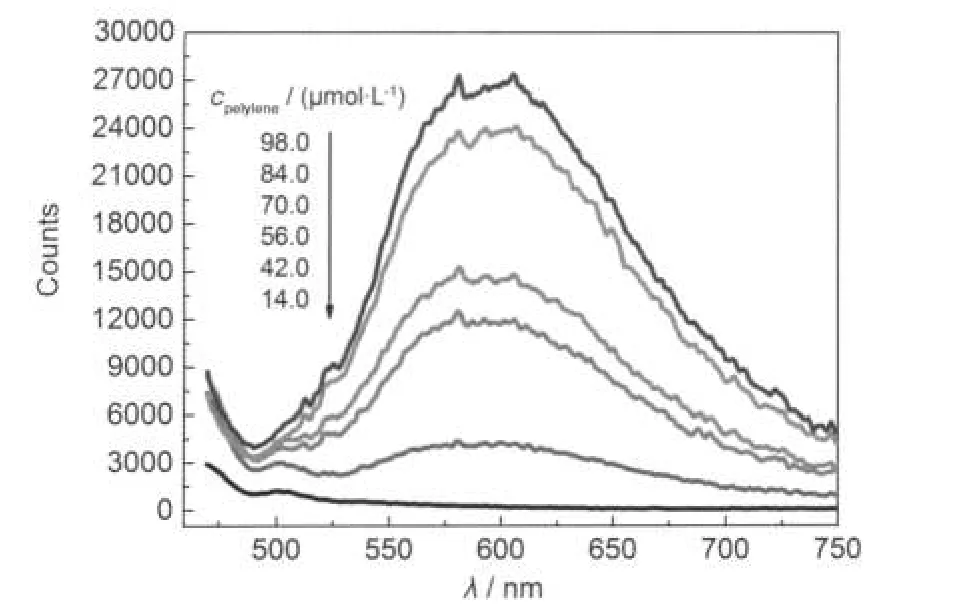
图9 苝在丙酮-水溶液中随浓度变化的发射光谱Fig.9 Concentration-dependent fluorescence spectra of perylene in acetone-water mixed solvent λex=465 nm;φwater=50.0%
4 结论
探讨了苝分子低聚体的形成条件和影响因素,荧光光谱和吸收光谱表明,即使在μmol·L-1数量级的低浓度下,含水的丙酮溶液中,苝也能够形成J聚集体,此聚集体能发荧光.当φwater=50.0%时,在苝的浓度小于40.0 μmol·L-1时苝仍以单分子形式存在,浓度继续增大则形成九聚体,且平衡常数数量级较大,有利于此聚集体生成.这一低聚体很可能就是晶核.这些信息对于揭示苝纳米晶的形成机理有重要参考价值.另外,其它芳香化合物分子间相互作用导致的光谱行为也可能出现类似的现象.45-48
(1)Marcey,L.W.Curr.Opin.Chem.Biol.2002,6,736.
(2)Zhang,X.H.;Guo,H.R.;Jiao,Z.;Yan,W.W.;Ruan,W.J.; Zhu,Z.A.Acta Phys.-Chim.Sin.2011,27(4),774. [张晓红,郭洪瑞,矫 志,闫伟伟,阮文娟,朱志昂.物理化学学报, 2011,27(4),774.]
(3) Chen,Z.J.;Lohr,A.;Saha-Möller,C.R.;Würthner,F.Chem. Soc.2009,38,564.
(4) Zhang,X.F.;Shen,T.Chin.Sci.Bull.1994,39,903.[张先付,沈 涛.科学通报,1994,39,903.]
(5)Wen,X.;Wang,S.J.;Gao,B.X.;Ba,X.W.Acta Chim.Sin. 2010,68,1876.[温 昕,王素娟,高保祥,巴信武.化学学报,2010,68,1876.]
(6) Huang,J.C.Study of theAggregate Structure in Organic Electron Transport Materials.Ph.D.Dissertation,Zhejiang University,Hanzhou,2007.[黄嘉驰.有机电子传输材料聚集态结构的研究[D].杭州:浙江大学,2007.]
(7) Oikawa,H.Bull.Chem.Soc.Jpn.2011,84(3),233.
(8) Ishino,H.;Iwai,S.;Iwamoto,S.;Okumura,T.;Nishimoto,T.; Nair,S.V.;Takayoshi K.;Eiji,T.Phys.Rev.B 2011,84(4), 1303.
(9) Xie,R.M.;Xiao,D.B.;Yao,J.N.Acta Phys.-Chim.Sin.2002, 18(1),34.[谢锐敏,肖德宝,姚建年.物理化学学报,2002,18 (1),34.]
(10) Scholl,R.;Seer,C.;Weitzenböck,R.Ber.Dtsch.Chem.Ges. 1910,43,2202.
(11) Langhals,H.Chem.Ber.1985,118(11),4641.
(12) Yuan,Z.L.;Yu,J.S.;Tao,S.L.;Jiang,Y.D.Nanotechnol. 2010,7(3),27. [袁兆林,于军胜,陶斯禄,蒋亚东.纳米科技, 2010,7(3),27.]
(13) Shi,M.M.;Chen,H.Z.;Wang,M.Acta Energiae Sola.Sin. 2006,27(6),525.[施敏敏,陈红征,汪 茫.太阳能学报, 2006,27(6),525.]
(14)Huang,J.C.;Yang,L.G.;Mo,X.;Shi,M.M.;Wang,M.;Chen, H.Z.Acta Chim.Sin.2007,65,1051.[黄嘉驰,杨立功,莫 雄,施敏敏,汪 茫,陈红征.化学学报,2007,65,1051.]
(15)Shi,M.M.;Chen,H.Z.;Sun,J.Z.;Ye,J.;Wang,M.Chem.J. Chin.Univ.2004,25(3),454.[施敏敏,陈红征,孙景志,叶 坚,汪 茫.高等学校化学学报,2004,25(3),454.]
(16)Yang,L.G.;Chen,L.;Shi,M.M.;Wang,M.;Chen,H.Z.Acta Chim.Sin.2007,65,2604.[杨立功,陈 林,施敏敏,汪 茫,陈红征.化学学报,2007,65,2604.]
(17) Davydov,A.S.Sov.Phys.Usp.1964,7,145.
(18)Kasha,M.;Rawls,H.R.;El-Bayoumi,M.A.Pure Appl.Chem. 1965,11,371.
(19) Kasai,H.;Nalwa,H.S.;Oikawa,H.;Nakanishi,H.Jpn.J.Appl. Phys.1992,31,L1132.
(20) Kasai,H.;Oikawa,H.;Okada,S.;Nakanishi,H.Bull.Chem. Soc.Jpn.1998,71,2597.
(21) Liu,J.S.;Li,Y.X.;Gao,F.;Wang,L.Spectrosc.Spectral Anal. 2005,25(1),76.[刘金水,李永新,高 峰,王 伦.光谱学与光谱分析,2005,25(1),76.]
(22) Wasielewski,M.R.Chem.Rev.1992,92,435.
(23)Yan,Y.;Guo,S.;Xiong,W.;Lu,T.;Li,Z.C.;Huang,J.B.;Fu, H.L.Acta Phys.-Chim.Sin.2006,22(1),1. [阎 云,郭 素,熊 玮,卢 婷,李子臣,黄建滨,付宏兰.物理化学学报,2006,22(1),1.]
(24) Zhang,X.F.;Xi,Q.;Zhao,J.J.Mater.Chem.2010,20,6726.
(25) Sun,J.Z.;Cao,J.;Xu,H.P.;Wang,M.Chem.J.Chin.Univ. 2006,27(2),323. [孙景志,曹 健,徐海鹏,汪 茫.高等学校化学学报,2006,27(2),323.]
(26) Sun,J.Z.;Yang,X.G.;Wang,M.Chin.Sci.Bull.2005,50(14), 1450.[孙景志,杨新国,汪 茫.科学通报,2005,50(14), 1450.]
(27) Wang,W.L.;Zhai,J.;Bai,F.L.;Ren,Y.J.;Zhang,B.;Cai,S. M.Photographic Sci.Photochem.2002,20(4),262.[王文龙,翟 锦,白凤莲,任焱杰,张 波,蔡生民.感光科学与光化学, 2002,20(4),262.]
(28) Yang,J.Y.;Gu,J.H.;Song,Y.L.Infrared Laser Eng.2006,35, 195.[杨俊义,顾济华,宋瑛林.红外与激光工程,2006,35, 195.]
(29) Ji,X.H.;Fu,H.B.;Xie,R.M.;Xiao,D.B.;Yao,J.N.Chin.J. Chem.2002,20,123.
(30) Ji,X.H.;Fu,H.B.;Cao,Y.A.;Xie,R.M.;Zhang,X.T.;Yao,J. N.Chem.J.Chin.Univ.2001,22(8),1394.[纪学海,付红兵,曹亚安,谢锐敏,张昕彤,姚建年.高等学校化学学报,2001,22 (8),1394.]
(31) Feng,J.Q.;Li,X.Y.Chemistry 2008,9,650.[冯君茜,李希友.化学通报,2008,9,650.]
(32) Feyter,S.D.;Miura,A.;Yao,S.;Chen,Z.J.;Würthner,F.; Jonkheijm,P.;Schenning,A.P.H.J.;Meijer,E.W.;Schryver,F. C.D.Nano Lett.2005,5(1),77.
(33)Zhang,X.J.;Zhang,X.H.;Wang,B.;Zhang,C.H.;Chang,J., C.;Lee,C.S.;Lee,S.T.J.Phys.Chem.C 2008,112,16264.
(34) Baba,K.;Kasai,H.;Nishida,K.;Nakanishi,H.Jpn.J.Appl. Phys.2011,50,010202.
(35)Wüthner,F.Chem.Commun.2004,No.24,1564.
(36) Wüthner,F.;Thalacker,C.;Diele,S.;Tschierske,C.Chem.Eur. J.2001,7(10),2245.
(37) Feng,J.Q.Synthesis and Properties of Novel Multifunctional Groups with Perylene Dimide.Ph.D.Dissertation,Shandong University,Jinan,2009. [冯君茜.以苝酰亚胺为构筑块的多功能团化合物的合成及性能研究[D].济南:山东大学, 2009.]
(38)Li,Y.;Han,W.W.;Liao,M.X.Acta Phys.-Chim.Sin.2009,25 (12),2493.[李 晔,韩伟伟,廖明霞.物理化学学报,2009, 25(12),2493.]
(39)Xie,B.Y.;Cao,Y.F.;Sun,J.Z.;Yang,X.G.;Wang,M.Chin. Sci.Bull.2007,52(19),2266.[解波雨,曹亚峰,孙景志,杨新国,汪 茫.科学通报,2007,52(19),2266.]
(40) Tidhar,Y.;Weissman,H.;Sharon,G.Chem.-Eur.J.2011,17 (22),6068.
(41) Baxter,N.J.;Williamson,M.P.;Lilley,T.H.;Haslam,E. J.Chem.Soc.Faraday Trans.1996,92(2),231.
(42)Zhao,D.H.;Moore,J.S.Org.Biomol.Chem.2003,1,3471.
(43) Zhang,X.F.Sci.China Ser.B 1994,37(11),1298.
(44) Zhang,X.F.;Xia,P.J.;Ma,J.S.;Xu,H.J.Chin.Sci.Bull. 1992,6,520.[张先付,夏培杰,马金石,许慧君.科学通报, 1992,6,520.]
(45) Ouyang,M.;Xing,W.Q.;Zhang,Y.J.;Jin,Y.X.;Zhang,C. Acta Phys.-Chim.Sin.2011,27(6),1516.[欧阳密,项文勤,张玉建,金燕仙,张 诚.物理化学学报,2011,27(6),1516.]
(46) Xiao,L.X.;Hu,S.Y.;Sun,S.;Chen,Z.J.;Qu,B.;Gong,Q.H. Acta Phys.-Chim.Sin.2011,27(4),977. [肖立新,胡双元,孙 胜,陈志坚,曲 波,龚旗煌.物理化学学报,2011,27(4), 977.]
(47)Peng,K.M.;Shao,W.L.;Wang,H.H.;Ying,X.;Wang,H.;Ji, L.N.;Liu,H.Y.Acta Phys.-Chim.Sin.2011,27(1),199.[彭开美,邵文莉,汪华华,应 晓,王 惠,计亮年,刘海洋.物理化学学报,2011,27(1),199.]
(48) Wang,K.P.;Wang,C.S.Acta Phys.-Chim.Sin.2011,27(3), 589. [王昆鹏,王长生.物理化学学报,2011,27(3),589.]
August 8,2011;Revised:November 14,2011;Published on Web:November 29,2011.
Formation and Spectral Properties of Perylene Oligomers
LIU Li-Min1ZHANG Xian-Fu1,2,*
(1College of Physics and Chemistry,Hebei Normal University of Science and Technology,Qinhuangdao 066004, Hebei Province,P.R.China;2MPC Technologies,Hamilton,ON,Canada L8S 3H4)
We report the conditions required for the formation of perylene oligomers,which are closely related to the crystal nuclei for the formation of perylene nanocrystal.The effects of water content and perylene concentration on aggregation were studied using fluorescence and absorption spectra.The spectra indicated that fluorescent J-type perylene oligomers were formed.An aggregation number of 9, and large equilibrium constant were obtained for the reaction.
Perylene;Aggregation;Crystal nuclei;Aggregation number;Equilibrium constant; Fluorescence
10.3866/PKU.WHXB201111292
*Corresponding author.Email:zhangxianfu@tsinghua.org.cn;Tel:+86-335-8387040.
The project was supported by the Natural Science Foundation of Hebei Province,China(B2010001518).河北省自然科学基金(B2010001518)资助项目
O642;O644
