沉淀法制备羟基磷灰石的工艺因素研究
2012-12-20张小立张照军
张小立,张照军,刘 英
(中原工学院,郑州450007)
羟基磷灰石(HAP)是目前公认的具有良好的生物相容性,并具有骨引导性即生物活性的陶瓷材料.
羟基磷灰石纳米微粒的制备方法概括起来可分为3大类:固相法[1-2]、液相法[3]和气相法[4-6].其中,液相法由于制备形式多样、操作简单、粒度可控等优点而倍受人们的重视.近年来,液相法制备纳米颗粒的新方法不断涌现,其中沉淀法是在综合各种液相法的基础上发展起来的一种制备纳米颗粒的技术.该方法具有实验设备简单、操作方便、产率高和制得的纳米颗粒大小均一等特点.
本文通过试验并结合前人的研究成果,对影响沉淀法制备纳米羟基磷灰石纯度的工艺因素进行研究,为其制备技术的规范化和系统化提供借鉴.
1 试验方法
试验中采用2组原料:Ca(NO3)2·4H2O(分析纯)和 H3PO4(分析纯)与Ca(NO3)2和 NH4H2PO4.将以上原料按Ca/P=1.67和Ca/P=1.00的比例溶于水,配制起始溶液,并将氨水逐滴滴加到配制的起始溶液中.溶液始终在恒温40℃下,用磁力搅拌器剧烈搅拌,调节pH值分别到8、10和12,继续搅拌30min后静置,并分别陈化5h、10h和22h,过滤、去离子水洗涤、无水乙醇洗涤并烘干.将烘干后的产物分别在600℃、700℃、900℃和1 000℃温度下煅烧,然后取出并冷却到室温,研磨后得到HAP粉末.
采用2组原料制备HAP的反应式分别如下:
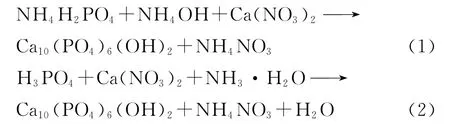
2 影响纯度的工艺因素
2.1 Ca/P比的影响
图1所示为Ca/P比分别为1.67和1.00时HAP试样的红外图谱.在红外光谱图中,1 400cm-1左右的红外吸 收峰是由 CO32-产 生的;3 640cm-1和601cm-1左右的吸收峰是由OH-产生的.由图1(a)可以看出,3 640cm-1左右的吸收峰明显,因而OH-的含量高;这说明当Ca/P=1.67时,试样制备过程中反应充分,HAP的纯度变得越来越高.而当Ca/P=1.00时,如图1(b)所示,红外光谱图中3 640cm-1左右的吸收峰明显消失,这说明HAP产出微弱.
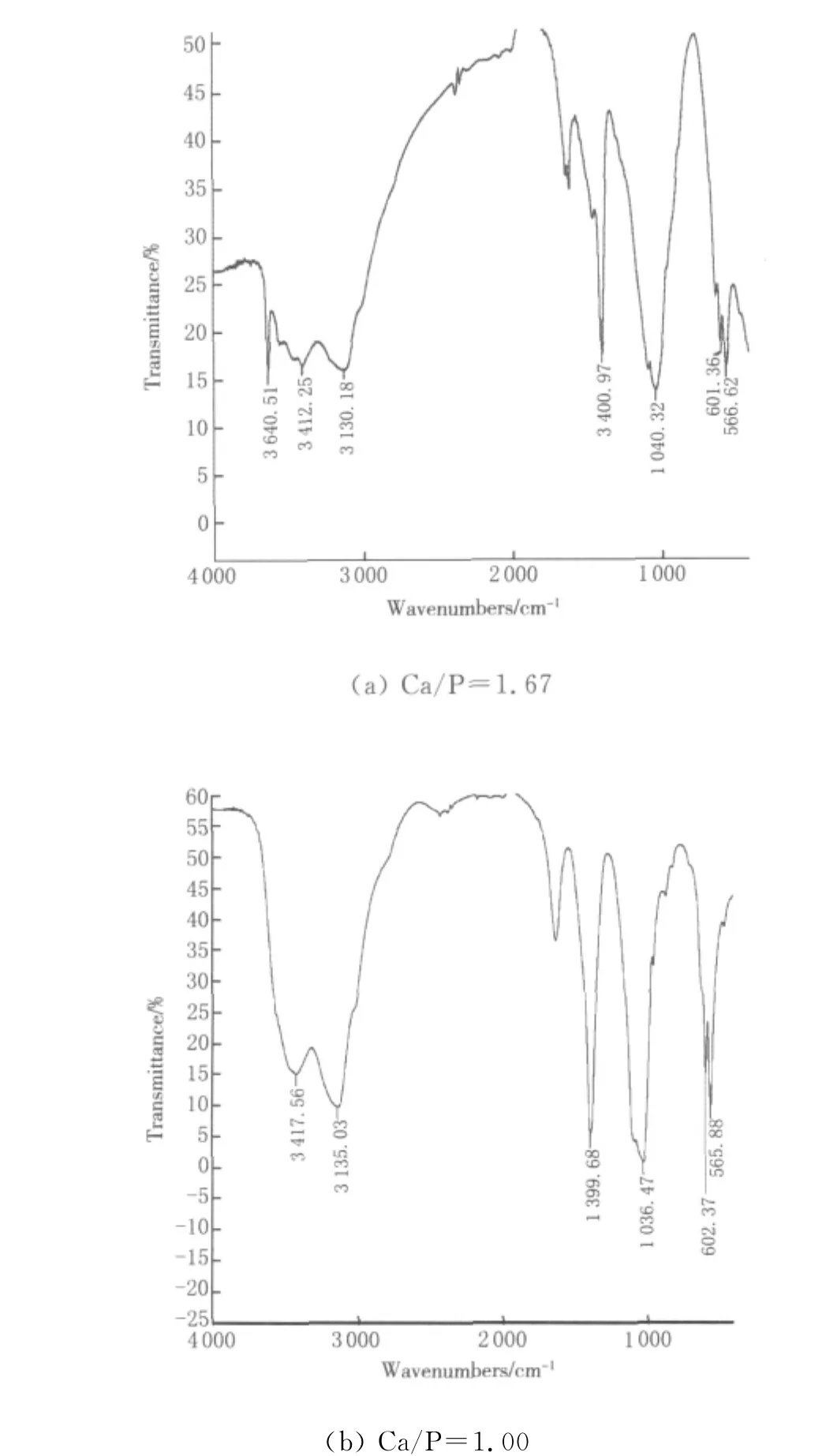
图1 不同Ca/P时HAP的红外图谱
2.2 pH值的影响
图2所示为pH值分别为8和10时反应产物HAP的红外图谱.可以看出,601cm-1左右的红外光谱震动幅度相同,而3 640cm-1左右的红外光谱震动幅度在pH为8时的值小于pH值为10时的值,故后者的OH-含量高.由此可知,在制备HAP粉末的过程中,pH值为10时制备的HAP粉末比pH值为8时制备的粉末纯度高.
2.3 陈化时间的影响

图2 不同pH值时HAP的红外图谱
图3所示为pH=10,不同陈化时间下所得HAP的红外图谱(没有经过煅烧).1 037cm-1左右的吸收峰是由于PO43-的吸收造成的,3 417cm-1左右的吸收峰是由于HAP吸收空气中的水蒸气造成的,1 400cm-1左右的吸收峰是由于CO32-的吸收造成的.由图3可知,随着陈化时间的延长,CO32-吸收峰越来越尖锐.这说明CO32-离子呈增加趋势.这是因为CO2逐渐溶于溶液形成CO32-而进入HAP晶格的缘故.这样的产物更接近人体骨骼成分.另一方面,随着陈化时间的延长,OH-1吸收峰越来越突出.这说明沉淀反应越来越充分,制备的HAP也越纯、越多.
2.4 煅烧温度的影响
图4所示为不同煅烧温度下所得HAP的红外图谱.从图4可以看出,样品中含有OH-基团.这说明样品具有羟基结构.
从图4(a)、(b)可看出,随着煅烧温度的升高,3 640cm-1左右的OH-吸收峰越来越尖锐,峰值越来越强.这说明随着温度的升高,羟基磷灰石中的羟基越来越突出,结晶程度越来越好.但是当温度超过1 000℃时,从图4(c)可看出,OH-已经变弱,这时HAP分解.

图3 不同陈化时间下HAP的红外图谱
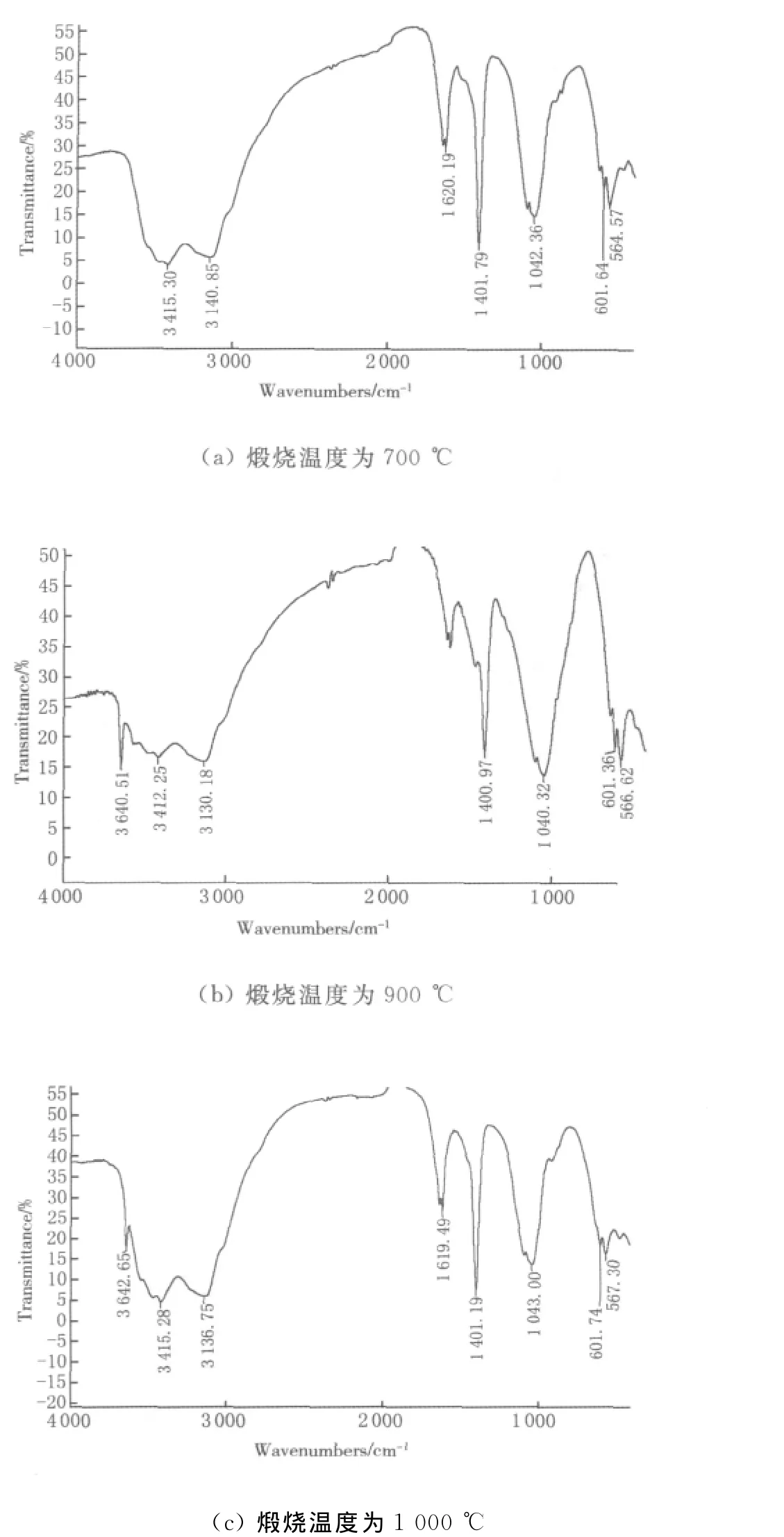
图4 不同煅烧温度下HAP的红外图谱
3 结 语
用化学沉淀法,通过控制反应条件可以制得HAP粉体.具体条件为:
(1)Ca/P比应为1.67;
(2)反应时溶液的pH值应在10~12之间;
(3)反应溶液陈化时间要达到10~22h;
(3)当煅烧温度在900~1000℃之间时,可得到结晶程度较好的HAP粉体.
[1]金艳,周玉所,李维军.生物陶瓷多孔羟基磷灰石的合成及应用[J].山东陶瓷,2001,24(2):6.
[2]李世普.生物医用材料导论[M].武汉:武汉工业大学出社,2000:120-123,48-49.
[3]Jie Fang.Fabrication of Pous Hydroxyapatite Cramics by Microwave Processing[J].Journal Mater.Res.,1992:7(2):864-878.
[4]Dominic Walsh,Joanne L,Brigid.Influence of Mosacchar Ides and Related Molecules on the Morphology of Hydroxyapatite[J].Journal Cryst Growth,1993,133:1-12.
[5]Suzuki S,Ohgaki M,Ichiyanagi M,etal.Preparation of Needle like Hydroxyapatite[J].Mater SciLett,1998,17:381-383.
[6]Binder G,Troll G.Coupledanion Substitution in Natural Carbon Bearing Apatites[J].Contribmin Petrol,1989,101:394-401.
