2-苯基-4-硒唑甲酸铜配合物的合成及其与DNA的作用*
2012-12-17赵国良陈吉妃沈金杯周玉凤
赵国良, 吕 鑫, 陈吉妃, 沈金杯, 周玉凤, 陈 鸳
(1.浙江师范大学化学与生命科学学院,浙江 金华 321004;2.浙江师范大学 行知学院,浙江 金华321004)
硒是生命活动的必需微量元素之一,它具有广泛的生物学作用:在抗氧化、抗衰老、保护心脏、预防和治疗肿瘤、维持正常免疫、生殖及内分泌功能等方面发挥着重要作用[1-2].全世界广泛存在着土壤缺硒的问题,我国缺硒情况更为严重.硒的摄入不足对人体健康有潜在的威胁,仅靠天然食品的补充难以得到根本的改善.因此,研发高效安全的补硒食品势在必行[3].由于无机硒试剂存在毒性高、风险大、吸收利用率低等问题,有机硒补剂的开发与研究一直被广为关注.
铜也是生命必需的微量元素,它在生命体中起着重要的作用,对于结缔组织的形成、神经系统的发育及骨骼的发育都十分必要.铜参与铁和能量的代谢,在许多酶反应中消耗分子氧而充当还原剂的作用[4-6].铜配合物不仅具有抗癌活性,还具有抗炎、抗溃疡、抗抽搐、抗糖尿病和抗诱变剂等作用[7-8].
20世纪80年代以来,人们合成出大量具有生物活性的有机硒化合物,其中硒唑类衍生物具有良好的抗肿瘤、抗菌作用,具有作为药物和药物中间体的潜在功能[9-13].为了制得具有更高生物活性的硒唑配合物,同时考虑到羧酸的配位能力和配位模式的多样性,本文以2-苯基-4-硒唑甲酸(HL)为配体,与Cu(NO3)2在水溶液中反应,制得了配合物 NH4[Cu2L5]HL·6H2O,并通过红外光谱、摩尔电导及热重分析等方法对配合物进行了表征,用X-射线单晶衍射法确定了配合物的晶体结构,用溴化乙锭荧光探针法测试了配合物与DNA的作用.
1 实验部分
1.1 仪器与试剂
碳、氢、氮含量用德国 Elementar公司 Vario ELⅢ型元素分析仪测定;铜含量用EDTA滴定法测定.美国Nicolet公司NEXUS 670型傅立叶变换红外光谱仪(FTIR),KBr压片,测定范围为400~4 000 cm-1;美国Perkin-Elmer公司LS55荧光分光光度计;瑞士 METTLER-TOLEDO公司TGA/SDTA 851e型热分析仪;德国Bruker公司APEX II CCD单晶衍射仪;上海雷磁仪器厂DDS-11A型电导率仪.
硒粉、硼氢化钠、苯甲腈、1,3-二氯丙酮、重铬酸钾、硝酸铜、溴化乙锭(EB)、三羟甲基氨基甲烷、无水乙醇、N,N'-二甲基甲酰胺(DMF)等试剂均为分析纯.小牛胸腺DNA(北京华美公司)为生化试剂,用0.1 mol·L-1NaCl溶液配制成200 μg·mL-1的溶液(DNA的起始浓度为 3.72×10-4mol·L-1),经测定 A260/A280=1.8 ~2.0,置4℃保存,在4 d内使用.Tris-HCl缓冲溶液的pH值为 7.40,其中 c(Tris)为 0.01 mol·L-1.
1.2 配合物的合成
配体按文献[14]合成,产物熔点169℃,与文献相符.
配合物的合成:称取1 mmol的硝酸铜溶于10 mL水中,加入过量的浓氨水制得铜氨溶液;另取1 mmol的硒唑甲酸于10 mL水中,加入浓氨水使其溶解.将两溶液混合后室温搅拌12 h,过滤,将滤液静置,数日后得到适合X-射线单晶衍射实验的绿色晶体,过滤后用无水乙醇洗涤,干燥,得产物0.22 g,产率约25%.
1.3 晶体结构测定及结构解析
选用大小为 0.185 mm ×0.121 mm ×0.037 mm的配合物单晶,在德国Bruker APEX II CCD单晶衍射仪上进行X-射线单晶衍射实验.用辐射Mo Kα 射线(λ =0.071 073 nm),在 1.53°≤2θ≤25.00°收集衍射点.衍射数据经LP因子校正,晶体结构由直接法解出.所有非氢原子的坐标通过全矩阵最小二乘法给出,并经各向异性温度因子修正.各向异性化所有非氢原子的温度因子后,对碳原子进行理论加氢.水上的氢通过Fourier合成得到,并对键长、键角加以限制(d(O—H)=0.085(2)nm,d(H—H)=0.130(2)nm).配合物最后一致性因子为 R1=0.065 8(I>2σ(I)),wR2=0.184 5.晶体结构分析工作在Pentium PC计算机上用SHELXS-97程序[15]完成.
1.4 配合物与DNA作用
10 mL比色管中加入2.0 mL溴化乙锭(EB)溶液(100 μg·mL-1),1.0 mL 小牛胸腺 DNA 溶液(200 μg·mL-1),2.0 mL Tris-HCl缓冲溶液(pH=7.40),放置2 h,加入不同量的配合物溶液(1×10-5mol·L-1的 DMF溶液),稀释至刻度,反应12 h,以251 nm为激发光波长,扫描混合体系在530~700 nm波长的荧光光谱.
2 结果和讨论
2.1 配合物的化学组成和红外光谱
配合物的元素分析wB测定值为:C 40.92%,H 3.03%,N 5.57%,Cu 7.22%.按配合物分子式C60H53N7Cu2O18Se6得 wB计算值为:C 41.12%,H 3.09%,N 5.62%,Cu 7.29%.红外光谱(KBr压片)σ/cm-1:3 415(m,br),3 098(s),1 624(vs),1 505(w);1 470(s),1 445(w),1 346(s),1 264(m),1 225(w),1 076(w),1 001(m),931(w),898(w),823(w),771(s),740(w),699(s),632(w),566(w),450(w),425(w).
由配合物的元素分析可知,配合物由2个中心离子Cu(Ⅱ)、5个2-苯基-4-硒唑甲酸根配体(L-1)、1个铵根离子、1个游离的2-苯基-4-硒唑甲酸分子(HL)和6个水分子组成.25℃时,1.0×10-3mol·L-1配合物DMF溶液的摩尔电导率为78.1 S·cm2·mol-1,故可知其在 DMF 中为1∶1电解质[16].说明合成产物为离子型配合物,其分子式可表示为 NH4[Cu2L5]HL·6H2O.取1 mL上述配合物DMF溶液,加入2滴2 mol·L-1NaOH溶液,再加入2滴奈斯勒试剂,有红棕色沉淀产生,证明配合物中有铵根离子存在,这与红外光谱和晶体结构测定的结果一致.
自由配体在3 441 cm-1和1 685 cm-1处分别出现υOH和υCOOH的伸缩振动,形成配合物后:υOH位移至3 415 cm-1处,且峰形明显变宽、变强,说明配合物中有水;1 685 cm-1处的υCOOH振动峰明显减弱,而在1 624 cm-1处出现了υas(—COO—)的不对称伸缩振动峰,在1 445 cm-1和1 346 cm-1处出现了υs(—COO—)的对称伸缩振动峰,其Δυ值分别为179 cm-1和278 cm-1,表明配体中羧基是以单齿和桥式二齿形式参与配位的[17].配合物在1 505 cm-1处的弱伸缩振动和771 cm-1处的强吸收峰可归属为硒唑环的振动峰[18];3 098 cm-1处强而尖的振动峰为铵根离子的
2.2 配合物的热重分析
在升温速率为10℃·min-1条件下,于空气气氛中测定了配合物在30~800℃的热分解情况.图1为配合物的TG-DTG曲线.从图1可以看出:配合物在30~143℃的失重率为7.02%,对应于失去配合物中的6个结晶水和1个氨分子(理论失重率为7.15%);在200~245℃的失重率为23.42%,对应于失去配合物中的1个游离的2-苯基-4-硒唑甲酸分子和其中2个配体中的苯基(理论失重率为23.07%);在245~570℃的失重率为52.68%,对应于配合物中配体的分解(理论失重率为53.59%);残留率为16.88%,与配合物中 Cu和 Se的质量分数(理论值为16.19%)基本相符.

图1 配合物的TG-DTG曲线
2.3 配合物的晶体结构
配合物的主要晶体学数据列于表1,主要的键长和键角列于表2和表3.

图2 配合物的分子结构(椭球率30%)

表1 配合物的晶体学数据

表2 配合物的主要键长
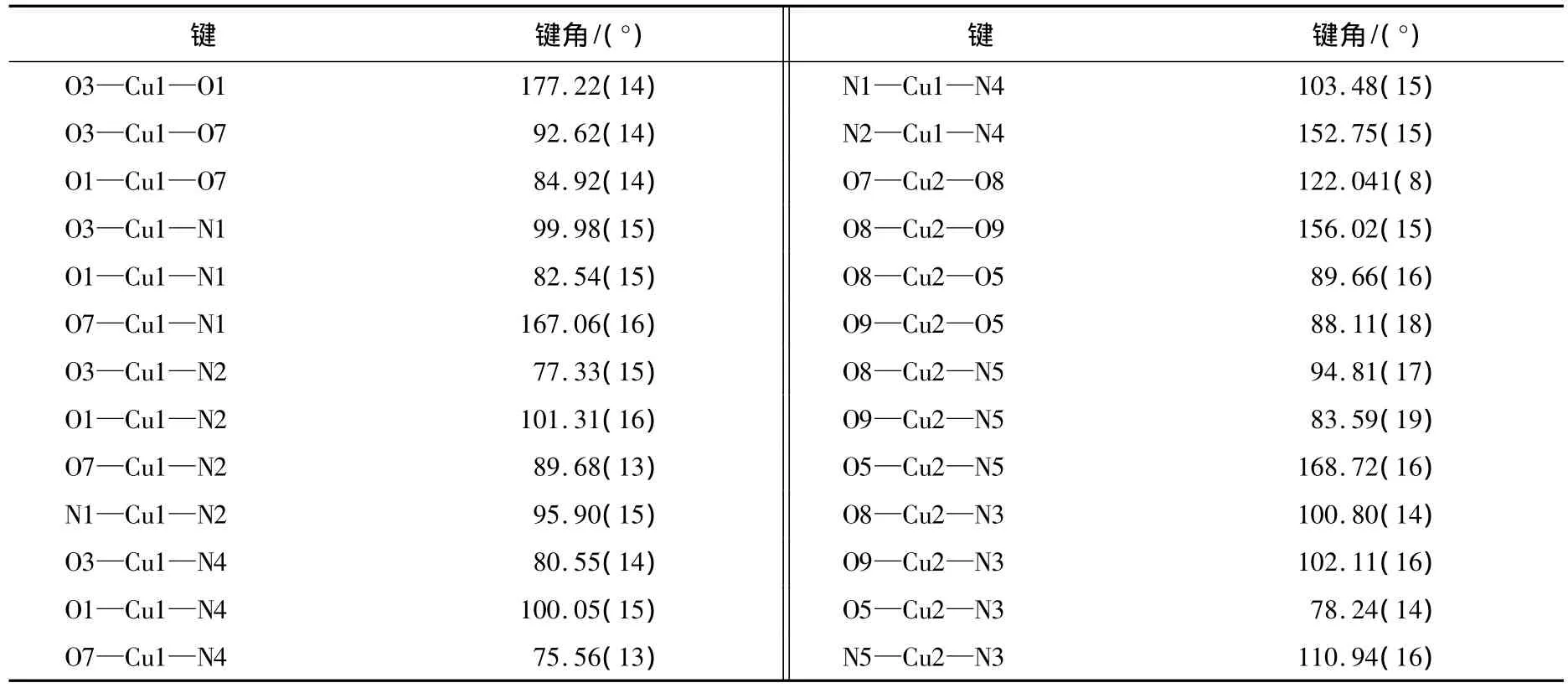
表3 配合物的主要键角
图2为配合物的分子结构图.由图2可知,该配合物为硒唑甲酸根桥连的双核结构,配合物的最小不对称单元中含有2个Cu(Ⅱ)离子、5个硒唑甲酸根配体(L-)、1个游离的硒唑甲酸分子(HL)、1 个 NH+4离子和6个晶格水分子.2个铜离子具有不同的配位环境和配位方式(见图3),Cu1离子与配位原子形成六配位的呈略畸变的八面体结构,而Cu2离子与配位原子形成五配位的呈略畸变的四方锥结构.其中:Cu1与3个硒唑甲酸根配位,配位形式均为双齿螯合模式,每个硒唑甲酸根利用1个羧基氧和1个硒唑氮原子与Cu1形成平面五元环结构,Cu1—O 键长为0.192 3(3)~0.202 9(2)nm,Cu1—N 键长为0.205 4(3)~0.241 2(4)nm,与文献[14]报道的铜配合物[Cu2L2(H2O)2]类似;Cu2也与3个硒唑甲酸根双齿螯合配位,其中2个硒唑甲酸根以1个羧基氧和1个硒唑氮原子与Cu2形成平面五元环结构,另外一个硒唑甲酸根利用1个羧基氧(O8)与 Cu2单齿配位,Cu2—O8键长为0.196 0(3)nm,与文献[19]报道的双核铜配合物[Cu2(H2tea)2(dca)2]2·H2O 中 Cu2+离子分别为五配位和六配位的情况类似.在该双核配位体系中:由于含2个Cu(Ⅱ)离子和5个2-苯基-4-硒唑甲酸根离子(L-),整个配位内界显-1价,外界的1个NH+4离子起平衡电荷的作用,使整个晶体电荷平衡;外界还有1个游离的2-苯基-4-硒唑甲酸分子和6个晶格水分子,铵根离子、晶格水分子、游离的2-苯基-4-硒唑甲酸分子和2-苯基-4-硒唑甲酸根之间存在氢键(见图4),具体地说,硒唑甲酸上的羧基与相邻晶胞结构中的水分子和相邻晶胞结构中的羧基与水分子形成4个强烈的氢键,从而将不同结构单元连接成为一个具有二维网状结构的配合物.

图3 Cu(Ⅱ)的配位环境

图4 配合物的分子堆积图(沿c轴方向)
2.4 配合物与DNA的作用
溴化乙锭(EB)为一共轭平面分子,其本身荧光很弱,但能专一性地插入DNA双螺旋内部的碱基对之间使其荧光显著增强.如果共存于EB-DNA体系中的药物分子也能与DNA发生类似于EB的插入作用,这个小分子就会竞争EB与DNA的结合位点,使EB-DNA体系的荧光猝灭,而且EB-DNA体系荧光猝灭的程度可以说明药物分子与DNA插入作用的强弱[20].
图5反映了配合物对EB-DNA复合体系的荧光猝灭情况.配合物在592 nm处没有荧光,DNA-EB体系在592 nm处发出强烈的荧光,随着配合物浓度的增加,EB-DNA复合体系的荧光发生了不同程度的猝灭,由此推测配合物与DNA发生了插入作用.根据 Stem-Volmer方程[21]:I0/I=1+Ksqr(其中:I0和I分别为EB-DNA体系与不同浓度的配合物加EB-DNA复合体系的荧光强度;r为配合物与DNA浓度之比)计算得到配合物与DNA作用的结合常数Ksq为193.84,表明该配合物对DNA的插入作用很强.通过比较文献[14]中的结合常数(Ksq=0.76),并从配合物的分子结构图可以看出,配合物分子中增加了5个五元环和1个四元环,这些螯合环的形成增加了配合物

图5 配合物对EB-DNA体系的荧光猝灭
分子中配体的平面性,使得配体更容易插入到DNA分子的碱基对中去竞争EB与DNA的结合位点,从而导致配合物的插入作用明显强于配体.
[1]Schwarz K,Foltz C M.Selenium as an integral part of factor 3 against dietary necrotic liver degeneration[J].J Am Chem Soc,1957,79(12):3292-3293.
[2]徐辉碧,黄开勋.硒的化学、生物化学及其在生命科学中的应用[M].武汉:华中理工大学出版社,1994:227.
[3]黄峙.食品硒源的生物学研究进展[J].食品科学,2001,22(5):90-94.
[4]王夔.生命科学中的微量元素[M].北京:中国计量出版社,1991:138-185.
[5]曹会兰.重要的微量元素铜[J].微量元素与健康研究,2001,18(3):73-74.
[6]吴茂江,涂长信.铜与人体健康[J].微量元素与健康研究,2005,22(5):64-65.
[7]Zhu Haojie,Liu Guoqing.Glutamate up-regulates P-glycoprotein expression in rat brain microvessel endothelial cells by an NMDA receptor-mediated mechanism[J].Life Sci,2004,75(11):1313-1322.
[8]何水样,曹文凯,陈军利,等.铜(Ⅱ)与2-羰基丙酸水杨酰腙配合物的合成、晶体结构和抑菌活性[J].高等学校化学学报,2002,23(6):991-995.
[9]Atsuyoshi N,Akihiro S,Fukumoto R,et al.Selenazoles(selenium compounds)facilitate survival of cultured rat pheochromocy-toma PC12 cells after serum-deprivation and stimulate their neuronal differentiation via activation of Akt and mitogen-activated protein kinase,respectively[J].Biochem and Biophys Res Comm,2007,352(2):360-365.
[10]AL-Rubaie Ali Z,AL-Masoudi Wasfi A,ALI Jameel Hameed,et al.Synthesis,reaction and antiviral activity of 2,4-diaryl-1,3-selenazoles[J].Journal of the Korean Chemical Society,2008,52(1):36-46.
[11]睢超霞,张俊苓,刘薇,等.2,1,3-苯并硒二唑金属配合物的固相合成与表征[J].精细化工中间体,2006,36(5):32-35.
[12]Barkigia K M,Renner M W,Senge M O,et al.Interplay of axial ligation,hydrogen bonding,self-assembly,and conformational landscapes in high-spin Ni(Ⅱ)porphyrins[J].J Phys Chem B,2004,108(7):2173-2180.
[13]Zhou Aiju,Zheng Shaoliang,Fang Yue,et al.Molecular tectonics:Self-complementary supramolecular Se center dot center dot center dot N synthons directing assembly of 1D silver chains into 3D porous molecular architectures[J].Inorg Chem,2005,44(13):4457-4459.
[14]赵国良,施霞,张均平,等.2-苯基-4-硒唑甲酸过渡金属配合物的合成、结构及生物活性研究[J].中国科学:B辑化学,2010,40(10):1525-1535.
[15]Sheldrick G M.SHELXL97.Program for the refinement of crystal structure[CP].Göttingen:University of Göttingen,1997.
[16]Geary W J.The use of conductivity measurements in organic solvents for the characterisation of coordination compounds[J].Coord Chem Rev,1971,7(1):81-122.
[17]祝智力,冯云龙,林鸿.金刚烷甲酸稀土(Nd(Ⅲ),La(Ⅲ))配合物[LnL3(HL)(H2O)]2·2EtOH·2H2O的合成和晶体结构[J].中国稀土学报,2005,23(5):641-644.
[18]中本一雄.无机和配位化合物的红外和拉曼光谱[M].黄德如,汪仁庆,译.北京:化学工业出版社,1986.
[19]徐敏,谢国标,梁燕媚,等.双核铜配合物[Cu2(H2tea)2(dca)2]2·H2O 的合成和晶体结构[J].化学试剂,2009,31(10):781-784.
[20]陈鹏.几种核酸荧光探针的研究及应用[D].福州:福州大学化学化工学院,2003.
[21]Lakowicz J R,Weber G.Quenching of fluorescence by oxygen.Probe for structural fluctuations in macromolecules[J].Biochem,1973,12(21):4161-4170.
