SBA-15负载高分散纳米NiO的丙烷氧化脱氢制丙烯催化性能
2012-12-11鲁怀乾翁维正黄传敬万惠霖
鲁怀乾 石 磊 何 冲 翁维正 黄传敬 万惠霖
(厦门大学,固体表面物理化学国家重点实验室,醇醚酯化工清洁生产国家工程实验室,化学化工学院化学系,福建厦门361005)
SBA-15负载高分散纳米NiO的丙烷氧化脱氢制丙烯催化性能
鲁怀乾 石 磊 何 冲 翁维正*黄传敬 万惠霖*
(厦门大学,固体表面物理化学国家重点实验室,醇醚酯化工清洁生产国家工程实验室,化学化工学院化学系,福建厦门361005)
采用浸渍法通过改变焙烧气氛制备了系列NiO/SBA-15(wNiO=20%)催化剂,并考察了催化剂的丙烷氧化脱氢(ODHP)反应性能.实验结果表明,与在静止和流动空气中焙烧的催化剂相比,在1%NO/He(VNO/VHe=1: 99)气氛中焙烧的NiO/SBA-15-NO具有优异的低温丙烷氧化脱氢制丙烯性能,在350°C时,丙烷的转化率和丙烯收率分别约达29%和13%.反应温度升至450°C时,丙烯的选择性仍保持在45%左右.X射线粉末衍射(XRD)和透射电镜(TEM)测试结果表明,1%NO/He气氛可有效抑制焙烧过程中NiO纳米颗粒的团聚,使NiO物种高分散于SBA-15的孔道中.H2-程序升温还原(H2-TPR)和O2-程序升温脱附(O2-TPD)测试结果表明,随着NiO在SBA-15上分散度的提高,催化剂的抗还原性增强,ODHP活性氧物种O-的含量增加,进而使1%NO/He气氛中焙烧的NiO/SBA-15-NO在较宽的温度范围内(350-450°C)均具有良好的丙烯选择性,并显著提高了催化剂的低温活性.
NiO/SBA-15;丙烷;氧化脱氢;丙烯;焙烧气氛
1 引言
纳米尺度的NiO具有优良的低温(<500°C)烷烃氧化脱氢催化性能,9-11但其在反应条件下容易被还原和烧结,导致催化剂失活.通过在NiO中添加Ti、Ce或Zr等第二组分可增强其抗还原能力,进而提高纳米NiO的ODHP活性和稳定性.12-17研究表明将NiO负载于Al2O3和SiO2等载体表面也有助于提高其抗还原性.18-20近期Li等21以十二烷基硫酸钠为模板剂制备了具有蠕虫状孔道的介孔NiO并用于ODHP反应.与纳米NiO相比,介孔NiO具有更好的抗高温还原性,同时介孔NiO固有的丰富的介孔孔道也有利于反应过程中的传质和传热,因此在较宽的温度范围内均表现出良好ODHP反应性能.可以预期,将NiO高度分散于大比表面积的介孔硅基分子筛上也可显著改善其ODHP性能.这一方面是由于NiO与SiO2之间的相互作用,有利于改善NiO纳米颗粒的抗还原和抗烧结性能,18另一方面介孔分子筛规则的孔道结构和SiO2的化学惰性有利于传质、传热和产物丙烯的脱附.但该催化剂的局限在于当NiO负载量较低时,催化剂的活性不佳,在较高的负载量下,NiO纳米颗粒则易在焙烧的过程中通过在载体表面的迁移而烧结,导致催化剂的ODHP性能迅速下降,故迄今为止尚未见到负载型NiO基催化剂用于ODHP反应的报道.近期de Jong等22,23报道了以1%NO/He(VNO/VHe=1:99)为焙烧气氛制备SBA-15负载的纳米NiO催化剂.研究表明1% NO/He气氛有助于降低硝酸镍前驱体在升温过程的分解速率,进而抑制NiO物种的烧结和团聚,在较高的负载量下仍可使NiO以较小的纳米颗粒高度分散于载体表面.本文以SBA-15为载体,以1% NO/He为焙烧气氛制备了高分散的NiO/SBA-15 (wNiO=20%)催化剂,并将其用于ODHP反应.通过对催化剂结构、表面性质的表征以及与在静止和流动空气中焙烧所得催化剂的对比,讨论了高分散NiO/ SBA-15催化剂的构效关系.
2 实验部分
2.1 催化剂的制备
SBA-15的制备:参照文献24方法,将8.0 g P123 (聚环氧乙烯-聚环氧丙烯-聚环氧乙烯三嵌段共聚物,EO20PO70EO20,AR,M=5800,Aldrich)溶解于300 mL 2 mol·L-1的盐酸水溶液,加入21.5 mL正硅酸四乙酯(TEOS,AR,国药集团化学试剂有限公司),继续在80°C水浴中反应24 h,而后将上述混合物转入聚四氟乙烯内衬的水热反应釜,在100°C老化24 h.所得白色固体用去离子水充分洗涤后在100°C烘干12 h,再于550°C焙烧6 h去除有机模板剂得到SBA-15.
采用浸渍法制备NiO/SBA-15(wNiO=20%)催化剂.SBA-15载体在110°C真空干燥4 h,冷却至室温后将其浸渍于计量的4 mol·L-1Ni(NO3)2·6H2O(AR,国药集团化学试剂有限公司)水溶液中,于80°C水浴中缓慢搅拌蒸干后,所得固体在120°C干燥12 h.干燥后的样品分别在下列条件下以1°C·min-1的速率升温至500°C,焙烧3 h制得催化剂样品.(1)置于加盖的坩埚中焙烧,记为NiO/SBA-15-Air(S).(2)在流速为90 mL·min-1的空气气流中焙烧,记为NiO/ SBA-15-Air(F).(3)在流速为90 mL·min-1的1%NO/ He气流中焙烧,记为NiO/SBA-15-NO.所得催化剂样品经压片、粉碎后筛取60-80目的颗粒备用.常规NiO样品由Ni(NO3)2·6H2O(AR,国药集团化学试剂有限公司)在马弗炉中以1°C·min-1升温至500°C焙烧3 h后制得,经压片、粉碎后筛取60-80目的颗粒备用.
2.2 催化剂的表征
X射线粉末衍射(XRD)实验在Panalytical Xʹpert Pro型X射线粉末衍射仪(荷兰)上进行.采用石墨单色器滤光,CuKα(λ=0.15406 nm)作为辐射源,管电压40 kV,管电流30 mA,扫描步长为0.0167°.小角XRD扫描范围为0.5°-5°,每步时间为2 s.常规XRD扫描范围为30°-90°,每步时间为20 s.各催化剂样品上NiO的平均粒径根据NiO(200)晶面衍射峰的半峰宽采用Scherrer公式计算得到:
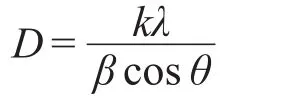
其中,D为晶粒的平均粒径(nm),常数k取0.89;λ为入射波长0.15406 nm;θ为衍射角度;β为晶粒因子函数的半高宽,单位为弧度,β=β-βo,β为实验中实测的半峰宽,βo为仪器展宽.
催化剂的比表面积、孔容和孔分布在Micromeritics Tristar 3000型物理吸附仪(美国)上测定.以氮气为吸附质,吸附温度为-196°C,催化剂用量约0.10 g.测试前,样品先在300°C抽空处理6 h.比表面积采用BET方法计算,孔径分布根据脱附曲线采用BJH方法计算.
催化剂的透射电镜(TEM)表征在Philips FEI Tecnai 30型透射电镜(荷兰)上进行,加速电压为300 kV.测试前,样品经研磨和超声分散(乙醇为分散剂)后,用喷有碳膜的铜网捞取悬浮液制样.
X射线光电子能谱(XPS)测试在PHI Quantum 2000 Scanning ESCA Microprobe型能谱仪(美国)上进行.测试时以Al-Kα为X射线辐射源,以表面污染碳的C 1s结合能(Eb=284.8 eV)为内标校正其他元素的结合能.通过积分求出各元素特征谱的峰面积,除以灵敏度因子,计算得到催化剂表面各元素的组成.
H2-程序升温还原(H2-TPR)实验在自行搭建的TPR-气相色谱(GC-950,上海海欣气相色谱仪器有限公司)装置上进行.以热导检测器(TCD)为检测器,H2/Ar(VH2:VAr=5:95)混合气为载气(20 mL·min-1)和还原气,O2/Ar(VO2:VAr=5:95)混合气为氧化气,催化剂用量50.0 mg(60-80目).实验前催化剂先在O2/Ar混合气中500°C处理1 h,降至室温后切入H2/ Ar混合气吹扫至基线平稳,再从室温开始以10°C· min-1的速率进行程序升温还原,终止温度为900°C.以液氮调制的乙醇固-液混合物为冷阱除去还原过程中生成的H2O.
催化剂的O2-程序升温脱附(O2-TPD-MS)实验在Micromeritics AutoChem II 2920型全自动化学吸附仪(美国)上进行.以高纯He(99.999%)为载气,O2/ He(VO2:VAr=1:4)混合气为吸附气和氧化气,催化剂用量为0.10 g.采用Hiden Analytical QIC-20型质四极质谱仪(英国)在线检测脱附O2(m/e=32)的质谱信号.实验前催化剂先在O2/He混合气中500°C处理1 h,待温度降至50°C后切入高纯He(20 mL·min-1)吹扫1 h,再从50°C开始以10°C·min-1的速率进行程序升温脱附,终止温度为900°C.
2.3 催化剂的性能评价
催化剂性能评价在固定床石英微型反应器中进行,石英管的内径约为5 mm,采用自制的电炉加热,控温热电偶紧贴于石英管外部,其测温端与催化剂床层中部对齐.催化剂用量为0.10 g,反应原料气组成为C3H8/O2/N2,体积比为1:1:4,反应空速(GHSV)为12000 mL·g-1·h-1.
反应尾气由气相色谱仪(GC-950,上海海欣气相色谱仪器有限公司)在线分析.以TCD为检测器,采用涂覆了角鲨烷的Al2O3柱和碳分子筛柱分析C3H8、C3H6、C2H4、C2H6、CH4、CO和CO2.以氢火焰离子化检测器(FID)为检测器,采用GDX-103色谱柱分析乙醛、丙烯醛、丙醛和丙酮等含氧有机物.反应尾气的管道辅以加热带,使其在进入FID取样阀前保持在125°C,以防反应产物冷凝.通过FID检测器取样阀后的尾气经冰水混合物冷阱除去其中的H2O和含氧有机物,再进入TCD的取样阀采样分析.
3 结果与讨论
3.1 催化剂的丙烷氧化脱氢性能
不同气氛下焙烧所得NiO/SBA-15催化剂的丙烷氧化脱氢制丙烯性能见图1.由图1A可知,在 350°C时各催化剂的丙烯选择性均比较接近,但丙烷转化率的差别较大.在静态空气中焙烧的NiO/ SBA-15-Air(S)上,丙烷的转化率和丙烯收率仅分别为2.4%和1.1%,相同反应条件下,于1%NO/He气流中焙烧的NiO/SBA-15-NO上丙烷的转化率和丙烯收率分别可达约29%和13%.这一结果优于目前文献中已报道的Ti-Ni-O,Ni-Zr-O和Ce-Ni-O等体系.14-16与介孔氧化镍催化剂相比,后者在450°C时才能获得相近的丙烯收率.21不同样品上丙烷转化率随温度的变化如图1B所示,随着温度的升高, NiO/SBA-15-Air(S)和NiO/SBA-15-Air(F)上丙烷的转化率逐渐增大,而NiO/SBA-15-NO上丙烷的转化率基本保持不变.在350-450°C温度区间内,当反应温度相同时,三种催化剂上丙烷转化率(C)的顺序为CNiO/SBA-15-Air(S)<CNiO/SBA-15-Air(F)<CNiO/SBA-15-NO.随温度的升高,NiO/SBA-15-Air(S)和NiO/SBA-15-Air(F)上丙烯的选择性均出现不同程度的下降,而NiO/ SBA-15-NO上丙烯选择性变化不大,在450°C时仍保持在45%左右(图1C).
3.2 催化剂的表征
催化剂的小角XRD和常规XRD图见图2.由图2A可知,经500°C焙烧后的样品均出现SBA-15的特征d100衍射峰,表明负载NiO后的样品仍保持了SBA-15所固有的有序结构.各个催化剂的常规XRD图上均可检测出位于2θ=37.2,43.3,62.8°的衍射峰,分别归属于NiO的(111)、(200)和(220)晶面的特征衍射峰,但不同样品上NiO衍射峰的强度不同.与其他两个样品相比,NiO/SBA-15-NO的衍射峰明显宽化.Scherrer公式的计算结果表明,NiO/ SBA-15-NO中NiO颗粒的平均粒径仅为4 nm,而在静态和流动空气中焙烧所得催化剂上NiO的平均粒径分别为19和10 nm.Wu等14在研究Ti-Ni-O体系上ODHP反应时发现,在相同的条件下,具有较小粒径的纳米NiO的丙烷转化率远高于粒径较大的NiO颗粒,这与本文的实验结果是一致的.

图1 不同气氛焙烧的NiO/SBA-15催化剂的ODHP性能Fig.1 ODHPperformance of the NiO/SBA-15 catalysts calcined under different atmospheresC:conversion,S:selectivity,Y:yield;catalysts calcined under static air,flowing air,and flowing 1%NO/He(VNO/VHe=1:99)mixture are denoted as NiO/SBA-15-Air(S),NiO/SBA-15-Air(F),and NiO/SBA-15-NO,respectively.reaction conditions:m(catalyst)=0.10 g,gas hourly space velocity (GHSV)=12000 mL·g-1·h-1,V(C3H8)/V(O2)/V(N2)=1:1:4;the data were collected after 30 min on stream; ODHP:oxidation dehydrogenation of propane

图2 不同气氛焙烧的NiO/SBA-15催化剂的小角(A)和宽角(B)XRD图Fig.2 Small-angle(A)and wide-angle(B)X-ray diffraction(XRD)patterns of the NiO/SBA-15 catalysts calcined under different atmospheres(a)NiO/SBA-15-Air(S);(b)NiO/SBA-15-Air(F);(c)NiO/SBA-15-NO
表1给出了各个催化剂的比表面积、孔容和平均孔径等数据.与SBA-15相比,负载NiO后样品的比表面积、孔容和孔径都出现不同程度的下降.由图3B的等温吸脱附曲线可以看出,所有样品均显示了典型的IV型吸脱附等温线和H1型滞后环.相比于载体SBA-15,负载NiO后,催化剂样品的毛细凝聚起始压力减小,同时显示出在较宽相对压力范围内扁平的滞后环,这可能是由于负载的NiO纳米颗粒的阻塞作用,形成了孔径较小的孔道(即“墨水瓶”形孔道),25图3A中b,c和d等样品上出现的两种孔径分布也证明了这一点.
催化剂的TEM照片如图4所示.图4a中可以明显观察到大片黑色区域(图中的圆圈区域),表明于静止空气中焙烧所得NiO/SBA-15-Air(S)催化剂上NiO物种发生了明显的团聚.当焙烧气氛改为流动空气时,NiO物种的团聚得到了一定程度的改善(图中箭头所指示的区域),但是NiO物种在SBA-15上的分布仍不太均匀.从NiO/SBA-15-NO的TEM照片可以看出,焙烧气氛改为1%NO/He后,NiO物种在SBA-15上的分散状况得以明显改善,这与XRD的表征结果也是一致的.de Jong等22采用原位XRD和热重-质谱(TG-MS)分析等手段研究了不同气氛中SBA-15负载硝酸镍的分解过程,结果表明采用1%NO/He为焙烧气氛可以消除分解过程中产生的氧自由基,降低硝酸盐的分解速率,从而抑制NiO纳米粒子的烧结,制得高分散的NiO/SBA-15催化剂.根据XPS的分析结果,可以算出各NiO/SBA-15催化剂表面的Ni/Si比(表1).由计算结果可知,NiO/ SBA-15-NO表面的Ni/Si比远小于在其他两种气氛中焙烧所得到的催化剂,表明在1%NO/He气氛中焙烧有助于使硝酸镍在SBA-15的孔道内部分解,23并可有效抑制分解后的NiO纳米颗粒向孔道外部迁移,阻止了NiO物种的团聚,进而显著提高NiO物种的分散度.
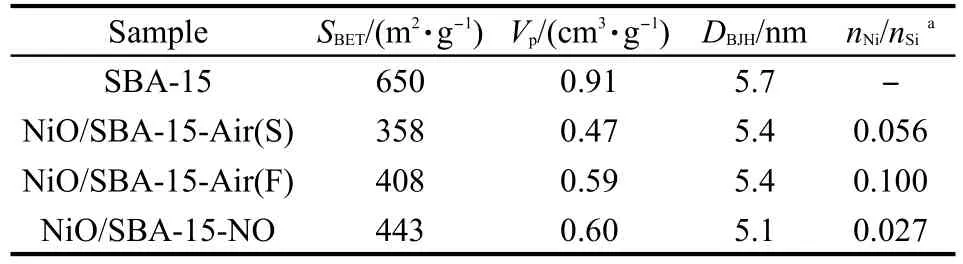
表1 SBA-15和不同气氛焙烧的NiO/SBA-15催化剂的物理性质和XPS表征结果Table 1 Physical properties and X-ray photoelectron spectroscopy(XPS)results of SBA-15 and the NiO/SBA-15 catalysts calcined under different atmospheres
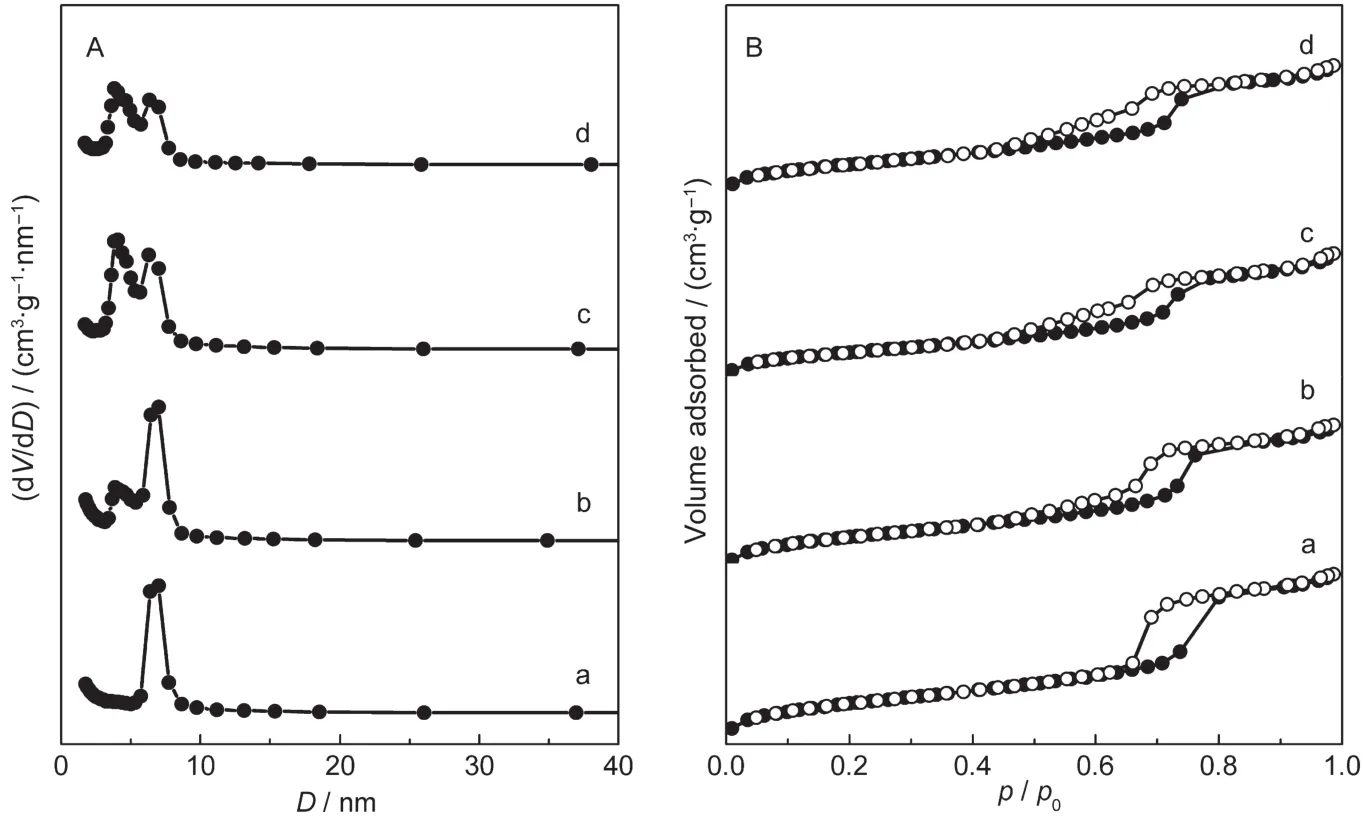
图3 SBA-15和不同气氛焙烧的NiO/SBA-15的孔径分布(A)和N2吸附-脱附等温线(B)Fig.3 Pore size distribution(A)and N2adsorption-desorption isotherms(B)of SBA-15 and NiO/SBA-15 catalysts calcined under different atmospheres(a)SBA-15;(b)NiO/SBA-15-Air(S);(c)NiO/SBA-15-Air(F);(d)NiO/SBA-15-NO
NiO基催化剂的抗还原性对其烷烃氧化脱氢性能有着重要影响.Ducarme和Martin26在研究NiO基催化剂上乙烷的氧化脱氢反应时发现,当反应处于稳态时,催化剂中绝大部分的Ni处于氧化态(Ni2+),一旦有少量的Ni2+被还原生成Ni单质(Ni0),乙烯的选择性迅速降为零.为了进一步探明不同气氛下焙烧样品的抗还原性能,对相关催化剂进行了H2-TPR表征,结果如图5所示.由图可知催化剂的H2-TPR图中均出现了两个还原峰,通过与常规NiO的H2-TPR图对比,可将低温(约370°C)还原峰归属为体相NiO的还原,参照相关文献,27-29可将位于约580°C的还原峰归属为与SBA-15具有较强相互作用的NiO物种的还原.从图中可以看出,NiO/SBA-15上高温还原峰的面积随NiO粒径的减小而增大,说明在1% NO/He中焙烧所得到的催化剂上与SBA-15具有较强相互作用的NiO物种的数量显著多于在其他两种气氛中焙烧所得的催化剂,这与XRD和TEM等表征所得到的NiO/SBA-15-NO样品上NiO物种分散度高于NiO/SBA-15-Air(S)和NiO/SBA-15-Air(F)的结论也是一致的.

图4 不同气氛焙烧的NiO/SBA-15催化剂的TEM照片Fig.4 Transmission electron microscopy(TEM)images of the NiO/SBA-15 catalysts calcined under different atmospheres(a)NiO/SBA-15-Air(S);(b)NiO/SBA-15-Air(F);(c)NiO/SBA-15-NO
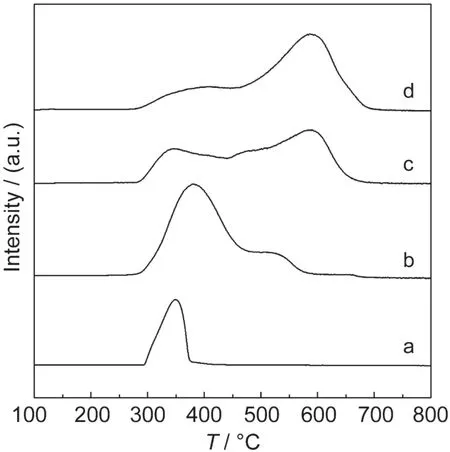
图5 NiO和不同气氛焙烧的NiO/SBA-15催化剂的H2-TPR图Fig.5 H2-temperature program reduction(H2-TPR) profiles of the NiO and NiO/SBA-15 catalysts calcined under different atmospheres(a)NiO;(b)NiO/SBA-15-Air(S);(c)NiO/SBA-15-Air(F); (d)NiO/SBA-15-NO
为了获得不同气氛焙烧的NiO/SBA-15上氧物种的相关信息,探明催化剂丙烷氧化脱氢性能差异的本质,我们对相关样品进行了O2-TPD-MS表征,所得结果见图6.NiO中的非化学计量氧物种主要为O-和,这些亲电性氧物种能够在低温下有效地活化烷烃分子.Chen等30,31采用O2-TPD-MS和脉冲反应等手段研究了NiO催化剂上乙烷氧化脱氢反应的活性氧物种,结果表明O-比和O2-(晶格氧)具有更高的乙烯选择性,一旦催化剂上的非化学计量氧耗尽并动用了NiO的晶格氧,就会发生裂解和深度氧化反应.如图6所示,常规NiO的O2-TPD-MS图上只出现一个位于700°C的脱附峰,可将其归属为NiO晶格氧的脱附,这与Zhang32和Turkey33等的实验结果一致.将NiO负载于SBA-15上后,除了位于700°C附近的晶格氧脱附峰外,还可以观察到位于180和400°C附近的脱附峰,它们源于NiO中非化学计量氧的脱附,其中位于180°C附近的脱附峰归属为的脱附,位于400°C附近的脱附峰归属为O-的脱附.34

图6 NiO和不同气氛焙烧NiO/SBA-15催化剂的O2-TPD-MS谱图Fig.6 O2-temperature program desorption-mass spectrum(O2-TPD-MS)profiles of the NiO and NiO/ SBA-15 catalysts calcined under different atmospheres(a)NiO;(b)NiO/SBA-15-Air(S);(c)NiO/SBA-15-Air(F); (d)NiO/SBA-15-NO
从图6中可以看出,SBA-15负载的NiO催化剂上位于180°C附近的脱附峰面积均很小,随着NiO粒径的减小,位于400°C附近的脱附峰面积逐渐增大,且峰温向低温方向移动,表明随NiO物种在SBA-15上分散程度的提高,催化剂上O-物种的含量逐渐增大.结合图1的催化剂性能评价结果可以看出,在相同的反应条件下,NiO/SBA-15上的丙烷转化率与其O2-TPD图中O-脱附峰的面积呈顺变关系;在丙烯选择性基本相同的情况下(如350°C),催化剂上O-物种的数量越多,丙烷的转化率也越高.据此可以合理地推断O-是NiO/SBA-15催化剂上丙烷氧化脱氢制丙烯反应的活性氧物种,这与Li等21得出的结论也是一致的.
4 结论
通过改变焙烧气氛制备了高分散的NiO/ SBA-15催化剂,并考察了其ODHP反应性能.与在静止和流动空气中焙烧的催化剂相比,1%NO/He气氛中焙烧的NiO/SBA-15-NO表现出更为优异的低温ODHP性能.在350°C时,NiO/SBA-15-NO上丙烷的转化率和丙烯收率分别可达约29%和13%,且该催化剂在较宽的温度范围内均表现出良好的ODHP性能,450°C时丙烯选择性仍保持在45%左右.NiO/SBA-15-NO催化剂优良的ODHP性能可以归结为以下两个原因:(1)催化剂的介孔结构有利于反应过程中的传质和传热以及抑制丙烯的深度氧化;(2)以1%NO/He为焙烧气氛可有效抑制NiO纳米颗粒在焙烧过程中的团聚,使NiO物种高分散于SBA-15的孔道中.NiO分散度的提高不仅有助于增强催化剂的抗还原性,也使得催化剂上O-物种的含量显著增加,而O-是ODHP反应的活性氧氧物种,能够在低温下有效活化丙烷,在保持较高丙烯选择性的同时可显著提高丙烷的转化率.
(1) Kung,H.H.Adv.Catal.1994,40,1.doi:10.1016/s0360-0564 (08)60655-0
(2) Chao,Z.S.;Ruckenstein,E.J.Catal.2004,222,17.doi: 10.1016/j.jcat.2003.11.004
(3) Cavani,F.;Trifiro,F.Catal.Today 1995,24,307.doi:10.1016/ 0920-5861(95)00051-G
(4)Liu,Y.M.;Cao,Y.;Yi,N.;Feng,W.L.;Dai,W.L.;Yan,S.R.; He,H.Y.;Fan,K.N.J.Catal.2004,224,417.doi:10.1016/ j.jcat.2004.03.010
(5) Chen,K.D.;Xie,S.B.;Bell,A.T.;Iglesia,E.J.Catal.2001, 198,232.doi:10.1006/jcat.2000.3125
(6) Guerrero-Pérez,M.O.;Bañares,M.A.Catal.Today 2006,113, 48.doi:10.1016/j.cattod.2005.11.009
(7)Argyle,M.D.;Chen,K.D.;Resini,C.;Krebs,C.;Bell,A.T.; Iglesia,E.J.Phys.Chem.B 2004,108,2345.doi:10.1021/ jp030989m
(8) Cassidy,F.E.;Hodnett,B.K.CATTECH 1998,2,173.
(9) Heracleous,D.E.;Lemonidou,A.A.J.Catal.2010,270,67. doi:10.1016/j.jcat.2009.12.004
(10) Heracleous,D.E.;Lemonidou,A.A.J.Catal.2006,237,162.
(11) Nakamura,K.;Miyake,T.;Konishi,T.;Suzuki,T.J.Mol.Catal. A:Chem.2006,260,144.doi:10.1016/j.molcata.2006.06.058
(12) Boizumault-Moriceau,P.;Pennequin,A.;Grzybowska,B.; Barbaux,Y.Appl.Catal.A:Gen.2003,245,55.doi:10.1016/ S0926-860X(02)00611-7
(13)Liu,Y.M.;Wang,L.C.;Chen,M.;Xu,J.;Cao,Y.;He,H.Y.; Fan,K.N.Catal.Lett.2009,130,350.doi:10.1007/s10562-009-9977-z
(14)Wu,Y.;He,Y.M.;Chen,T.;Weng,W.Z.;Wan,H.L.Appl.Surf. Sci.2006,252,5220.doi:10.1016/j.apsusc.2005.08.002
(15)He,Y.M.;Wu,Y.;Chen,T.;Weng,W.Z.;Wan,H.L.Catal. Commun.2006,7,268.doi:10.1016/j.catcom.2005.09.015
(16) Wang,C.C.;Li,J.H.;Sun,Y.F.;Zhu,X.Q.;Huang,C.J.; Weng,W.Z.;Wan,H.L.Acta Phys.-Chim.Sin.2011,27, 2421.[汪彩彩,李建辉,孙毅飞,朱晓权,黄传敬,翁维正,万惠霖.物理化学学报,2011,27,2421.]doi:10.3866/PKU. WHXB20110932
(17)Li,J.H.;Wang,C.C.;Huang,C.J.;Weng,W.Z.;Wan,H.L. Catal.Lett.2010,137,81.doi:10.1007/s10562-010-0333-0
(18)He,S.F.;Wu,H.M.;Yu,W.J.;Mo,L.Y.;Lou,H.;Zheng,X. M.Int.J.Hydrog.Energy 2009,34,839.
(19) Tomiyama,S.;Takahashi,R.;Sato,S.;Sodesawa,T.;Yoshida, S.Appl.Catal.A:Gen.2003,241,349.doi:10.1016/S0926-860X(02)00493-3
(20)Song,Y.Q.;Liu,H.M.;Liu,S.Q.;He,D.H.Energy Fuels 2009,23,1925.doi:10.1021/ef800954a
(21)Li,J.H.;Wang,C.C.;Huang,C.J.;Sun,Y.F.;Weng,W.Z.; Wan,H.L.Appl.Catal.A:Gen.2010,382,99.doi:10.1016/ j.apcata.2010.04.034
(22) Sietsma,J.R.A.;Friedrich,H.;Broersma,A.;Versluijs-Helder, M.;Jos van Dillen,A.J.;de Jongh,P.E.;de Jong,K.P.J.Catal. 2008,260,227.doi:10.1016/j.jcat.2008.10.007
(23) Sietsma,J.R.A.;Meeldijk,J.D.;den Breejen,J.P.;Versluijs-Helder,M.;Jos van Dillen,A.J.;de Jongh,P.E.;de Jong,K.P. Angew.Chem.Int.Edit.2007,46,4547.doi:10.1002/anie. 200700608
(24) Zhao,D.Y.;Feng,J.L.;Huo,Q.S.;Melosh,N.;Fredrickson, G.H.;Chmelka,B.F.;Stucky,G.D.Science 1998,279,548. doi:10.1126/science.279.5350.548
(25) Li,C.L.;Zhang,Q.H.;Wang,Y.;Wan,H.L.Chin.J.Catal. 2008,29,37.[李常丽,张庆红,王 野,万惠霖.催化学报, 2008,29,37.]
(26) Ducarme,V.;Martin,G.A.Catal.Lett.1994,23,97.doi: 10.1007/BF00812135
(27) He,S.F.;Jing,Q.S.;Yuan,W.J.;Mo,L.Y.;Lou,H.;Zheng,X. M.Catal.Today 2009,148,130.doi:10.1016/j.cattod. 2009.03.009
(28)Mile,B.;Stirling,D.;Zammitt,M.A.;Lovell,A.;Webb,M. J.Catal.1988,114,217.doi:10.1016/0021-9517(88)90026-7
(29) Lensveld,D.J.;Mesu,J.G.;van Dillen,A.J.;de Jong,K.P. Microporous Mesoporous Mat.2001,44-45,401.
(30) Chen,T.;Li,W.Z.;Yu,C.Y.Chin.J.Catal.1998,19,37. [陈 铜,李文钊,于春英.催化学报,1998,19,37.]
(31) Chen,T.;Li,W.Z.;Yu,C.Y.;Jin,R.C.;Xu,H.Y.Stud.Surf. Sci.Catal.2000,130,1847.doi:10.1016/S0167-2991(00) 80470-X
(32) Zhang,X.J.;Liu,J.X.;Yi,J.;Xie,Y.C.Appl.Catal.A:Gen. 2003,240,143.doi:10.1016/S0926-860X(02)00426-X
(33) Turky,A.M.Appl.Catal.A:Gen.2003,247,83 doi:10.1016/ S0926-860X(03)00089-9
(34) Iwamoto,M.;Yoda,Y.;Egashira,M.;Seiyama,T.J.Phys. Chem.1976,80,1989.doi:10.1021/j100559a008
May 25,2012;Revised:July 9,2012;Published on Web:July 9,2012.
Highly-Dispersed NiO Nanoparticles on SBA-15 for Oxidative Dehydrogenation of Propane to Propylene
LU Huai-Qian SHI Lei HE Chong WENG Wei-Zheng*HUANG Chuan-Jing WAN Hui-Lin*
(State Key Laboratory of Physical Chemistry of Solid Surfaces,National Engineering Laboratory for Green Chemical Productions of Alcohols,Ethers and Esters,Department of Chemistry,College of Chemistry and Chemical Engineering,Xiamen University, Xiamen 361005,Fujian Province,P.R.China)
A series of NiO/SBA-15(wNiO=20%)catalysts were prepared by impregnating SBA-15 with an aqueous solution of nickel nitrate followed by calcining under three different atmospheres.The resulting materials were studied with regard to the oxidative dehydrogenation of propane(ODHP)to propylene. Compared to the catalysts calcined under either static or moving air,the NiO/SBA-15-NO catalyst calcined under flowing 1%NO/He(VNO/VHe=1:99)atmosphere demonstrated greater activity for this reaction at low temperature.Propylene yield of~13%with propane conversion of~29%was obtained at 350°C and the propylene selectivity remained at about 45%even when the reaction temperature was raised to 450°C. X-ray diffraction(XRD),transmission electron microscopy(TEM),H2-temperature program reduction (H2-TPR),and O2-temperature program desorption(O2-TPD)characterizations were used to investigate the intrinsic differences between these NiO/SBA-15 catalysts.It was found that NiO species in the catalyst calcined under 1%NO/He atmosphere were highly dispersed inside the mesopores of SBA-15.With the increasing of NiO dispersion on the support,the quantity of NiO species with a reduction temperature above 450°C increased significantly.In addition,the density of O-species on the catalyst calcined under 1%NO/He was much higher than that in the case of the other two samples.These factors are responsible for the superior performance of the NiO/SBA-15-NO catalyst for the ODHP reaction over the temperature range 350 to 450°C.
NiO/SBA-15;Propane;Oxidative dehydrogenation;Propylene;Calcination atmosphere
10.3866/PKU.WHXB201207091
∗Corresponding authors.WENG Wei-Zheng,Email:wzweng@xmu.edu.cn;Tel:+86-592-2185192.
WAN Hui-Lin,Email:hlwan@xmu.edu.cn;Tel:+86-592-2186569.
The project was supported by the National Key Basic Research Program of China(973)(2010CB732303),National Natural Science Foundation of China(21173173,21073148,21033006),Programfor InnovativeResearchTeamof theMinistryof Educationof China(IRT1036),andKey Scientific Project of Fujian Province,China(2009HZ0002-1).
国家重点基础研究发展计划(973)(2010CB732303),国家自然科学基金(21173173,21073148,21033006),教育部创新团队项目(IRT1036)和福建省重大科技专项(2009HZ0002-1)资助项目
O643
