基于人芳香酶的雄甾烷衍生物抗乳腺癌构效关系研究
2012-11-26赵宪国符兰波
王 强,乔 梁,马 晨,赵宪国,符兰波,蔡 虹
(中南民族大学 药学院,武汉430074)
芳香酶(AR)是还原型烟酞胺腺嘌呤二核苷酸二磷酸盐(NADPH)-细胞色素P450还原酶,在体内可催化睾酮、雄烯二酮向雌酮、雌二醇转化,又称为雌激素合成酶,还是唯一已知的脊椎动物体内催化转化雄性激素成为雌二醇的酶[1].其催化反应见图1,芳香化酶参与此反应过程的最后一步,是此过程的关键酶和限速酶.芳香酶的活性和芳香酶的mRNA在正常乳腺组织和乳腺肿瘤中都存在[2].
乳腺癌是妇女常见的恶性肿瘤,其发病与内分泌失调有关[3],即体内雌激素水平病理性上升后与乳腺肿瘤细胞内的雌激素受体(ER)结合,刺激肿瘤组织生长,现乳腺癌内分泌药物治疗已经取代了手术切除和射线照射内分泌器官的内分泌疗法[4].因2/3的乳腺癌是雌激素依赖性的,乳腺组织局部高雌激素水平的微环境,是乳腺癌发生的重要原因,它们能在雌激素减少后得以消退.芳香酶抑制剂(AI)能特异性的导致芳香酶失活,阻断芳构化反应,抑制雌激素的生成,降低血液中雌激素水平,成为乳腺癌治疗的一种全新思路[5-8].现已开发上市了三代AR抑制剂作为治疗乳腺癌的二线或三线药物,美国、日本等已经广泛用于临床.
计算机辅助药物设计是通过模拟和计算受体与配体的这种相互作用,进行先导化合物的优化与设计.它作为一种实用化的工具已介入到药物研究的各种环节[9].因药物分子的形状的细微差异会造成很大的活性改变[10],分子对接可模拟小分子化合物与生物大分子的作用方式[11].通过计算预测两者间的结合模式和亲和力,进行药物的虚拟筛选[12].它首先产生一个填充受体分子表面的口袋或凹槽的球集,再生成一系列假定的结合位点,依据受体表面的这些结合点与配体分子的距离匹配原则,将配体分子投映到受体分子表面,来计算其结合的模式和亲和力,并对计算结果打分,评判配体与受体的结合程度[13].
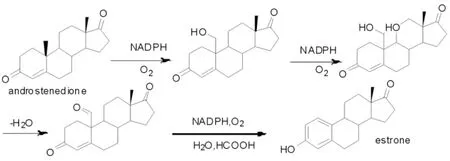
图1 芳香酶的催化作用Fig.1 The catalytic activity of aromatase
本文针对人类胎盘芳香酶细胞色素P450受体复合物(PDB,ID:3EQM),利用Sybyl软件中Surflex模块进行分子对接,在此基础上研究其构效关系,建立相应的评价模型,为该类天然产物或合成类似物的衍生化提供理论依据,期望获得高活性的先导化合物.
1 实验部分
1.1 药物设计工具
Sybyl是美国Tripos公司为从事药物及相关领域研究的用户提供全面的药物设计工具,可从小分子出发进行3D-QSAR的研究,或从受体出发进行基于结构的药物设计,还能从药效基团出发进行数据库的检索.本实验采用SybylⅩ1.10版本.
1.2 芳香酶晶体数据的准备
在蛋白晶体数据库(http://www.pdb.org/pdb/home/home.do)中下载编号为3EQM的蛋白晶体结构(图2),使用 Sybyl/Biopolymer[16]模块对蛋白晶体结构加氢原子,并对蛋白分子加载AMBER7 FF99电荷,对原有小分子抑制剂加载Gasteiger-Hückel电荷,与设计部分小分子电荷一致.在晶体结构中提取出原有小分子抑制剂的结构,以确定对接位点.
1.3 配体小分子的准备
利用 ZINC 数据库(http://zinc.docking.org),基于雄甾烷类基本母核结构(图3),设定90%相似度,通过相似性搜索得到5045个雄甾烷类似化合物.再通过Sybyl/Database模块将这些化合物转换成备选配体小分子数据库.
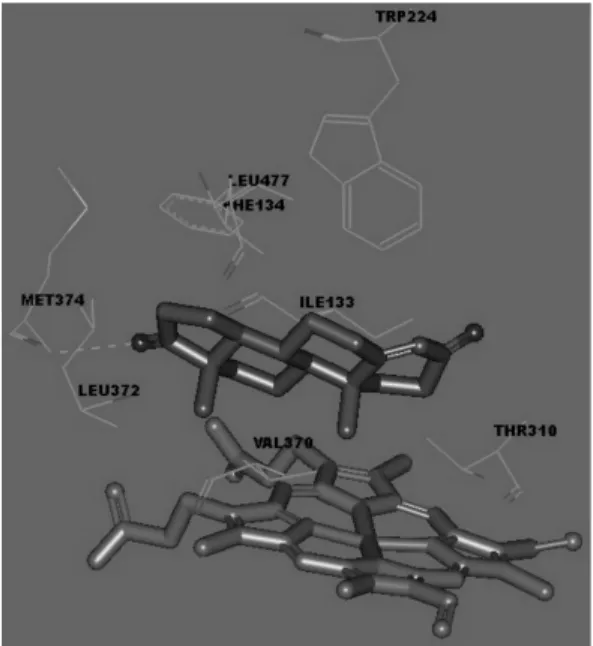
图2 原晶体复合物Fig.2 Former crystal complex
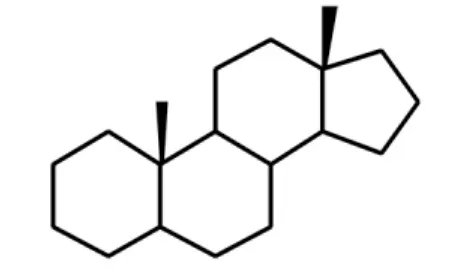
图3 雄甾烷类母核结构Fig.3 Mother nuclear strcture of androstane
1.4 分子对接
将初步筛选得到的备选配体小分子数据库,使用Sybyl/SurFlex模块与人芳香酶的晶体结构进行对接,所有的分子构建和对接计算工作均在方正文祥E520上,基于Linux系统完成,计算中使用的各项参数除非特别说明均采用缺省值.
2 结果与讨论
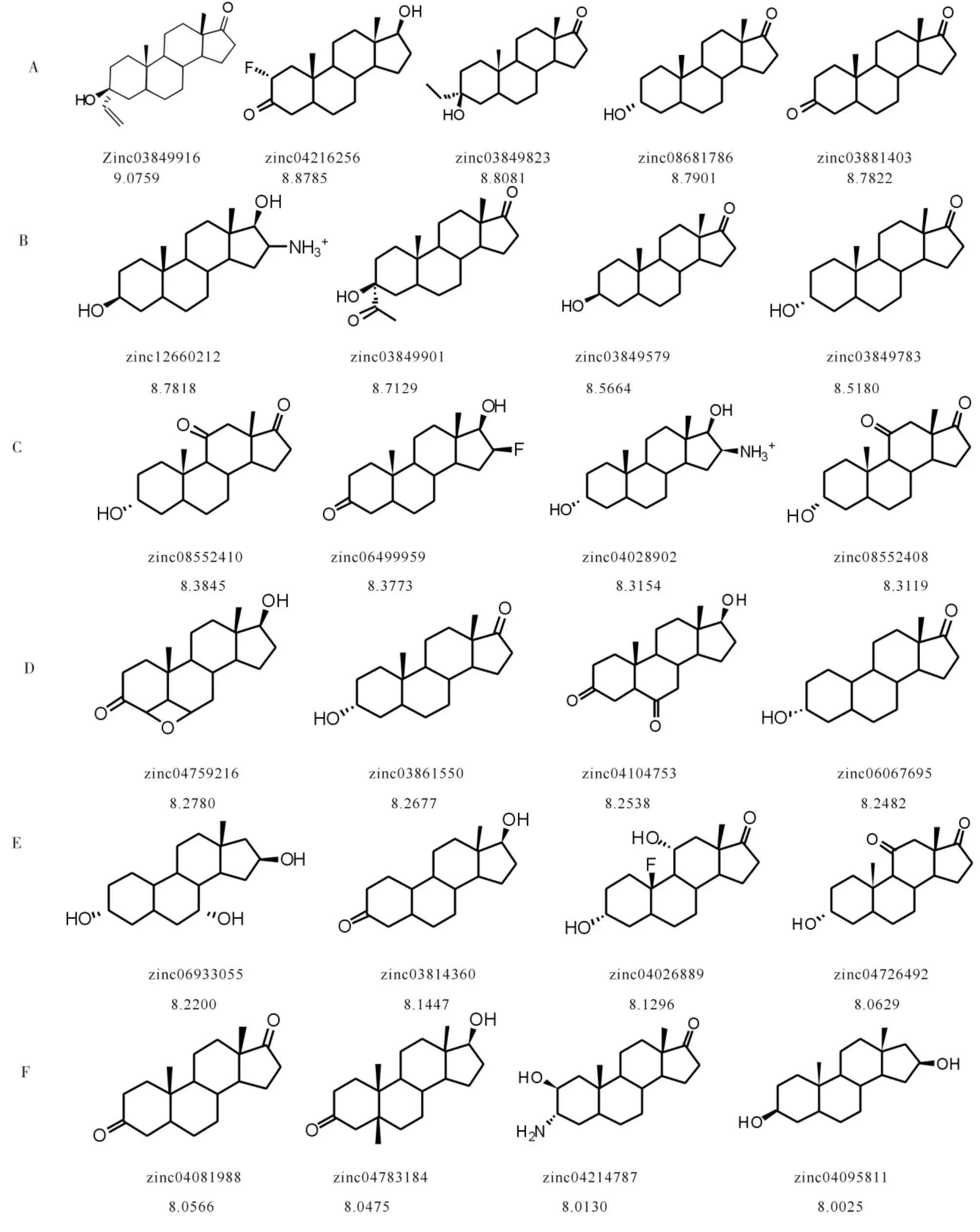
图4 中靶化合物及对接打分Fig.4 Target compounds and docking score
通过自带打分函数筛选出打分值较好的25个化合物作为中靶化合物结果见图4.由图4可见,所列化合物对接打分都在8.0以上,表明这些化合物与靶点蛋白均有较好的亲和性,其中,化合物zinc03849916表现最优,对接打分达到9.0以上.化合物zinc03849916的配体小分子与3EQM的 对接结果见图5.由图5可见,化合物3-C位羟基O与MET374的α-氨基H形成氢键,20-C位羰基O与THR310的羟基H形成氢键,即3-C位有氢键受体取代,20-C位有氢键供体取代.这是化合物zinc03849916不同于原有抑制剂的地方.在原抑制剂的结合构象(图1)中可见,原抑制剂以20-C位羰基O与 MET374的 α-氨基 H形成氢键,而zinc03849916在此发生了翻转,这也是该化合物得分较高的原因之一.
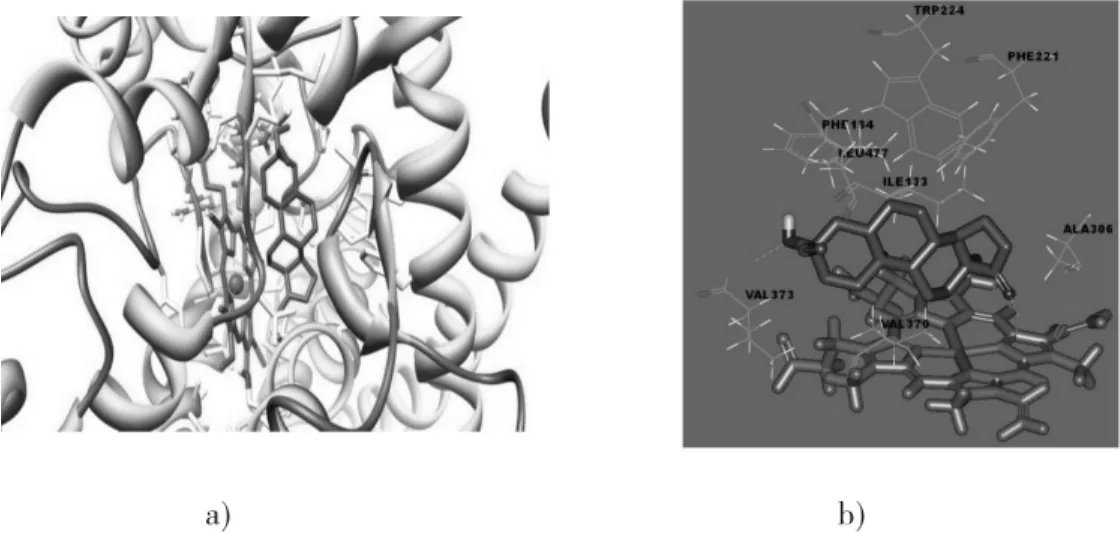
图5 化合物zinc03849916的配体小分子与3EQM的对接结果Fig.5 Docking results of compound zinc03849916 ligand molecules and 3EQM
其他24个化合物的对接结果中,结合构象与原抑制剂类似(图3).此外,打分排第2的化合物zinc04216256的配体小分子与3EQM的对接结果见图6.在由图6可见,以20-C位羰基O与MET374的α-氨基H形成氢键,在铁卟啉上方,有ILE133、PHE134、PHE221、ALA306、THR310、 VAL370、MET374及LEU477的疏水侧链围绕形成的疏水口袋将甾体化合物的四环疏水母核包裹起来,形成比较稳定的疏水性相互作用,这种现象在所有25个中靶化合物的对接结果中均可见.

图6 化合物zinc04216256的配体小分子与3EQM的对接结果Fig.6 Docking results of compound zinc04216256 ligand molecules and 3EQM
3 结语
在25个中靶化合物中,除去第1个打分最高的化合物,多以类似于原有抑制剂的方式与芳香酶活性位点结合,如以20-C位羰基O与MET374的α-氨基H形成氢键,在铁卟啉上方,ILE133、PHE134、PHE221、ALA306、THR310、VAL370、MET374 及LEU477的疏水侧链围绕形成的疏水口袋将甾体化合物的四环疏水母核包裹起来,形成比较稳定的疏水性相互作用.故认为在甾体母核20-C位上有氢键受体取代是这类化合物产生抑酶活性的关键,而在3-C位引入氢键供受体也有利于提高化合物抑酶活性.
[1]Thompson E A,Siiteri P K.Utilization of oxygen and reduced nicotinamide adenine dinucleotide phosphate by human placentalmicrosomes during aromatization of androstenedione[J].J Biol Chem,1974,249(17):5364-5372.
[2]Ericson J F.An evaluation of the OECD 308 water/sediment systems for investigating the biodegradation of pharmaceuticals[J].Environ Sci Technol,2007,41(16):5803-5811.
[3]Santen R J.Potential clinical role of new aromatase inhibitors[J].Steroids,1987,50(4/6):575-593.
[4]唐 斌,曾希志.乳腺癌内分泌治疗的生物学基础[J].实用肿瘤杂志,1997,12(4):191-193.
[5]Pérez Carrión R,Alberola Candel V,Calabresi F,et al.Comparison of the selective aromatase inhibitor formestane with tamoxifen as first-line hormonal therapy in postmenopausal women with advanced breast cancer[J].Ann Oncol,1994,5(Sup 7):S19-24.
[6]Goss P E,Powles T J,Dowsett M,et al.Treatment of advanced postmenopausal breast cancer with an aromatase inhibitor,4-hydroxyandrostenedione:phase II report[J].Cancer Res,1986,46(9):4823-4826.
[7]Miller W R.Aromatase inhibitors mechanism of action and role in the treatment of breast cancer[J].Sem in Oncol,2003,30(4):3-11.
[8]Miller W R,Dixon M J.Local endocrine effects of aromatase inhibitors with the breast[J].J Steroid Biochem Mol Biol,2001,79(1/5):93-102.
[9]Jorgensen W L.The many roles of computation in drug discovery[J].Science,2004,303(5665):1813-1818.
[10]Gross B A,Mindea S A,Pick A J,et al.Medical management of cushing disease[J].Neurosurg Focus,2007,23(3):E10.
[11]Pettersen E F,Goddard T D,Huang C C,et al.UCSF Chimera—a visualization system for exploratory research and analysis[J].J Comput Chem,2004,25(13):1605-1612.
[12]Polanski J,Gieleciak R.The comparative molecular surface analysis(CoMSA)with modified uniformative variable elimination-PLS (UVE-PLS) method:application to the steroids binding the aromatase enzyme[J].J Chem Inf Comput Sci,2003,43(2):656-666.
[13]Rarey M,Kramer B,Lengauer T,et al.A fast flexible docking method using an incrementalconstruction algorithm[J].J Mol Biol,1996,261(3):470-489.
