新型3(4)-噻吩甲氧基邻苯二甲腈的合成
2012-11-21张股林邵超英张学斌李洪启
张股林, 邵超英, 张学斌, 李洪启
(东华大学 化学化工与生物工程学院 生态纺织教育部重点实验室,上海 201620)
邻苯二甲腈又称酞腈,是一种重要的有机合成中间体,广泛用于酞菁颜料、高热阻聚酰胺纤维、二甲苯基二异氰酸酯塑料及脱硫催化剂等的合成[1,2]。酞菁作为一种功能材料,广泛应用于许多高新技术领域。为了满足不同应用领域的特殊要求,通常要对酞菁金属配合物的分子结构进行适当的调整和修饰,如在酞菁的周环上引入适当的功能性取代基,而这些取代基一般都在合成前驱体时引入。
本文以自制的3-硝基邻苯二甲腈(1)或4-硝基邻苯二甲腈(2)为原料,分别与噻吩甲醇反应合成了两个新化合物——3-(2-噻吩甲氧基)邻苯二甲腈(3)或4-(2-噻吩甲氧基)邻苯二甲腈(4, Scheme 1),其结构经UV,1H NMR,13C NMR, IR和MS表征。
1 实验部分
1.1 仪器与试剂
UOIRW型显微熔点仪(温度未校正);U-3310型紫外可见吸收光谱仪;Bruker Avance 400型核磁共振仪(CDCl3为溶剂,TMS为内标);Avatar 380型红外光谱仪;Agilent 6000 LC-MS型质谱仪。
1[3],2[3], 2-噻吩甲醇[4]按文献方法合成,其余所用试剂均为分析纯。
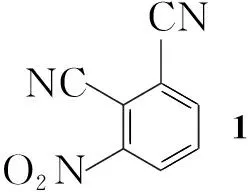
Scheme1
1.2 3和4的合成
在反应瓶中加入1 1.57 g(9.07 mmol),无水DMF 4 mL, 2-噻吩甲醇0.95 mL(7.56 mmol)及无水碳酸钾3.2 g,搅拌下于90 ℃反应6 h。倒入50 mL冰水中,待冰全部溶化后过滤,滤饼经硅胶柱层析(洗脱剂:石油醚/乙酸乙酯)纯化得3。
用2代替1,用类似方法合成4。
3: 白色固体,产率85%, m.p.128.0 ℃~129.7 ℃;1H NMRδ: 7.65~7.60(m, 1H, ArH), 7.39~7.32(m, 3H, ArH), 7.17(d,J=3.5 Hz, 1H, ArH), 7.03(dd,J=5.0 Hz, 3.6 Hz, 1H, ArH), 5.44(s, 2H, a-H);13C NMRδ: 162.73, 138.69, 136.63, 130.08, 129.48, 129.31, 127.90, 119.79, 119.50, 117.44, 115.06, 107.97, 68.81(Ca); ESI-MSm/z: 262.9{[M+Na]+}。
4: 白色固体,产率83%, m.p.102.8 ℃~104.2 ℃;1H NMRδ: 7.73(d,J=8.8 Hz, 1H, ArH), 7.40(dd,J=5.1 Hz, 1.2 Hz, 1H, ArH), 7.35(d,J=2.6 Hz, 1H, ArH), 7.28(d,J=2.6 Hz, 1H, ArH), 7.16(d,J=3.6 Hz, 1H, ArH), 7.05(dd,J=5.1 Hz, 3.5 Hz, 1H, ArH), 5.33(s, 2H, a-H);13C NMRδ: 161.19, 136.42, 135.26, 128.07, 127.41, 127.16, 120.01, 119.77, 117.54, 115.55, 115.17, 107.88, 65.84(Ca); ESI-MSm/z: 263.0{[M+Na]+}。
2 结果与讨论
2.1 表征
(1) UV
3和4的UV谱图见图1。从图1可以看出,3和4分别在310 nm~318 nm和295 nm~304 nm出现较强的吸收峰。3比4的吸收更强且发生了明显红移。这种现象可以认为是3在分子内不能共轭的两个芳香环相互间的位阻较4更大,使得苯环与噻吩环更趋向于共平面结构,芳香环内共轭电子流动性较强,因而使3的UV吸收产生红移。
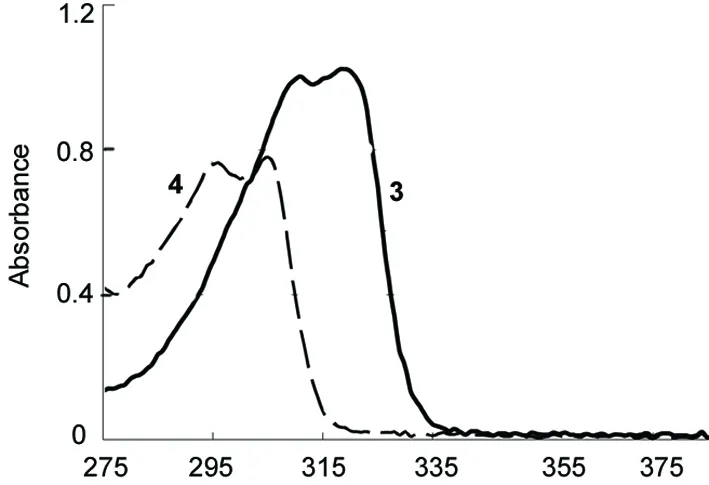
λ/nm图1 3和4的UV谱图Figure 1 UV spectra of 3 and 4
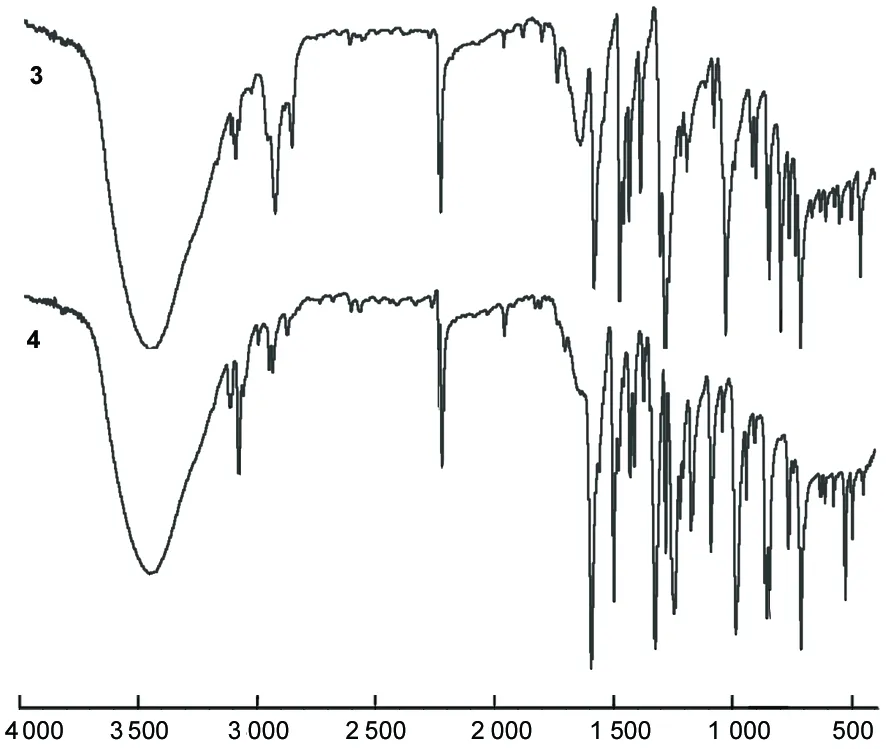
ν/cm-1图2 3和4的IR谱图Figure 2 IR spectra of 3 and 4
(2) IR
3和4的IR谱图见图2。从图2可见,2-噻吩甲醇的3 314 cm-1的吸收峰消失,而在2 226 cm-1(3)和2 218 cm-1(4)出现C≡N吸收峰,分别表明了-OH消失和-CN形成。 1 027 cm-1, 1 280 cm-1和1 089 cm-1, 1 280 cm-1吸收峰的出现分别证明了C-O-C键的形成;3和4分别在1 472 cm-1, 1 582 cm-1和1 499 cm-1, 1 593 cm-1处出现明显的芳香环特征吸收,在2 921 cm-1和2 950 cm-1处出现CH2O中的C-H伸缩振动峰。
(3) NMR
在3和4的1H NMR谱中,位于7.65~7.03和7.73~7.05的吸收分别来自于苯环和噻吩环上的6个氢。进一步的研究表明,3和4的亚甲基质子(a-H)的化学位移呈现较明显的区别。3的a-H化学位移为5.44,而4为5.33,两者的Δδ为0.11。一般认为3的噻吩环与氰基的距离较4近,使3的噻吩环与苯环更趋于远距离而更利于共平面。所以3的两个芳香环的环电流作用更明显而使得a-H更倾向于向低场移动。在13C NMR谱图中,3的Ca化学位移为68.81,相对于4的65.84向低场位移了2.97,进一步证实3的两个芳香环比4的两个芳香环更趋向于共平面的结论。
另外,MS显示了3和4的分子量均为240,与理论值吻合。
熔点测试结果显示,3由于分子的平面性更强,分子间排列更紧密,因而熔点(128.0 ℃~129.7 ℃)明显高于4(102.8 ℃~104.2 ℃)。
2 结论
合成了两个新型的酞菁前驱体3-硝基邻苯二甲腈(3)和4-硝基邻苯二甲腈(4)。首次从紫外吸收光谱角度预测3和4的构象,并用1H NMR,13C NMR和熔点测试证实了两者在构象上可能的变化,为进一步研究合成具有3-(2-噻吩甲氧基)取代的酞菁提供参考。3和4的合成与表征为完善酞菁材料的研究准备了一类新型的中间体。
[1] Rizaev R G K O, Mirataev M M O, Sheinin V E,etal. Method for preparing phthalonitriles[P].US 4 439 371,1984.
[2] Zhou X, Li J, Wang X,etal. Oxidative desulfurization of dibenzothiophene based on molecular oxygen and iron phthalocyanine[J].Fuel Processing Technology,2009,90(2):317-323.
[3] Bian Y, Wang R, Jiang J,etal. Synthesis,spectroscopic characterisation and structure of the first chiral heteroleptic bis(phthalocyaninato) rare earth complexes[J].Chemical Communications,2003:1194-1195.
[4] 韩相恩,屈琦超,吴玉彬,等. 新型噻吩席夫碱及其酯化产物合成与性能[J].应用化学,2009,26(8):935-938.
