双氧桥联四核二丁基锡(2,4,6-三甲基)苯甲酸酯配合物的合成、结构、量子化学及热稳定性研究
2012-11-09蒋伍玖邝代治庾江喜冯泳兰张复兴王剑秋
蒋伍玖 邝代治 庾江喜 冯泳兰 张复兴 王剑秋
双氧桥联四核二丁基锡(2,4,6-三甲基)苯甲酸酯配合物的合成、结构、量子化学及热稳定性研究
蒋伍玖 邝代治*庾江喜 冯泳兰 张复兴 王剑秋
(功能金属有机材料湖南省普通高等学校重点实验室,衡阳师范学院化学与材料科学系,衡阳 421008)
2,4,6-三甲基苯甲酸(TMBA)与(n-Bu)2SnO反应,合成氧桥联的四核二丁基锡(2,4,6-三甲基)苯甲酸酯配合物{[(n-Bu)2Sn(2,4,6-TMBA)]2O}2,经元素分析、1H NMR、13C NMR、IR和X-射线衍射表征分子结构,该配合物晶体属三斜晶系,空间群P1,晶体学参数:a=1.272 56(2)nm,b=1.322 73(2)nm,c=1.437 25(3)nm,α=111.197 0(10)°,β=99.691 0(10)°,γ=111.790 0(10)°,Z=1,V=1.962 35(6)nm3,Dc=1.368 g·cm-3,μ(Mo Kα)=1.308 mm-1,F(000)=828,R=0.040 9,wR=0.109 1。 配合物以 Sn2O2平面四元环中心对称,每个桥联氧原子还连接一个环外锡,形成双氧桥联四核二丁基锡结构。环上与环外Sn原子均呈现五配位畸变三角双锥构型。利用量子化学G03W软件,在Lanl2dz基组对配合物的稳定性、分子轨道能量、原子净电荷布居及前沿分子轨道组成进行了研究。并通过热重分析对配合物进行了热稳定性研究。
有机锡氧化合物;合成;晶体结构;量子化学;热稳定性
近年来,有机锡氧化合物因其丰富的结构及在催化等领域的重要应用,引起人们极大地兴趣[1-5]。运用有机锡氧化物与有机羧酸[6-10]、磷(膦)酸[11-14]或磺酸[15]反应是一种合成有机锡氧簇合物的重要方法,我们在前期的研究中报道了含Sn2O2结构的有机锡氧簇合物[7-9,16-19]。本文通过2,4,6-TMBA(2,4,6-TMBA=2,4,6-三甲基苯甲酸)与(n-Bu)2SnO反应,合成了Sn2O2骨架结构和氧桥联的有机锡氧簇合物{[n-Bu2Sn(TMBA)]2O}2,在Lanl2dz基组对该配合物的稳定性、分子轨道能量、原子净电荷布居及前沿分子轨道组成进行了研究。
1 实验部分
1.1 仪器和试剂
所有试剂均为化学纯。IR用日本岛津FTIR-8700 红外光谱仪(4 000~400 cm-1,KBr压片)测定;1H和13C NMR用Bruker AVANCE-400核磁共振仪(TMS内标,CDCl3溶剂)测定;元素分析用PE-2400(Ⅱ)元素分析仪测定;晶体结构用Bruker SMART APEXⅡCCD单晶衍射仪测定;热重曲线是在美国TA仪器公司的TGA Q50热分析仪上进行,实验条件为N2气氛,升温速率为10℃·min-1;熔点用北京泰克XT-4双目体视显微熔点测定仪测定(温度计未经校正)。
1.2 配合物的合成
取 0.249 g(1 mmol)(n-Bu)2SnO 和 0.146 g(1 mmol)2,4,6-TMBA于30 mL甲醇中,搅拌混合后,回流反应8 h,冷却,过滤,旋转蒸发除去部分溶剂,低温放置数天,析出无色晶体0.275 g,收率为68%,熔点:177~178 ℃。 元素分析(C72H116O10Sn4):实测值(计算值,%):C 53.43(53.50),H 7.17(7.23)。 IR(KBr,cm-1):2 959(s),2 926(s),2 864(s),1 622(s),1 537(vs),1 439(s),1 398(s),1 329(s),1 178(w),1 103(w),829(w),689(w),631(m),486(m)。1H NMR(CDCl3,400 MHz),δH:0.87 ~0.94 (m,8 ×3H,CH3),1.36 ~1.46 (m,8 ×4H,CH2CH2),1.71~1.86(m,8×2H,Sn-CH2),2.25~2.31(m,12×3H,Ar-CH3),6.80(s,4×2H,Ar-H)。13C NMR(CDCl3,100 MHz),δC:20.01,20.98(Ar-CH3),13.50(CH3),25.81~29.91(Sn-CH2-CH2-CH2),128.33~137.57(Ar),177.09,177.12(COO)。
1.3 晶体结构测定
选取一颗大小为 0.20 mm×0.20 mm×0.20 mm的晶体,在单晶衍射仪上,采用经石墨单色化的Mo Kα 射线(λ=0.071 073 nm),于 296(2)K,以 φ-ω扫描方式收集数据。 在 1.62°≤θ≤25.00°及 h=-15~15,k=-14~15,l=-16~17 范围内共收集 25 132 个衍射点,其中独立衍射点 6 886个(Rint=0.028 0),可观察衍射点5 431个(I>2σ(I))。全部数据经Lp因子和经验吸收校正。晶体结构由直接法解出,全部非氢原子坐标在差值Fourier合成中陆续确定,理论加氢法给出氢原子在晶胞中的位置坐标。对氢原子和非氢原子分别采用各向同性和各向异性热参数进行全矩阵最小二乘法修正,结构解析用Shelxtl[20]程序完成。
配合物晶体属三斜晶系,空间群P1,晶胞参数a=1.272 56(2)nm,b=1.322 73(2)nm,c=1.437 25(3)nm,α=111.197 0(10)°,β=99.691 0(10)°,γ=111.790 0(10)°,Z=1,V=1.962 35(6)nm3,Dc=1.368 g·cm-3,μ(Mo Kα)=1.308 mm-1,F(000)=828,R=0.040 9,wR=0.109 1,w=1/[σ2(Fo2)+(0.057 8P)2+2.604 7P],其中 P=(Fo2+2Fo2)/3,GOF=1.063,差值Fourier图最高和最低残余电子密度峰 Δρmax=1 125 e·nm-3,Δρmin=-649 e·nm-3。
CCDC:837504。
1.4 量子化学计算
根据晶体结构的各原子坐标位置,考虑到配合物的对称性,为节省计算机时,取其中一个结构单元用于 Gaussian03W[21]程序的 B3lyp/Lanl2dz基组上,在P4计算机上进行量子化学单点计算[7-8,22]。
2 结果与讨论
2.1 谱学表征
在红外图谱中,高频区羧基缔合峰消失,出现丁基的特征吸收 (2 959、2 926和 2 864 cm-1),486、631和687 cm-1出现新的吸收峰表明配合物中有Sn-C、Sn-O-Sn和Sn-O键的生成[23],配合物的羧基不对称伸缩振动峰出现在1 622和1 537 cm-1处,对称伸缩振动峰出现在1 398和1 328 cm-1处,其差值Δν(COO)分别为 294和139 cm-1,说明配合物中存在两种类型的羧基,一类是以单齿形式与锡原子配位,另一类是以双齿桥式与锡原子配位[24],该结果与X-射线单晶衍射结果一致。
在1H NMR谱中,其各组峰的积分面积之比与理论推测结构的各组质子数相对吻合;在13C NMR谱中,177.09和177.12 ppm处出现双峰, 可推测在配合物中存在两种类型的羧基碳原子,这与红外及X-射线单晶衍射结果相印证。
2.2 晶体结构
配合物的主要键长和键角列于表1,分子结构见图1。从分子结构图和键参数可以看出,该配合物存在 1 个以 Sn1、O5、Sn1i、O5i构成的 Sn2O2平面中心四元环,该环的中心就是分子的对称中心,四元环上的2个桥联氧原子均为三配位,除与2个环上锡(Sn1,Sn1i)链接外,还分别与 2个环外锡(Sn2,Sn2i)连接,形成了1个双氧桥联四核二丁基锡结构;其中 Sn1-O5:0.217 1(2)nm,Sn1-O5i:0.203 62(18)nm,Sn2-O5:0.202 8(2)nm,Sn1i-O5-Sn1:103.79(9)°,O5i-Sn1-O5:76.21(9)°,与文献[25-27]报道差异不大。 在晶体结构中Sn原子除与O原子相连外,还分别连接着2个正丁基,并有4个苯甲酸根离子与其中Sn原子配合。4个苯甲酸配体以两种不同的的方式与Sn原子配位,第一类配体通过羧基O3和O4原子以桥式双齿配位方式与1个环外Sn2原子和1个环上锡Sn1i原子相连,键长为 Sn2-O3:0.231 2(3)nm,Sn1i-O4:0.227 0(3)nm;另外一类苯甲酸配体通过羧基O1原子以单齿配位方式与环外Sn2原子连接,键长为 Sn2-O1:0.216 3(2)nm。

配合物四元环上Sn1原子周围,桥联氧原子O5和羧基氧原子O4i占据了三角双锥的2个轴向位置,2个丁基C原子C25、C21和另1个桥联氧原子O5i占据了三角双锥赤道平面上的3个位置,处于轴向位置的O5和O4i与处于赤道位置的C25、C21和O5i原子的键角数据分别为 O5i-Sn1-O4i:89.18(8)°,C21-Sn1-O4i:82.51(13)°,C25-Sn1-O4i:89.51(14)°,O5i-Sn1-O5:76.21(9)°,C25-Sn1-O5:102.02(13)°,C21-Sn1-O5:96.64(13)°,均明显偏离了 90°,赤道位置的3个原子C25、C21和O5i与中心Sn原子之间的夹角之和为 359.04°,与 360°偏离不大,说明处于赤道的3个原子与中心Sn原子有较好的共平面性,处于轴向位置的键角 O5-Sn1-O4i:163.66(9)°,偏差 180°线性很大。中心Sn原子与赤道位置的3个原子之间的键长相差 0.002 2~0.009 08 nm,与轴向位置的2个O原子的键长相差了0.009 9 nm。由它们的键角和键长可知,中心锡原子与配位原子构成五配位畸变三角双锥构型。环外Sn2原子与环上Sn1原子相类似,也是五配位的畸变三角双锥构型。

表1 配合物主要键长和键角Table 1 Selected of bond lengths(nm)and bond angles(°)of the complex
2.3 量子化学研究
2.3.1 前沿轨道能量
配合物计算涉及101原子,501个原子基函,1 281个初始高斯函数,161个α电子,161个β电子。结构单元的整体稳定性与体系总能量和前沿轨道的能量密切相关,算得该分子结构单元的总能量ET=-1 788.308 727 98 a.u.,EHOMO=-0.186 93 a.u.,ELUMO=-0.163 93 a.u.,可见总能量和占有轨道能量级均较低,最高占有轨道与最低未占有轨道的能量间隙只有0.023 a.u.,表明结构稳定。从氧化还原或电荷转移的角度分析,最高占有轨道为绝对值较大的负值,|EHOMO|越大说明从HOMO上电离电子越困难,因此,配合物较难失去电子,其基态较稳定。
2.3.2 分子轨道组成
为探索配合物的成键特征,对配合物分子轨道进行系统分析,用参与组合的各类原子的轨道系数的平方和来表示该部分在分子轨道中的贡献,并经归一化。把配合物原子分为七部分:(a)丁基碳原子C(Ⅱ);(b)芳环上甲基碳原子C(Ⅱ);(c)芳环碳原子C(Ⅱ);(d)羧基 C(Ⅱ);(e)H 原子;(f)O 原子;(g)Sn原子;前沿占有轨道和未占有轨道各取5个,计算结果见表2和图2。
在最高占有轨道组成中,氧原子对HOMO的贡献48.77%最大;其次是碳原子,对HOMO的贡献为43.62%(其中36.30%来自芳环上碳原子的贡献);其他原子对HOMO的贡献则相对较少,锡原子占HOMO成分6.13%;氢原子1.47%。
在最低未占有轨道组成中,各原子对LUMO的贡献发生较明显变化,锡原子对LUMO的贡献达48.73%;碳原子对LUMO的贡献38.89%(34.63%来自丁基碳原子贡献);氧原子贡献为10.02%;氢原子贡献为2.35%。
比较HOMO与LUMO的轨道成份,发现配合物从基态向激发态电子转移时,主要是碳原子向锡原子轨道转移,形成电荷转移配合物。
2.3.3 电荷布居
由Mulliken布居分析得到结构单元的原子电荷布居规律和特征:(1)中心Sn1、Sn2原子失去较多电子而荷较高正电 1.135 029、1.493 708;所有氢原子均荷正电,但苯环上的氢比其他碳上的氢荷更高正电;羧基碳原子和苯环上连有取代基的碳原子均荷正电;其它原子均荷负电。(2)与苯环相连的甲基碳原子荷较高负电;与Sn原子直接相连的原子荷负电相对集中,分别为 C11-0.821 89,C15-0.801 77,C16-0.809 78,C38-0.770 41,O3-0.313 31,O4-0.487 86,O5-0.829 51,O18-0.570 32。 (3)锡原子通过Sn-C键和Sn-O键将电荷转移到C和O上,这些键极性较强,因此,Sn-C和Sn-O键的稳定性有限,较易发生分子碎裂。(4)苯环的电荷布居虽差异较大,但仍遵守电荷分布的基本规律。

表2 配合物的分子轨道组成(B3lyp/Lanl2dz)Table 2 Calculated some frontier molecular orbitals composition(%)of the complex at Lanl2dz level

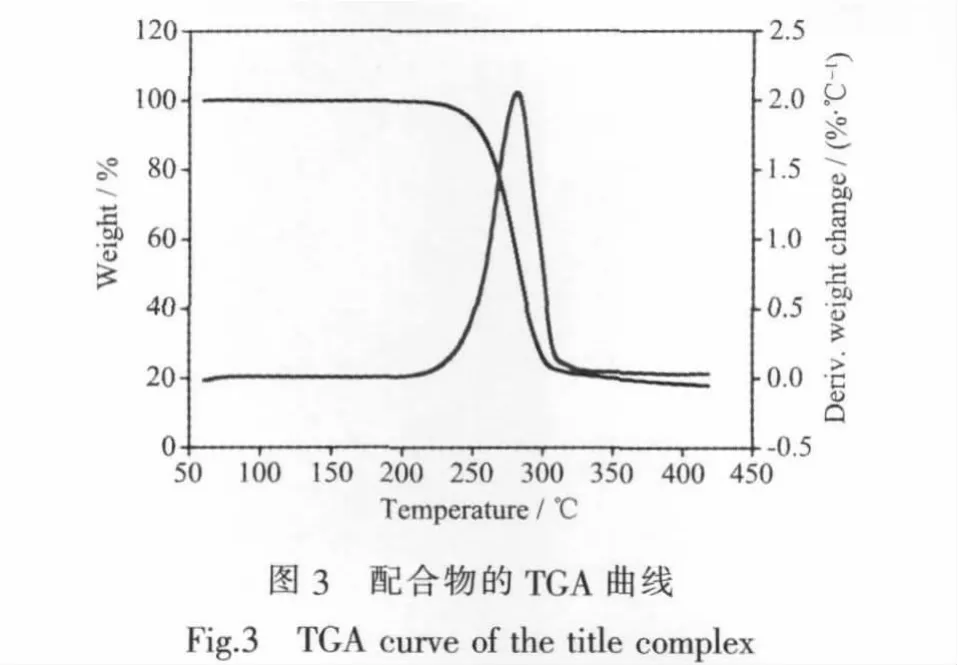
2.4 热稳定性分析
配合物的TGA如图3所示。随温度的升高,配合物在216~328℃区间经过热失重,对应于配合物分子失去8个丁基和4个2,4,6-TMBA,最后稳定在约 18.61%,残余物为 SnO2(理论值 18.65%)。 上述热分析结果表明该配合物结构在216℃之前是可以稳定存在的。
[1]Chandrasekhar V,Nagendran S,Azhakar R,et al.Journal of the American Chemical Society,2005,127(8):2410-2411
[2]Chandrasekhar V,Thilagar P,Bickley J F,et al.Journal of the American Chemical Society,2005,127(33):11556-11557
[3]Ma C L,Han Y W,Zhang R F.Analytical Sciences,2007,23:x89-x90
[4]Chandrasekhar V,Suriya Narayanan R,Thilagar P.Organometallics,2009,28(20):5883-5888
[5]Chandrasekhar V,Gopal K,Thilagar P.Accounts of Chemical Research,2007,40(6):420-434
[6]Chandrasekhar V,Gopal K,Singh P,et al.Organometallics,2009,28(15):4593-4601
[7]KUANG Dai-Zhi(邝代治),FENG Yong-Lan(冯泳兰),ZHANG Fu-Xing(张复兴),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2010,26(12):2160-2164
[8]ZHANGFu-Xing(张复兴),WANGJian-Qiu(王剑秋),KUANG Dai-Zhi(邝代治),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2009,25(2):213-217
[9]DENGYi-Fang(邓弈芳),CHENMan-Sheng(陈满生),ZHANG Chun-Hua(张春华),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2009,25(12):2229-2232
[10]Nagendran S,Bansal S,Cordes A W,et al.Organometallics,2002,21(15):3297-3300
[11]Chandrasekhar V,Sasikumar P,Thilagar P.Organometallics,2007,26(18):4386-4388
[12]Chandrasekhar V,Baskar V,Gopal K,et al.Organometallics,2005,24(21):4926-4932
[13]Chandrasekhar V,Baskar V,Steiner A,et al.Organometallics,2004,23(6):1390-1395
[14]Chandrasekhar V,Baskar V,Steiner A,et al.Organometallics,2002,21(21):4528-4532
[15]Chandrasekhar V,Baskar V,Boomishankar R,et al.Organometallics,2003,22(18):3710-3716
[16]ZHANGFu-Xing(张复兴),WANGJian-Qiu(王剑秋),KUANG Dai-Zhi(邝代治),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2009,25(10):1812-1817
[17]WANGJian-Qiu(王剑秋),ZHANGFu-Xing(张复兴),KUANG Dai-Zhi(邝代治),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2007,23(5):871-874
[18]ZHANG Chun-Hua(张春华),CHEN Man-Sheng(陈满生),KUANG Dai-Zhi(邝代治),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2005,21(9):1386-1388
[19]CHEN Man-Sheng(陈满生),KUANG Dai-Zhi(邝代治),ZHANG Chun-Hua(张春华),et al.Chinese J.Struct.Chem.(Jiegou Huaxue),2005,24(11):1249-1253
[20]Sheldrick G M.SHELXTL,Version5.03.Madison,WI,USA:Siemens Analytical X-ray Division,1994.
[21]AEleen F,Michael J F,Gary W T.Gaussian03User′s Reference,Second Edition.Wallingford,CT,USA:Gaussian,Inc,2005.
[22]FENG Yong-Lan(冯泳兰),KUANG Dai-Zhi(邝代治),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2011,27(9):1793-1797
[23]Vatsa C,Jain V K,Das T K,et al.J.Organomet.Chem.,1990,396:9-18
[24]WENG Shi-Fu(瓮诗甫).Fourier Transform Infrared Spectroscopy.2th Ed.Beijing:Chemical Industry Press,2010:305-306
[25]YIN Han-Dong(尹汉东),XUE Sheng-Cai(薛绳才),WANG Qi-Bao(王其宝).Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2004,20(4):421-425
[26]YIN Han-Dong(尹汉东),XUE Sheng-Cai(薛绳才),WANG Qi-Bao(王其宝).Chem.J.Chinese Universities(Gaodeng Xuexiao Huaxue Xuebao),2005,26(4):631-633
[27]MEI Ze-Min(梅泽民),SUN Kai(孙凯),ZHU Chao-Guang(朱超光),et al.Journal of Northeast Normal University:Natural Science Edition(Dongbei Shifan Daxue Xuebao),2010,42(3):94-97
Synthesis,Crystal Structure,Quantum Chemistry and Thermal Stability of the Bis-Oxygen-Bridged Tetranuclear Dibutyltin(2,4,6-trimethyl)benzoate
JIANG Wu-Jiu KUANG Dai-Zhi*YU Jiang-XiFENG Yong-Lan ZHANG Fu-Xing WANG Jian-Qiu
(Key Laboratory of Functional Organometallic Materials of Hengyang Normal University,College of Hunan Province;Department of Chemistry and Material Science,Hengyang Normal University,Hengyang,Hunan 421008,China)
An organooxotin complex of{[n-Bu2Sn(2,4,6-TMBA)]2O}2has been synthesized by the reaction of n-Bu2SnO with 2,4,6-TMBA and characterized by IR,1H NMR,13C NMR and elemental analysis.The crystal structure has been determined by X-ray diffraction.It crystallizes in the monoclinic,space group P1,with a=1.272 56(2)nm,b=1.322 73(2)nm,c=1.437 25(3)nm,α=111.197 0(10)°,β=99.691 0(10)°,γ=111.790 0(10)°,Z=1,V=1.962 35(6)nm3,Dc=1.368 Mg·m-3,μ(Mo Kα)=1.308 mm-1,F(000)=828,R=0.037 2,wR=0.096 1.This complex belongs to centrosymmetric structure mode with a four-membered central endocyclic Sn2O2unit in which the bridging oxygen atoms are tri-coordinated.Each bridging oxygen atom also connects with an exocyclic tin atom.The endocyclic and exocyclic tin atoms all are five-coordinated in a distorted trigonal bipyramidal geometry.The stabilities,some frontier molecular orbital energies,the populations of the atomic net charges and composition characteristics of some frontier molecular orbital of the complex have been investigated.The complex was studies by TGA analysis.CCDC:837504.
organooxotin compound;synthesis;crystal structure;quantum chemistry;thermal stability
O614.43+2
A
1001-4861(2012)11-2363-06
2012-02-12。收修改稿日期:2012-06-26。
湖南省自然科学基金(No.11JJ3021),湖南省教育厅创新平台项目(No.10K010),湖南省科技计划项目(No.2010JT4041),功能金属有机材料
湖南省普通高校重点实验室开放基金(No.10K02),衡阳市科技计划项目(No.2011KG56),衡阳师范学院青年项目(No.11A28)资助项目。
*通讯联系人。 E-mail:hnkdz@yahoo.com.cn;会员登记号:S06N8374M1012。
