四溴代对苯二甲酸构筑的铜(Ⅱ)、钴(Ⅱ)配合物的合成及晶体结构
2012-11-09高玲玲吕旭燕刘建锋胡拖平
刘 艳 高玲玲 吕旭燕 刘建锋 胡拖平
(中北大学理学院,太原 030051)
四溴代对苯二甲酸构筑的铜(Ⅱ)、钴(Ⅱ)配合物的合成及晶体结构
刘 艳 高玲玲 吕旭燕 刘建锋 胡拖平*
(中北大学理学院,太原 030051)
以四溴代对苯二甲酸(H2TBTA)及邻菲咯啉(phen)为配体,在相同反应条件下,得到2个金属-有机配合物{[Cu(phen)2(TBTA)]·CH3OH·H2O}n(1)和[Co(HTBTA)2(phen)2](2),并用元素分析、单晶X射线衍射、红外及热重分析对其进行了表征。配合物1和2显示出不同的结构,前者为一维链状结构而后者为单核零维结构。配合物1和2通过氢键作用及π-π相互作用显示出三维结构。
四溴代对苯二甲酸;氢键;π-π相互作用;金属-有机配合物
0 引 言
近年来,金属-有机配合物因其在光、磁、吸附、分子识别、离子交换、催化等领域中具有潜在的应用价值而备受关注,已成为配位化学的研究热点之一[1-7]。目前,由于芳香二羧酸类配体具有多样的配位模式,及其在结构上表现出的刚性和稳定性,已经被广泛应用于合成配位聚合物[8-11]。然而,对于苯环上取代基位阻较大的芳香二羧酸配体用于合成配合物的研究较少[12-14]。如四溴代对苯二甲酸(H2TBTA),配体具有以下特征:一方面,处于对位的2个羧基具有丰富的配位模式(如图1所示),可以构筑多种具有不同拓扑结构的配合物;另一方面,苯环上的溴原子取代基具有较大空间位阻,影响所构筑的配合物的空间取向[15-17]。此外,在合成时加入辅助配体对配合物的结构有较大的影响,如邻菲咯啉(phen)具有鳌合配位模式可以阻止结构框架进一步扩大,而其具有的平面多芳环容易形成π-π相互作用等超分子相互作用力[18-21]。因此,本研究用四溴代对苯二甲酸(H2TBTA)和邻菲咯啉(phen)与过渡金属盐构筑了2个金属-有机配合物:{[Cu(phen)2(TBTA)]·CH3OH·H2O}n(1)和[Co(HTBTA)2(phen)2](2),并对其晶体结构及热稳定性进行了表征。
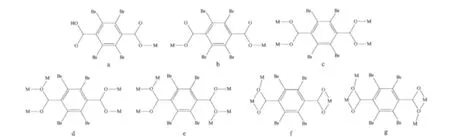
图1 TBTA2-的配位模式Fig.1 Schematic presentation of the coordination modes in TBTA2-
1 实验部分
1.1 实验仪器及试剂
所用的药品及试剂均为分析纯,通过商业渠道购买,未经纯化处理直接应用。实验中使用的水全部为蒸馏水。元素分析:Vario EL元素分析仪;晶体结构:Bruker Smart Apex II CCD面探测X射线单晶衍射仪;热重分析:ZCT-A型热重分析仪(在空气氛围下,升温速率为10℃·min-1)。
1.2 配合物的合成
配合物1的合成:准确称取H2TBTA(10 mg,0.02 mmol)和 phen(10 mg,0.06 mmol)用 5 mL 蒸馏水溶解并加入试管底部,然后将Cu(NO3)2·3H2O(20 mg,0.08 mmol)的甲醇(5 mL)溶液小心滴加到试管中。用保鲜膜密封试管口,静置。1周后得到适合X射线单晶衍射分析的蓝色块状晶体,产率为56%。基于C33H22Br4CuN4O6的元素分析结果:理论值(%):C 41.560,H 2.325,N 5.875; 实验值 (%):C 41.19,H 1.94,N 5.41。 主要的红外吸收峰(cm-1):3 432(vs),1 605(vs),1 518(s),1 387(s),1 300(s),1 016(w),848(w),725(m),569(w)。
配合物2的合成:除金属盐用Co(NO3)2·6H2O(20 mg,0.07 mmol)代替 Cu(NO3)2·3H2O 外,其他实验条件与合成配合物1相同,1周后得到红色块状单晶,产率:45%。基于C40H18Br8CoN4O8的元素分析结果:理论值(%):C 34.795,H 1.314,N 4.058;实验值(%):C 34.42,H 1.704,N 4.31。主要的红外吸收峰(cm-1):3 440(vs),1 780(s),1 613(vs),1 510(s),1 380(s),1 300(s),1 075(m),856(w),725(m),565(w)。
1.3 配合物1和2晶体结构的测定
配合物1和2的单晶结构是在室温下,用石墨单色化的 Mo Kα(λ=0.071 073 nm)作为辐射光源,在Bruker Smart Apex II CCD衍射仪上进行测定。结构解析和精修分别用SHELXTL程序的SHELXS和SHELXL完成[22-23]。晶体结构由直接法解出,非氢原子均作各向异性精修。所有氢原子通过理论加氢得到。配合物1和2的相关晶体学数据见表1,部分键长和键角列于表2。
CCDC:854134,1;854133,2。

表1 配合物1和2的主要晶体学参数Table 1 Crystallographic data and structural refinement summary for complexes 1 and 2
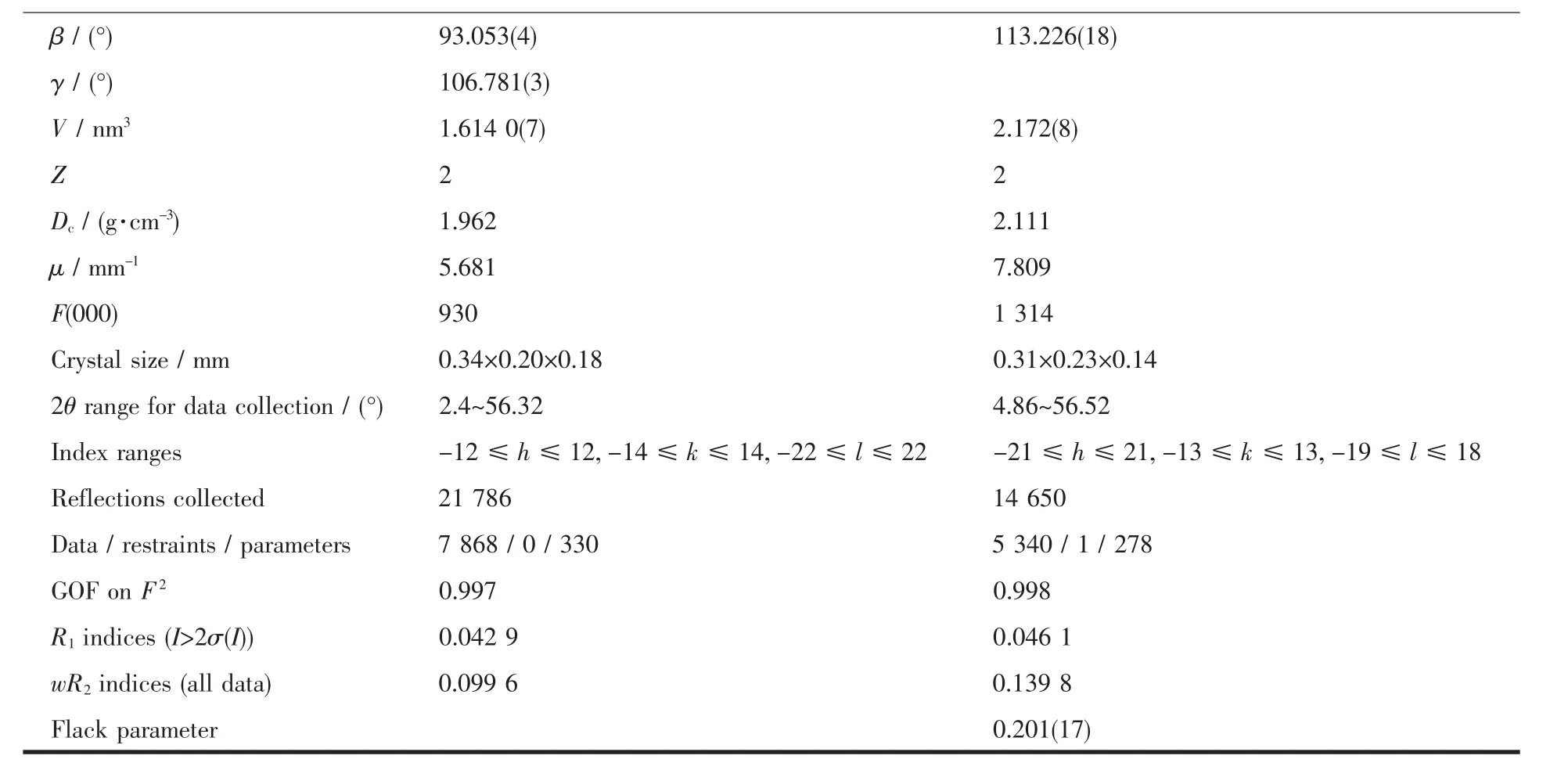
续表1

表2 配合物1和2的主要键长键角Table 2 Selected bond lengths(nm)and bond angles(°)for complexes 1 and 2
2 结果与讨论
2.1 配合物1和2的结构分析
2.1.1 {[Cu(phen)2(TBTA)]·CH3OH·H2O}n(1)
X射线单晶衍射结果表明,配合物1属于三斜晶系P1空间群,具有无限聚合链结构。如图2所示,1的不对称单元包含1个Cu(Ⅱ)离子、2个phen分子、2个晶体学独立且中心对称的TBTA2-离子、1个甲醇分子和1个水分子。结构中的2个TBTA2-离子均采取反式(trans)单齿桥联配位模式连接相邻的Cu(Ⅱ)金属离子,并拓展为一维波浪型配位聚合链(图3),其中Cu…Cu之间的间隔分别为1.018 9和1.125 5 nm。由于Br原子有较大的空间位阻,使得TBTA2-离子中的羧基所在的平面几乎垂直于苯环平面(两者之间的二面角为94.487°)。
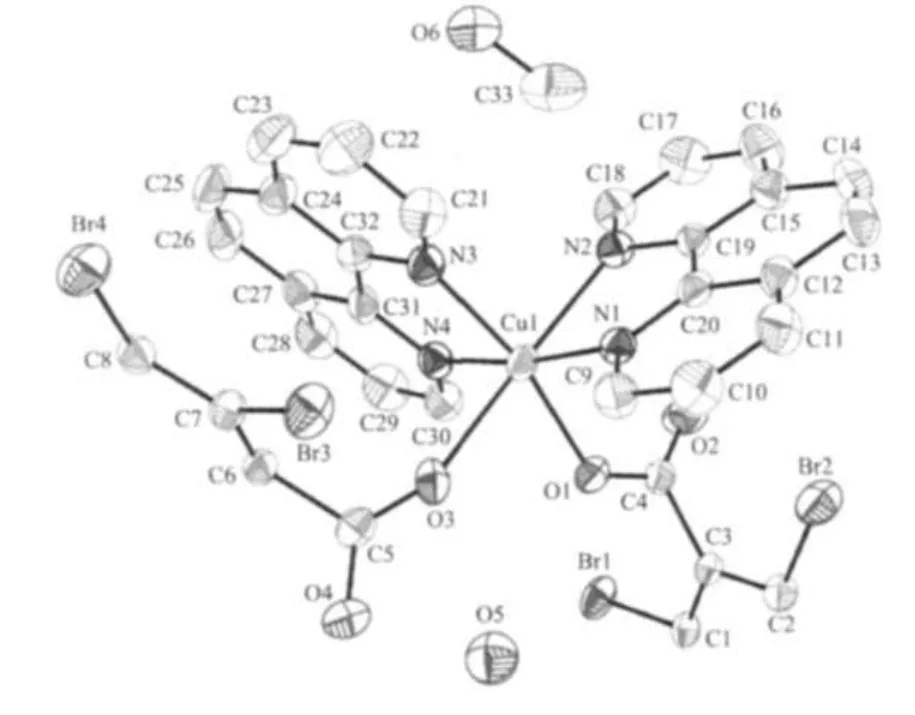
图2 配合物1的晶体不对称单元图Fig.2 Asymmetric unit of 1
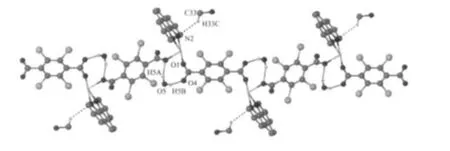
图3 配合物1的一维链结构Fig.3 1D chain motif of 1
此外,TBTA2-中未配位的2个O原子与游离的溶剂水分子中的2个H原子之间形成氢键作用(O(5)-H(5A)…O(1),O(5)-H(5B)…O(4)),溶剂甲醇分子中与C原子连接的H原子和phen中的N原子也形成了氢键(C(33)-H(33C)…N(2))。这些氢键作用(表3)将溶剂分子固定在一维聚合链的两侧,增强了链内分子间的相互作用。
在这一维链中,2个phen分子中的苯环平面与TBTA2-配体的苯环平面平行。Cg(1)是六元环 N(3)-C(21)-C(22)-C(23)-C(24)-C(32)的质心,Cg(2)是六元环C(6)-C(7)-C(8)-C(6)ii-C(7)ii-C(8)ii(ii1-x,1-y,-1-z)的质心,Cg(3)是六元环C(24)-C(25)-C(26)-C(27)- C(31)-C(32)的质心,这3个六元环之间存在的π-π相互作用(表4)是一维链稳定存在的主要原因(如图4)。进一步分析这些聚合链的排列方式发现最近链与链之间的Cu…Cu距离为1.075 9 nm,因此,这些链之间没有弱相互作用。

图4 配合物1中的π-π相互作用Fig.4 π-π interactions of 1
2.1.2 [Co(HTBTA)2(phen)2](2)
配合物2属于单斜晶系C2空间群,为单核零维结构。每个结构单元中心的Co(Ⅱ)离子被2个HTBTA-离子的2个氧原子和2个phen分子的4个氮原子所包围(键长键角数据见表2),呈现六配位的变形八面体构型。
与1类似,HTBTA-离子中的羧基也与溴取代的苯环相互垂直,其二面角为93.762°和84.146°。phen分子所在平面与HTBTA-离子中的苯环平面平行。Cg(4)是六元环N(1)-C(1)-C(2)-C(3)-C(4)-C(12)的质心,Cg(5)是六元环C(4)-C(5)-C(6)-C(7)-C(11)-C(12)的质心,Cg(6)是六元环 C(14)-C(15)-C(16)-C(17)-C(19)-C(20)的质心。单核分子的这3个六元环之间存在较强的π-π相互作用(表4,图5)。
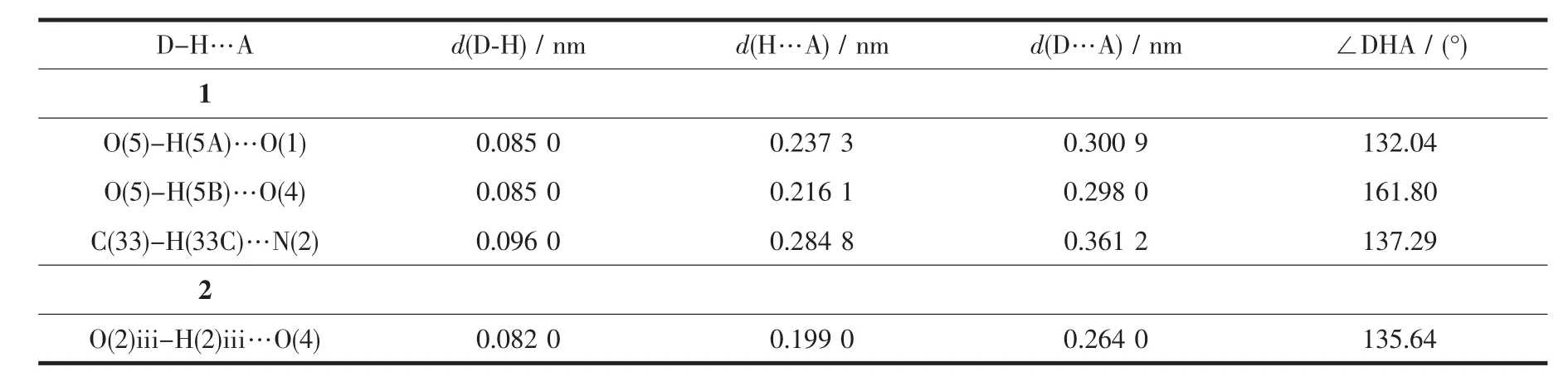
表3 配合物1和2中氢键的键长键角Table 3 Hydrogen bond lengths and bond angles for complexes 1 and 2
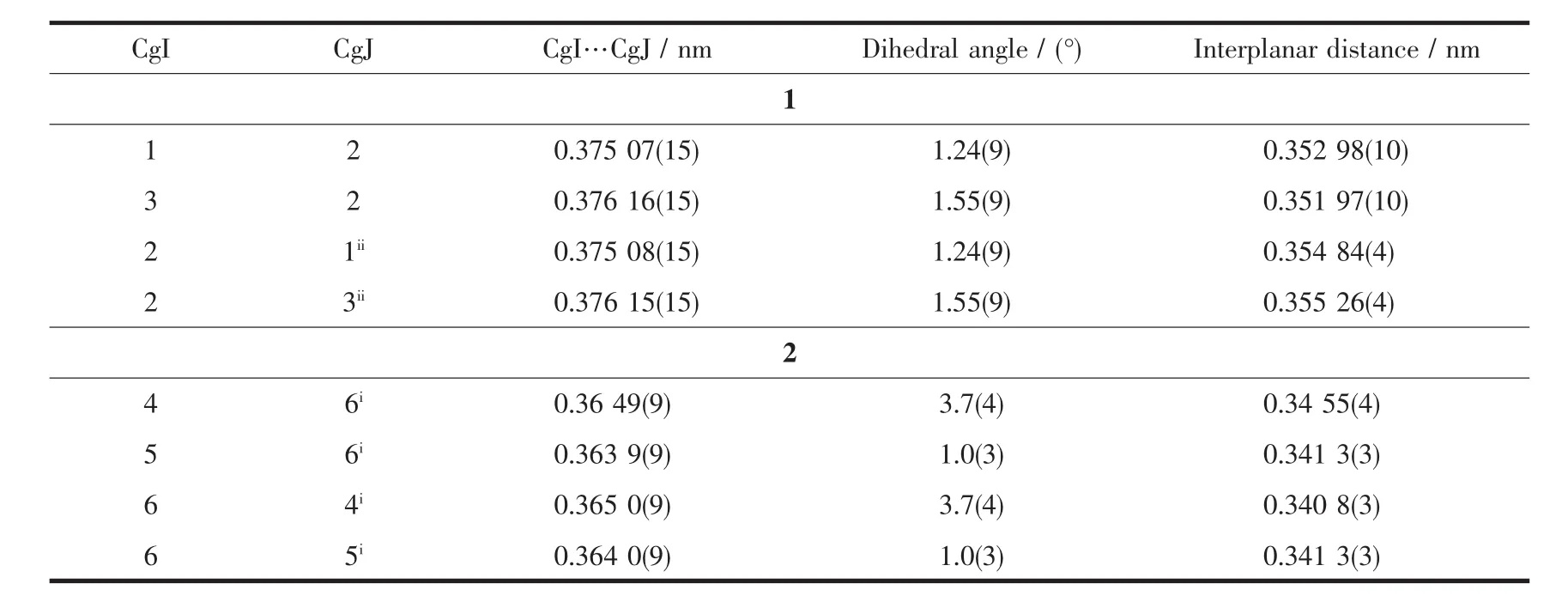
表4 配合物1和2中的π-π相互作用Table 4 π-π interactions of complexes 1 and 2
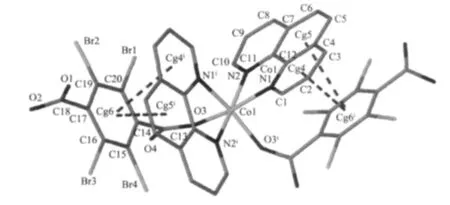
图5 配合物2的晶体结构及π-π相互作用Fig.5 Crystal structure and π-π interactions of 2
与1不同的是,2中HTBTA-离子的2个羧基中的1个没有去质子化,故其结构不能拓展为一维 链而表现为单核零维结构。从图6中可以看出,未参与配位的氧原子与相邻的HTBTA-离子中羧基上的质子之间存在强的氢键作用(O(2)iii-H(2)iii…O(4),iii-1/2-x,-1/2+y,-1-z),把4个相邻的单核结构连接起来形成了二维平面结构。若将氢键作用看做配位连接线,锌离子作为节点,那么这一复杂的结构就可以简化为(4,4)连接网(图7)。
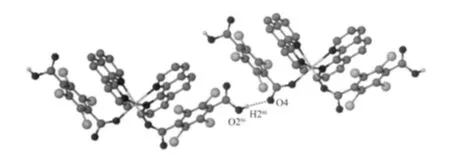
图6 配合物2中的分子间的氢键作用Fig.6 Intermolecular hydrogen bonding interactions of 2
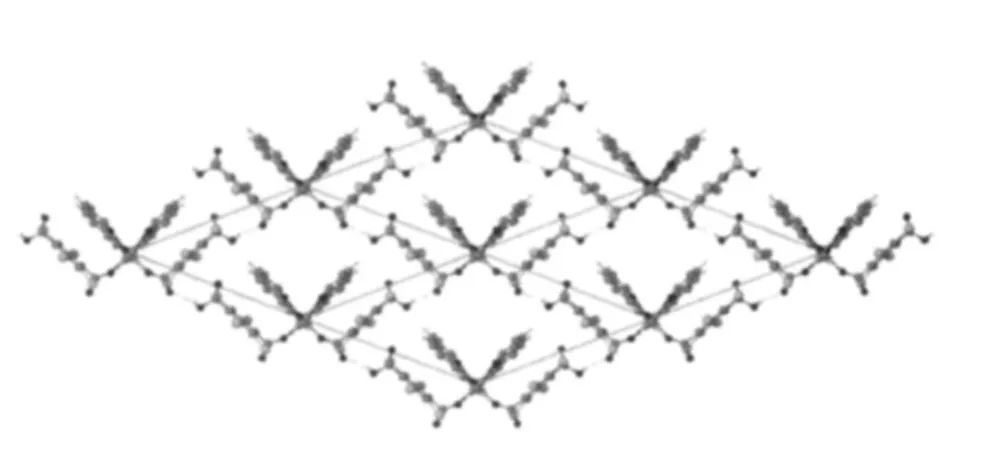
图7 配合物2中的二维(4,4)网状结构Fig.7 2D supramolecular architecture with(4,4)net
2.2 配合物1和2的红外光谱分析
从配合物1和2的红外谱图中可以看出,在3 432和 1 518 cm-1(配合物1)及3 440和1 510 cm-1(配合物2)处出现的特征峰可以分别归属于晶体游离水分子中O-H键和phen分子中-N=C-键的伸缩振动。配合物1中1 605和1 387 cm-1处出现的2个峰分别归属于羧基的反对称和对称伸缩振动。2个峰之间的差值为218 cm-1,表明配合物1中羧酸分子为单齿配位,这与结构分析相吻合。而在配合物2中,不但在1 613和1 380 cm-1处出现羧基的2个特征吸收峰,而且在1 780 cm-1处也有特征吸收,表明配合物2中的羧基也是单齿配位且没有完全去质子化,这也与结构分析结果相吻合。
2.3 配合物1和2的热重分析
配位聚合物1和2在室温下稳定存在且不溶于水与甲醇溶剂,二者的热稳定性用热重分析技术(TGA)进行测试,结果见图8和图9。
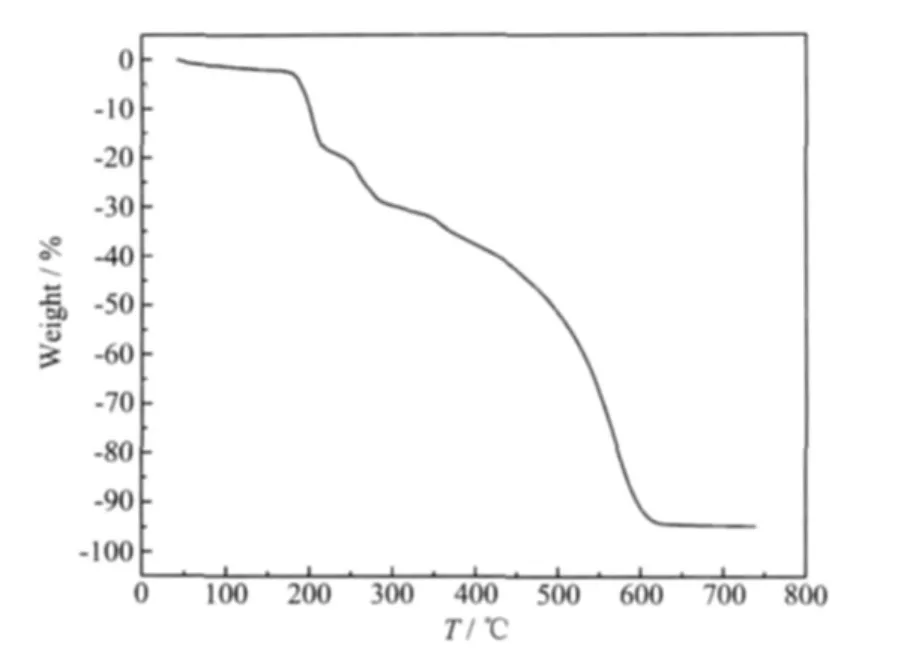
图8 配合物1中的热重曲线图Fig.8 Thermogravimetric analysis for complex 1

图9 配合物2中的热重曲线图Fig.9 Thermogravimetric analysis for complex 2
配合物1的热重分析见图8,在190℃时2个客体溶剂分子失去(实际值:5.34%,理论值:5.25%)。温度升高到447℃时重量损失为42.72%,对应于失去配位的phen分子(理论值:43%)。继续升温时配合物开始分解,直到624℃失重结束。配合物2的热重分析见图9,在200℃前几乎没有失重,直到加热到429℃时失重29.5%,对应于失去2个配位的phen分子(计算值:26.07%)。温度进一步升高时,配合物2开始分解。
[1]Liu Y L,Eubank J F,Cairns A J,et al.Angew.Chem.Int.Ed.,2007,46(18):3278-3283
[2]Cahill C L,Daniel D T,Frisch M.CrystEngComm,2007,9:15-26
[3]Maspoch D,Ruiz-Molina D,Veciana J.Chem.Soc.Rev.,2007,36:770-818
[4]Férey G.Chem.Soc.Rev.,2008,37:191-214
[5]Zhang J P,Chen X M.J.Am.Chem.Soc.,2008,130:6010-6017
[6]Lin X,Jia J H,Hubberstey P,et al.CrystEngComm,2007,9:438-448
[7]Kitagawa S,Matsuda R.Coord.Chem.Rev.,2007,251:2490-2509
[8]Li H,Eddaoudi M,O′Keeffe M,et al.Nature,1999,402:276-279
[9]Vodak D T,Braun M E,Kim J,et al.Chem.Commun.,2001,24:2534-2535
[10]Eddaoudi M,Kim J,Rosi N,et al.Science,2002,295:469-472
[11]Spencer E C,Howard J A K,McIntyre G J,et al.Chem.Commun.,2006,3:278-280
[12]JIN Mei-Fang(靳梅芳).Thesis for the Master of Shandong University(山东大学硕士论文).2010.
[13]Li Cheng-Peng(李程鹏).Thesis for the Doctorate of Tianjin University(天津大学博士论文).2009.
[14]JIN Mei-Fang(靳梅芳),DAI Fang-Na(戴昉娜),SUN Dao-Feng(孙道峰).Chinese J.Struct.Chem(Jiegou Huaxue),2010,29:1834-1840
[15]Li C P,Tian Y L,Guo Y M.Inorg.Chem.Commun.,2008,11:1405-1408
[16]Li C P,Tian Y L,Guo Y M.Polyhedron,2009,28:505-510
[17]Li C P,Yu Q,Zhang Z H,et al.CrystEngComm,2010,12:834-844
[18]LIU Jian-Feng(刘建风),CHEN Ji-Fei(陈吉妃),ZHAO Guo-Liang(赵国良).Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2011,27(1):100-106
[19]TAI Xi-Shi(台夕市),DU Lian-Cai(杜连彩),ZHAO Zeng-Bing(赵增兵).Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2011,27(3):575-579
[20]LI Xiu-Mei(李秀梅),WANG Qing-Wei(王庆伟),LIU Bo(刘博),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2011,27(6):1207-1211
[21]LI Chang-Hong(李昶红),LI Wei(李薇),TAN Xiong-Wen(谭雄文),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2011,27(6):1129-1132
[22]Sheldrick G M.SHELXS97,Program for the Solution of Crystal Structure,University of Gottingen,Germany,1997.
[23]Sheldrick G M.SHELXL97,Program for the Refinement of Crystal Structure,University of Gottingen,Germany,1997.
Syntheses and Crystal Structures of Two Complexes(Cu(Ⅱ) and Co(Ⅱ))Based on 2,3,5,6-Tetrabromoterephthalic Acid
LIU Yan GAO Ling-Ling LV Xu-Yan LIU Jian-Feng HU Tuo-Ping*
(Department of Chemistry,North University of China,Taiyuan 030051,China)
Two metal-organic complexes,namely{[Cu(phen)2(TBTA)]·CH3OH·H2O}n(1)and[Co(HTBTA)2(phen)2](2)have been constructed from 2,3,5,6-tetrabromoterephthalic acid (H2TBTA)and 1,10-phenanthroline(phen)ligands in the same method,then characterized by elemental analysis,single-crystal X-ray diffraction,IR and thermal gravimetric analysis(TGA)techniques.Their crystal structures show different structure motifs:1D chain(1)and mononuclear molecule (2)metal-organic networks,respectively.The 3D structures of the 1 and 2 are constructed by hydrogen bonding and π-π interactions.CCDC:854134,1;854133,2.
2,3,5,6-tetrabromoterephthalic acid;H-bonding;π-π interactions;metal-organic complexes
O614.81+2;O614.121
A
1001-4861(2012)08-1623-06
2011-11-28。收修改稿日期:2012-05-10。
山西省国际科技合作课题(No.2011081022)资助项目。*
。 E-mail:hutuopingsx@yahoo.com.cn
