Ag3PO4的可见光光催化性能及机理分析
2012-11-09王韵芳樊彩梅
王韵芳 樊彩梅
(太原理工大学化学化工学院,太原 030024)
Ag3PO4的可见光光催化性能及机理分析
王韵芳 樊彩梅*
(太原理工大学化学化工学院,太原 030024)
采用沉淀置换法制备了可见光光催化剂Ag3PO4,利用XRD、UV-Vis及XPS等对其进行了结构特性分析,以水中微污染有机物的降解评价了Ag3PO4的光催化活性,并通过活性物种及能带结构的分析对催化剂的光催化机理进行了推测。结果表明,Ag3PO4的带隙能约为1.9 eV、催化剂表面存在的Ag+可捕获光生e-、催化剂的价带电位较低,这有利于Ag3PO4在可见光照射下产生的e--h+的分离及活性物种·OH的形成。经60 min可见光光催化反应,15 mg·L-1的甲基橙和腐殖酸的降解率分别达97%和82%,比同等条件下TiO2-P25的降解率还高40%和25%,光催化剂Ag3PO4的用量为0.6 g·L-1。
Ag3PO4;沉淀置换法;可见光;光催化
0 引 言
太阳能的利用及环境污染的控制是人类面临和亟待解决的重大课题。自Fujishima和Honda[1]发现采用TiO2作为光阳极进行紫外光照射可分解H2O为H2和O2以来,纳米TiO2半导体光催化氧化技术在环境污染治理领域得到了广泛的关注[2-3]。然而,常用的宽带隙光催化材料TiO2因量子化效率低(约4%)[4]且光催化反应只能在紫外光下进行[5],大大限制了其对太阳光的利用。因此,探索和开发能高效利用太阳光的新型半导体光催化剂是当今研究的热点问题。
最近,Yi课题组[6-7]研究发现半导体Ag3PO4具有较好的可见光光催化活性,Umezawa等[8]也报道了采用密度泛函理论计算以分析Ag3PO4具有良好可见光光催化活性的原因,而对于Ag3PO4在光催化降解水中有机物的研究还未见报道。
1 实验部分
1.1 催化剂的制备
将稍过量的 NaHCO3溶液缓慢滴入 40 mL 0.1 mol·L-1的AgNO3溶液中得白色浑浊液1,滴加完毕后,于室温下继续搅拌2.5 h;然后,将相应量的0.1 mol·L-1K2HPO4溶液缓慢滴入浑浊液1中即得Ag3PO4沉淀,于室温下继续搅拌5 h,经离心分离并用蒸馏水和无水乙醇洗涤催化剂样品,最后再在80℃下干燥24 h,即可制备出Ag3PO4光催化材料[9],过程反应方程式可表示为:
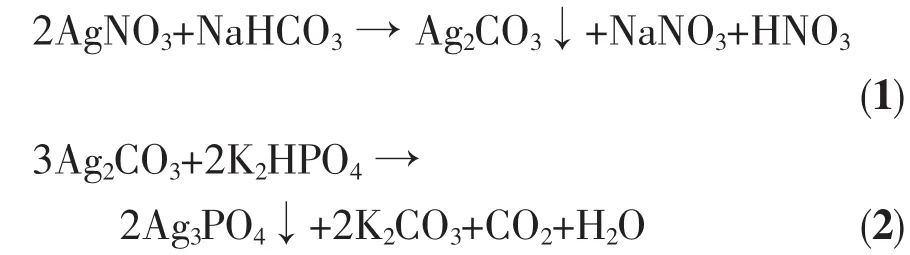
1.2 催化剂的表征
样品的晶体结构采用Rigaku D/max-2500V型X射线衍射仪分析,X射线源为Cu Kα线,经Kα2剥离处理,λ=0.154 06 nm,加速电压为40 kV,电流为100 mA,扫描速度8°·min-1,扫描范围2θ为5°~65°,步长为0.02°。样品的光电子能谱采用ESCAL-ab 220i-XL型光电子能谱仪分析,激发源为Al Kα射线,功率约为300 W,分析时的基础真空为3×10-4Pa,所测元素的结合能均以C1s峰(284.6 eV)作为内标校正;催化剂粉体的UV-Vis吸收光谱采用Varian Cary50紫外-可见分光光度计测定,扫描范围为200~800 nm,数据在室温下的空气氛围中进行采集。
1.3 光催化降解实验
实验采用自制的圆柱形石英玻璃管反应器,反应器的底部可通入空气,有效容积为70 mL。侧光源采用500 W的氙灯,灯外安装有冷却水夹套以维持恒定的反应温度。每次实验将0.03 g的催化剂加入到50 mL 15 mg·L-1的甲基橙(MO)或腐殖酸(HA)溶液中,整个反应装置放置于一个覆盖有铝箔纸的黑箱子中以防止光的泄露。反应过程中每隔10 min取样1次,经离心分离后采用紫外可见分光光度计测定有机物的浓度。有机物的剩余率为:η=C/C0× 100%,式中,C和C0分别为t时刻MO/HA的浓度和MO/HA的初始浓度。在整个实验中将催化剂的活性与 TiO2-P25进行了比较。TiO2-P25的表面积约为50 m2·g-1,锐钛矿/金红石质量之比约为80/20。
2 结果与讨论
2.1 催化剂的表征
综上所述,我国的经济得到了飞快的发展,城市化建设进程不断加快,产生了大量的交通问题,如交通排放物对环境的污染、交通拥堵以及交通事故频繁发生等问题,使人们越来越追求交通的顺畅性和环保性。近年来,物联网技术的不断发展为解决交通问题带来了很多好的技术支持,给智慧交通的发展带来了很好的动力和新的发展方向,从而便于交通系统的智能化发展,为交通服务和决策提供数据方面的支持,这样不仅可以合理地使用交通设施,还能改善交通拥堵的情况,从而为人们的生活提供顺畅便利的交通环境。
2.1.1 XRD分析
图1为所制备Ag3PO4样品的XRD图。经与PDF标准卡 (No.06-0505)对照,XRD图中的衍射角2θ为20.92°、29.74°、33.36°、36.66°、47.88°、52.76°、55.12°、57.4°、61.74°分别属于Ag3PO4的(110)、(200)、(210)、(211)、(310)、(222)、(320)、(321)、(400)各晶面的特征衍射峰,且峰形尖锐,说明所制备Ag3PO4催化剂的晶化完整。
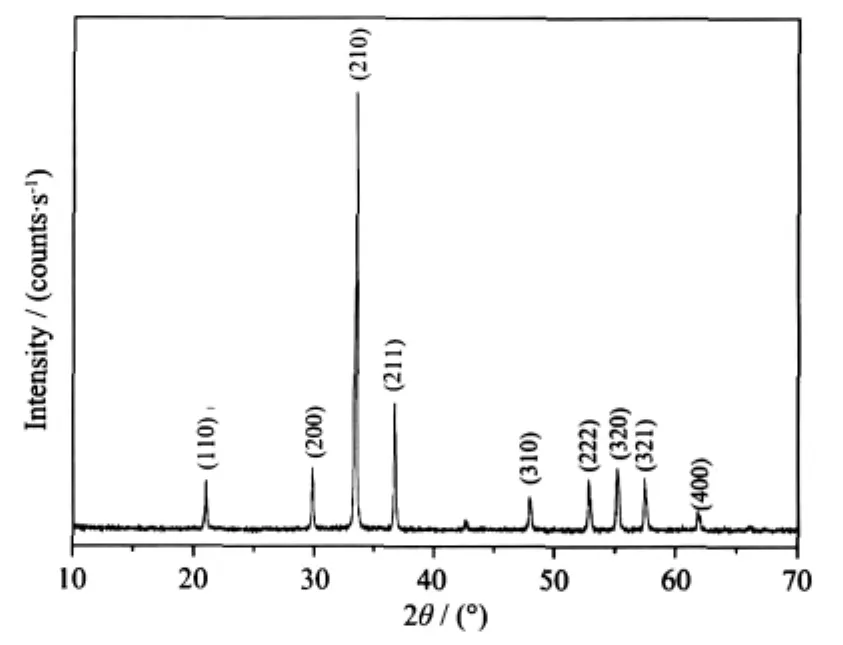
图1 Ag3PO4的XRD图Fig.1 XRD pattern of Ag3PO4
2.1.2 UV-Vis吸收光谱
图2为所制备Ag3PO4样品与TiO2-P25的紫外可见吸收光谱。由图可看出,TiO2-P25在紫外区具有强烈的吸收,而Ag3PO4的吸收边缘明显位于可见光区域内,且在400~800 nm整个可见光谱范围内均有明显的吸收。考虑到Ag3PO4为间接半导体,以(αhν)1/2对hν作图可获得Ag3PO4的带隙能,其结果显示Ag3PO4的带隙能约为1.9 eV,这与文献中报道的相吻合。
2.1.3 XPS分析
为了揭示催化剂的表面结构特性,我们采用XPS对样品进行了详细分析。反应前后Ag3PO4样品的XPS图谱如图3所示。图3(a)为XPS全谱图的比较,图中显示反应前后的样品中均含有Ag、P、O及C原子。Ag3d的高分辨谱图如3(b)所示,反应前Ag3PO4中Ag3d5/2和3d3/22个自旋峰分别位于367.7和373.7 eV,这表明反应前催化剂表面的Ag原子主要以Ag+[10]或Ag2O[11]存在。反应后Ag3d5/2和3d3/2的自旋峰位于367.9和373.9 eV,且2个峰的结合能之差ΔEb=Eb(3d3/2)-Eb(3d5/2)接近于6.0 eV,这表明反应后催化剂表面的Ag原子是以Ag0存在的[12-13]。图3(c)为O1s的高分辨能谱,样品的O1s经分峰后可分为530.4和532.3 eV 2个吸收峰。其中,530.4 eV归属于Ag2O中的O元素[14],而532.3 eV归属于P-O和O-H中的O元素[15]。图3(d)为样品的P2p高分辨能谱。由图可见,反应前P2p的结合能为132.5 eV而在反应后为133.0 eV,经分析可知该峰归属于P中的P元素[16],且在反应后催化剂的P2p向高结合能方向移动,这说明催化剂表面的P2p在反应前后发生了较大的化学位移。
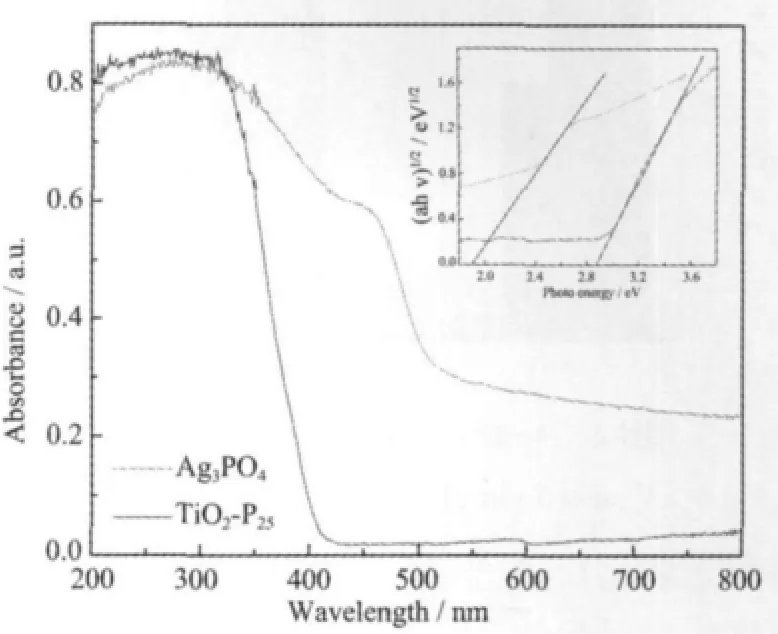
The inset is the(αhν)1/2~hν curve图2 Ag3PO4及TiO2-P25的UV-Vis光谱Fig.2 UV-Vis spectra for Ag3PO4and TiO2-P25
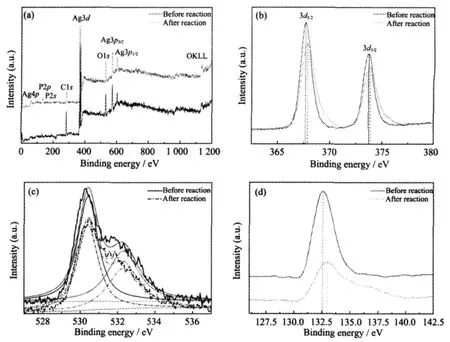
图3 反应前后Ag3PO4的XPS谱图Fig.3 XPS spectra of Ag3PO4before reaction and after reaction
2.2 Ag3PO4的可见光光催化活性
图4为60 min后不同过程在可见光下对MO和HA的光催化降解情况,其中包括吸附过程(只加催化剂不照光)、光氧化过程(只照光不加催化剂)及光催化过程(加催化剂照光)。为了对比说明同等条件下TiO2-P25的光催化情况也列入图中。由图可见,Ag3PO4对MO和HA的吸附作用分别为2.5%和15.4%。经60 min照射后,MO和HA光氧化降解率分别为2.5%和2%,而在同等条件下Ag3PO4对MO和HA的光催化降解作用分别为97%和72.3%,比同等条件下TiO2-P25的降解作用提高了约40%和25%。该结果表明,虽然存在催化剂对有机物的吸附作用和光氧化作用,但是,两种有机物的降解主要是光催化作用引起的。
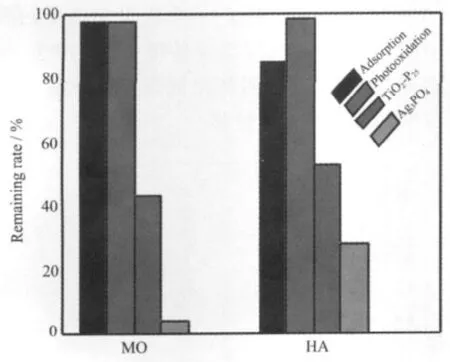
图4 Ag3PO4的可见光光催化活性Fig.4 Visible light photocatalytic activity of Ag3PO4
2.3 可见光光催化机理的研究
2.3.1 清除剂及N2对Ag3PO4可见光降解甲基橙的影响
光催化活性通常是由催化剂的表面积、带隙能、光生电子的氧化电位及 e--h+的分离等因素决定的[17]。 在实验中, 在反应系统中加入 AgNO3和NaHCO3分别作为e-、h+的清除剂[18-19],甲醇(∶=1∶4)作为清除表面及体相束缚·OH的清除剂[20],以考察光催化过程中的活性物种对MO降解的影响。通入N2以考察O2的作用[21]。实验结果如图5所示。由图可见,当加入e-、h+的清除剂AgNO3和NaHCO3时,MO的降解率均有提高,这说明两者的加入使半导体Ag3PO4在可见光下产生的e--h+进一步分离,从而使MO的降解有所提高。相比较而言,在加入NaHCO3时MO的降解率增加的更为明显,这说明在Ag3PO4的可见光光催化过程中,h+对MO的降解作用要高于e-的作用。若·OH在降解中起着关键作用,则当·OH清除剂甲醇加入时MO的降解率将有所降低。由图5可见,甲醇加入后特别是在反应后期时MO的降解率明显降低,这表明·OH在该过程中为主要的活性物种。另外,与通入空气相比,N2通入时MO的降解率明显降低了,这主要是因为N2通入时降低了溶解氧捕获光生电子而产生·浓度而致。
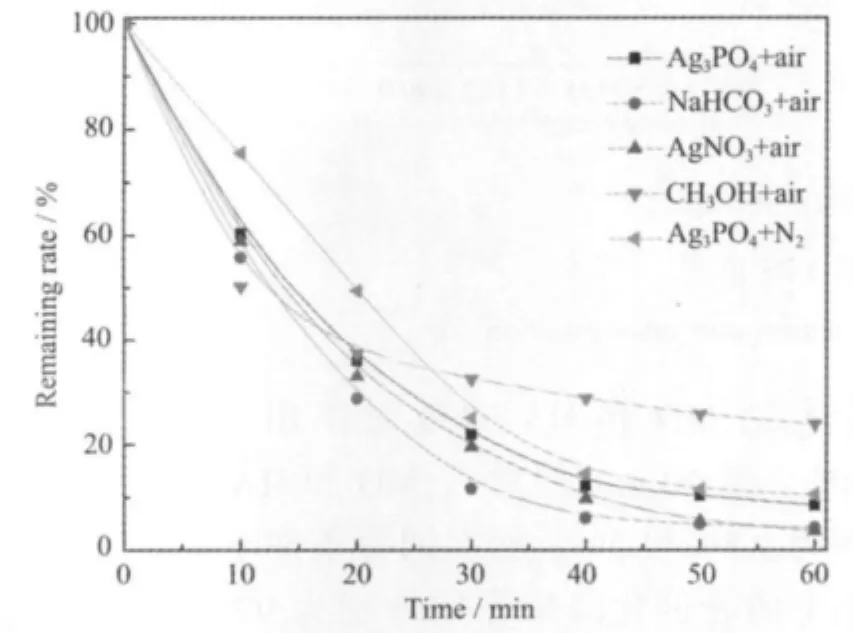
图5 清除剂及N2对甲基橙降解的影响Fig.5 Effects of scavenger and N2on degradation of MO
2.3.2 带隙结构及可见光光催化机理
Ag3PO4的价带电位和导带电位可用以下经验公式进行估算[22-23]:

式中EVB、ECB和Eg分别为半导体的价带电位、导带电位及带隙能 (根据UV-Vis数据其值约为1.9 eV);X为半导体的电负性,其值可由半导体组成原子的几何平均值求得,Ag3PO4的X值约为5.96 eV;Ee为绝对真空度下相对于参考电极氧化还原水平的标度因数 (约为4.5 eV)。根据 (3)式可计算出Ag3PO4的 EVB=2.41 eV,ECB=0.51 eV(vs NHE)。由Ag3PO4的价带电位可知其氧化电位略低于锐钛相TiO2(2.70 eV),这将有利于光生h+与OH-反应而产生·OH自由基[24],从而提高了Ag3PO4在可见光照射下产生光生h+的氧化能力。
根据结合XPS分析结果、清除剂影响及Ag3PO4的带隙结构,推测出Ag3PO4在可见光作用下降解水中有机物的机理如图6所示。首先,Ag3PO4在可见光照射下产生了光生e--h+对。其次,催化剂表面存在的Ag+捕获e-而还原为单质Ag,这大大促进了e--h+对的分离。此外,因催化剂的价带电位为+2.41 eV略低于OH/H2O(2.27 eV),h+易于与OH-反应生成· OH自由基。因此,Ag3PO4在可见光下具有较好的光催化活性。
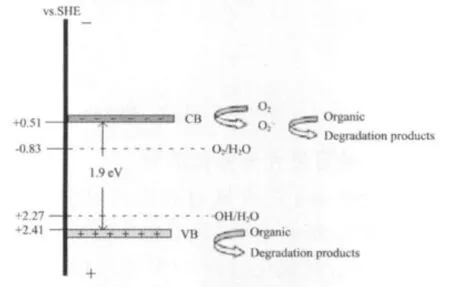
图6 Ag3PO4光催化机理示意图Fig.6 Photocatalytic mechanism scheme of Ag3PO4
3 结 论
采用沉淀置换法制备了一种新型的Ag3PO4可见光光催化剂,以中性条件下水中微污染有机物的降解考察了Ag3PO4的光催化活性,并对其进行了物理、化学特性表征及活性物种测试和带隙结构分析,得出以下结论:
(1)Ag3PO4具有间接半导体结构,其带隙能约为1.9 eV,材料本身对可见光表现出明显的吸收性能。
(2)Ag3PO4催化剂表面的Ag+可捕获光生e-而还原为单质银,实现了e--h+对的有效分离;Ag3PO4的价带电位略低于OH/H2O(2.27 eV),有利于光生h+与OH-反应而产生活性物种OH自由基,从而提高了Ag3PO4的可见光光催化活性。
(3)在模拟太阳光照射下,0.6 g·L-1Ag3PO4经60 min可使初始浓度为15 mg·L-1的MO和HA的降解率分别达97%和82%,比同等条件下TiO2-P25的降解率还高了40%和25%。
[1]Fujishima A,Honda K J.Nature,1972,238:37-38
[2]Zhang Z,Xu D,Shen M,et al.J.Water Sci.Technol.,2011, 63:424-431
[3]Erzsébet S B,Otília M,Ottó H,et al.J.Water Res.,2011, 45:1617-1628
[4]Michael R H,Scot T M,Choi W,et al.J.Chem.Rev.,1995, 95:69-96
[5]CHEN Si(陈思),LI Kan(李侃),XU Yun-Lan(徐云兰),et al. Chinese J.Water Purif.Technol.(Jingshui Jishu),2009,28: 55-59
[6]Yi Z G,Ye J H,Kikugawa N,et al.J.Nat.Mater.,2010,9: 559-564
[7]Yi Z G,Withers R L,Liu Y.J.Electrochem.Commun., 2011,13:28-30
[8]Umezawa N,Shuxin O,Ye J H.J.Phys.Rev.B,2011,83: 035202-1-8
[9]MA Pei-Yan(马 培 燕),WU Yan(吴 燕).CN Patent, 201010516084.6.2011-2-17.
[10]ZHANG Li-Yuan(张理元),LIU Zhong-Xin(刘钟馨),YU Xiao-Long(于晓 龙),et al.J.Funct.Mater.(Gongneng Cailiao),2010,41:2169-2173
[11]ZHANG Xi-Yao(张西尧),PAN Xin-Yu(潘新宇),ZHANG Yi-Feng(张琦锋),et al.Acta Phys.-Chim.Sin.(Wuli Huaxue Xuebao),2003,19:203-207
[12]Yu J,Xiong J,Cheng B,et al.J.Appl.Catal.B:Environ., 2005,60:211-221
[13]Sun L,Li J,Wang C L,et al.J.Hazard.Mater.,2009,171: 1045-1050
[14]WANG Jin-Qing(王金清),YANG Sheng-Rong(杨生荣), WANG Bo(王博),et al.Chinese J.Chem.Phys.(Huaxue Wuli Xuebao),2003,16:41-44
[15]Ren T Z,Yuan Z Y,Azioune A,et al.Langmuir,2006,22, 3886-3894
[16]Yi H H,Yu Q F,Tang X L,et al.J.Ind.Eng.Chem.Res., 2011,50:3960-3965
[17]Pan C S,Zhu Y F.J.Environ.Sci.Technol.,2010,44:5570-5574
[18]JIANG Li(蒋丽),YUAN Jian(袁坚),SHANGGUAN Wen-Fen(上官文峰),et al.J.Wuhan Univ.Technol.(Wuhan Ligong Daxue Xuebao),2010,25:919-923
[19]Hu C,Peng T W,Hu X X,et al.J.Am.Chem.Soc.,2010, 132:857-862
[20]Yin M C,Li Z S,Kou J H,et al.J.Environ.Sci.Technol., 2009,43:8361-8366
[21]PanCS,ZhuYF.J.Environ.Sci.Technol.,2010,44:5570-5574
[22]Li Y Y,Wang J S,Yao H C,et al.J.Mol Catal.A:Chem., 2011,334:116-122
[23]Lü J,Kako T,Li Z S,et al.J.Phys.Chem.C,2010,114: 6157-6162
[24]Ma X G,Lu B,Li D,et al.J.Phys.Chem.C,2011,115: 4927-4934
Ag3PO4:Visible Light Photocatalytic Performance and Mechanism
WANG Yun-FangFAN Cai-Mei*
(College of Chemistry and Chemical Engineering,Taiyuan University of Technology,Taiyuan030024,China)
Visible light photocatalytic material Ag3PO4was prepared by precipitation replacement method and characterized by using XRD,UV-Vis and XPS.The photocatalytic activity was evaluated by means of degradation of micro-organic pollutants in water.The photocatalytic mechanism was discussed based on the active species during photocatlytic process and band structure.The results showed that the band gap was about 1.9 eV,Ag+on the catalyst surface might capture photoelectron e-and the lower valence band potential of Ag3PO4.All of these would help for Ag3PO4to separate e--h+pairs generated under visible light irradiation and the formation of reactive species·OH.After 60 min visible light irradiation,the degradation rate of methyl orange and humic acid with initial concentration of 15 mg·L-1reached 97%and 82%,respectively,by using 0.6 g·L-1Ag3PO4.This result is better than that of TiO2-P2540%and 25%at the same experimental conditions.
silver phosphate;precipitation replacement method;visible light;photocatalysis
O614
A
1001-4861(2012)02-0347-05
2011-05-07。收修改稿日期:2011-09-01。
国家自然科学基金(No.20876104)、山西省科技攻关基金(No.20090311082)资助项目。*
。E-mail:fancm@163.com
猜你喜欢
杂志排行
无机化学学报的其它文章
- 含喹啉氧基乙酰胺型配体的锌配合物的合成、晶体结构及荧光性质
- 5-氨基双四唑富氮配位化合物的合成、结构及其对高氯酸铵的热分解影响
- Sr2MgSi2O7∶Tb3+,Li+荧光粉的合成和发光机理
- Sm3+含量对BaSmxFe12-xO19(x≤0.4)铁氧体纳米纤维结构和磁性能的影响
- 用NH4F络合还原法制备的炭载Pd催化剂对甲酸分解的催化性能和甲酸氧化的电催化性能
- Effects of Strontium Nitrate on the Proliferation,Differentiation and Mineralization Function of Primary Mouse Osteoblasts in vitro
