左氧氟沙星热敏型耳用凝胶的制备及其性能检测
2012-11-01李聪杨希之敖华飞孔德秋
李聪 杨希之 敖华飞 孔德秋
化脓性中耳炎是耳鼻咽喉科常见疾病,其病理改变主要是中耳鼓室黏膜化脓性炎症,主要的治疗方式是抗菌药物的使用。左氧氟沙星是一种广谱、高效的喹诺酮类抗菌药;泊洛沙姆407是研究、应用最为广泛的一种热敏型凝胶,且具有低温时为液态,温度升高时转变为凝胶的反向热敏凝胶特性。这样便可以液体形式给药,药液在中耳内立刻转变成凝胶,能够达到延长药物在中耳内的滞留时间,提高药物生物利用度的效果。目前在眼部[1]、直肠[2]、阴道[3]给药系统中都有过应用报道,但在耳科罕见类似报道,故我们以泊洛沙姆407为基质制备耳用凝胶,并对其体外释放性能进行检测。
1 材料与方法
1.1 材料 左氧氟沙星(上海楷洋生物有限公司);泊洛沙姆407(poloxamer 407,P407;商品名为普朗尼克F127,平均相对分子质量:11500,上海楷洋生物有限公司);左氧氟沙星对照品(中国药品生物制品检定所);其他试剂均为分析纯。等渗磷酸盐缓冲液(phosphate buffered saline,PBS)(1000 mL溶液中含NaH2PO41.60 g,Na2HPO47.58 g,NaCl 4.32 g,调 pH 值至7.40)。
MD100-1电子天平(上海天平仪器厂),88-I型定时恒温磁力搅拌器(上海司乐仪器有限公司),DK-8D型电热恒温槽(上海精宏实验设备有限公司),Smart Spec型分光光度计(BIO-RAD公司,美国),TK-20A型透皮扩散试验仪(上海锴凯科技贸易有限公司)。
1.2 方法
1.2.1 左氧氟沙星热敏型凝胶的制备 采用冷溶法制备,称取不同质量的P407,用注射用水配成等量不同浓度的溶液。另外称取等量左氧氟沙星加入各种溶液中,使各溶液中左氧氟沙星浓度为3 g/L,磁力搅拌器搅拌均匀,置4℃左右冰箱冷藏溶胀24 h,使凝胶充分溶胀,分散均匀,得澄清溶液。
1.2.2 相转变温度的测定 分别对不同浓度的P407溶液和上述制备的含左氧氟沙星的P407凝胶溶液进行相转变温度测定。取一定量的溶液置于试管中,将温度计插入凝胶溶液中,将试管置于恒温水浴中,缓慢升温,升温速率约每1~2 min升高1℃;后将试管倾斜90°,观察内容物不流动时的温度称为相转变温度。每个样品测3次,结果取平均值,根据适宜耳用的相转变温度选择合适的样品浓度。
1.2.3 体外释放度的测定
1.2.3.1 紫外吸收光谱及测定波长的选择 取处方量左氧氟沙星,用注射用水稀释成约10 mg/L溶液。另外选择按处方比例配制的释放介质——等渗PBS,以注射用水为空白对照在200~400 nm波长的范围内扫描,得到紫外吸收光谱(图1)。结果表明:左氧氟沙星在293 nm的波长处有最大吸收,而PBS在此波长吸收甚微,两者能较好分离,故选择293 nm为测定波长。
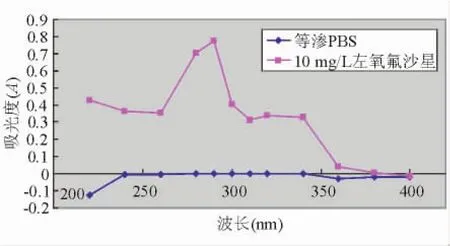
图1.紫外吸收光谱图
1.2.3.2 标准曲线的绘制 精密称取左氧氟沙星对照品50 mg,置于50 mL量瓶中;加释放介质溶解稀释至刻度,定容摇匀,作为对照品储备液。分别精密量取对照品储备液 0.30、0.45、0.60、0.75、0.90、1.05 mL,分别置于100 mL量瓶中,加释放介质至刻度摇匀。以释放介质为空白对照,在293 nm波长处测定不同浓度左氧氟沙星溶液的吸光度(A),结果在 3.0、4.5、6.0、7.5、9.0、10.5 mg/L 浓度时,A 分别为 0.213、0.328、0.453、0.586、0.704、0.793。以浓度(C)对吸光度进行线性回归,得回归方程为 C(mg/L)=12.582A+0.2976(r=0.9986,n=6),继而表明左氧氟沙星的检测浓度在3.0~10.5 mg/L范围内和吸光度呈良好的线性关系。
1.2.3.3 精密度试验 按照“1.2.3.2”项下的方法制备高、中、低 3 种浓度(10.5、6.0、3.0 mg/L)的左氧氟沙星对照液各3份,室温闭光放置,分别于同一天不同时间测定5次,计算日内左氧氟沙星吸光度的相对标准差(relative standard deviation,RSD)为 1.032%(n=5);再分别于5 d内每天测定1次,计算日间RSD为1.639%,结果均符合方法学要求。
1.2.3.4 回收率试验 精密量取已知含量(3 g/L)的左氧氟沙星热敏型凝胶2 ml,共6份,分别置于50 mL量瓶中;分别精密加入左氧氟沙星对照品储备液3.0、4.0、5.0 mL,每个浓度各 2 份,加释放介质至刻度摇匀;再精密量取1 mL,置于50 mL量瓶中,加释放介质稀释至刻度、摇匀,分别测定吸光度,结果见表1。
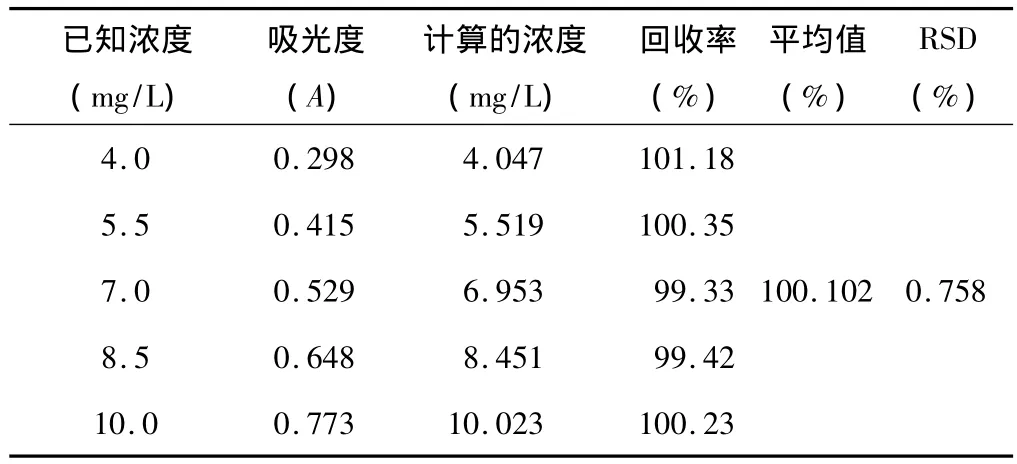
表1 回收率试验结果(n=5)
由表1可见:回收率结果符合方法学要求。
1.2.3.5 重复性试验 平行精密量取5份左氧氟沙星热敏型凝胶各1 mL,分别置于500 mL量瓶中;加释放介质稀释至刻度摇匀,分别测定吸光度并计算左氧氟沙星的含量,RSD为0.61%,结果显示试验方法重复性良好。
1.2.4 体外凝胶释药试验 选用Franz立式扩散池模型,采用TK-20A型透皮扩散试验仪。将透皮扩散试验仪的水浴箱控制在36.0℃恒温,转速为180转/min;分别在给药池和接受池内加入配制的左氧氟沙星热敏型凝胶和等渗PBS(保证PBS与皮面之间充分接触,无气泡),每隔一定时间取样1 mL,然后补加相同体积的PBS。以释放介质为空白对照,测量不同时间点取样的吸光度,进而得到不同时间点的左氧氟沙星热敏型凝胶的累计药物释放量。
2 结果
2.1 左氧氟沙星热敏型凝胶处方的设计 制备左氧氟沙星热敏型凝胶的目的主要是使该给药系统在低温时为流动性较好的液态,而中耳灌注后能够在体温下发生相转变,形成半固体凝胶。本实验考察了不同浓度的P407溶液(16%、17%、18%、19%、20%)相转变温度,同时考察了不同浓度的P407添加一定量的左氧氟沙星(3 g/L)后对凝胶相转变温度的影响,结果见图2。
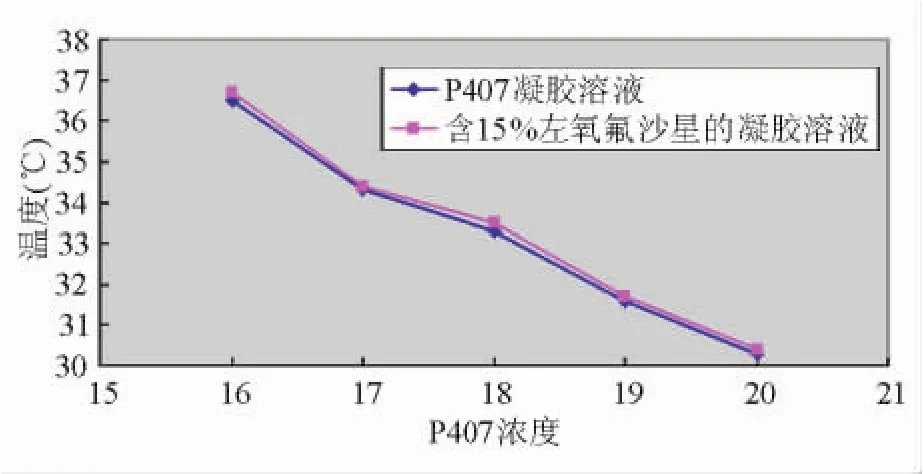
图2.不同溶液条件的P407浓度与凝胶温度的关系
结果表明:随着聚合物中P407浓度的增加,相转变温度逐渐降低;左氧氟沙星的加入对P407的相转变温度影响不大。以最接近人体中耳内的温度34℃左右作为相转变温度筛选的依据,因浓度为17%的P407溶液在34℃时已形成凝胶,故选择此浓度为耳用热敏型凝胶的基质。
2.2 左氧氟沙星热敏型凝胶体外释药的测定 根据相转变温度的检测结果,选择浓度为17%的P407左氧氟沙星溶液(3 g/L)进行体外药物累积释放量的测定,结果见图3。

图3.左氧氟沙星耳用热敏型凝胶累计释放曲线
结果表明:制备的左氧氟沙星耳用热敏型凝胶在体外释放过程中无突释效应,在160 h时的累积药物释放量已接近90%,释药基本完全,表明其具有较好的控释性。将左氧氟沙星耳用热敏型凝胶累计释放曲线进行零级释药曲线拟合,得方程 y=0.4798x+9.2214(r=0.9872),结果符合方法学意义,即以等渗PBS为释放介质,左氧氟沙星耳用热敏型凝胶释放符合零级释药方程。
3 讨论
目前化脓性中耳炎的主要治疗方式[4]为全身和局部应用抗菌药物。全身应用抗菌药物的缺点是药物达到患处的浓度较低,故需要的治疗周期较长,对机体其他组织的影响较大。传统的局部应用抗菌药,如滴耳液,虽然克服了全身用药对其他组织的影响,提高了患处局部药物浓度,但是由于中耳的解剖结构特点,药物很容易从穿孔和咽鼓管流出,造成药物在局部的作用时间短。虽然增加用药次数可一定程度上维持局部药物浓度,但给患者使用带来不便。
化脓性中耳炎是由于细菌如葡萄球菌和肺炎链球菌等通过鼻咽管侵入中耳腔后感染,引起的中耳鼓室黏膜化脓性炎症,其病理改变主要局限在中耳鼓室内,我们认为主要的治疗方式是局部抗菌药物的使用。但传统用药很难使抗菌药物在局部保持较长的作用时间,因此如何保持抗菌药物在局部的长时间作用一直是研究化脓性中耳炎治疗的关键。理想中的制剂应当满足2个条件:①较好的缓释性,能长期释药;②作用时间长,在鼓室内能够长时间滞留。故我们结合当前药剂学研究进展,将热敏型凝胶应用于耳用药物的制备。
热敏型凝胶是一种环境敏感型凝胶,选用其中的P407作为左氧氟沙星热敏型耳用凝胶的基质,具有表面活性和良好的安全性[5]。相关研究[6]表明它还具有较好的控释性及足够的药物携带量、良好的耐受性及易生物降解等优点。我们对自备的左氧氟沙星耳用热敏型凝胶体外释药进行了测定,在160 h时累积药物释放量接近90%,释药基本完全,且释放符合零级释药方程,故基本符合理想制剂的条件。
我们选用较为直观简单的倾斜法来确定相转变温度,经过多次重复实验的检测,最终确定以浓度为17%的P407溶液作为热敏型凝胶的基质。该浓度的P407相转化温度为34.4℃,最接近人体中耳内鼓室的温度。在体外释放性能检测中,我们验证了左氧氟沙星在紫外吸收光谱293 nm波长处有最大的吸收光谱,与相关文献报道相符;而选作释放介质的等渗PBS在293 nm波长处吸收甚微,因此选定293 nm为测定左氧氟沙星热敏型凝胶体外释药浓度的波长有理论意义。研究凝胶类药物体外释放,通常可采用立式扩散池或者透析袋法。鉴于制备的左氧氟沙星耳用凝胶的特性,在能较好地模拟人体中耳环境的基础上,采用立式Franz扩散池来检测凝胶药物的释放,稳定性好、操作方便、测定准确。
将P407作为左氧氟沙星的缓释载体制成左氧氟沙星热敏型凝胶,体外实验取得较好效果,但是否适合应用于体内尚未知。本课题组将做进一步的研究,以期使之成为中耳炎治疗的理想制剂。
[1]Ma WD,Xu H,Wang C,et al.Pluronic F127-g-poly(acrylic acid)copolymers as in situ gelling vehicle for ophthalmic drug delivery system[J].Int J Pharm,2008,350(1/2):247-256.
[2]Fawaz F,Koffi A,Guyot M ,et al.Comparative in vitro-in vivo study of two quinine rectal gel formulations[J].Int J Pharm,2004,280(1/2):151-162.
[3]徐玉红,曾繁涛,王蔓琳,等.甲硝唑阴道用原位凝胶的处方设计及体外质量评价[J].中国药师,2008,11(9):1025-1027.
[4]Sakamoto T,Nakagawa T,Horie RT,et al.Inner ear drug delivery system from the clinical point of view[J].Acta Otolaryngol Suppl,2010,130(2):101-104.
[5]Blonde JM,Baird L,Fulfs JC,et al.Dose-dependent hyperlipidemia in rabbits following administration of poloxamer 407 gel[J].Life Sci,1999,65(21):261-266.
[6]Lee SH,Lee JE,Baek WY,et al.Regional delivery of vancomycin using pluronic F-127 to inhibit methicillin resistant Staphylococcus aureus(MRSA)growth in chronic otitis media in vitro and in vivo[J].J Control Release,2004,96(1):1-7.
