生鲜牛乳中过氧化氢的电极检测
2012-10-27孔维琴陈志伟高广恒周万里朱思荣史建国赵建飞
孔维琴,陈志伟*,高广恒,周万里,朱思荣,史建国,赵建飞
(1.山东理工大学化学与工程学院,山东 淄博 255049;2.山东理工大学分析测试中心,山东 淄博 255049;3.山东省科学院生物研究所,山东 济南 250014;4.石家庄君乐宝乳业有限公司,河北 石家庄 050221)
生鲜牛乳中过氧化氢的电极检测
孔维琴1,陈志伟2,*,高广恒3,周万里3,朱思荣3,史建国3,赵建飞4
(1.山东理工大学化学与工程学院,山东 淄博 255049;2.山东理工大学分析测试中心,山东 淄博 255049;3.山东省科学院生物研究所,山东 济南 250014;4.石家庄君乐宝乳业有限公司,河北 石家庄 050221)
优化生鲜牛乳中过氧化氢电极检测的工作条件,研究样品处理方法对检测结果的影响,重点比较电极法与过氧化氢试纸条法和淀粉-碘化钾法的检出率及误判率,验证生鲜牛乳中过氧化氢的电极检测法的可靠性。结果表明:在0~10mg/L和10~80mg/L范围内电极法的检出率为分别为100%和93.33%,误判率为7.14%和7.89%。试纸条法和淀粉-碘化钾法的检出率分别为0%和83.33%,误判率分别为100%和20%。与过氧化氢试纸条法和淀粉-碘化钾法相比,电极法能够对生鲜牛乳中过氧化氢进行定量检测并具有较好的可靠性,有利于实现生鲜牛乳中过氧化氢的快速现场检测。
生鲜牛乳;过氧化氢;电极法;检测
过氧化氢是一种强氧化剂,具有消毒、杀菌和漂白等功能,被广泛应用于乳品[1]、水发产品[2]及鱼类干货[3]等食品的保鲜防腐和无菌包装。研究表明,生鲜牛乳中残留过量过氧化氢会影响其中αs-酪蛋白、牛血清蛋白等[4]蛋白质的性质,降低生鲜牛乳的营养价值,而且具有致癌、加速衰老、诱导心血管疾病等毒副作用[5]。为了保障乳品安全,减少过量使用或滥用过氧化氢所引起的中毒事件[6],建立一种准确快速检测生鲜牛乳中过氧化氢的方法很有必要。
早在1957年,美国官方分析化学师协会(association of analytical communities,AOAC)曾公布利用二氧化钛(TiO2)与硫酸制成的显色剂可以定性判断生鲜牛乳中是否存在过氧化氢(AOAC Offical method 957.08 hydrogen peroxide in milk)。1967年Amin等[7]提出分光光度法,Gilliland[8]提出酶法,Ferrier等[9]提出四氯化钛法检测生鲜牛乳中过氧化氢。Abbas等[10]采用基于Fenton反应的荧光法对生鲜牛乳中过氧化氢进行检测。GB/T 23499—2009《食品中残留过氧化氢的测定方法》[11]中推荐采用碘量法和钛盐比色法[12]测定食品中过氧化氢含量,但对蛋白含量高的液体样品需添加除蛋白试剂进行样品前处理。此外还有过氧化氢试纸条法和淀粉-碘化钾法。本实验采用电极法检测生鲜牛乳中过氧化氢,能有效克服现有方法操作繁琐、灵敏度差和成本高的缺点,实现简便、快速、准确地检测生鲜牛乳中残留过氧化氢的目的。
1 材料与方法
1.1 材料与试剂
生鲜牛乳 蒙牛乳业泰安有限责任公司和石家庄君乐宝乳业有限公司;过氧化氢试纸条(110011 Peroxide Test) 德国默克(Merck)集团;草酸钠(工作基准试剂) 天津风船化学试剂科技有限公司;高锰酸钾(分析纯) 莱阳市康德化工有限公司;30g/100mL H2O2(分析纯) 莱阳经济技术开发区精细化工厂;淀粉-碘化钾溶液;硫酸(1+15):量取10mL浓硫酸,放入150mL水中;0.2mol/L的Na2HPO4溶液;0.2mol/L的NaH2PO4溶液。
1.2 仪器与设备
SBA-50C电极 山东省科学院生物研究所;PHS-3C型pH计 上海精密仪器有限公司;CT15RT高速冷冻离心机 上海天美生化仪器设备工程有限公司;FA1604分析天平 上海天平仪器厂;SK5200LH超声波清洗机上海科导超声仪器有限公司;DHG-9240A恒温干燥箱上海一恒科学仪器有限公司。
1.3 方法
1.3.1 配制溶液
0.1mol/L的高锰酸钾标准溶液:参考文献[13]的方法配制和标定。标定30% H2O2:参考文献[14]的方法称量和测定。配制质量浓度为10mg/L的过氧化氢标准溶液,同时配制过氧化氢质量浓度为1、2、4、5、6、8、10mg/L的生鲜牛乳样品溶液。
1.3.2 仪器定标
首先,将电极的清洗时间、反应时间和等待时间分别设置为50、30s和5s,定标值为10。然后开机,用进样针准确吸取30μL过氧化氢标准溶液,待进样灯闪烁时迅速注入反应池,数据稳定后读取数据。重复上述操作,直至定标指示灯停止闪烁,表明定标成功。
1.3.3 测定样品
定标后,用清洗干净的进样针准确吸取30μL样品溶液进样,其余步骤同1.3.2节操作。每个样品重复进样3次,取3次数据的平均值为最终测定值。并以样品质量浓度/(mg/L)为X轴,测定值/(mg/L)为Y轴作数据曲线。
1.3.4 数据处理
利用统计学SPSS(statistical product and service solution)16.0软件中的Explore程序,得到显著水平为0.05时过氧化氢质量浓度为5mg/L的生鲜牛乳样品的电极测定值的置信区间,并以此作为统计判断依据。利用统计学SPSS 16.0软件中的Crosstabs程序进行列联表检验,判断电极法与过氧化氢试纸条法和淀粉-碘化钾法之间是否存在显著性差异。
2 结果与分析
2.1 优化电极工作条件
2.1.1 清洗时间的选择
在不改变其他电极参数的前提下,将清洗时间分别设置为50、100s和150s,然后测定同一批次生鲜牛乳配制的过氧化氢质量浓度为0、5、10mg/L的3个样品,考察清洗时间对生鲜牛乳样品测定结果的影响。结果表明,同一样品在不同清洗时间下的测定值相同,即对电极清洗50s能满足实验对电极清洁程度的需要。因此清洗时间选择50s。
2.1.2 缓冲液pH值的选择
在不改变其他电极参数的前提下,分别采用pH值为6.5、6.7、6.9、7.1、7.3、7.5的0.02mol/L磷酸盐缓冲液作为电极缓冲液,然后测定同一批次生鲜牛乳配制的过氧化氢质量浓度为0、2、4、6、8、10mg/L的6个样品,考察缓冲液pH值对生鲜牛乳样品测定结果的影响。同时与缓冲剂(pH7.25)条件下测定的结果对比。结果(图1)表明,pH值为7.25时测定得到的数据曲线斜率最大,即在相同的浓度梯度内,在该pH值条件下,电极对电流信号最敏感,得到的测定值最可靠,因此缓冲液pH值选择7.25。
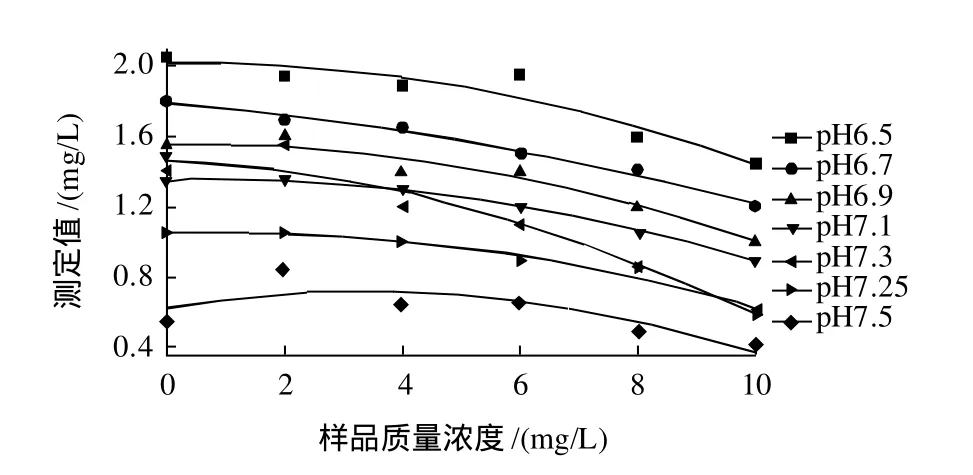
图1 缓冲液pH值对生鲜牛乳测定的影响Fig.1 Effect of buffer pH on the detection of hydrogen peroxide in raw whole milk
2.2 不同样品处理方法对测定的影响
2.2.1 煮沸对生鲜牛乳测定的影响
选用同一批次的生鲜牛乳配制过氧化氢质量浓度为0、1、5、10mg/L的4个样品,然后在优化的电极工作条件下对煮沸处理前后的样品分别进行测定,考察煮沸对电极测定结果的影响。结果表明,煮沸后的测定值较煮沸前降低0.6~1mg/L。这可能是因为煮沸使得生鲜牛乳内部的保鲜平衡体系被打破,部分过氧化氢分解造成的。
2.2.2 脱脂对生鲜牛乳测定的影响
选用同一批次的生鲜牛乳配制过氧化氢质量浓度为0、1、5、10mg/L的4个样品,然后在优化的电极工作条件下分别对脱脂处理(20℃,8000r/min,10min)前后的样品进行测定,考察脱脂对电极测定结果的影响,结果见表1。由表1可知,生鲜牛乳和脱脂牛乳的电极测定值完全相同。因此,脂肪对电极测定生鲜牛乳样品中过氧化氢不存在干扰。
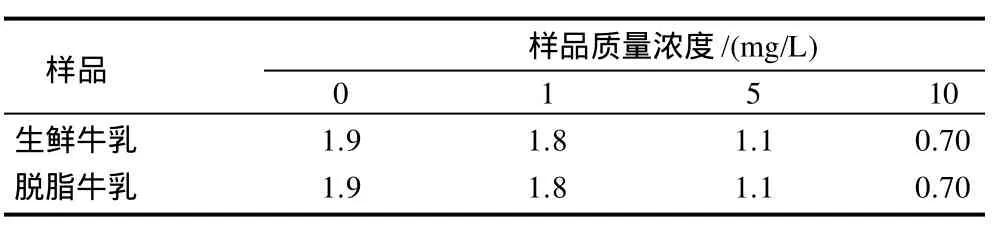
表1 生鲜牛乳与脱脂牛乳的电极测定结果Table 1 Results obtained for detection of hydrogen peroxide in raw whole milk and skim milk using the electrode method
2.2.3 稀释对测定的影响
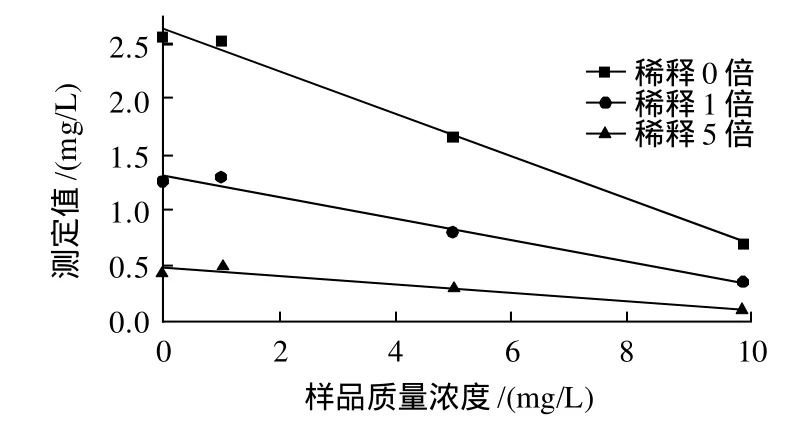
图2 稀释对生鲜牛乳测定的影响Fig.2 Effect of dilution ratio on the detection of hydrogen peroxide in raw whole milk
选用同一批次的生鲜牛乳配制过氧化氢质量浓度为0、1、5、1mg/L的4个样品,然后在优化的电极工作条件下,将配制好的生鲜牛乳样品分别稀释0倍、1倍和5倍后进行测定,考察稀释前后电极测定结果的变化。结果(图2)表明,测定值随稀释倍数近似成倍数减少,并且曲线下降趋势趋于平缓。因此,稀释并不能提高电极测定生鲜牛乳样品的灵敏度。
2.3 与其他方法的比较
随机选取21个批次的生鲜牛乳配制21个过氧化氢质量浓度为5mg/L的样品,利用电极法对21个生鲜牛乳样品进行测定。随机选取8个批次的生鲜牛乳配制过氧化氢质量浓度为0、6、7、8、9、10mg/L的生鲜牛乳样品,考察电极法与过氧化氢试纸条法的测定结果。随机选取6个批次的生鲜牛乳配制过氧化氢质量浓度为10、20、50、60、80mg/L的生鲜牛乳样品,考察电极法与淀粉-碘化钾法的测定结果,结果见表2、3(电极测定值以“平均值±标准误”的形式表示)。
依据GB 23499—2009《食品中残留过氧化氢的测定方法》中碘量法和钛盐比色法的检出限,将质量浓度大于5mg/L的生鲜牛乳样品作为研究对象,并定义检出率和误判率的计算公式如下:


表2 电极法和过氧化氢试纸条法的测定结果(n=8)Table 2 Comparative results obtained for detection of hydrogen peroxide in raw whole milk using the electrode method and paper indicator test(n=8)

表3 电极法和淀粉-碘化钾法的测定结果(n=6)Table 3 Comparative results obtained for detection of hydrogen peroxide in raw whole milk using the electrode method and starch-potassium iodide method (n=6)
利用SPSS 16.0软件对来自21个批次过氧化氢质量浓度为5mg/L的生鲜牛乳样品的电极测定值进行统计分析,删除离群值后得到5mg/L的电极测定值在置信度为95%时的置信区间是(2.47,2.85)。由2.1节和2.2节实验发现在0~10mg/L范围内生鲜牛乳样品的电极测定值随着过氧化氢质量浓度的增加而减少,因此判定电极测定值低于2.47的样品质量浓度均大于5mg/L。在10~80mg/L范围内,判定电极测定值超出95%置信区间(2.47,2.85)的样品质量浓度均大于5mg/L。
统计结果显示:电极法在0~10mg/L和10~80mg/L范围内的检出率分别为100%和93.33%,误判率分别为7.14%和7.89%。试纸条法和淀粉-碘化钾法的检出率分别为0%和83.33%,误判率分别为100%和20%。电极法检出率为比试纸条法和淀粉-碘化钾法分别高100%和10%,而7%左右的误判率较之这两种方法明显偏低。依据统计学卡方检验知识,利用SPSS 16.0软件的Crosstabs程序统计可知,显著水平为0.05时电极法与过氧化氢试纸条法之间存在显著性差异(x2=72.053,P<0.05),而电极法与淀粉-碘化钾法之间差异不显著(x2=0.647,P>0.05)。
3 结 论
电极法测定生鲜牛乳中过氧化氢的工作条件和样品处理方法非常简单。电极检测时可以将样品直接注入反应池,无须对样品进行处理,最大程度保留了残留的过氧化氢,使测定结果更准确可靠。电极检测的最佳清洗时间50s、最佳反应时间30s、最适pH7.25,能满足生鲜牛乳中过氧化氢现场检测的要求。与过氧化氢试纸条法和淀粉-碘化钾法相比,电极法成功地实现了生鲜牛乳中过氧化氢的快速、准确、低成本检测,为生鲜牛乳中过氧化氢的限量分析提供一种新方法。
[1] 姜竹茂, 韩起文, 谭源, 等. 乳品加工中的清洗消毒与保鲜技术[J].包装与食品机械, 2005, 23(6): 48-51.
[2] 张薇薇, 杨怡, 陈培超, 等. 钼酸铵分光光度法测定水发产品中过氧化氢残留量[J]. 现代预防医学, 2008, 35(8): 1556-1557.
[3] 王秀季, 蔡春, 张立坚. 鱼类干货中过氧化氢(H2O2)残留的测定[J]. 广东微量元素科学, 2007, 14(3): 38-40.
[4] GRINDROD J, NICKERSON T A. Changes in milk proteins treated with hydrogen peroxide[J]. Journal of Dairy Science, 1967, 50(2): 142-146.
[5] 刘海峰, 柴春彦, 刘国艳. 壳聚糖-胶体金修饰丝网印刷电极测定过氧化氢[J]. 上海交通大学学报, 2008, 26(4): 264-268.
[6] 张之论. 灭菌乳中污染过氧化氢所致食物中毒的证实[J]. 中国流行病学杂志, 2004, 25(9): 765-768.
[7] AMIN V M, OISON N F. Spectrophotometric determination of hydrogen peroxide in milk[J]. Journal of Dairy Science, 1967, 50(4): 461-464.
[8] GILLILAND S E. Enzymatic determination of residual hydrogen peroxide in milk[J]. Journal of Dairy Science, 1969, 52(3): 321-324.
[9] FERRIER L K, OISON N F, RICHARDSON T J. Analysis of hydrogen peroxide in milk using Titanium tetrachloride[J]. Journal of Dairy Science. 1970, 53(5): 598-599.
[10] ABBAS M E, LUO Wei, ZHU Lihua, et al. Fluorometric determination of hydrogen peroxide in milk by using a Fenton reaction system[J]. Food Chemistry, 2010, 120(1): 327-331.
[11] 国家食品质量监督检验中心(上海), 上海市质量监督检验技术研究院. GB/T 23499—2009 食品中残留过氧化氢的测定方法[S]. 北京:中国标准出版社, 2009.
[12] 巢国强, 张辉, 葛宇. 钛盐比色法测定消毒生鲜牛乳中残留过氧化氢的含量[J]. 食品与机械, 2007, 23(6): 93-94.
[13] 国家质量监督检验检疫总局. GB/T 601—2002 化学试剂标准滴定溶液的制备[S]. 北京: 中国标准出版社, 2002.
[14] GB 22216—2008 食品添加剂: 过氧化氢[S]. 北京: 中国标准出版社, 2009.
Electrode Detection of Hydrogen Peroxide in Raw Whole Milk
KONG Wei-qin1,CHEN Zhi-wei2,*,GAO Guang-heng3,ZHOU Wan-li3,ZHU Si-rong3,SHI Jian-guo3,ZHAO Jian-fei4
(1. School of Chemical Engineering, Shandong University of Technology, Zibo 255049, China;2. Analytical and Testing Center, Shandong University of Technology, Zibo 255049, China;3. Biology Institute, Shandong Academy of Sciences, Jinan 250014, China;4. Shijiazhuang Junlebao Dairy Co. Ltd., Shijiazhuang 050221, China)
An analytical method for determining hydrogen peroxide in raw whole milk was developed using a platinum-silver electrode. Electrode working conditions and sample pretreatment were optimized. The results obtained for the positive rate and false positive rate of hydrogen peroxide by the proposed electrode method, hydrogen peroxide test strip method and starchpotassium iodide method were compared to validate the reliability of the electrode method. The electrode method provided detection rates of 100% and 93.33% and false detection rates of 7.14% and 7.89% for hydrogen peroxide in the ranges of 0-10 mg/L and 10-80 mg/L, respectively; in contrast, detection rates of 0% and 83.33% and false detection rates of 100% and 20% were obtained using the hydrogen peroxide test strip method and the starch-potassium iodide method, respectively. In conclusion, the electrode method allows reliable, rapid, on-the-spot quantitative detection of hydrogen peroxide in raw milk.
raw whole milk;hydrogen peroxide;electrode method;detection
TS202.3
A
1002-6630(2012)18-0177-04
2011-07-09
国家自然科学基金面上项目(31071538);山东省科学仪器设备技术攻关项目(2008GG2TC01011-5);山东省优秀中青年科学家科研奖励基金项目(2007BS06021)
孔维琴(1986—),女,硕士研究生,研究方向为应用化学。E-mail:kongweiqin1986@163.com
*通信作者:陈志伟(1972—),男,教授,博士,研究方向为生物化学及分析测试。E-mail:chen@sdut.edu.cn
