氨基酸与丙二醛反应体系的荧光光谱
2012-10-25孙艳辉孟金秀贾小丽彭曼莉
孙艳辉,孟金秀,贾小丽,彭曼莉
(滁州学院生物与食品工程学院,安徽滁州 239012)
氨基酸与丙二醛反应体系的荧光光谱
孙艳辉,孟金秀,贾小丽,彭曼莉
(滁州学院生物与食品工程学院,安徽滁州 239012)
采用荧光光谱法研究氨基酸与丙二醛的反应,考察反应时间、pH和浓度对赖氨酸与丙二醛反应体系发射光谱的影响,并对不同种类的氨基酸与丙二醛反应进行比较。结果表明,氨基酸与丙二醛反应生成了400nm激发、460nm发射的荧光物质,该反应在中性条件下易于进行,并随时间延长产物增多,反应体系中,丙二醛浓度高于赖氨酸浓度有利于生成荧光产物。不同氨基酸与丙二醛反应产物的荧光强度差异明显,精氨酸、赖氨酸、甘氨酸、苯丙氨酸、组氨酸等五种氨基酸易与丙二醛反应,脯氨酸、羟脯氨酸、色氨酸未能与丙二醛反应生成荧光物质。
赖氨酸,丙二醛,氨基酸,荧光光谱
食品在加工贮藏过程中易发生脂肪氧化,造成营养物质损失和异味产生;同时,脂肪氧化次级产物攻击蛋白质,引起氨基酸侧链修饰、蛋白质主链断裂和蛋白质分子间共价交联[1-2]。其中,丙二醛(Malondialdehyde,MDA)是最重要的脂肪氧化次级产物,具有很强的生物反应活性,几乎能攻击所有的生物大分子,导致其结构的改变和功能的丧失[3-4]。贺洪等[5]采用紫外吸收光谱研究了赖氨酸对丙二醛的清除作用,发现在400nm处产生了新的吸收峰。Glomb M A等[6]的研究表明,在室温和中性pH条件下MDA能与生物分子中的氨基特别是精氨酸,组氨酸,赖氨酸残基反应,引起蛋白交联。邓燕等[7]的研究表明MDA与牛磺酸反应产生一种类似脂褐素(Ex.392~395nm/Em.456~364nm)的荧光产物1,4-二氢吡啶衍生物。这些研究仅对部分氨基酸或蛋白质中的氨基酸残基进行研究,而采用荧光分析方法对全部自由氨基酸与MDA反应的研究尚未见报道。因此,本文采用荧光光谱法对自由氨基酸与MDA的反应进行探讨,先系统考察pH、时间、浓度对赖氨酸与MDA反应的产物荧光强度的影响,进而考察不同种类的氨基酸与MDA反应的荧光产物情况。
1 材料与方法
1.1 材料与仪器
十九种氨基酸 北京科康生物科技有限公司;1,1,3,3-四乙氧基丙烷 阿拉丁试剂有限公司;盐酸等 均为分析纯。
Cary eclipse型分子荧光分光光度计 Varian,美国瓦里安公司;精密天平,恒温水浴锅。
1.2 实验方法
1.2.1 MDA的配制 按照王爱国[8]的方法,先配制1.5×10-4mol的1,1,3,3-四乙氧基丙烷水溶液,加入1mol/L盐酸1m L和超纯水50m L,将溶液在50℃的水浴中放置1h,即成MDA溶液。1mol的1,1,3,3-四乙氧基丙烷完全水解后可得1mol的MDA。冷却后定容至100m L,4℃冷藏保存。
1.2.2 反应体系的配制 将MDA和氨基酸按1∶1摩尔比配制,去离子水分别定容至刻度,摇匀,置于37℃恒温水浴锅中反应1h,水浴冷却至25℃后测定荧光光谱。
1.2.3 荧光光谱的绘制 以400nm为激发波长,420~600nm波长范围内扫描得到荧光发射光谱;以460nm为发射波长,350~450nm波长范围内扫描得到荧光发射光谱;固定Δλ=60nm,在240~700nm波长范围内进行扫描得到同步荧光光谱;扫描时激发狭缝5nm,发射狭缝10nm。波长扫描速度为600nm/min。
1.2.4 pH对赖氨酸MDA反应体系荧光发射光谱的影响 采用1mol/L HCl和1mol/L NaOH调节赖氨酸MDA反应体系的pH为1.8、2.2、2.6、3.0、3.7、6.0、6.6、6.9、7.2、9.4、10.5、12后,按1.2.2方法反应后测定荧光发射光谱。
1.2.5 时间对赖氨酸MDA反应体系荧光发射光谱的影响 pH为6.0的赖氨酸MDA反应体系分别按按1.2.2方法反应0.5、1、1.5、2、3h后测定荧光发射光谱。1.2.6 浓度对赖氨酸MDA反应体系荧光发射光谱的影响 pH为6.0的赖氨酸MDA反应体系,赖氨酸浓度为0.01mmol/L时,MDA浓度分别为0.01、0.02、0.03、0.04、0.05mmol/L;赖氨酸浓度为0.01mmol/L时,MDA浓度分别为0.01、0.02、0.03、0.04、0.05mmol/L;按1.2.2方法反应2h后,测定荧光发射光谱。
1.2.7 不同种类氨基酸与MDA反应的体系荧光发射光谱 二十种氨基酸,按氨基酸浓度为0.05mmol/L、MDA浓度为0.05mmol/L配制反应液;采用1mol/L HCl和1mol/L NaOH调节反应液的pH为6,按1.2.2方法反应2h后测定荧光发射光谱。
1.2.8 色氨酸MDA反应体系的荧光发射光谱 按色氨酸浓度为0.05mmol/L、MDA浓度为0.05mmol/L配制反应液;采用1mol/L HCl和1mol/L NaOH调节反应液的pH为6,按1.2.2方法反应5、7、15、24、48h后测定同步荧光光谱。
1.3 实验数据处理方法
采用Matlab 9.0软件作图。
2 结果与讨论
2.1 赖氨酸MDA反应体系的激发光谱与发射光谱
对赖氨酸MDA体系反应1h后按1.2.2方法扫描激发光谱与发射光谱,结果可以发现,赖氨酸MDA体系在400nm波长处有最大吸收,在461nm波长处有最大发射,而赖氨酸、丙二醛在该处均不出峰,说明赖氨酸MDA体系反应产生了新物质。该物质的荧光特征和邓燕等人的研究结果一致[7],说明该物质可能是类脂褐质。为研究方便,后续研究均是对反应体系的发射光谱开展(Ex.400nm)探讨。

图1 赖氨酸MDA反应体系的激发光谱和与发射光谱Fig.1 The excited and emission fluorescence spectroscopy of lysine-MDA system
2.2 pH对赖氨酸MDA反应体系荧光发射光谱的影响
pH对赖氨酸MDA反应体系荧光发射光谱的影响如图2所示。由图2可以看出,pH为1.8时,赖氨酸MDA反应体系的荧光强度最低,随着pH由低到高,赖氨酸MDA反应体系荧光强度先升高,在pH为6.0时为最大,然后降低。这说明,偏中性的反应体系有利于赖氨酸与MDA反应,这与贺洪的研究结果一致[5]。后续研究过程中反应体系pH选为6.0。

图2 pH对赖氨酸MDA反应体系荧光发射光谱的影响Fig.2 Effectof pH on the emission fluorescence spectroscopy of lysine-MDA system
2.3 反应时间对赖氨酸MDA反应体系荧光发射光谱的影响
赖氨酸MDA反应体系荧光发射光谱随时间变化的结果如图3所示。由图3可以看出,随着反应时间的延长,赖氨酸MDA反应体系的在461nm处的荧光强度越来越大。这说明产生的荧光物质越来越多。后续研究的反应时间定为2h。

图3 反应时间对赖氨酸MDA反应体系荧光发射光谱的影响Fig.3 Effectof reaction time on the emission fluorescence spectroscopy of lysine-MDA system
2.4 浓度对赖氨酸MDA反应体系荧光发射光谱的影响
赖氨酸与MDA浓度比例发生变化时,其荧光产物的量也发生变化,结果如图4所示。由图4可以看出,当赖氨酸浓度固定为0.01mmol/L时,随着丙二醛浓度从0.01mmol/L升高到0.05mmol/L时,反应体系的荧光强度升高;而当赖氨酸浓度固定为0.05mmol/L时,随着丙二醛浓度从0.01mmol/L升高到0.05mmol/L时,反应体系的荧光强度升高,但最终的荧光强度比较小;这说明,反应体系中,丙二醛浓度越高于赖氨酸浓度时,荧光强度越高。已有文献表明:一定条件下高浓度的MDA能够形成乙醛,两分子MDA和一分子乙醛能与带初级氨的化合物反应生成二羟吡啶加成物[9-10],这与本实验结果一致。

图4 赖氨酸与MDA浓度比对反应体系荧光发射光谱的影响Fig.4 Effectof concentration on the emission fluorescence spectroscopy of lysine-MDA system
2.5 酸性侧链和碱性侧链与MDA反应的荧光发射光谱
为研究氨基酸种类与丙二醛反应的荧光特征,首先分别对酸性侧链氨基酸(谷氨酸、天冬氨酸、谷氨酰胺、天冬酰胺),碱性侧链氨基酸(组氨酸、赖氨酸、精氨酸)与MDA体系的荧光发射光谱进行扫描,结果如图5所示。
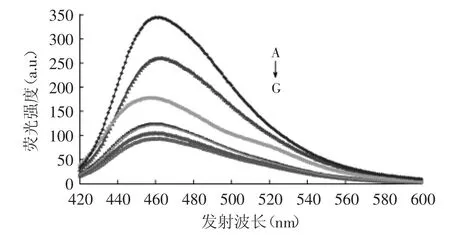
图5 酸性侧链和碱性侧链氨基酸与MDA反应的荧光发射光谱Fig.5 The emission fluorescence spectroscopy of lacid or basic chain AA-MDA system
由图5可以看出,精氨酸与MDA反应体系的荧光强度最高,赖氨酸次之、组氨酸第三、谷氨酸、天冬氨酸、谷氨酰胺、天冬酰胺相差不大。对于酸性和碱性侧链来说,氨基酸易于电离,易于发生反应。其中,精氨酸的氨基、亚氨基最有利于反应,荧光强度最高。赖氨酸、组氨酸也是同样道理[11]。
2.6 短小侧链氨基酸与MDA反应的荧光发射光谱
对苏氨酸、丝氨酸、亮氨酸、甘氨酸与MDA反应体系的荧光发射光谱进行扫描,结果如图6所示。由图6可以看出,甘氨酸与MDA反应体系的荧光强度最高,丝氨酸的次之、苏氨酸的第三、丙氨酸的最小。这与甘氨酸的结构有关,在甘氨酸、丝氨酸、苏氨酸和丙氨酸四种氨基酸中,甘氨酸其空间位阻最小,反应最易进行,反应体系的荧光强度最大[11]。
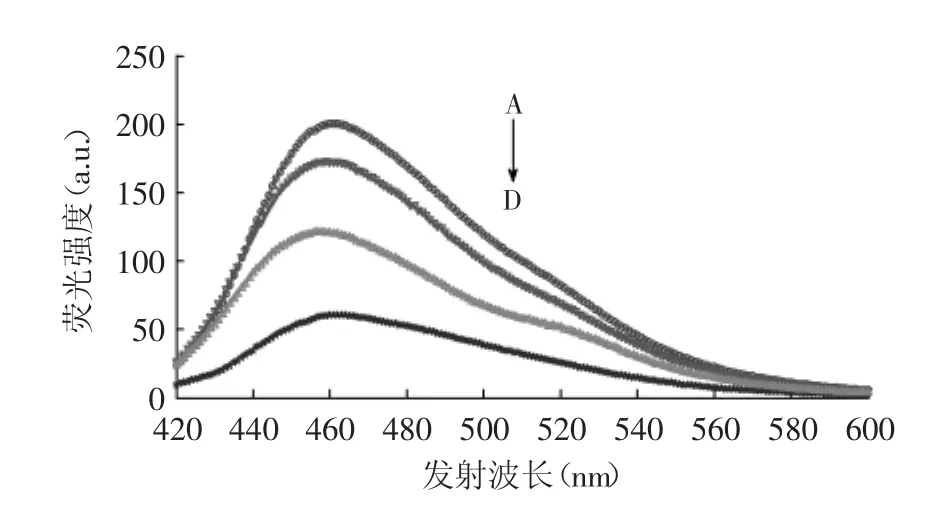
图6 短小侧链氨基酸与MDA反应的荧光发射光谱Fig.6 The emission fluorescence spectroscopy of little side chain AA-MDA system
2.7 长大侧链氨基酸与MDA反应的荧光发射光谱
对色氨酸、酪氨酸、苯丙氨酸、异亮氨酸、亮氨酸、缬氨酸、甲硫氨酸、脯氨酸和羟脯氨酸与MDA反应体系的荧光发射光谱进行扫描,结果如图7所示。由图7可以看出,苯丙氨酸与MDA反应体系的荧光强度最高,甲硫氨酸、异亮氨酸、亮氨酸、缬氨酸相差较小、酪氨酸的反应峰微小,色氨酸、脯氨酸和羟脯氨酸不能与MDA反应产生。这与长大侧链氨基酸的结构有关,侧链长大导致空间位阻大,反应难于进行,反应体系的荧光强度就越小。另外,脯氨酸和羟脯氨酸没有单独的氨基,故反应难于进行[11]。

图7 长大侧链氨基酸与MDA反应的荧光发射光谱Fig.7 The emission fluorescence spectroscopy of long side chain AA-MDA system
对不同反应时间的色氨酸MDA体系的同步荧光光谱进行扫描,结果如图8所示。由图8可以看出,随反应时间的延长,色氨酸荧光强度逐渐降低,未发现新的荧光峰出现。说明MDA对色氨酸具有荧光猝灭作用,二者未产生新的荧光物质。这可能是色氨酸的吲哚环结构抑制了其与MDA的反应。

图8 色氨酸与MDA反应体系的同步荧光光谱Fig.8 The synchronouns fluorescence spectroscopy of tryptophan-MDA system
3 结论
赖氨酸与丙二醛反应生成400nm激发、460nm发射的荧光物质,该反应在中性条件下易于进行,并且随时间延长荧光产物增多;反应体系中,丙二醛浓度高于赖氨酸浓度有利于生成荧光产物。不同氨基酸与丙二醛反应产物的荧光强度差异明显,精氨酸、赖氨酸、甘氨酸、苯丙氨酸、组氨酸等五种氨基酸易与丙二醛反应,而脯氨酸、羟脯氨酸、色氨酸未能与丙二醛反应生成荧光物质。
[1]崔旭海.肉蛋白氧化机制及氧化对肉制品品质和功能性的影响[J].食品工业科技,2009,30(6):338-341.
[2]黄莉,孔保华,李菁,等.氧化引起肉及肉制品品质劣变的机理及影响因素[J].食品科学,2011,32(9):319-323.
[3]Li S J,King A J.Structural changes of rabbit myosin subfragment altered by malonaldehyde,a byproduct of lipid oxidation[J].JAgric Food Chem,1999,47(8):3124-3129.
[4]王贵.肌肽的抗羰基应激作用:肌肽与丙二醛的反应机理研究[D].长沙:湖南师范大学,2010.
[5]贺洪,刘庆伟,刘慧敏.pH对赖氨酸保护作用影响的研究[J].湘潭师范学院学报:自然科学版,2009,31(12):30-33.
[6]Requena JR,Fu M X,Ahmed M U,et al.Quantlfication malondialdehyde and 4-hydroxynonenal adducts to lysine residus in native and oxidized human low-density liPo Protein[J]. Bioehem J,1997,322(1):317-325.
[7]邓燕,何农跃,许利剑,等.两种非蛋白氨基酸的新功能:与丙二醛相互反应的机制[J].化学学报,2010,68(23):2457-2462.
[8]王爱国,罗广华.羟自由基启动下的脱氧核糖降解及其产物的TBA反应[J].生物化学与生物物理进展,1993,20(2):150-152.
[9]Xu D,Thiele GM,Kearley M L,etal.Epitope characterization of malondialdehyde-acetaldehyde adducts using an enzymelinked immunosorbent assay[J].Chem Res Toxicol,1997,10(9):978-986.
[10]Tuma D J,Thiele G M,Xu D,et al.Acetaldehyde and malondialdehyde react together to generate distinct Protein adducts in the liver during long-term ethanol administration[J]. Hepatology,1996,23(4):872-880.
[11]王璋,许时婴,汤坚.食品化学[M].北京:中国轻工业出版社,2002:124-129.
Fluorescence spectroscopy of the reaction system between am ino acid and malondialdehyde
SUN Yan-hui,MENG Jin-xiu,JIA Xiao-li,PENG M an-li
(School of Bio&Food Engineering,Chuzhou University,Chuzhou 239012,China)
The reac tion between am ino acid and malondialdehyde(MDA)was stud ied by fluorescence spectroscopy.The effec t of time,pH and concentration on the em ission spectroscopy of lysine-MDA system was researched,and the reaction charactertic of 19 kinds of am ino acid w ith MDA was compared.The result showed the p roduct of AA-MDA system had Ex.400nm and Em.460nm,easier to happen under the neutral cond ition,w ith the reaction time p rolonged,the fluorescence p roduct inc reased.The concentration of MDA was much more than that of lysine,more fluorescence p roduct increasing.The fluorescence intensity had significant d ifference among kinds of AA-MDA.Arginine,lysine,histidine and g lycine could easier react w ith MDA to p roduce fluorescence p roduct,while p roline,hyd roxyp roline and tryp tophan could not.
lysine;malond ialdehyde;am ino acid;fluorescence spectroscopy
TS201.2
A
1002-0306(2012)22-0042-04
2012-08-28
孙艳辉(1978-),男,博士,副教授,研究方向:食品质量安全。
国家自然科学基金项目(30901129);安徽省农产品质量与安全特色专业基金项目(20101032)。
