脂肪来源干细胞移植与急性心肌梗死研究现状
2012-10-23陈宇朴海南
陈宇,朴海南
急性心肌梗死(acute myocardial infarction,AMI)是临床危重症,治疗难度大,致残率、病死率均较高,严重危害人们的身心健康,也给社会医疗卫生事业带来了沉重的负担。目前,临床广泛应用的最有效救治手段仍为在一定时间窗内进行冠状动脉血运重建,以挽救濒死心肌。但显而易见的是,心肌凋亡和坏死的启动已造成不可逆损伤,梗死心肌的功能缺失及结构重塑均成为目前临床治疗难以逾越的障碍。而事实上,应该接受血运重建的患者中仅有约半数接受了及时的血运重建术[1]。再生医学的发展却独辟蹊径,直截了当地指出了一条可能的未来之路--心肌细胞成形术。
在干细胞研究蓬勃发展的大背景下,细胞治疗从实验室到临床,从分子生物学水平到细胞生理学研究,向我们展示出在急性心肌梗死治疗应用领域的广阔前景。利用干细胞多向分化的潜能进行组织或器官的修复成为可能。目前,多数实验提示干细胞移植治疗心肌梗死,能够改善心肌梗死后心功能、提高患者生活质量。在这些实验中,移植用“种子”细胞的选择亦不尽相同。自2001年ZUK等[2]从人吸脂术来源的脂肪组织中获得具有间质细胞表型特点和多向分化潜能的独特细胞群(PLA Cells)以来,对脂肪来源干细胞(adipose-derived stem cells,ADSCs)的研究和应用迅猛发展。ADSCs以其独特的优势(易取材、获取简便、患者容易接受、不涉及伦理问题)得到研究者的推崇。
1 脂肪来源干细胞及其作为“种子”细胞的研究
ZUK等[2]在2001年从人吸脂术取得的脂肪组织中分离出一群特殊的细胞群,并将其命名为processed lipoaspirate cells(PLA Cells)。在体外培养扩增,表现出良好的增殖能力与多向分化的潜能。体外扩增后,表现出成纤维细胞样的细胞形态,进行免疫组化,SMA、FⅧ、ASO2分子表达均为阳性,表现出纤维母细胞的分子特征。根据其研究,认为这类细胞可能成为细胞治疗新的候选“种子”。在次年的研究论文中,ZUK更进一步提出人脂肪组织是可获取多能干细胞的来源之一,它们和当时已经有较多研究的间充质干细胞一样,同样来源于中胚层。通过RT-PCR、Western Blot技术从基因表达层面证明其具有多向分化的能力[3]。在他们的实验中,将PLA cell与人骨髓间充质干细胞(MSC)进行比较,发现许多共同的CD分子标记,但也有其独特的分子表达。如:PLA cell表达CD49而MSC未见表达,而BMC表达的CD106在PLA中却未见表达(表1)。
应用各种不同的诱导剂和方法可使PLA细胞向诸如骨、软骨、神经、肌细胞的祖细胞方向横向分化。国内段炼等[4]亦通过对成人脂肪干细胞的体外培养、传代研究了其生物学特性,发现ADSCs具有间充质细胞的特征,但不表达造血干细胞的特征分子(CD31、CD45等),体外扩增传代后仍稳定的表现为二倍体核型,成瘤风险低,且由于未见主要免疫原性分子的表达,推测具有免疫逃逸特性,可用于异体移植。在实际研究中发现ADSCs基本上是一组以原始间质细胞为主的混杂细胞群。事实上,对于ADSCs的研究已不仅仅局限于组织再生,在免疫调节方面也有相关的报道。Kang等[5]以ADSCs与宿主免疫细胞共同培养发现上清液中存在可溶性细胞因子,部分炎性因子(如TNF-α)含量降低,而IL-6、TGF-β、IFN-γ含量则显著增加,即使在促细胞分裂素存在的情况下,白细胞的增殖仍然受到抑制。这些研究无疑展示出ADSCs作为移植用供体细胞的合理性和优越性。
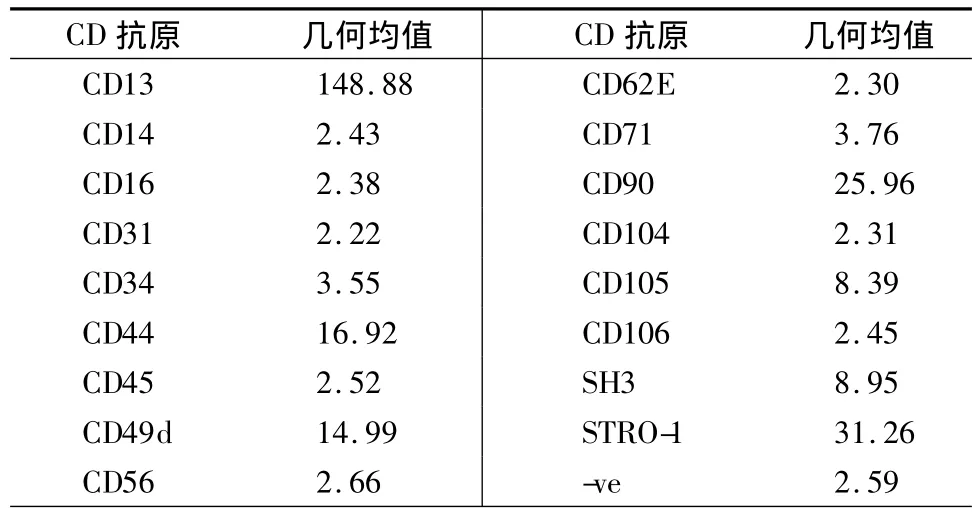
表1 未经诱导的PLA细胞CD分子的表达(流式细胞仪)
2 ADSCs向心肌样细胞的分化研究
在早期的ADSCs研究中,就已经发现诸如cTNI、cTNT、β-MHC、ANP、β-action等肌源性或心肌特异性分子的表达。许多体外应用诱导剂促ADSCs向心肌样细胞分化的实验得到了更具心肌细胞特性的细胞。常用诱导剂或方法:5-氮杂胞苷(5-aza)、某些细胞因子、心肌细胞或提取液共培养法等。张卫泽等[6]观察AngⅡ对ADSCs的诱导分化作用并从形态学、免疫组化分析上与5-aza相比较,发现AngⅡ在诱导ADSCs分化为心肌样细胞效能上与5-aza相当,但AngⅡ诱导后未见细胞毒性,ADSCs凋亡远少于5-aza组,且AngⅡ还有促进ADSCs聚集生长的效应。甚至在国内和国外均有部分研究者称ADSCs分化的心肌样细胞具有类似心肌的自律性特征。张端珍等[7]以5-aza对ADSCs进行体外诱导见到类似心肌细胞的节律性搏动。Metzele等[8]则以人ADSCs在体外与鼠坏死心肌细胞共培养见到具有节律收缩性的细胞。但是,在ADSCs的体外培养及向心肌细胞的诱导分化实验中大多数报道却并未见到自发节律性搏动的心肌样细胞。关于诱导心肌样细胞的鉴定方法主要集中于CD分子特征、特异蛋白及mRNA的表达等生物分子学水平。就目前的实验而言,还难以在体外获得一个由ADSCs分化而来的具有完整的肌丝、肌浆网等结构并完全具备自律性、收缩性、传导性、兴奋性、舒张性的心肌细胞。
3 心肌梗死后心肌ADSCs移植的研究
在上述体外实验进行的同时,心肌梗死后ADSCs移植的研究也在蓬勃发展。Fraser等[9]的研究小组将新分离的ADSCs以LacZ进行标记后移植给心肌梗死后的鼠模型,观察发现在鼠心肌梗死区见到相当数量的LacZ阳性细胞,并且这些LacZ阳性细胞可与宿主细胞融合,也表达Nkx2.5、肌钙蛋白I、肌球蛋白重链等心肌特异蛋白分子,宿主心脏功能亦得到了改善。Hwangbo等[10]也对心肌梗死的鼠进行了脂肪干细胞移植,他们做了多方面指标的测定,包括超声心功能评价(FS、EF、LVESD、LVEDD)、组织学评价(梗死区毛细血管密度观察)、免疫组化检测,较为全面的反映了移植后梗死心肌的功能、重构等问题。在他们的实验中,采取于心肌梗死后一周行细胞移植,并分别于移植后1天、1周、2周和4周行心脏超声检查。实验观察到EF、FS在移植后第4周明显优于PBS对照组(P<0.05),心室肌厚度也优于PBS组(P<0.01),局部血管增生密度高于 PBS组(P<0.01)。这些结果充分说明ADSCs移植在心肌梗死治疗中的有益作用。Leobon等[11]则利用他们改进的方法培育出脂肪来源的心肌样细胞并移植于鼠的急性梗死心肌中,同样观察到心脏功能、组织学结构得到改善。另一方面的实验有van der Bogt等[12]以ADSCs和BM-MSCs分组移植于鼠梗死心肌(心肌梗死后立即移植),报告两组与对照组比较并未见心功能有明显改善和获益,而且观察到移植细胞的大量死亡。就在同年,Cai等[13]却发表了观点不同的报道。根据他们的研究结果,ADSCs移植后促进梗死区血管再生和神经芽生,有效的保护了心功能。移植细胞可持续存活达到1月,但没有证据表明这些细胞可直接转化为宿主的心肌组织而发挥替代作用。而这一观点得到了国际脂肪治疗科学联合会的认同。国内学者李宾公等[14]亦于较早进行了ADSCs移植治疗大鼠急性心肌梗死的研究,其结果表明ADSCs可以促进梗死后心肌的血管再生,改善心脏功能,同时也观察到移植后梗死局部某些细胞因子(如VEGF)的表达水平升高。目前研究的主流报道依然显示出ADSCs移植在心肌梗死治疗中的有益作用[15-20]。
4 ADSCs移植改善心功能的机制探讨
从上述一系列的研究中不难看出,各家对ADSCs移植后心脏功能的改善程度是不尽相同的。但比较一致的观察结果是移植细胞很少在体内形成具有完备功能的再生心肌从而发挥替代作用。大多数植入的干细胞都会随着时间的延长而死亡。正如前述van der Bogt等的研究,即使在那些细胞移植后心功能得到改善的研究中也极少发现心肌组织的大面积再生,或者说植入干细胞转化为宿主心肌而发挥相应的功能。在心肌梗死的急性期,梗死区及其周围的内环境是相当不稳定的。大量的炎性细胞随着各种炎性趋化因子的浓度升高向梗死区聚集,加重心肌细胞的损伤。而干细胞植入后两周内仅有少于2%的植入细胞能存活下来,因此,其有效性机制的研究重点已转向植入干细胞的旁分泌因子[21]。Kang等[5]发现犬ADSCs与坏死心肌细胞培养的上清液能够抑制宿主免疫细胞的增殖,进一步分析发现其中含有的可溶性细胞因子有免疫调节的作用,减轻炎性反应。Shah[22]概括干细胞治疗改善心功能的机制为三个方面:血管再生、心肌再生、免疫调节(抑制炎症),而这三方面作用又发挥其下游效应-心肌细胞凋亡减少、瘢痕增生减轻(优化重构)。以目前的认识,干细胞的血管内皮样细胞及心肌样细胞分化、旁分泌功能主导了上述三个促使心功能改善的机制。而由于干细胞植入后,存活或者心肌样分化的细胞数量极少(如前述),旁分泌作用的地位自然就突显出来了。近十年的研究,认识到ADSCs的有益作用与其分泌的各种细胞因子是密不可分的。在实验中已经发现的可溶性分子包括肝细胞生长因子、粒细胞及巨噬细胞集落刺激因子、肿瘤坏死因子、血管内皮生长因子、IL-6、IL-7、IL-8、IL-11、神经生长因子、脂肪因子及其他多种未被鉴定的分子[23]。研究者提出心肌梗死后治疗,细胞还是生长因子的选择问题,显然是想探讨在实际情况下更为直接有效的心肌梗死的生物治疗途径。Kang等[24]则在心肌梗死后接受冠脉支架置入术的患者中开展了临床实验。他们将以接受支架置入术的患者随机分为周围血干细胞冠脉内注入组、粒细胞集落刺激因子(G-CSF)+周围血干细胞冠脉内注射组、对照组。通过对心功能和冠状动脉血运重建的评测发现,G-CSF并没有加重炎症反应和缺血,G-CSF+细胞治疗组及细胞治疗组运动耐量及左室射血分数较对照组均明显改善,但在G-CSF+细胞治疗组支架内再狭窄发生率却显著增加,实验亦因此而被终止。Prosper[25]指出虽然细胞再生和细胞因子应用于治疗心肌梗死极具新意和吸引力,但应该将临床安全性放在首要位置,以患者获益为最终目标。van Dijk等[26]在研究中还发现心肌梗死后纤连蛋白在梗死区及其周边表达增加,而这种蛋白可促使ADSCs粘附聚集和增殖,从而可能促进梗死局部心肌的修复。可见,目前对干细胞及其分泌因子在体内的具体效应和总体作用并不十分清楚也难以准确把握,单纯地把ADSCs或其它种类多能干细胞移植在AMI治疗中表现的获益归结为某一种机制的作用是不恰当的。总之,以系统观来看待和应用实验室得到的成果,需要了解在AMI时局部内环境特殊而剧烈的变化(炎症、缺血)甚至是整个机体的变化(应激)[27-29];而ADSCs在此种环境下的生物学行为的调控仍是须要面对的难题。如前提到的部分研究者[5,30]用坏死心肌或心肌细胞裂解液与脂肪干细胞共培养来观察其分化和细胞因子的表达就部分地模拟AMI时的内环境。从诸多的研究中,我们了解到AMI时的局部内环境可以导致植入的ADSCs死亡,但另一方面,其中的部分因子又诱导ADSCs向心肌样细胞分化并分泌诸如抗凋亡、抗炎、多种生长因子改善细胞间质环境、促进修复。
5 问题和展望
脂肪干细胞的发现及研究在时间上晚于造血干细胞和骨髓干细胞,但其表现出的部分优越性却有目共睹,尤其给更便捷地临床应用带来了希望。无数事实告诉我们,在临床治疗中“无损害”原则应是医者具备的基本素质,而ADSCs治疗的安全性仍存争议,成瘤性、致心律失常和支架内再狭窄都缺乏长期的观察,因此也是值得关注的问题。所以ADSCs治疗方法真正走向临床仍有相当长的道路。目前,关于心肌梗死后细胞植入的最佳时机和细胞量(密度)均无定论,干细胞植入途径和方法也有待探讨;一批新型生物工程材料的出现及技术改进也给干细胞移植载体提供了新的选择。总之,ADSCs用于治疗急性心肌梗死是一个崭新的领域,它给我们带来进一步改善心梗预后的希望,同时也带动了对ADSCs自身的潜能更深入的研究。
[1]Fox KA.Registries and surveys in acute coronary syndrome[J].Eur Heart J,2006,27(19):2260-2262.
[2]Zuk PA,Min Zhu,Mizuno H,et al.Multilineage cells from human adipose tissue:Implications for cell-based therapies[J].Tissue Eng,2001,7(2):211-228.
[3]Zuk PA,Zhu M,Ashjian P,et al.Human adipose tissue is a source of multipotent stem cells[J].Mol Biol Cell,2002,13(12):4279-4295.
[4]段炼,宋智钢,徐志云,等.成人脂肪干细胞的生物学特性[J].解剖学杂志,2009,32(4):448-450.
[5]Kang JW,Kang KS,Koo HC,et al.Soluble factors-mediated immunomodulatory effects of canine adipose tissue-derived mesenchymal stem cells[J].Stem Cell Dev,2008,17(4):681-693.
[6]张卫泽,樊艳,陈永清,等.血管紧张素Ⅱ对成人脂肪间充质干细胞向心肌细胞分化的影响[J].第四军医大学学报,2008,29(8):692-695.
[7]张端珍,盖鲁粤,刘宏伟,等.脂肪干细胞与间充质干细胞体外诱导分化为心肌细胞的差别[J].生理学报,2008,60(3):341-347.
[8]Metzele R,Alt C,Bai X,et al.Human adipose tissue-derived stem cells exhibit proliferation potential and spontaneous rhythmic contraction after fusion with neonatal rat cardiomyocytes[J].Faseb J,2011,25(3):830-839.
[9]Fraser JK,Schreiber R,Strem B,et al.Plasticity of human adipose stem cells toward endothelial cells and cardiomyocytes[J].Nat Clin Pract Cardiovasc Med,2006,3(Suppl 1):S33-37.
[10]Hwangbo S,Kim J,Her S,et al.Therapeutic potential of human adipose stem cells in a rat myocardial infarction model[J].Yonsei Med J,2010,51(1):69-76.
[11]Leobon B,Roncalli J,Joffre C,et al.Adipose-derived cardiomyogenic cells:in vitro expansion and functional improvement in a mouse model of myocardial infarction[J].Cardiovasc Res,2009,83(4):757-767.
[12]van der Bogt KE,Schrepfer S,Yu J,et al.comparison of transplantation of adipose tissue-and marrow-derived mesenchymal stem cells in the infracted heart[J].Transplantation,2009,87(5):642-652.
[13]Cai L,Johnstone BH,Cook TG,et al.IFATS collection:Human adipose tissue-derived stem cells induce angiogenesis and nerve sprouting following myocardial infarction,in conjunction with potent pressrvation of cardiac function[J].Stem Cell,2009,27(1):230-237.
[14]李宾公,曾秋棠,王红祥,等.脂肪基质干细胞移植治疗大鼠急性心肌梗死[J].中华急诊医学杂志,2006,15(4):306-309.
[15]Yamada Y,Wang X,Yokoyama S,et al.Cardiac progenitor cells in brown adipose tissue repaired damaged myocardium[J].Biochem Biophys Res Commun,2006,342(2):662-670.
[16]Martinez-Estrada OM,Munoz-Santos Y,Julve J,et al.Human adipose tissue as asource of Flk-1+cells:new method of differentiation and expansion[J].Cardiovase Res,2005,65(2):328-333.
[17]Valina C,Pinkernell K,Song YH,et al.Intracoronary administration of autologous adipose tissue-derived stem cells improves left ventricular function,perfusion,and remodeling after acute myocardial infarction[J].Eur Heart J,2007,28(21):2667-2677.
[18]方芳,杨天伦,谢秀梅,等.自体脂肪干细胞治疗心肌梗死的实验研究[J].中国医学工程,2007,15(2):152-162.
[19]Schnke-Layland K,Strem BM,Jordan MC,et al.Adipose tissue derived cells improve cardiac function following myocardial infarction[J].J Surg Res,2009,153(2):217-223.
[20]Mazo M,Planat-Benard V,Abizanda G,et al.Transplantation of adipose derived stromal cells is associated with functional improvement in a rat model of chromis myocardial infarction[J].Eur J Heart Fail,2008,10(5):454-462.
[21]Murry CE,Field LJ,Menasche P,et al.Cell-based cardiac repair reflections at the 10-year point[J].Circulation,2005,112(20):3174-3183.
[22]Shah VK,Shalia KK.Stem cell therapy in acute myocardial infarction:A pot of gold or pandora's box[J].Stem Cells Int,2011,2011(5):1-20.
[23]Salqado AJ,Reis RL,Sousa NJ,et al.Adippose tissue derived stem cells secretme:soluble factors and their roles in regenerative medicine[J].Curr Stem Cell Res Ther,2010,5(2):103-110.
[24]Kang HJ,Zhang SY,Park KW,et al.Effects of intracoronary infusion of peripheral blood stem-cells mobilized with granulocyte-colony stimulating factor on left ventricular systolic function and restenosis after coronary stenting in myocardial infaction:the MAGIC cell randomized trial[J].Lancet,2004,363(9411):751-756.
[25]Prosper F.Regenerative cell therapy after myocardial infarction:cells or growth factors[J]?Res Esp Cardiol,2005,58(3):238-240.
[26]van Dijk A,Niessen HW,Ursem W,et al.Accumulation of fibronection in the heart after myocardial infarction:a putative stimulator of adhesion and proliferation of adipose-derived stem cells[J].Cell Tissue Res,2008,332(2):289-298.
[27]Zhang M,Methot D,Poppa V,et al.Cardiomyocyte grafting for cardiac repair:graft cell death and anti-death strategies[J].J Mol Cell Cardiol,2001,33(5):907-912.
[28]Azarnoush K,Maurel A,Sebbah L,et al.Enhancement of the functional benefits of skeletal myoblast transplantation by means of coadministration of hypoxia-inducible factor 1alpha[J].J Thorac Cardiovasc Surg,2005,130(1):173-179.
[29]Wang QD,Sjoquist PO.Myocardial regeneration with stem cells:pharmacological possibilities for efficacy enhancement[J].Pharmacol Res,2006,53(4):331-340.
[30]李宾公,曾秋棠,王红祥,等.心肌细胞裂解液诱导人脂肪基质干细胞分化为心肌样细胞的研究[J].Chin J Crit Care Med,2006,26(4):280-282.
