乙酸乙烯酯接枝改性海藻酸钙凝胶微球
2012-10-19漆亮亮英晓光张卫英
漆亮亮,英晓光,李 晓,张卫英,徐 雯
(福州大学化学化工学院,福建 福州 350108)
研究开发
乙酸乙烯酯接枝改性海藻酸钙凝胶微球
漆亮亮,英晓光,李 晓,张卫英,徐 雯
(福州大学化学化工学院,福建 福州 350108)
为了降低海藻酸钙凝胶微球的溶胀度,以乙酸乙烯酯(VAc)对海藻酸钠进行自由基接枝共聚,进而制备具有较低溶胀度的聚乙酸乙烯酯改性海藻酸钙(Ca-SA-PVAc)凝胶微球。红外光谱表明,改性之后海藻酸钙的分子上生成新的化学键;热重分析表明,改性微球受热失水行为发生变化,热稳定性提高;扫描电镜表明,改性微球结构孔隙结构发达;接枝反应条件如反应温度、VAc的浓度、引发剂用量、海藻酸钠浓度、钙离子浓度及反应时间等对改性凝胶微球在生理盐水中的抗溶胀性具有不同程度的影响。通过改变反应条件以控制接枝反应参数,可以获得溶胀行为可控的改性海藻酸钙凝胶微球。
海藻酸钠;乙酸乙烯酯;接枝反应;溶胀度;凝胶微球
海藻酸钙由β-1,4-D-甘露糖醛酸(M)和α-1,4- L-古罗糖醛酸(G)两种结构单元组成,具有廉价、可降解、生物相容性良好和原料易得等优点,已广泛应用于药物载体、细胞培养基、分离提纯、控制释放、医用敷料等领域[1-2]。但是,海藻酸钙在水中易溶胀,在一定程度上限制了它的应用。近年来,许多研究者通过共聚、氧化、硫化、单元耦合、酰胺化等方法对海藻酸盐进行改性[3]。化学改性主要是通过单体与海藻酸盐骨架上的—OH 和—COO-进行接枝反应,而单体与—COO-的反应会造成改性产物对钙离子的凝胶能力变差[4]。因此,对海藻酸钠的—OH进行接枝改性的方法引起了越来越多研究者的兴趣。Işıklan等[5]将衣康酸接枝共聚到海藻酸钠上,考察了接枝条件对接枝参数的影响;Gao等[6]制备了聚(2-二甲氨基)-异丁烯酸乙酯接枝氧化海藻酸钠,并考察了牛血清蛋白的控制释放行为;Laurienzo等[7]制备出了乙二醇接枝共聚海藻酸钠;Arpit Sand,M ithilesh等[8-9]分别将N-乙烯基-2-吡咯烷酮、2-丙烯酰胺羟基酸接枝到海藻酸钠上;英晓光等[10]通过在海藻酸盐凝胶体系中添加少量纤维素醚并使用戊二醛交联的方法,制备了互传网络改性大分子及乳液双印迹海藻酸钙凝胶微球;李志勇等[11]将氧化海藻酸钠与十二胺接枝反应,并进行了药物包埋释放实验。但是,这些研究大多数考察接枝反应条件对接枝参数的影响,没有进一步对反应条件影响改性海藻酸钙的溶胀度做系统的研究,而水凝胶材料的溶胀性为,在许多应用场合又具有至关重要的影响。
聚乙酸乙烯酯(PVAc)链段的疏水性在一定程度上可以帮助提高海藻酸盐凝胶的抗溶胀性,并且可以构建共价交联点,降低海藻酸钙的溶胀度。海藻酸钙凝胶材料溶胀的机理主要是离子交联剂Ca2+与水中的 Na+、H+等发生交换,钙离子交联密度的下降导致海藻酸钙三维网络的伸展,最终凝胶材料溶胀[12]。因此,在生理盐水中测定改性凝胶微球的溶胀度可以检验改性效果。
本工作拟采用乙酸乙烯酯为功能单体,选用特定的氧化还原引发体系,对海藻酸盐的羟基进行自由基接枝改性,而尽量保留接枝产物的羧基不被破坏,仍然可与钙离子交联而凝胶化。通过改变接枝反应条件来影响接枝参数,从而达到溶胀度可控的目的。进而讨论了凝胶体系中齐聚物的生成对溶胀度的影响机理。
1 实验部分
1.1 主要试剂与材料
海藻酸钠(sodium alginate,SA)、乙酸乙烯酯(vinyl acetate,VAc,使用前提纯),化学纯,上海国药化学试剂厂;氯化钙,分析纯,上海豪恩化学厂;亚硫酸钠,化学纯,浙江永嘉化学试剂厂;过硫酸钾(potassium peroxydisulfate,KPS,使用前重结晶),化学纯,上海恒新化学试剂厂;无水乙醇,分析纯,浙江三鹰化学试剂有限公司。
1.2 接枝反应和改性海藻酸钙凝胶微球的制备
在盛有一定量去离子水的三口烧瓶中,缓慢加入SA,在磁力搅拌作用下溶解并通氮气30 min,加入氧化还原引发剂(KPS-Na2SO3)和单体(VAc),待反应到指定时间后终止反应。利用锐孔法[13],将接枝聚合物溶液滴入CaCl2水溶液,交联反应一段时间后,将凝胶微球取出并过滤,干燥。
1.3 SA接枝率的测定
将一定量乙醇加入接枝产物中,待其完全沉淀后,充分搅拌,移除乙酸乙烯酯齐聚物和残余反应物并抽滤,将沉淀物干燥,称重。接枝率G用式(1)计算。

式中,W1和WSA分别代表干燥后的沉淀物和海藻酸钠的质量,g。
1.4 VAc转化率的测定
将接枝产物干燥,称重。转化率C用式(2)计算。
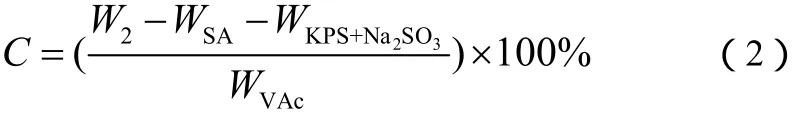
式中,W2为产物干重,g;WKPS+Na2SO3代表引发剂总质量,g;WVAc代表VAc总质量,g。
1.5 接枝反应速率的计算
接枝反应速率R[mol/(L·s)]利用式(3)计算。

式中,M代表VAc的相对摩尔质量,为86.09 g/mol;V代表反应体系的总体积,L;t代表反应时间,s。
1.6 微球溶胀度的测定
准确称取一定质量的干态微球,放于50 m L的生理盐水(25℃)中充分溶胀至平衡,过滤并除去微球表面的浮水,称重。用式(4)计算溶胀度S。

式中,W3和W4分别代表微球溶胀前和溶胀平衡后的质量,g。
1.7 红外光谱分析
将乙醇加入样品中,完全除去VAc齐聚物和残留单体后,将沉淀抽滤、干燥、研磨,用KBr压制成片,设定红外分析仪(Spectrum-2000)上温度为25 ℃,扫描范围为400~4500 cm-1,绘制样品红外吸收谱图。
1.8 热重分析
准确称取20~30 mg干态样品放于研钵中,设置综合热分析仪(STA409PG)的加热速度为10 ℃ /min,在氮气的保护下程序加热直到 1000 ℃,绘制样品的热重分析曲线。
1.9 微球形貌分析
将改性前后的微球在液氮下淬冷,在真空冷冻干燥箱内干燥,用JFC-1200型镀膜仪镀膜,将干燥好的样品观察面朝上粘紧,在扫描电镜(HITACHI S-4800)下观察样品结构。
2 结果与讨论
2.1 Ca-SA-PVAc微球的形成机理
PVAc改性海藻酸钙分子结构的形成机理如图1所示。海藻酸钠骨架上羟基上的氢被引发剂夺取而形成大分子自由基,进而在VAc分子上发生加成反应,并进行链增长。反应结束后,通过锐孔法将接枝产物滴入Ca2+溶液中,海藻酸钠结构单元中的两个均聚古罗糖醛酸(G)嵌段经过协同作用结合,中间形成了亲水空间,当这些空间被Ca2+占据,Ca2+会与古罗糖醛酸上多个氧原子发生螯合作用,使得海藻酸钠链间紧密结合,通过与接枝链段和共价交联点的协同作用,最终导致凝胶三维网络凝胶微球的形成[14]。
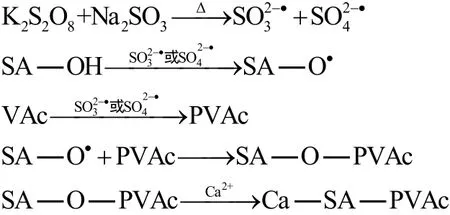
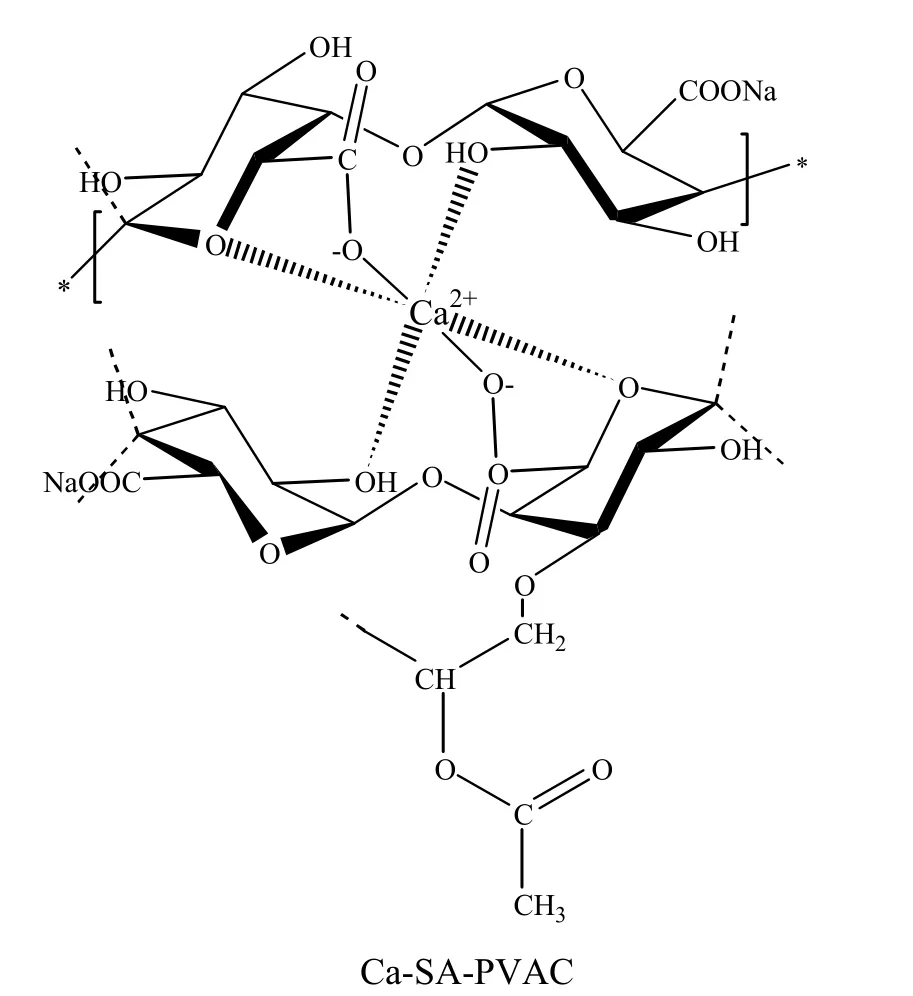
图1 PVAc改性海藻酸钙分子结构的形成机理与Ca-SA-PVAc结构示意图
2.2 微球结构分析
2.2.1 红外光谱和热重分析
图2(a)为改性前后SA的红外光谱图,从图中可知,3446.5 cm-1为O—H的伸缩振动峰,改性SA在此处的峰减弱,说明接枝反应后—OH减少;1617 cm-1和1407 cm-1分别为COO-的非对称与对称伸缩振动,改性前后峰强度不变,说明SA上的COO-没有破坏;1030 cm-1和1101.3 cm-1分别为乙酸酯类C—O非对称和对称伸缩振动的特征峰,改性SA在此处加强,说明体系羰基数量增多,则可推断聚PVAc接枝到了SA上。图2(b)为改性前后SA微球的热重分析图。在30~180 ℃,微球中自由水的迅速丢失造成质量明显下降,改性微球中由于疏水基团的引入使得自由水与改性海藻酸钙的结合力减弱,因而失水的速度更快。在 180~280 ℃,海藻酸钙上的羧基分解为 CO2,造成凝胶微球的质量进一步下降。改性微球中PVAc的引入使得失去CO2的速度稍微减缓。海藻酸钙50%失重率的温度为410 ℃,而改性海藻酸钙则为525 ℃,说明改性后微球的热稳定性提高。
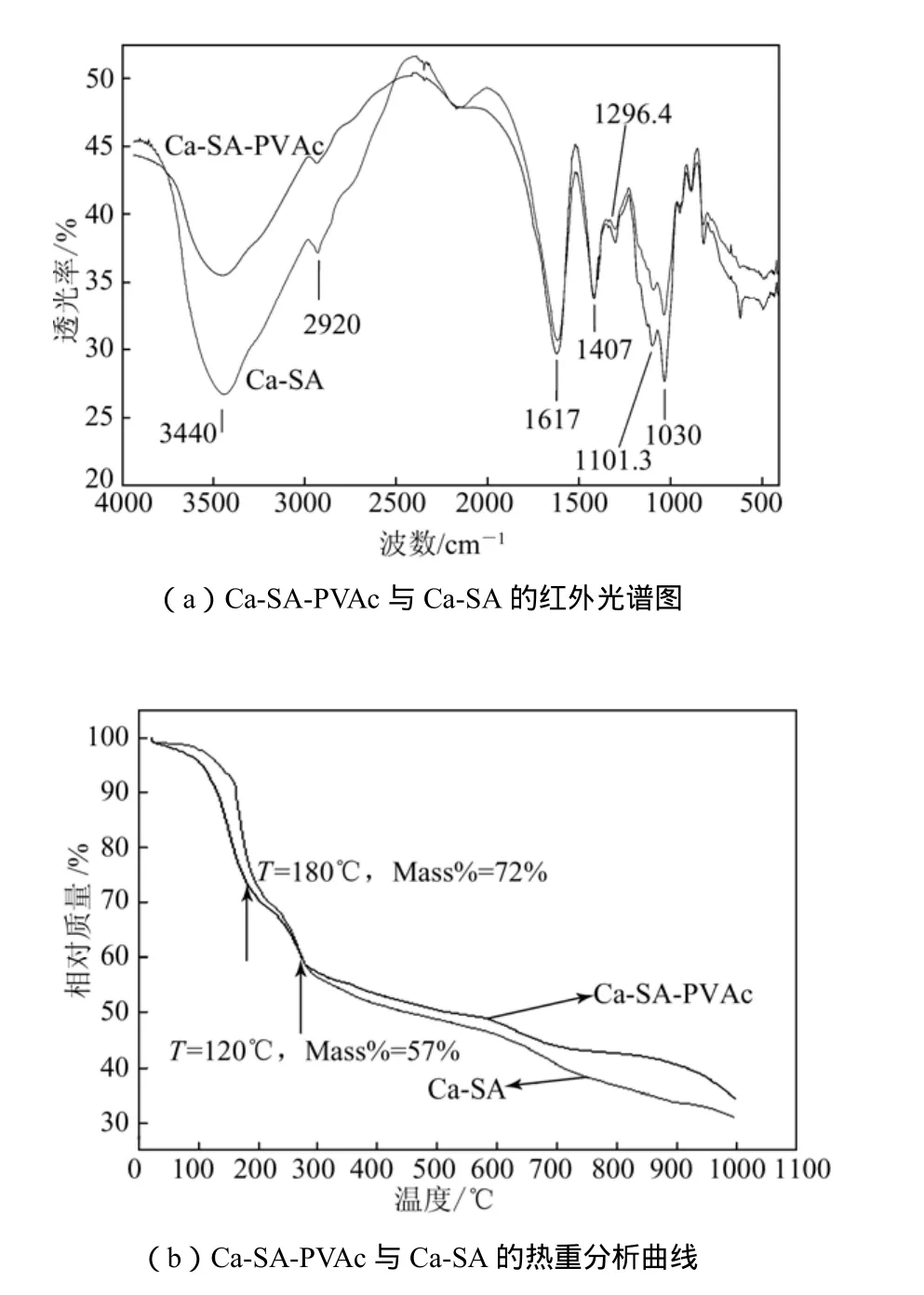
图2 SA和改性SA微球的红外光谱和热重分析图
2.2.2 SEM分析
通过 SEM可以观察微球的显微结构。如图 3所示,(a)和(c)为Ca-SA微球的SEM图,(b)和(d)为Ca-SA-PVAc微球的SEM图。(a)图的微球结构紧密,而(b)图微球表面蓬松,呈现多孔结构,(c)图微球表面布满微孔,微孔大小在微米级别,而(d)图在微米级别下微球表面平整,说明其孔隙远大于微米级别。这是由于PVAc的引入增加了疏水链段,使Ca2+交联密度下降,导致改性微球的孔隙结构发达。
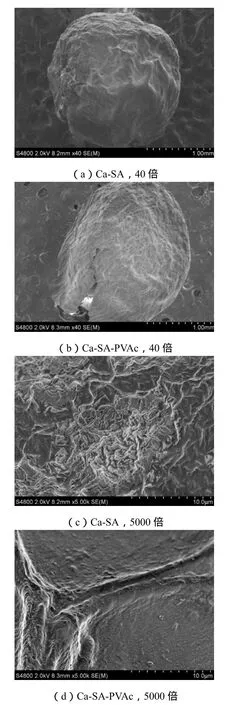
图3 干态微球的SEM图
2.3 接枝反应条件对凝胶微球溶胀度的影响
2.3.1 聚合温度对反应接枝参数和微球溶胀度的影响
如图4所示,转化率、接枝率和溶胀度的变化随反应温度整体上呈现先增后减的趋势。36~54 ℃,温度上升造成分子运动加剧,反应体系黏度下降,分子间碰撞概率加大,转化率和接枝率迅速上升;54~57 ℃,随着温度的继续升高,过多自由基之间的碰撞终止导致引发效率低下,接枝率和转化率下降。36~42 ℃,接枝率和转化率基本保持不变,因而溶胀度也基本不变;42~48 ℃,微球中PVAc含量增多使海藻酸钙中羧基密度降低,降低了钙离子交联密度,溶胀度上升;48~54 ℃,随着转化率和接枝率进一步提高,PVAc占主导地位,最终溶胀度下降;54~57 ℃,虽然接枝参数下降,但是温度的上升造成 SA引发位点的增加,PVAc构建的共价交联点增多,同时,亲水基团羟基减少,支链增多,分子间纠缠形成的物理交联作用增大,使得溶胀度下降。
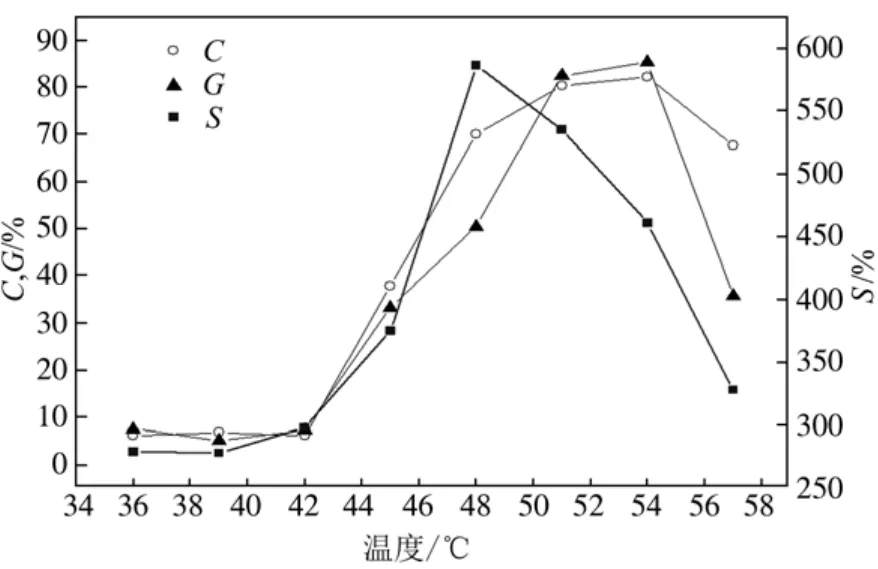
图4 温度的改变对VAc的转化率(C)、SA的接枝率(G)和溶胀度(S)的影响
图5是以lgR(Y)对1/T×103(X)的线性拟合,得出线性回归方程为Y= 20.17569-7.79197×10-3X,相关系数r=-0.93792,根据阿伦尼乌斯公式求得活化能为64.7 kJ/mol,比文献中的数据43.9 kJ/mol[5]大,由此可知接枝反应所需要的活化能较高,因而反应在36~42 ℃的低温下接枝率和转化率很低。
2.3.2 VAc含量对反应接枝参数和微球溶胀度的影响
如图6所示,当VAc的浓度由2.16×10-3mol/L变化到3.25×10-2mol/L时,转化率和接枝率呈现逐渐上升的趋势,这是由于单体浓度的增大使得单体与单体、单体与大分子自由基之间的碰撞概率增大,因而转化率与接枝率总体呈上升趋势。当 VA c浓度低于1.52×10-2mol/L时,SA的接枝率很低,这是因为在低浓度下,VAc与大分子自由基的碰撞概率少,因而降低了接枝反应发生的可能性;相对而言,此时的转化率就高了很多。当VAc浓度高于1.52×10-2mol/L时,SA的接枝率呈现逐渐增大的趋势,并且与转化率的差距逐渐缩小,这是因为随着单体浓度的增加,VAc与大分子自由基的碰撞概率逐渐增大,因而更多的单体倾向于接在海藻酸钠大分子链上。对于微球的溶胀度,当单体浓度低于1.95×10-2mol/L时,溶胀度逐渐下降,这是由于转化率和接枝率的提高,组分中PVAc的含量增多,疏水基团的增加使得微球溶胀度下降;但当单体浓度高于1.95×10-2mol/L时,随着单体含量的增加,溶胀度逐渐上升,这是由于转化率和接枝率的继续提高,羧基基团密度降低,钙离子交联也相应减少,因此溶胀度上升。由以上分析可知,聚合反应VAc浓度对接枝反应参数的影响将导致产物溶胀度的相应变化。

图5 lg R对1/T×103的线性关系
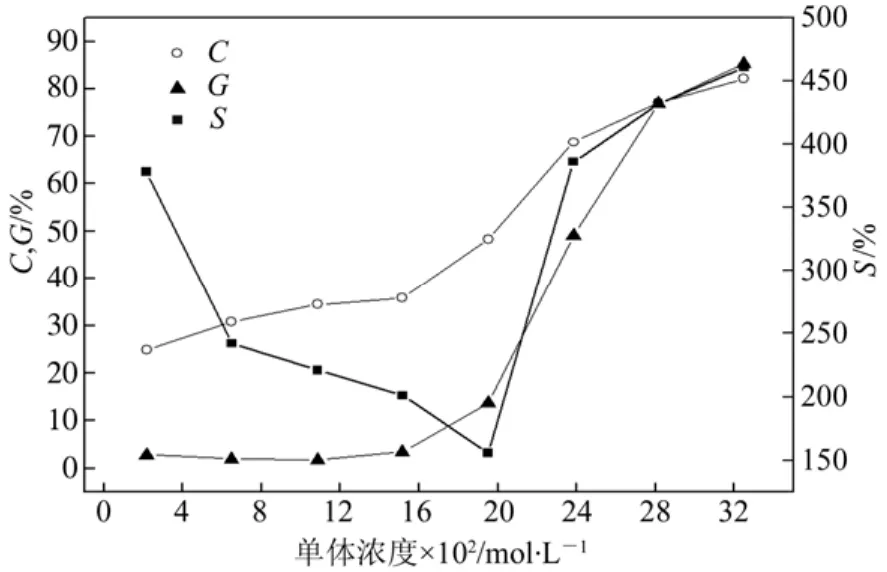
图6 VAc含量对VAc转化率(C)、SA的接枝率(G)和溶胀度(S)的影响
2.3.3 引发剂含量对微球溶胀度和形貌的影响
引发剂用量也是影响改性微球性质的重要因素。从图7中可以看出,当引发剂含量为0.17%~ 0.81%时,接枝率迅速上升,溶胀度迅速下降,这是由于随着引发剂用量的增加,大分子自由基密度增加,聚合速率加快,从而接枝率提高,疏水基团的增加使得溶胀度下降。当引发剂含量由0.97%增至1.12%时,SA的接枝率和溶胀度均下降,推测是由于过量的 KPS使得海藻酸钠上C—C键发生断裂,生成二醛结构,其反应机理如图8(a)所示,氧化的SA进一步与VAc发生接枝反应,因而溶胀度也迅速下降[15]。由于反应过程脱水,因而利用式(1)计算的接枝率与实际偏低,随着引发剂用量继续增多,SA氧化越严重,因而计算出的接枝率越小。红外分析表明[图8(b)],当引发剂浓度由0.81%增加至1.28%时,接枝产物在1737.6 cm-1处多了一个醛基振动吸收峰,说明海藻酸钠发生部分氧化反应,致使邻羟基被破坏,造成凝胶成球性能变差[图8(d)]。

图7 引发剂含量对SA接枝率(G)和微球溶胀度(S)的影响
还原剂与氧化剂的摩尔比也将影响产物的溶胀行为。如表1所示,当还原剂与氧化剂的摩尔比由0.57升到0.83时,溶胀度下降,接枝率上升。这是由于随着 Na2SO3用量的增多,引发剂的半衰期越短。自由基数量越多,海藻酸钠骨架上的接枝位点越多,促进接枝率提高,因而溶胀度由 106%迅速降到39.3%;当还原剂与氧化剂的摩尔比由0.83升到1.15时,微球的溶胀度增大,接枝率下降。这是由于随着 Na2SO3用量的继续增多,瞬间产生过多的自由基,重新碰撞并耦合的概率增加,使引发效率低,接枝率下降,溶胀度由39.3%升到158%。
2.3.4 海藻酸钠浓度对微球溶胀度的影响
如图9所示,随着海藻酸钠浓度的增加,微球的溶胀度呈现逐渐增大的趋势。这是由于随着 SA浓度的增大,反应体系的黏度增大,分子运动的阻力越大,造成VAc与大分子自由基之间的碰撞概率越少,且黏度的增加使引发剂扩散阻力增大,加剧了引发剂之间的碰撞,引发效率越低,因而SA接枝率降低,溶胀度增大。
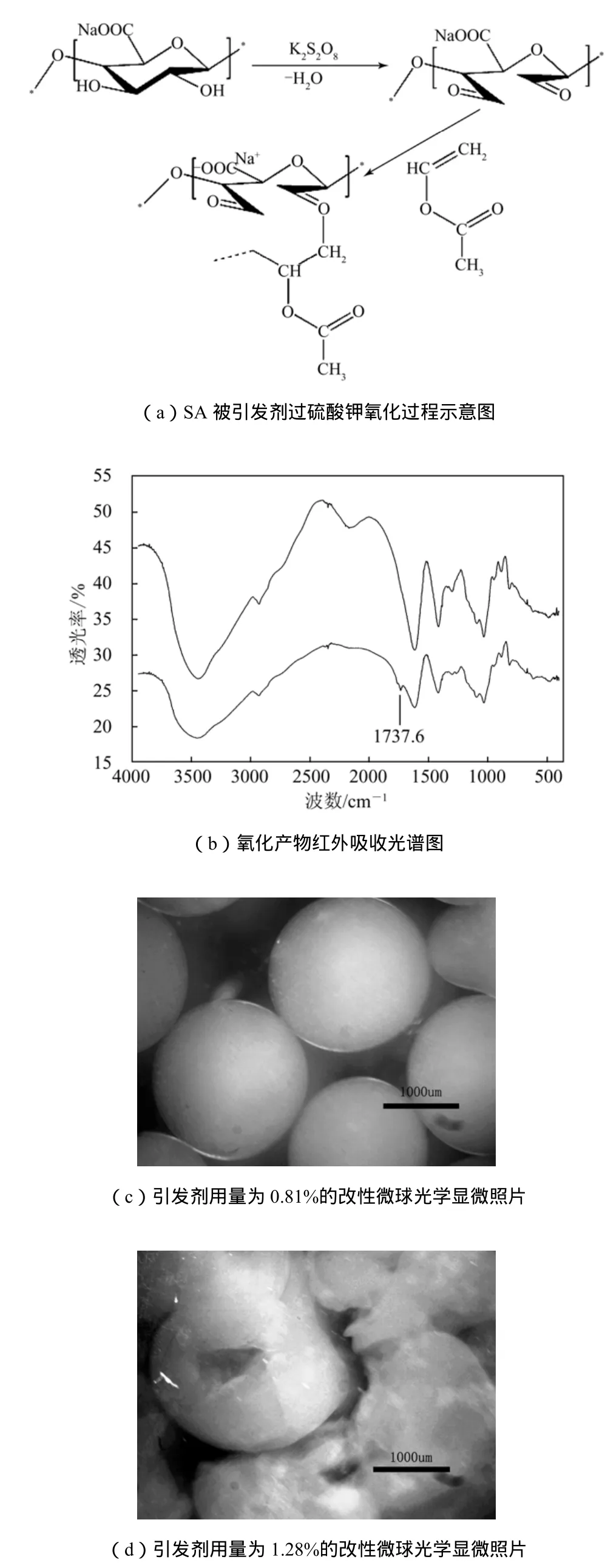
图8 引发剂含量对改性微球形貌的影响
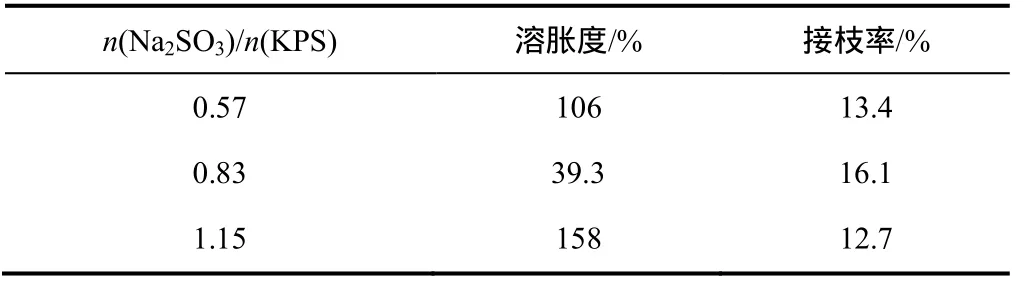
表1 还原剂与氧化剂摩尔比对微球溶胀度和接枝率的影响
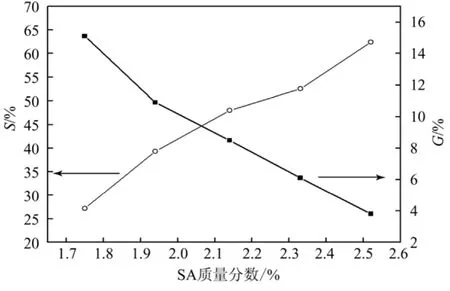
图9 SA浓度对微球溶胀度(S)的影响
2.3.5 反应时间对微球溶胀度的影响
由图10可知,反应时间由0.5 h改变到3 h,微球的溶胀度和接枝率均呈现先增加后减少的趋势。对于接枝率的这种变化,其他研究者也增作过记载。吴宏等[16]在乙酸乙烯酯接枝海藻酸钙凝胶的研究中发现,接枝率在3 h左右达到最高,然而并未作出适当的解释;Işıklan等[5]在对衣康酸接枝海藻酸钙的反应中,也发现了类似现象,并且认为其原因是海藻酸钙骨架上接枝数量的增加以及单体在接枝处的链增长。这种观点把溶胀度增长的原因直接归结为随着反应时间的延长,接枝率和转化率的同步增长带来的网络疏松和不规则化效果;而后续的溶胀度下降现象则是由于疏水性的提高和交联度的增大。作者认为,把接枝率提高作为解释溶胀度变化的原因在一定程度上是合理的,然而具有片面性。按照这种解释,当使用较高的单体浓度时,溶胀度的峰值应该出现得更早。而事实上,当使用较高浓度的单体进行改性的时候,溶胀度的峰值并未如预期一样在较短的时间出现。原因就是这种理论并未考虑到齐聚物的生成。而在海藻酸钠溶液中,高分子溶液的黏度对自由基运动的阻碍作用又是十分明显的。因此必然生成少量游离在海藻酸钙网络中的乙酸乙烯酯齐聚物。溶胀度的变化也与这种现象有关。
如图 10可知,保持其它条件不变,令乙酸乙烯酯的浓度分别为0.065 mol/L和0.13 mol/L,溶胀度峰值几乎同时出现,而VAc含量为0.13 mol/L的样品溶胀度明显高于0.065 mol/L,这是因为随着VAc浓度的增高,接枝于海藻酸钠链段上的乙酸乙烯单体数量并未有显著变化;而生成于海藻酸钠网络之间的齐聚物数量则有增多的趋势。一方面齐聚物填充于海藻酸钙网络中间,造成网络结构疏松、羧基密度减少;另一方面由于过多的齐聚物阻碍了海藻酸钙的桥接结构的生成,钙离子的交联密度降低,最终导致溶胀度的偏高。当反应时间大于1.5 h,大分子链段之间的共价交联作用导致溶胀度下降。
2.3.6 CaCl2浓度对微球溶胀度和形貌的影响
如图11所示,CaCl2浓度由1% g/g变化到5% g/g,溶胀度呈现迅速下降的趋势。这是由于钙离子交联密度的增加导致三维网络结构更加紧凑,最终导致微球溶胀度的下降。当钙离子过量时,两个以上的海藻酸分子链与过量的钙离子共同作用,产生“凝胶带”,水凝胶网络变得更加致密,因而溶胀度降低[17]。当CaCl2浓度大于4.5%时,微球的成球性能变差。这由于随着CaCl2浓度的增加,溶液密度增大,使滴下的微球不能立刻与Ca2+发生交联反应,未交联的SA由于自身的流动性而变形。
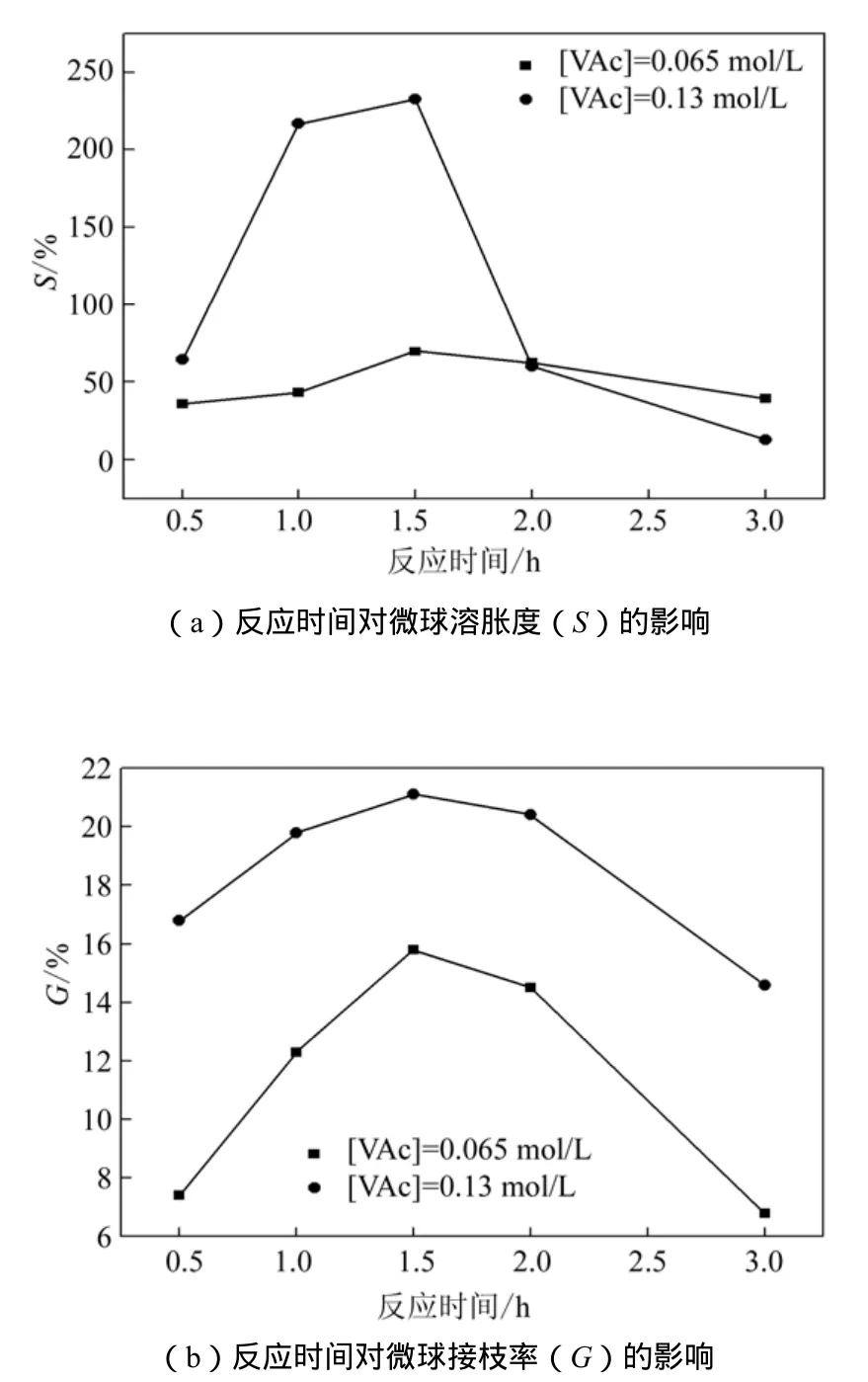
图10 不同单体浓度下,反应时间对微球溶胀度及接枝率的影响
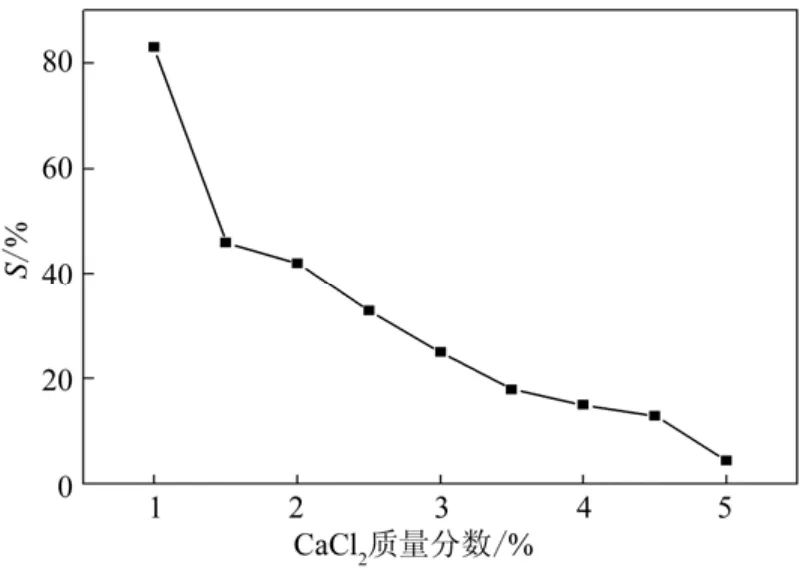
图 11 CaCl2浓度对微球溶胀度(S)的影响
3 结 论
鉴于PVAc的疏水性以及在海藻酸钙分子链之间形成的共价交联作用,将乙酸乙烯酯聚合物链段接枝到海藻酸钙上,可以改变和调节海藻酸钙凝胶微球的溶胀度。影响改性凝胶微球溶胀度的主要因素是钙离子的交联密度、乙酸乙烯酯接枝率和 SA的转化率、聚合物的物理交联密度等。在较高反应程度的范围内,溶胀度随着接枝率和转化率升高而降低,这是引入疏水基团、共价交联点生成共同作用的结果。但当反应程度较低时,乙酸乙烯酯接枝率和转化率的上升导致钙离子交联密度的下降;同时,较多齐聚物在海藻酸钙网络中形成孔隙,阻碍了钙离子桥接结构的生成,从而使溶胀度升高。随着钙离子交联密度的增加,凝胶微球的三维网络结构稳定,抗溶胀能力增大。此外,聚合物的物理交联密度受到海藻酸钠溶液浓度的影响,也会改变微球的溶胀度。乙酸乙烯酯接枝改性海藻酸钙凝胶微球的溶胀度可控,提高了海藻酸盐凝胶类吸附分离功能材料的结构稳定性,为凝胶微球类功能材料的制备提供了一种新型途径。
[1] Pasparakis George,Bouropoulos Nikolaos. Swelling studies and in vitro release of verapam il from calcium alginate and calcium alginate–chitosan beads[J].International Journal of Pharmaceutics,2006,323(1):34-42.
[2] Mandal Sanchita,Kumar Basu Sanat,Sa Biswanath. Ca2+ion cross-linked interpenetrating network matrix tablets of poly acrylam ide-grafted-sodium alginate and sodium alginate for sustained release of diltiazem hydrochloride[J].Carbohydrate Polymers,2010 82(3):867-873.
[3] Yang Jisheng,Xie Yingjian,He Wen. Research progress on chem ical modification of alginate:A review[J].Carbohydrate Polymers,2011,84(1);33-39
[4] 张连飞,宋淑亮,粱浩,等. 海藻酸钠接枝聚合物研究进展[J]. 中国生化药物杂志,2009,30 (4):281-284.
[5] Işıklan Nuran,Kurşun Fatma,Inal Murat. Graft copolymerization of itaconic acid onto sodium alginate using benzoyl peroxide[J].,Carbohydrate Polymers,2010,79(3):665-672.
[6] Gao Chunmei,Liu M ingzhu,Chen Shilan,et al. Preparation of oxidized sodium alginate-graft-poly [(2-dimethylam ino) ethyl methacrylate] gel beads andin vitrocontrolled release behavior of BSA[J].International Journal of Pharmaceutics,2009,371(1) :16-24.
[7] Laurienzo P,Malinconico M,Motta A,et al. Synthesis and characterization of a novel alginate-poly(ethylene glycol) graft copolymer[J].Carbohydrate Polymers,2005,62(3):274-282.
[8] Yadav M ithilesh,Kumar M ishra Dinesh,Sand Arpit,et al. Modification of alginate through the grafting of 2-acrylam idoglycolic acid and study of physicochemical properties in terms of swelling capacity,metal ion sorption,flocculation and biodegradability[J].Carbohydrate Polymers, 2011,84(1):83-89.
[9] Sand Arpit,Yadav M ithilesh,Kumar Mishra Dinesh,et al. Modification of alginate by grafting ofN-vinyl-2-pyrrolidone and studies of physicochem ical properties in terms of swelling capacity,metal-ion uptake and flocculation [J].Carbohydrate Polymers,2010, 80(4):1147-1154.
[10] 英晓光,张凤菊,张立广,等. 互穿网络改性的蛋白质印迹海藻酸钙微球[J]. 天津大学学报,2011,44(2):134-140
[11] 李志勇,倪才华,熊诚,等. 海藻酸钠的疏水改性及释药性能研究[J]. 化学通报,2009,1:93-96.
[12] Davidovich-Pinhas Maya,Bianco-Peled Havazelet. A quantitative analysis of alginate swelling [J].Carbohydrate Polymers,2010 ,79(4) :1020-1027.
[13] Ying Xiaoguang,Cheng Guoxiang,Liu Guipei,et al. Specific rebinding property of protein macromolecularly imprinted polymer m icrospheres based on calcium alginate hydrogelviagas jetting-dropping method[J].Journal of Applied Polymer Science,2010,117(4):2331-2339
[14] Thom David,Grant Gregor T,Morris Edw in R,et al. Characterization of cation binding and gelation of polyuronates by circular dichroism[J].Carbohydrate Research,1982,100(1):29-42
[15] Sen G,Singh P,Pal S. M icrowave-initiated synthesis of polyacrylamide grafted sodium alginate: Synthesis and characterization[J].Journal of Applied Polymer Science,2010,115:63-71
[16] 吴宏,萧聪明,林小东,等. KSP引发乙酸乙烯酯与海藻酸钙小球接枝共聚反应[J].化工科技,2002,10(5):17-18.
[17] Marit Sletmoen,Kurt I Draget,Bjørn T Stokke. Alginate oligoguluronates as a tool for Tailoring properties of Ca-Alginate gels[J].Macromolecular Symposia,2010,291-292(1):345-353.
Preparation of polyvinyl acetate-grafted-calcium alginate beads
QI Liangliang,YING Xiaoguang,LI Xiao,ZHANG Weiying,XU Wen
(School of Chemistry & Chemical Engineering,Fuzhou University,Fuzhou 350108,Fujian,China)
In order to reduce the swelling ratio of calcium alginate beads,vinyl acetate (VAc) was grafted on sodium alginate (SA) by free radical copolymerization,and vinyl acetate grafted calcium alginate (Ca-SA-PVAc) beads w ith low swelling ratio were prepared. FTIR indicated that new chemical bond was formed in modified alginate molecule. TGA showed that the rate of bound moisture loss of modified alginate beads was changed and its heat stability was improved. SEM showed that Ca-SA-PVAc beads had well-developed pore structure. The effects of reaction conditions,such as grafting reaction temperature,monomer and initiator concentrations,percentage of alginate and calcium chloride,grafting reaction time on swelling ratio in 0.9%NaCl solution were studied. By changing reaction conditions and consequently grafting reaction parameters,the swelling ratio of grafted beads could be controlled.
sodium alginate;vinyl acetate;grafting reaction;swelling ratio;hydrogel m icrosphere
O 636.1+1
A
1000–6613(2012)–07–1555–08
2012-02-23;修改稿日期:2012-03-02。
福州大学科技发展基金(2010-XY-8)及福建省教育厅科技计划A类(JA11021)项目。
漆亮亮(1986—),男,硕士研究生。联系人:英晓光,讲师,硕士生导师。E-mail yxg@fzu.edu.cn。
