基于荧光共轭聚电解质的小檗碱检测
2012-10-19黄红梅
肖 毅,何 娟,黄红梅,李 莎
(化学生物学及中药分析教育部重点实验室,湖南师范大学化学化工学院,湖南长沙410081)
0 引言
共轭聚合物作为一种具有π-π*共轭分子导线结构和显著放大效应的新型荧光探针,在化学和生物传感研究方面倍受瞩目[1]。共轭聚电解质把共轭聚合物的光电性质和聚电解质的水溶性结合起来,具有检测简便、灵敏度高、响应快和适用范围广等特点,可用于水环境以及生命体系中的传感检测,并可进一步提高对于带有相反电荷猝灭剂检测的灵敏度。近年来,共轭聚电解质已被广泛用于蛋白质[2~3]、DNA[4]、糖类[5]等生物分子以及水环境中金属离子[6]的检测。
小檗碱是重要的季铵类生物碱,具有显著的抗微生物活性[7],已广泛用于治疗细菌性痢疾,肠内寄生虫感染和沙眼感染。此外,小檗碱还具有抗肿瘤和抗糖尿病的疗效[8~9]。目前已报道的用于定量检测小檗碱的方法主要有荧光分析法[10]、分光光度法[11]、电化学法[12]及高效液相色谱法[13]等。其中荧光分析法具有快速、灵敏、选择性好的优点,但基于共轭聚电解质的荧光分析法用于小檗碱等药物的定量检测还很少有报道。
该文首次以含磺酸根侧链的PPE类共轭聚电解质PPESO3作为探针,基于阴离子磺酸侧链与小檗碱季铵阳离子的静电相互作用,PPESO3的荧光可被小檗碱显著猝灭,从而建立了高灵敏检测小檗碱的新方法。这为进一步拓展共轭聚合物在药物方面的监测奠定了基础,同时也为研究药物与大分子之间的相互作用提供了借鉴。
1 实验部分
1.1 仪器与试剂
荧光光谱在F-4500荧光光谱仪(日立)上测定;紫外可见光谱在UV-2450紫外可见分光光度计(日本岛津)上测定;1H NMR在核磁共振仪Bruker DMX 500上测定,DMSO-d6为溶剂。
PPESO3配成 2.54×10-4mol/L 的储备液 (浓度以重复单元计);小檗碱(购于湖南省药检所)配成2.53×10-3mol/L的储备液;所有的试剂均为市售分析纯,实验用水为超纯水。 pH=1.00~9.00的柠檬酸-磷酸氢二钠(H3Cit-Na2HPO4)缓冲体系用 0.1 mol/L柠檬酸和 0.2 mol/L磷酸氢二钠配制,pH < 2.20,pH > 8.00 的缓冲溶液分别用盐酸和氢氧化钠调节。
1.2 实验方法
1.2.1 PPESO3的合成
参照文献[14~15]方法通过Sonogashira偶联反应合成PPESO3、P1,其化学结构式如图 1所示,并通过核磁共振、红外等对其结构进行了确认。
图1 PPESO3,P1的结构示意图Fig.1 The structures of PPESO3and P1
1.2.2 荧光光谱
PPESO3储备液用缓冲液稀释至 5.0×10-6mol/L,取2 mL置于比色皿中,检测其荧光强度I0(λex/em=438/533 nm)。加入不同浓度小檗碱溶液(体积小于10 μL),稳定后检测荧光强度I。以I0/I衡量其对PPESO3的荧光猝灭效率。P1(λex/em=401/424 nm)与小檗碱的作用采用上述同样的步骤进行分析。
1.2.3 紫外吸收光谱
用缓冲液将PPESO3储备液稀释至3.0×10-5mol/L,取2 mL底液置于比色皿中,加入不同浓度的小檗碱(体积小于10 μL),测量混合溶液的紫外吸收光谱。
2 结果与讨论
2.1 PPESO3对小檗碱的荧光响应
图2考察了PPESO3对小檗碱的响应。从图可以看出,随着小檗碱浓度增加,PPESO3的荧光强度显著下降,而其最大发射峰位置没有发生改变。进一步地研究可知,小檗碱的浓度在7.5×10-8mol/L~4.0×10-6mol/L 范围内与 PPESO3的荧光猝灭程度I0/I呈良好的线性关系,检出限达到8.7×10-9mol/L(S/N=3), 其相应的线性回归方程和相关系数分别为 y=0.426 77+0.017 63x,r=0.997 9, 小檗碱猝灭 PPESO3的 Stern-Volmer常数 KSV为 1.76×107L/mol, 这 说 明 小 檗 碱 与PPESO3有很强的相互作用,这可能与PPESO3的磺酸基阴离子侧链与小檗碱的季铵阳离子之间可以通过静电作用有关。因此,可以通过测定PPESO3的荧光猝灭程度来定量检测小檗碱。
2.2 离子侧链对小檗碱的荧光响应影响
为了证实侧链电荷对小檗碱的检测起主导作用,考察了带相反电荷侧链的共轭聚电解质对小檗碱传感放大性能的影响。图3给出了季铵根阳离子侧链的P1加入小檗碱后引起其荧光猝灭的效率。从图可以看出,小檗碱猝灭PPESO3(KSV为 1.76×107L/mol)的效率是 P1 的(KSV=3.49×105L/mol)50.4倍。P1具有与PPESO3类似的共轭结构,猝灭效果却远不及PPESO3。这说明PPESO3对小檗碱高灵敏的响应主要是由于带负电侧链磺酸基与生物碱小檗碱的季铵阳离子通过强的静电相互作用形成复合物,导致了PPESO3的荧光被显著地猝灭;而小檗碱即使在高浓度时对P1的猝灭效果也不明显,这可能与季铵根侧链与小檗碱的季铵阳离子之间存在静电相互排斥作用使得P1与小檗碱的距离拉远,难以相互靠近有关。
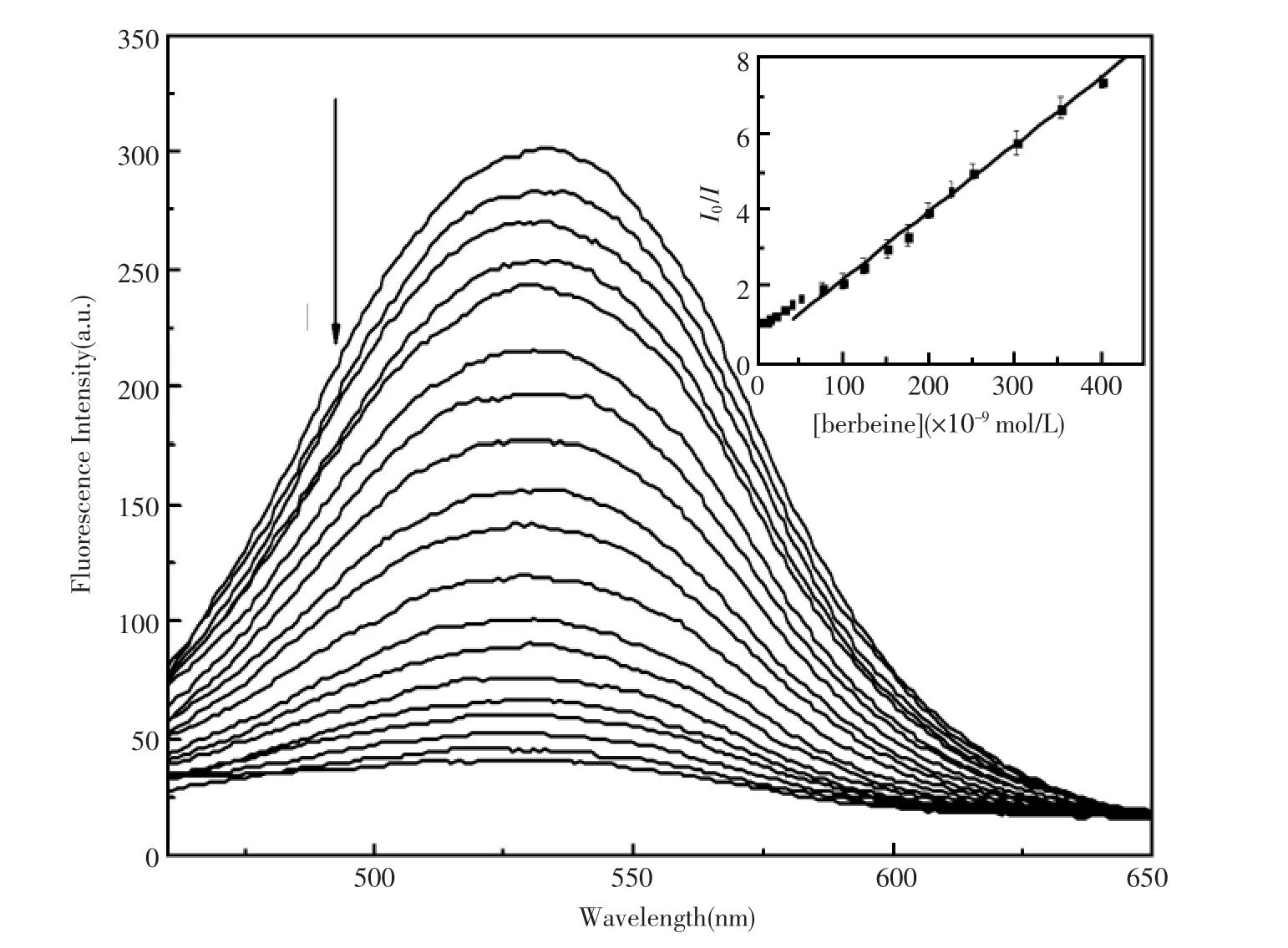
图2 PPESO3中加入不同浓度的小檗碱后的荧光光谱(λex/em=438/533 nm,pH=2.00)插图:荧光猝灭效率(I0/I)随小檗碱浓度变化的工作曲线[PPESO3]=5.0×10-6mol/LFig.2 Fluorescence spectra of PPESO3(5.0×10-6mol/L)with successive addition of berberine at pH2.00 Inset:Plot of the relative fluorescence quenching(I0/I)of PPESO3as a function of different concentration of berberine
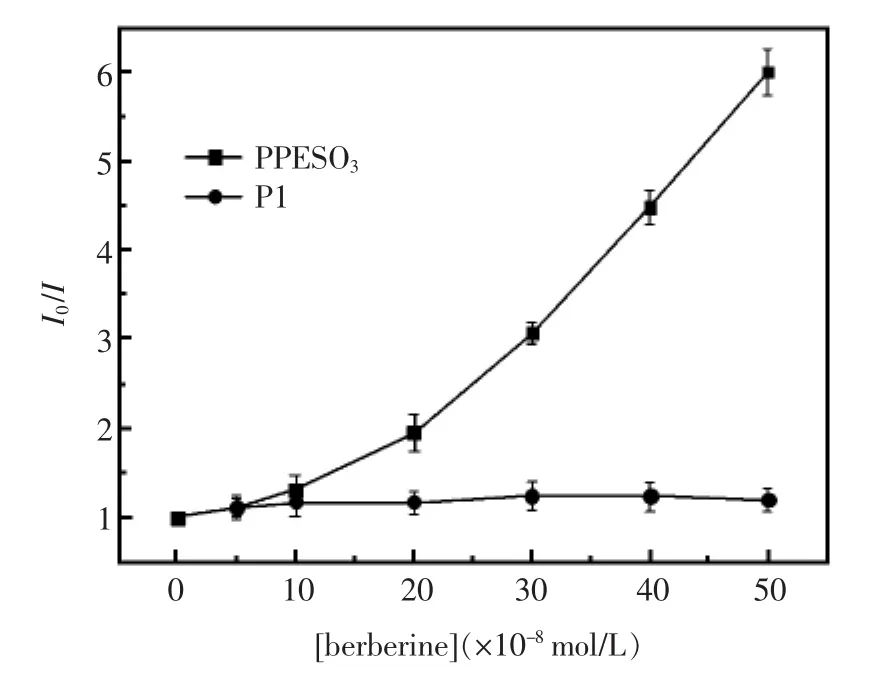
图3 不同浓度的小檗碱猝灭PPESO3,P1溶液的荧光[PPESO3]=[P1]=5.0×10-6mol/LFig.3 The fluorescence quenching of PPESO3,P1 by different concentrations of berberine.[PPESO3]=[P1]=5.0×10-6mol/L
2.3 小檗碱与PPESO3相互作用的紫外-可见光谱
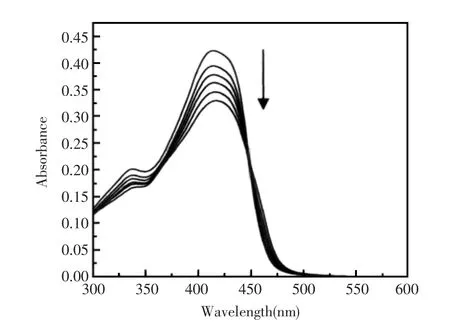
图4 PPESO3加入小檗碱后的紫外-可见吸收光谱图(pH=2.00的柠檬酸-磷酸氢二钠缓冲液)Fig.4 UV-vis absorption spectra of PPESO3in the presence of various concentration of berberine(0,1.0×10-7,3.0×10-7,5.0×10-7,7.0×10-7,1.0×10-6mol/L)in Na2HPO4-H3Cit buffer solution at pH2.00.[PPESO3]=3.0×10-5mol/L
小檗碱与PPESO3作用的紫外-可见吸收光谱见图4,从图中可以看出,PPESO3在416 nm处存在特征吸收峰,随着小檗碱的加入,特征吸收峰发生减色效应,同时伴随着轻微红移,说明了小檗碱与含磺酸侧链的阴离子共轭聚电解质PPESO3发生了相互作用。而含季铵阳离子侧链的P1在加入小檗碱后,特征吸收峰并未发生红移现象,说明静电作用在小檗碱与PPESO3的相互作用中占主导地位。
2.4 pH对小檗碱猝灭PPESO3荧光的影响
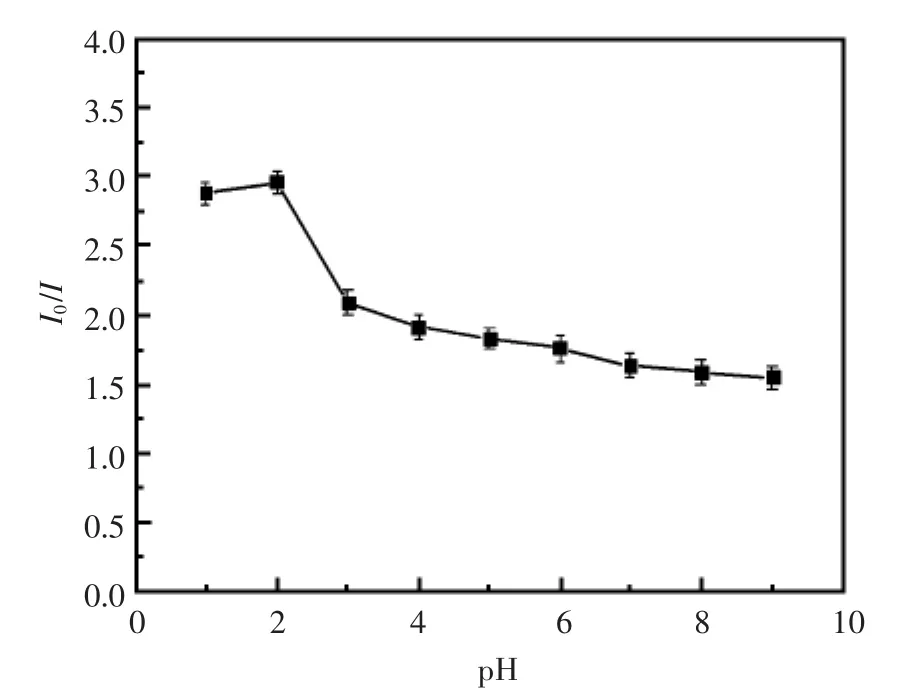
图5 不同pH柠檬酸-磷酸氢二钠缓冲溶液中小檗碱对PPESO3的荧光猝灭Fig.5 The effect of pH on the PPESO3(5.0×10-6mol/L)fluorescence quenching(I0/I)by berberine(1.4×10-7mol/L)in H3Cit-Na2HPO4buffer solution
图5考察了pH对小檗碱猝灭PPESO3的荧光效率的影响。从图中可以看出,当pH>2.00时,随着pH的增加,荧光猝灭效率逐渐下降,这可能是由于缓冲溶液中的阴离子竞争性地与小檗碱的季铵阳离子发生静电相互作用,从而导致了PPESO3与小檗碱之间的作用减弱。而当pH<2.00时,小檗碱对PPESO3的荧光猝灭影响不大,略有降低。以下实验选择pH=2.00进行。
2.5 反应时间的考察
在 H3Cit-Na2HPO4(pH=2.00)缓冲溶液中,考察PPESO3/小檗碱相互作用达到稳定所需要的时间。结果表明,体系达到稳定所需要的时间在1~2 min之内,PPESO3作为探针可实现对小檗碱的快速检测。
2.6 干扰检测
为了评价该方法对小檗碱检测的选择性,考察了金属离子、氨基酸和维生素等对小檗碱检测的影响。在pH=2.00的H3Cit-Na2HPO4缓冲溶液中,PPESO3浓度为 5.0×10-6mol/L,小檗碱浓度为1.4×10-7mol/L,加入干扰物后的相对误差如表1所示。结果表明,大部分外来物质,如常见的金属离子Li+、Mg2+,氨基酸GSH和维生素C等在很高的浓度水平而对PPESO3的小檗碱检测影响不大。然而,一些重金属离子,如Cu2+、Pb2+对检测的干扰较大,能容忍的浓度水平较低。与小檗碱具有类似结构的生物碱对PPESO3的荧光也具有显著的猝灭效果,因此,PPESO3可作为水环境中选择性检测生物碱的荧光探针。
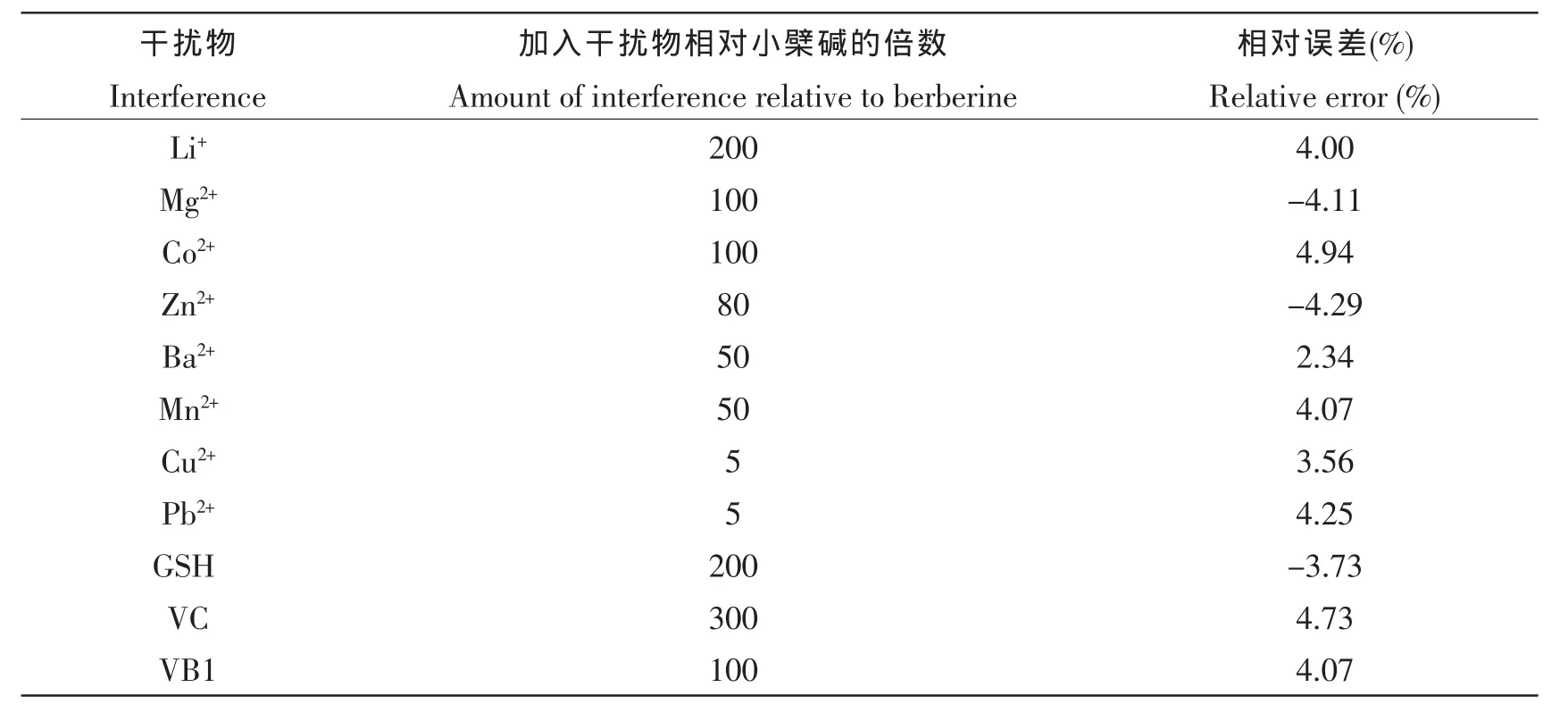
表1 干扰物对PPESO3检测小檗碱的影响Tab.1 Effect of interferences on the detection of berberine
3 结论
该文利用阴离子型共轭聚电解质作为荧光探针,基于其与小檗碱有很强的静电结合作用引起了共轭聚电解质荧光显著地猝灭,发展了一种简便、快速、高灵敏度地检测小檗碱的新方法。结果表明,在优化条件下,采用该方法检测小檗碱的线性范围为 7.5×10-8mol/L~4.0×10-6mol/L,检出限为8.7×10-9mol/L(S/N=3)。该方法拓展了共轭聚合物在药物方面的检测应用,并为探究药物与大分子之间的相互作用提供了可能的途径。
[1]Thomas S W,Joly D G,Swager T M.Chemical sensors based on amplifying fluorescent conjugated polymers[J].Chem.Rev.,2007,107:1 339~1 386.
[2]Feng X,Liu L,Wang S,et al.Water-soluble fluorescent conjugated polymers and their interactions with biomacromolecules for sensitive biosensors[J].Chem.Soc.Rev,2010,39(7):2 411~2 419.
[3]Aberem M B,Najari A,Ho H A,et al.Protein detecting arrays based on cationic polythiophene-DNA-aptamer complexes[J].Adv.Mater.,2006,18:2 703~2 707.
[4]Brouard D,Viger M L,Bracamonte A G,et al.Label-free biosensing based on multilayer fluorescent nanocomposites and a cationic polymeric transducer[J].ACS Nano,2011,5(3):1 888~1 896.
[5]DiCesare N,Pinto M R,Schanze K S,et al.Saccharide detection based on the amplified fluorescence quenching of a water-soluble poly(phenylene ethynylene)by a boronic acid functionalized benzyl viologen derivative[J].Langmuir,2002,18(21):7 785~7 787.
[6]Hu Y Q,Xiao Y,Huang H M,et al.An anion-conjugated polyelectrolyte designed for the selective and sensitive detection of silver(I)[J].Chem.Asian J.,2011,6:1 500~1 504.
[7]国家药典委员会编.中华人民共和国药典 (一部)[M].北京:化学工业出版社,2005,214.
[8]Fukuda K,Hibiya Y,Mutoh M,et al.Inhibition by berberine of cyclooxygenase-2 transcriptional activity in human colon cancer cells[J].J Ethnopharmacol,1999,66(2):227~233.
[9]Chueh W H,Lin J Y.Berberine,an Isoquinoline Alkaloid in Herbal Plants,Protects Pancreatic Islets and Serum Lipids in Nonobese Diabetic Mice[J].J.Agric.Food Chem,2011,59(14):8 021~8 027.
[10]Cao M,Liu M G,Cao C,et al.A simple fluorescence quenching method for berberine determination using water-soluble CdTe quantum dots as probes[J].Spectrochimica Acta Part A,2010,75:1 043~1 046.
[11]Sakai T.Spectrophotometric determination oftrace amounts of quaternary ammonium salts in drugs by ionpair extraction with bromophenol blue and quinine[J].Analyst,1983,108:608~614.
[12]洪如.小檗碱的电化学行为研究[J].化学工程与装备,2010,(7):26~27.
[13]郭锦明,王跃飞,胡丽萍.黄连生物碱的HPLC-MS分析 [J].中成药,2011,33(1):110~113.
[14]张涛,范宏亮,周建光,等.重要传感材料荧光共轭聚合物PPESO3的一种新的简便合成路线[J].高等学校化学学报,2006,27(5):853~855.
[15]Pu K Y,Pan S Y H,Liu B.Optimization of interactions between a cationic conjugated polymerand chromophore-labeled DNA for optical amplification of fluorescent sensors[J].J.Phys.Chem.B,2008,112(31):9 295~9 300.
