替比夫定治疗乙型肝炎e抗原阳性慢性乙型肝炎48周疗效观察和安全性评价
2012-10-17刘幼昆
方 清 艾 丽 刘幼昆
三峡大学第一临床医学院 湖北省宜昌市中心人民医院感染性疾病科,湖北宜昌 443000
乙型肝炎病毒(HBV)感染可能导致急慢性肝炎。全球大约有三分之一的人过去或现在感染HBV,其中约有3.6亿为慢性感染者[1-2]。持续的HBV感染可能进展为肝纤维化,肝硬化和肝细胞癌[3-4]。治疗慢性乙型肝炎(CHB)的首要目标是清除或持久性抑制HBV在体内的复制,从而减轻肝脏的炎症、坏死和纤维化病变,减少和阻止肝硬化及肝细胞性癌的发生[5]。替比夫定(Telbivudine,LdT)为人工合成的胸腺嘧啶脱氧核苷类抗乙肝病毒HBV药物,是美国食品与药品安全管理局2006年10月、中国国家食品药品监督管理局2007年2月批准的第四种抗病毒药物,为慢性乙肝的抗病毒治疗提供了更多的选择。本研究旨在观察替比夫定治疗乙型肝炎e抗原(HBeAg)阳性慢性乙型肝炎患者的临床疗效和安全性,期望为CHB患者制订更加有效的核苷(酸)类似物抗病毒治疗方案提供更充分的依据。
1 资料与方法
1.1 一般资料
2009年8月~2010年8月三峡大学第一临床医学院宜昌市中心医院感染科就诊的HBeAg阳性慢性乙型肝炎患者100例,诊断均符合2005年《慢性乙型肝炎防治指南》的诊断分型标准[5]。采用随机分组方法进行实验对比,全部病患均属于自愿接受实验,符合本组的选择标准,将符合入组标准者按1∶1随机分配到治疗组和对照组。研究共纳入患者100例,其中,治疗组49例,对照组51例。两组的人口学特点和基线特征总体上保持均衡,差异无统计学意义(P>0.05),具有可比性。见表1。
表1 两组一般资料比较(±s)
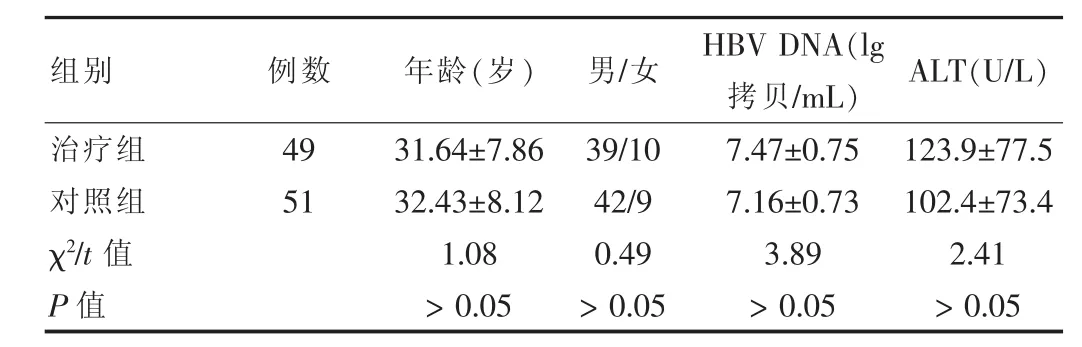
表1 两组一般资料比较(±s)
组别 例数 年龄(岁) 男/女 HBV DNA(lg拷贝/mL) ALT(U/L)治疗组对照组χ2/t值P值49 51 31.64±7.86 32.43±8.12 1.08>0.05 39/10 42/9 0.49>0.05 7.47±0.75 7.16±0.73 3.89>0.05 123.9±77.5 102.4±73.4 2.41>0.05
1.2 入选标准和排除标准
入选标准:有慢性HBV感染史,乙型肝炎表面抗原(HBsAg)阳性>6 个月,HBeAg阳性,年龄>16 岁;罗氏 Cobas amplicor HBV monitor方法检测HBV DNA水平≥106拷贝/mL;丙氨酸氨基转移酶(alanine aminotransferase,ALT)在正常值1.5~10.0 倍正常值上限范围;血清总胆红素≤42.75 μmol/L;凝血酶原时间比正常值延长不大于3 s或国际标准化比率≤2.23;血清白蛋白≥30 g/L;血清肌酸酐水平<1.5倍正常值上限;治疗前6个月内未接受过抗病毒治疗。
排除标准:合并甲型肝炎病毒 (HAV)、丙型肝炎病毒(HCV)、丁型肝炎病毒(HDV)、戊型肝炎病毒(HEV)、艾滋病病毒(HIV)感染;合并自身免疫性或代谢性肝病,药物性肝炎;肝脏失代偿表现(如肝性脑病、腹水等)和(或)失代偿性肝硬化者。
1.3 方法
治疗组和对照组分别接受每天1次口服600 mg替比夫定(商品名:素比伏,诺华公司)和10 mg阿德福韦酯(商品名:代丁,天津药物研究院药业有限责任公司)治疗,疗程均为48周,排除其他的用药及治疗方法。治疗效果监测指标为:血清HBV DNA下降,HBV DNA转阴,HBeAg血清转换,ALT复常等。
1.4 检测
血清HBV DNA定量PCR法检测采用罗氏Cobas amplicor HBV monitor,Qiagen公司血清核酸抽提试剂,其最低检测值为300拷贝/mL。血清ALT检测采用HITACHI 7170型全自动生化分析仪检,正常值上限为40 U/mL。血清HBV免疫标志物(HBVM)采用酶联免疫吸附法(上海科华生物公司试剂)测定。上述检测,在治疗前,治疗12、24、48周各进行1次。疗效的主要监测指标为:血清HBV DNA下降,HBV DNA转阴,HBeAg血清学转换,ALT复常等。
1.5 统计学方法
采用SPSS 13.0软件进行统计分析,计量资料采用均数±标准差(±s)表示,两独立样本的计量资料采用t检验,重复测量的计量资料采用方差分析,计数资料和率的比较采用χ2检验,秩和检验评价安全性指标。以P<0.05为差异有统计学意义。
2 结果
2.1 两组治疗前后血清HBV DNA水平比较
治疗前两组血清HBV DNA水平差异无统计学意义,随治疗时间延长,HBV DNA水平均出现明显下降,特别是在12周时下降幅度最为明显。48周时,治疗组血清HBV DNA平均下降值高于对照组,差异有高度统计学意义(P<0.01)。见表2。
表2 两组治疗前后血清HBV DNA水平比较(±s,lg拷贝/mL)
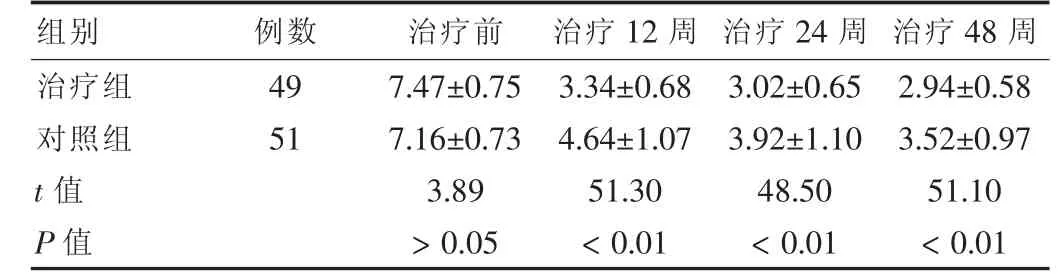
表2 两组治疗前后血清HBV DNA水平比较(±s,lg拷贝/mL)
组别 例数 治疗前 治疗12周 治疗24周 治疗48周 治疗组对照组49 51 t值 P值7.47±0.75 7.16±0.73 3.89>0.05 3.34±0.68 4.64±1.07 51.30<0.01 3.02±0.65 3.92±1.10 48.50<0.01 2.94±0.58 3.52±0.97 51.10<0.01
治疗期间治疗组的血清HBV DNA转阴率均明显高于对照组,尤其是在12周时最为明显。在48周时,治疗组血清HBV DNA转阴率为65.3%,而对照组为41.2%,差异有高度统计学意义(P<0.01)。见表3。
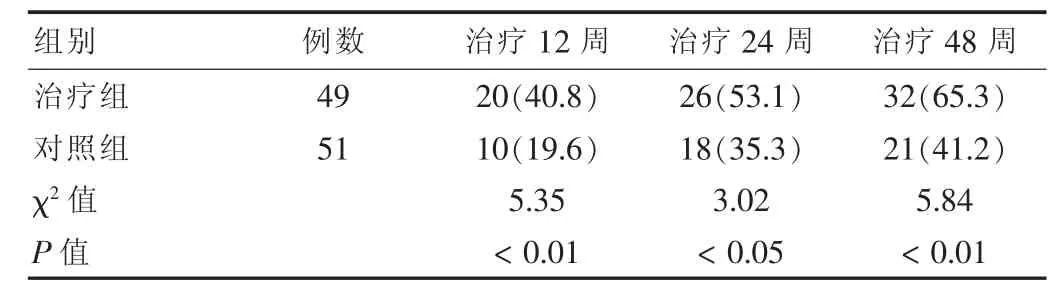
表3 两组治疗前后HBV DNA转阴情况比较[n(%)]
2.3 两组各治疗时间点血清HBeAg转换情况比较
治疗48周,治疗组和对照组的血清HBeAg血清转换率分别为18.4%和11.8%,差异无统计学意义(P>0.05)。见表4。
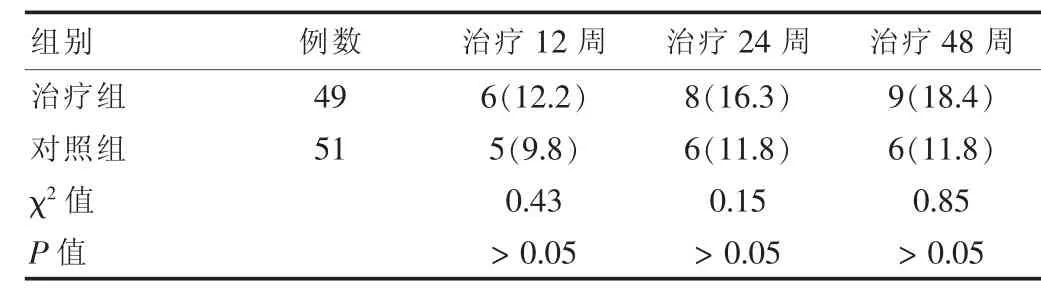
表4 两组各治疗时间点血清HBeAg转换率比较[n(%)]
2.4 两组ALT复常情况比较
治疗48周时,治疗组和对照组的血清ALT复常率分别为 73.5%(36/49)和 68.6%(35/51),差异无统计学意义(P >0.05)。
2.5 安全性分析
两组患者总的不良事件发生率分别为53.1%(26/49)和52.9%(27/51),差异无统计学意义(P > 0.05)。 两组不良事件基本相同,主要是上呼吸道感染、轻度的全身乏力、头痛、恶心、皮疹、腹泻、血肌酸肌酶(CK)升高等。
3 讨论
替比夫定(D-L-2-脱氧胸腺嘧啶苷)是一类用于治疗慢
2.2 两组治疗前后HBV DNA转阴情况比较
性乙型肝炎的左旋核苷类似物,具有特异性、强效抑制 HBV的作用,但对艾滋病病毒和其他病毒没有活性[6]。替比夫定与其他左旋核苷类似物如拉米夫定等可能存在交叉耐药性,与拉米夫定相比,国内外多项研究表明替比夫定在抑制HBV效果及组织学应答方面均优于拉米夫定[7-9],也优于阿德福韦酯[10]。
在本研究中,100例患者按照随机分配法分至替比夫定组和阿德福韦酯组,两组资料具有可比性。本文结果显示,在治疗12、24和48周等不同时间点,两组的HBVDNA平均水平不断下降,HBVDNA转阴率不断升高,治疗组优于对照组,差异有高度统计学意义(P<0.01),与文献报道一致;血清HBeAg转换率分别为18.4%和11.8%,差异无统计学意义(P>0.05);血清 ALT复常率分别为 73.5%(36/49)和 68.6%(35/51),差异无统计学意义;两组患者总的不良事件发生率分别为 53.1%(26/49)和 52.9%(27/51),差异无统计学意义(P>0.05)。结果表明替比夫定比阿德福韦酯具有更强的抗HBV能力,在对HBV复制抑制的程度和HBVDNA转阴率等方面优于阿德福韦酯,但是两种药物治疗48周后血清HBeAg转换率均较低、ALT复常率和总的不良事件发生率等方面差异亦无统计学意义,可能需要更长疗程的观察。
[1]Lok AS.Prevention of hepatitis B virus-related hepatocellular carcinoma[J].Gastroenterology,2004,127(5 suppl 1):303-309.
[2]Ganem D,Prince AM.Hepatitis B virus infection-Natural history and clinical consequences[J].N.Engl.J.Med,2004,350:1118-1129.
[3]Yuen MF,Wong DK,Sablon E,et al.HBsAg seroclearance in chronic hepatitis B in the Chinese:virological,histological,and clinical aspects[J].Hepatology,2004,39:1694-1701.
[4]Montalto G,Cervello M,Giannitrapani L,et al.Risk factors and natural history of hepatocellular carcinoma epidemiology [J].Ann N Y Acad Sci,2002,963:13-20.
[5]中华医学会肝病学分会,中华医学会感染病学分会.慢性乙型肝炎防治指南[J].中华流行病学杂志,2006,27(1):79-88.
[6]Bryant ML,Bridges EG,Placidi L,et al.Antiviral L nucleosides specific for hepatitis B virus infection[J].Antimicrob Agents Chemother,2001,45(1):229-235.
[7]Lai CL,Rosmawati M,Lao J,et al.Telbivudine is superior to lamivudine in reducing hepatitis B virus DNA in patients with chronic hepatitis B infection[J].Gastroenterology,2002,123(6):1831-1838.
[8]Lai CL,Gane E,Hsu CW,et al.Two-year results from the GLOBE Trial in patients with chronic hepatitis B:greater clinical and antiviral efficacy for Telbivudine (LdT) vs Lamivudine[J].Hepatology,2006,44(suppl 1):222.
[9]Jia JD,Hou JL,Yin YK,et al.Two-year results of a phase Ⅲcomparative trial of telbivudine vs lamivudine in Chinese patients[J].Hepatology,2007,46(Suppl 1):189.
[10]Bzowej N,Chan LYH,Lai CL,et al.A randomized trial of Telbivudine(LdT)vs Adefovir for HBeAg-positive chronic hepatitis B:final week 52 results[J].Hepatology,2006,44(suppl 1):1005.
