培美曲塞单药治疗复治晚期肺腺癌45例临床观察
2012-09-21董益忠张亚平毕延智盛桂凤凌扬
董益忠 张亚平 毕延智 盛桂凤 凌扬
肺癌是目前恶性肿瘤发病率最高肿瘤之一,其病死率位于所有肿瘤之首。非小细胞肺癌(NSCLC)占肺癌的80%,其中65%~70%的患者确诊时失去手术机会,已属晚期。对于这部分NSCLC治疗手段有限,其中以姑息性化疗为主要治疗手段之一,目前国际推荐标准的一线化疗方案是第三代化疗药物(吉西他滨、紫杉醇、多西他赛、长春瑞宾等)联合铂类为主的方案[1],Meta分析表明一线化疗能延长晚期NSCLC生存期,提高患者生存质量,但显示中位生存期多为8~10个月,近期有效率仅30%~40%,其疗效已达平台,因此对复发或初治无效的晚期NSCLC治疗,需引入新的药物及治疗方法。2004年8月抗叶酸多靶点化疗药物培美曲塞(pemetrexed),已被美国批准用于晚期NSCLC的二线治疗。本临床观察回顾2008年3月~2011年12月应用培美曲塞治疗45例晚期复发性肺腺癌,观察其疗效和耐受性。现报道如下。
1 资料与方法
1.1 一般资料 2008年3月~2011年12月苏州大学附属常州肿瘤医院收治的一线及一线以上治疗失败的晚期复发性肺腺癌患者45例,45例患者中男性25例,女性20例,年龄34~82岁,中位年龄56岁。病理学或细胞学证实肺腺癌,有可测量的临床观察指标;肺内原发灶35例,纵隔及浅表淋巴结转移30例,肺内转移16例,肝脏转移12例,脑转移8例,骨转移13例,恶性胸腔积液10例。肝、肾功能及血象正常,近1个月内未接受其他抗肿瘤治疗。
1.2 既往治疗情况 既往经手术治疗者30例;行放射治疗者18例;接受1个化疗方案治疗者18例;接受2个化疗方案患者12例;接受3个及以上化疗方案患者9例;曾接受靶向治疗的6例。化疗方案主要是吉西他滨、紫杉醇、长春瑞滨、多西他赛与顺铂或卡铂等不同方案的联合治疗。45例患者的临床资料见表1。
1.3 治疗方案 单药方案 培美曲塞500mg/m2,第1d静脉滴注,每3周1个周期。化疗2周期后复查相关检查,对可测量病灶予以疗效评估。病灶缩小者继续原方案治疗,进展者更换治疗方案。化疗前参照药物说明书进行预处理:口服叶酸400μg/d在化疗前1周开始给予,持续到治疗结束;在用药前1周肌内注射维生素B121000μg,且每9周重复1次;地塞米松4.0mg,每日2次口服,在用药前1d、当天和第2d。
1.4 疗效及不良反应评价 化疗后2个周期进行疗效评价,毒副反应每周期进行评价。近期疗效按照RECIST1.1标准评价,分为完全缓解(CR)、部分缓解(PR)、稳定(SD)和进展(PD);毒副反应根据WHO关于抗癌药物毒性反应评定标准评价分0~4级;所以患者均有完整的随访资料,随访时间截止2012年1月20日。研究观察指标为中位无疾病进展期(PFS)、中位生存期(OS)、1年生存率和毒副反应。中位PFS从用培美曲塞化疗开始计算。
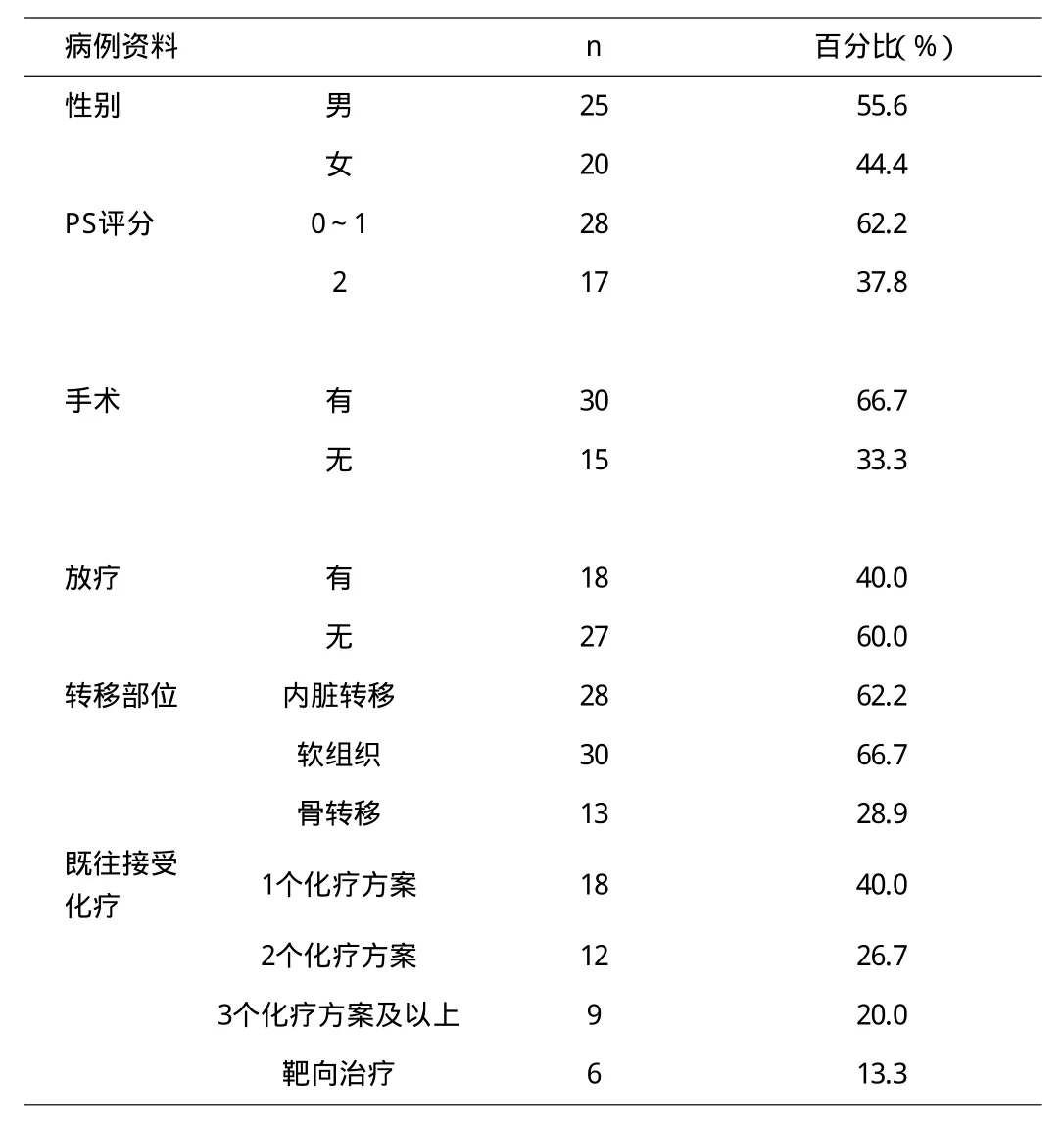
表1 45例复治晚期肺腺癌患者一般资料
2 结果
2.1 疗效 45例患者共完成138个周期化疗,中位周期数为3.1个周期(2~8个周期)。45例患者全部接受了至少2周期化疗,均可评估疗效。其中无CR0例,PR12例,SD18例,PD15例,疾病控制率66.7%(30/45)。中位PFS为3.1个月,中位生存期为6.6个月,1年生存率24.5%。
2.2 不良反应 主要不良反应为骨髓抑制,其中Ⅰ/Ⅱ度粒细胞减少发生率为31.1%(14/45),Ⅲ/Ⅳ度粒细胞减少发生率和4.4%(2/45),Ⅰ/Ⅱ度血小板下降发生率22.2%(10/45),未有Ⅲ/Ⅳ度血小板下降发生病例,Ⅰ/Ⅱ度贫血发生率为17.8%(8/45),没有Ⅲ/Ⅳ度贫血发生病例。其次消化道反应,Ⅰ/Ⅱ度和Ⅲ/Ⅳ度恶心、呕吐发生率为13.3%(6/45)和2.2%(1/45),Ⅰ/Ⅱ度和Ⅲ/Ⅳ度疲乏感为13.3%(6/45)和0(0/45)。总体不良反应轻微,耐受性好,无治疗相关性中断出组病例,具体不良反应见表2。
3 讨论
培美曲塞是一种结构上含有核心为吡咯嘧啶基团的抗叶酸制剂,通过抑制胸苷酸合成酶(TS)、二氢叶酸还原酶(DHFR)和甘氨酰胺核苷甲酰基转移酶(GARFT)的活性,破坏细胞内叶酸依赖性的正常代谢过程,抑制细胞复制,从而抑制肿瘤的生长[2]。
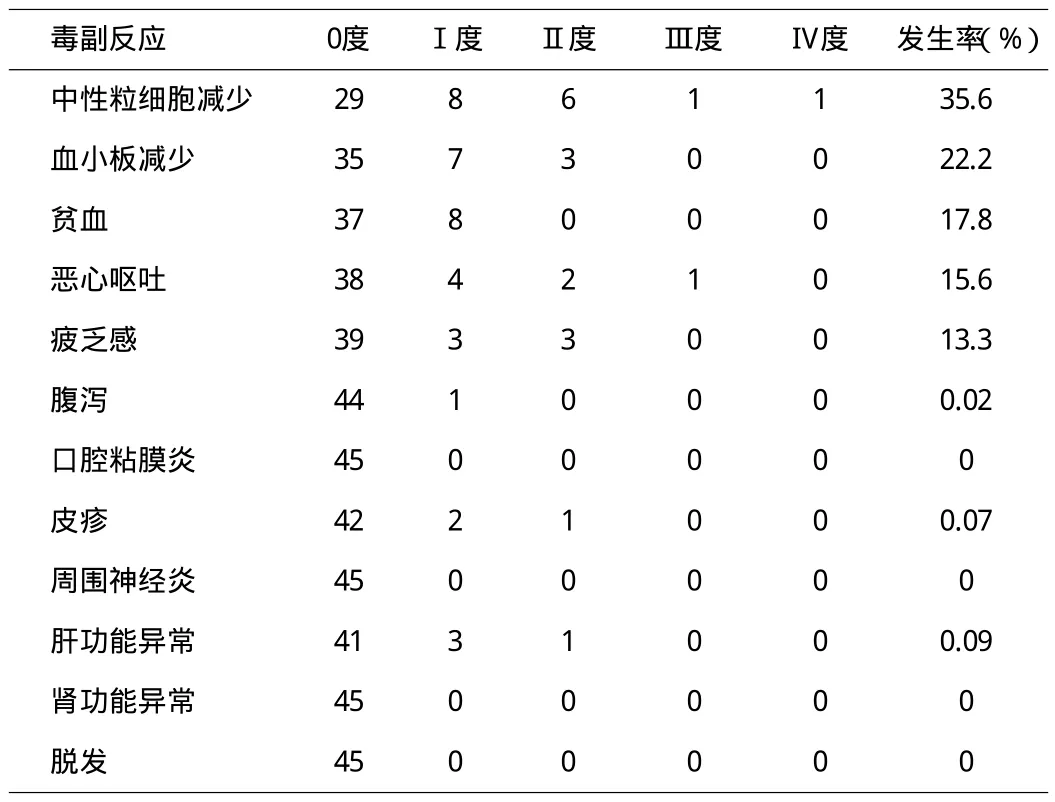
表2 培美曲塞单药治疗复治晚期肺腺癌的毒副反应
研究表明,培美曲塞体外能明显抑制间皮瘤细胞系(MSTO-211H、NCI-H2052)的生长,且培美曲塞与顺铂联合有协同作用,目前已成为晚期恶性间皮瘤的标准治疗药物[3]。培美曲塞联合顺铂、卡铂、紫杉醇、多西紫杉醇、奥沙利铂、伊立替康等其他化疗药物治疗晚期NSCLC的Ⅱ临床研究取得较好疗效[4-5]。Hanna报道1项571例患者入组的对比单药培美曲塞与多西他赛二线治疗NSCLC大型随机Ⅲ期临床研究(JMEI),其结果显示无论其中位生存期(8.3个月 vs 7.9个月)、总体治疗有效率(9.1% vs 8.8%),还是中位疾病无进展生存期与1年生存率(均为2.9月和29.7%),均无显著性差异,但是培美曲塞组其中性粒细胞下降、粒细胞减少性发热及脱发等药物性不良反应显著降低,有统计学差异[6]。基于此项研究,培美曲塞已经在2004年8月被美国FDA已批准为晚期或转移性NSCLC二线标准治疗药物。在2006年ASCO年会上Demarinis再次报道JMEI随访2年后更新分析,发现两组仍然没有统计学意义,从而进一步证实了初期得出的结论。
同时,Scagliotti等报道1项Ⅲ期随机临床试验(JMBD),观察培美曲塞联合顺铂对照吉西他滨联合顺铂一线治疗局部进展期或转移性NSCLC疗效,结果提示培美曲塞联合顺铂在治疗腺癌中生存期优于吉西他滨联合顺铂组(12.6个月 vs 10.9个月),在大细胞癌患者中也得到相似结果(10.4个月 vs 6.7个月),并证明差异有显著性。而鳞癌患者情况恰恰相反,吉西他滨联合顺铂在治疗鳞癌方面的中位生存期优于培美曲塞联合顺铂(10.8个月vs 9.4个月),并证明差异有显著性,提示培美曲塞对非鳞癌有优势[7]。同样肺癌病理组织类型影响培美曲塞治疗疗效结果同样也在培美曲塞联合同步胸部放疗治疗局部晚期NSCLC临床研究中得以证实。GALGB30407试验用培美曲塞/卡铂联合同步胸部放疗治疗局部晚期NSCLC:总的生存时间鳞癌为18个月,非鳞癌为22个月;18个月总生存率鳞癌为48%,非鳞癌为56%[8]。目前对于这一现象最可能的一种解释是胸苷酸合成酶(TS)在NSCLC各型别间的表达水平不同有关。研究显示可能正是鳞癌中TS过表达降低了其对抗叶酸代谢药物敏感性。Ceppi等检测56例NSCLC标本中TS表达水平与肿瘤组织学类型及恶性程度有关,发现TS的表达肺鳞癌明显高于肺腺癌[9]。
基于以上研究,本临床观察选择的病例均为晚期肺癌,病理类型选择腺癌。临床结果显示:无CR病例,只有12例PR,但疾病控制率高达66.7%,总中位PFS为3.1个月,中位生存期为6.6个月,1年生存率为24.5%。分析原因与观察病例中60%接受过二线甚至二线以上的治疗,为反复多次治疗病例,这是总体有效率不高的原因,但临床结果与国外报道类似,远期生存较满意。由于观察病例均给予补充叶酸和维生素B12,不良反应比较轻微,只有1例病例出现Ⅳ度粒细胞下降,经G-CSF升白处理好恢复,耐受性较好。
培美曲塞作用机制独特,对晚期复治非鳞癌肺癌其疗效确切,毒副反应轻,患者耐受性良好,值得在临床推广。
[1] Schiller JH,Harrington D,Belani CP,et ai.Comparison of four chemotherapy regimens for advanced non-small cell lung cancer[J].N Engl J Med,2002,346(2):92-98.
[2] Calvert H.An overview of folate metabolism:features relevant to the action and toxicities of antifolate anticancer agents[J].Semi Oncol,1999,26(Suppl):3-10.
[3] Vogelzang NJ,Rusthoven JJ,Symanowski J,et al.Phase Ⅲ study of pemetrexed in combination with cisplatin versus cisplatin alone in patients with malignant pleural mesothelioma[J].J Clin Oncol,2003,21(34):2636-2644.
[4] Monnerat C,Le Chevalier T.Review of the pemetrexed and gemcitabine combination in patients with advanced-stage non-small cell lung cancer[J].Ann Oncol 2006,17(Suppl 5):86-90.
[5] de Marinis F,de Santis S,de Petris L.Second-line chemotherapy for non-small cell lung cancer[J].Ann Oncol,2006,17(suppl 5):68-71.
[6] Hanna N,Shepherd FA,Fossella FV,et al.Randomized phase Ⅲ trial of pemetrexed versus docetaxel in patients with non-small cell lung cancer previously treated with chemotherapy[J].J Clin Oncol,2004,22(9):1589-1597.
[7] Scaglioti GV,Parikh P,von Pawel J,et al.Phase Ⅲ study comparing cisplatin plus gemcitatine with cisplatin plus pemetrexed in chemotherapy:naive patients with advancedstage non-small cell lung cancer[J].J Clin Oncol,2008,26(21):3543-3551.
[8] Govindan R,Bogart J,Wang X ,et al.Phase Ⅱ study of pemetrexed carboplatin and thoracic radiation with without cetuximab in patients with locally advanced unresectable non-small cell lung cancer:GALGB 30407[J].J Clin Oncol,2009,27:a7550.
[9] Ceppi P,Volante M,Saviozzi S,et al.Squamous cell carcinoma of the lung compared with other histotypes shows higher messenger RNA and protein levels for thymidylate synthase[J].Cancer,2006,107(7):1589-1596.
