红藤消炎灌肠液微生物限度检查方法的验证试验
2012-09-16王伟东
● 王伟东
红藤消炎灌肠液具清热解毒,活血化瘀功效,临床用于附件炎、盆腔炎。其成分为大血藤、野菊花、蒲公英、地丁、败酱草、三棱、莪术(醋制)、桃仁、延胡索(醋制)、香附(醋制)、木香等11味中药,因处方中多味药有抗菌、消炎的作用,对试验菌采用常规方法做微生物限度检查时,对阳性试验菌干扰,阳性试验菌的回收率达不到药典要求的不低于70%。我们采用薄膜过滤法[1],按中国药典2010年版二部相关规定[2]进行试验,结果表明,该法省时、易操作,适用于红藤消炎灌肠液微生物限度检查。
1 材料
1.1 仪器 净化工作台(szk-202安徽省蚌埠净化设备有限公司)、隔水式恒温培养箱(PYX_DHS-40*50上海市跃进医疗器械厂)、立式灭菌器(3260J山东新华医疗器械有限公司)、薄膜过滤器(杭州泰林生物技术有限公司)、集菌仪(H601杭州高得医疗器械有限公司)。
1.2 培养基 营养肉汤培养基、营养琼脂培养基、改良马丁氏液体培养基、改良马丁氏琼脂培养基、甘露醇氯化钠琼脂培养基、溴化十六烷三甲胺琼脂培养基,均由北京陆桥技术有限公司生产。
1.3 稀释剂 氯化钠-蛋白胨缓冲液,北京陆桥技术有限公司生产。
1.4 菌种 大肠埃希菌[CMCC(B)44102]、金黄色葡萄球菌[CMCC(B)26003]、铜绿假单胞菌[CMCC(B)10104]、枯草芽孢杆菌[CMCC(B)63501]、白色念珠菌[CMCC(F)98001]、黑曲霉[CMCC(F)98003]由中国药品生物制品检定所提供,所有菌种均为第4代。
1.5 样品 红藤消炎灌肠液(500ml/瓶),黄石市中医院制剂室提供。
2 方法
2.1 细菌数、霉菌和酵母菌数检查方法的验证
2.1.1 菌液制备 接种大肠埃希菌、金黄色葡萄球菌、枯草芽孢杆菌的新鲜培养物至营养肉汤培养基中,35℃培养18~24h,取上述新鲜培养物1ml,用0.9%无菌氯化钠溶液,稀释至活菌数50~100cfu·ml-1,备用。接种白色念珠菌的新鲜培养物至改良马丁氏液体培养基中,25℃培养18~24h,取上述新鲜培养物 1ml,用0.9%无菌氯化钠溶液,稀释至活菌数50~100cfu·ml-1,备用。接种黑曲霉的新鲜培养物至改良马丁氏琼脂斜面培养基中,25℃培养1周,加5ml的0.9%无菌氯化钠溶液,洗下霉菌孢子,吸出菌液,用标准比浊管比浊,取上述新鲜培养物1ml,用0.9%无菌氯化钠溶液,稀释至活菌数50 ~100cfu·ml-1,备用。
2.1.2 供试液制备 吸取样品10ml至有无菌玻璃珠的250ml三角烧瓶中,加90ml无菌的稀释液,混匀,使成1∶10的供试液。取上述供试液10ml(相当于样品1ml),加入100ml无菌稀释液中,混匀,过滤,接着用200ml的稀释剂冲洗,消除抑菌成分后,取出滤膜,菌面朝上,贴于规定的琼脂平板上培养。
2.1.3 回收率测定
(1)试验组:分别取1∶10的供试液10ml(相当于样品1ml),各加入100ml无菌稀释液中,混匀,过滤,接着用400ml的稀释剂冲洗,预留100ml稀释剂各加入大肠埃希菌、金黄色葡萄球菌、枯草芽孢杆菌、白色念珠菌、黑曲霉菌各1ml(50~100cfu·ml-1),按薄膜过滤法,取出滤膜,菌面朝上,贴于规定的琼脂平板上,置规定温度培养24~72h,逐目观察结果。
(2)菌液组:除不加供试液外,其余操作同试验组。
(3)供试品对照组:除不加菌悬液外,其余操作同试验组。
(4)稀释剂对照组:用稀释液取代供试液,其余操作同试验组。
2.1.4 回收率计算 验证试验进行3次独立的平行试验,并分别计算各试验菌每次试验的回收率。
(1)试验组的菌回收率=

(2)稀释剂对照组的菌回收率=

2.2 控制菌检查方法的验证
2.2.1 试验组 分别取1∶10的供试液10ml(相当于样品1ml),各加入100ml无菌稀释液中,混匀,过滤,接着用400ml的稀释剂冲洗,预留100ml稀释剂,分别加入金黄色葡萄球菌液1ml(50~100cfu·ml-1)、铜绿假单胞菌液1ml(50~100cfu·ml-1),按薄膜过滤法过滤,取出滤膜,菌面朝上,分别贴于甘露醇氯化钠琼脂培养基、溴化十六烷三甲胺琼脂培养基中35℃培养24h。
2.2.2 阴性对照组:用稀释剂10ml,替代供试液及验证菌液,按试验组进行检查和培养。
2.2.3 阳性对照组:除不加供试液外,其余操作同试验组。
3 结果
3.1 细菌数、霉菌和酵母菌数测定方法的验证结果 回收率见表1,该试验对5种菌种的回收率均高于70%。
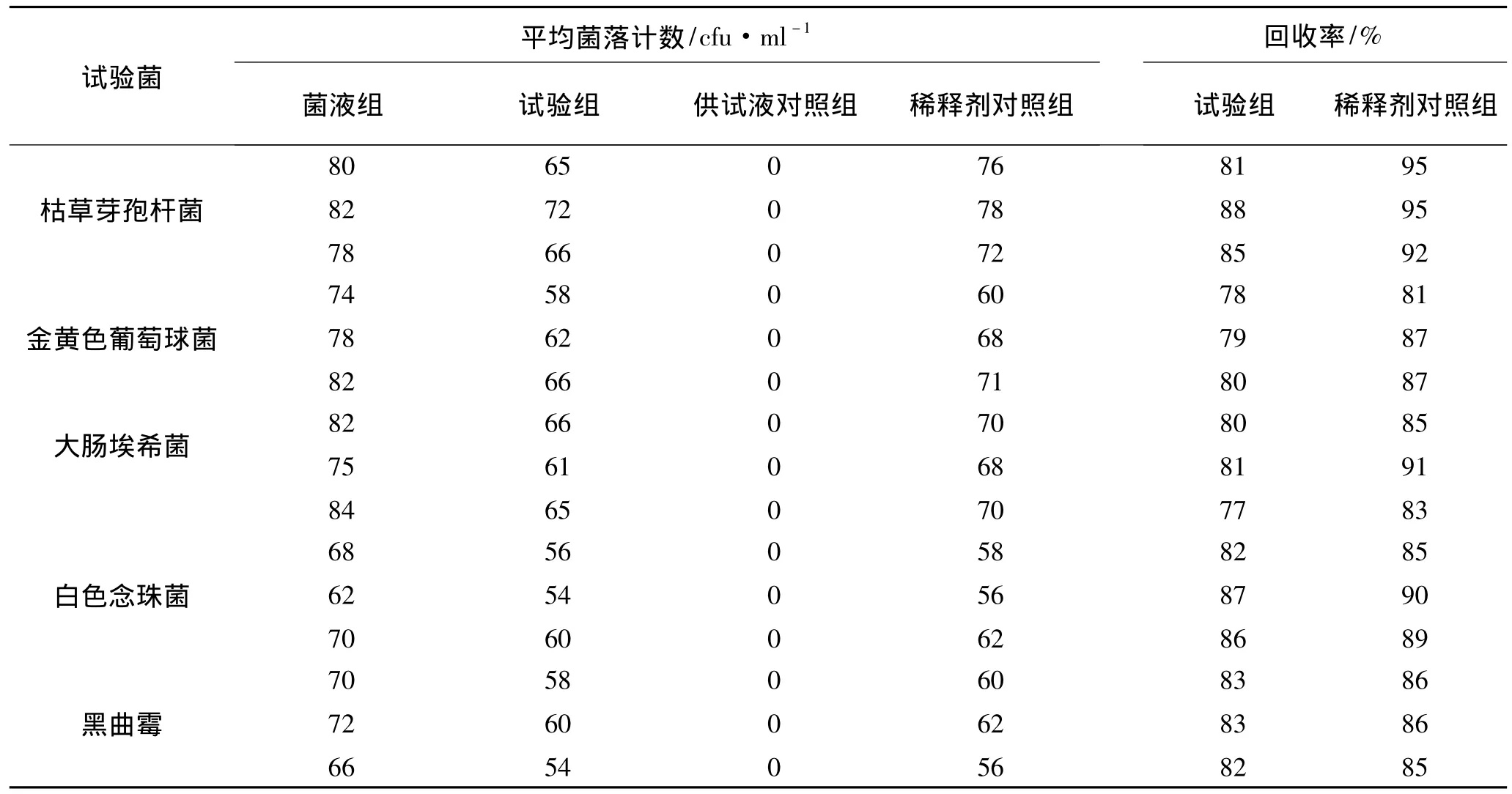
表1 薄膜过滤法菌落计数及回收率测定
3.2 控制菌检查方法的验证结果 试验组检出金黄色葡萄球、铜绿假单胞菌;阳性对照组检出金黄色葡萄球、铜绿假单胞菌;阴性对照组无菌生长。该方法能检出金黄色葡萄球、铜绿假单胞菌,适合于该制剂的控制菌检查。
4 讨论
药品的微生物限度检查结果受许多因素的影响,在进行微生物检测时,只有在该检测条件下的样品浓度不足以抑制污染微生物的生长,才能使供试品中污染的微生物得以真实反映。因此,药品的微生物限度检查应通过验证试验证明所采用的方法是适宜的,方可使用[3]。中药制剂多为含有多种成分的复方制剂,同时生产中使用含抑菌作用的辅料以及加入抑菌剂或防腐剂等原因,影响微生物检查结果的因素更多,必须采取合适的试验方法去除制剂的抑菌作用,才能真实反映制剂受污染的程度[4]。
通常,对无抑菌作用的制剂可用常规法进行微生物限度检查,对抑菌作用较弱的制剂可通过稀释培养基来消除其抑菌作用。本文作者实际工作中对红藤消炎灌肠液进行微生物限度检查时,发现该制剂具有很强的抑菌活性,不能直接采用常规法或稀释培养基法。本文采用薄膜过滤法,去除其抑菌活性成分,进行验证试验。为保证试验的科学性和准确性,本试验严格按照《中国药典》规定,选择5种菌株进行验证,结果表明,采用薄膜过滤法可有效消除红藤消炎灌肠液抑菌作用,各菌回收率均>70% ,同时控制菌的检查方法能有效检出控制菌,该方法适合红藤消炎灌肠液的微生物限度检查。
[1]马绪荣,苏德模.药品微生物学检验手册[M].北京:科学出版社.
[2]国家药典委员会.中国药典2010年版(二部)[M].北京:中国医药科技出版社,2010:附录 XIJ,107.
[3]曹雄伟.最新药品微生物检验方法与操作标准规范及无菌隔离技术实用手册.上卷[S].北京:中国中医药出版社,2009:261.
[4]陈华龙,王莉蓓,谭莉萍.姜胆咳喘片微生物限度检查方法的验证[J].中国实验方剂学杂志,2010,(11):67.
