心理语言、胃电起搏和穴位刺激协同对功能性消化不良患者血浆脑肠肽的影响
2012-09-14杨春敏张洪领唐合兰韩全力
杨春敏,陈 英,范 勤,张洪领,唐合兰,杜 斌,贾 敏,韩全力,李 静
空军总医院干部病房消化科,北京 100142
心理语言、胃电起搏和穴位刺激协同对功能性消化不良患者血浆脑肠肽的影响
杨春敏,陈 英,范 勤,张洪领,唐合兰,杜 斌,贾 敏,韩全力,李 静
空军总医院干部病房消化科,北京 100142
目的 研究心理语言、穴位刺激、胃电起搏同步协同治疗方法(Coordinated Treatment of Psychological language,Acupuncture point stimulation and Gastric pacing,CTPAG)治疗难治性功能性消化不良的临床疗效和可能的脑肠肽机制。方法 选取80例难治性功能性消化不良患者,随机分为两组:口服药物组(n=38)和CTPAG组(n=42),比较两组受试者临床疗效以及血浆胃动素(MTL)、瘦素(LEP)、降钙素基因相关肽(CGRP)浓度的差异。结果 与口服药物组比较,CTPAG组中临床症状评分明显下降,疗效明显升高;血浆MTL浓度升高,血浆LEP、CGRP浓度下降,差异具有显著性(P<0.05)。结论 心理语言、穴位刺激和胃电起搏协同治疗难治性功能性消化不良疗效优于常规口服药物,这种疗效与血浆MTL水平的上调,血浆LEP、CGRP水平的下调密切相关。
功能性消化不良;心理语言、穴位刺激和胃电起搏协同治疗;胃动素;瘦素;降钙素基因相关肽
功能性消化不良 (functional dyspepsia,FD)是一组常见的功能性胃肠道疾病,约占消化专科门诊的20% ~40%[1],而其中有相当一部分患者为难治性FD患者,病程漫长,反复治疗效果欠佳,严重影响患者身心健康和生活质量。由于引起FD的发病机制复杂,单纯药物治疗或物理疗法效果欠佳,人们对新的治疗方法非常期待。在以往研究基础上,我们研制出一种集心理语言疏导、中医穴位刺激、胃电起搏为一体的新型治疗仪(专利号200620139011.9),将三者通过计算机技术结合在一起产生协同效应(Coordinated Treatment of Psychological language,Acupuncture pointstimulation and Gastric pacing,CTPAG),本文主要评价该法对难治性FD的临床症状的改善情况,并探索该法治疗FD可能的脑肠肽机制。
1 资料与方法
1.1 一般资料与分组 选取我院2009年2月-2011年3月门诊难治性FD患者共80例,入选标准:根据罗马III FD诊断标准[2]初步筛选出FD患者,因目前国内外尚缺乏难治性FD的标准,我们根据FD患者的症状、治疗过程、疗效,筛选出症状较重,病程>1年,反复多次治疗未见明显改善的患者为难治性FD。排除标准:妊娠和哺乳期妇女;患有严重器质性疾病及腹部手术病史者;治疗前1周用过促胃肠动力药物或抗焦虑药物者。按事先编制好的随机数字表随机分成两组,口服药物组(n=38)(均未进行精神心理治疗):口服多潘立酮,10 mg,3次/d+法莫替丁20 mg,2次/d,10 d为1个疗程,治疗1个疗程;CTPAG组(n=42):CTPAG治疗1次/d,每次20 min,10 d为1个疗程,治疗1个疗程。口服药物组中患者男19例,女19例,平均年龄 (48.1 ±3.2)岁,平均 BMI=21.5 kg/m2;CTPAG组中患者男21例,女21例,平均年龄(47.8±2.5)岁,平均 BMI=22.1 kg/m2,两组一般资料具有可比性,差异无统计学意义。
1.2 实验方法
1.2.1 心理语言、穴位刺激、胃电起搏同步协同治疗(Coordinated Treatment of Psychological language,Acupuncture point stimulation and Gastric pacing,CTPAG)原理:①心理科医生设计针对FD对胃肠放松治疗的特殊语音背景,通过计算机软件控制达到根据语音变化贯穿并引导穴位刺激、胃电起搏电流的输出,使语音、穴位刺激、胃电起搏协调工作、同步正强化。② 胃起搏正、负极置于胃窦、胃体在体表的投影部位,采用1.1~1.2倍内源性胃慢波频率(intrinsic gastric slowwave frequency,IGF)的类正弦基波叠加一系列双极脉冲方波(频率10 Hz,脉宽为50 ms)进行起搏。③在双侧足三里及内关穴位分别固定安置一硅橡胶电极1.5 cm2,然后将电极连于中频电治疗仪,输出2 kHz的调制中频刺激电流,调制波为方波和指数波,调制频率1~150 Hz。在20 min内,有数十个以上程序步,每一步均将所有各项中频电治疗参数作各种变化,处方的程序自动输出。对经络穴位产生一种独特的电刺激按摩和电运动刺激的作用,刺激电流为20 mA。
1.2.2 症状评分指标:FD最常见的症状如:上腹胀、上腹痛、早饱、嗳气、反胃、恶心、呕吐、食欲不振、发生频率等症状按病情轻重程度标为0~10分。视觉模拟评分量表法(visual analog scale,VAS):所有入组患者在治疗前1天及治疗后第1天分别对症状逐项打分,并进行总计,作为自我评分。医生问诊症状评分标准:1分:轻度,症状轻微,需注意才能感觉到;2分:中度,自觉症状明显,但不影响工作和生活;3分:重度,自觉症状明显,影响工作和生活。将以上症状逐项打分并进行总计,作为医生评分。疗效评价:经患者视觉模拟症状评分及医生评分,症状积分下降百分比>50%,认为疗效显著;症状积分下降百分比>25%,但≤50%为疗效一般;症状积分下降百分比≤25%为无效。
1.2.3 血浆胃动素、瘦素及降钙素基因相关肽的测定:胃动素、瘦素、降钙素基因相关肽的测定均采用放射免疫分析,试剂盒由北京科美东雅生物技术有限公司提供,操作按说明书,由专人操作。
1.3 统计学处理 应用 SPSS 11.0软件进行统计学处理,组间比较采用t检验,计量资料以 x-±s表示,组内比较采用配对t检验;组间比较采用成组t检验,计数资料用%表示,采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 临床症状评分 根据治疗前后患者VAS和医生问诊症状评分,组内比较,无论是口服药物组还是CTPAG组,治疗后的评分均较治疗前低,差异有统计学意义(P<0.05或0.01);组间同一时间段比较,口服药物组与CTPAG组在治疗前评分差异无统计学意义,但在治疗后,CTPAG的评分显著低于口服药物组,差异有统计学意义(P<0.01)。根据疗效评价分析,患者自评分和医生评分CTPAG组的显著效果率[显著效果率(%)=显著效果例数/总例数×100%]均高于口服药物组(81.0%vs 63.2%,81.0%vs 73.7%,P<0.05,见表1、2)。
表1 两组治疗前后临床症状评分的比较(x-±s)Tab 1 Scores of clinical symptom before and after treatment(±s)

表1 两组治疗前后临床症状评分的比较(x-±s)Tab 1 Scores of clinical symptom before and after treatment(±s)
与本组治疗前比较,aP<0.05,bP<0.01;与口服药物组治疗后比较,cP <0.01
分组 例数 VAS 医生问诊症状评分口服药物组38治疗前 23.9 ±1.2 10.1 ±0.8治疗后 20.5 ±0.3a 8.8 ±0.4aCTPAG组 42治疗前 24.8 ±0.5 9.6 ±0.8治疗后 14.6 ±0.7bc 5.5 ±0.2bc

表2 两组治疗后临床症状疗效的比较[例数(%)]Tab 2 Curative effects of clinical symptom after treatment[n(%)]
2.2 血浆脑肠肽浓度的测定 组内比较,无论是口服 药物组还是CTPAG组,治疗后MTL均明显升高,LEP均明显下降,CGRP均明显下降,差异具有统计学意义(P<0.05)。组间比较,在治疗前,口服药物组与CTPAG组的MTL、LEP、CGRP值均相近,差异无统计学意义,但治疗后,CTPAG组与口服药物组比较,MTL升高更显著,LEP下降更显著,CGRP下降也更显著,差异有统计学意义 (P<0.05,见表3)。
表3 两组治疗前后血浆MTL、LEP、CGRP浓度的比较(±s)Tab 3 Comparison of plasma concentrations of MTL,LEP,and CGRP before and after treatment(±s)
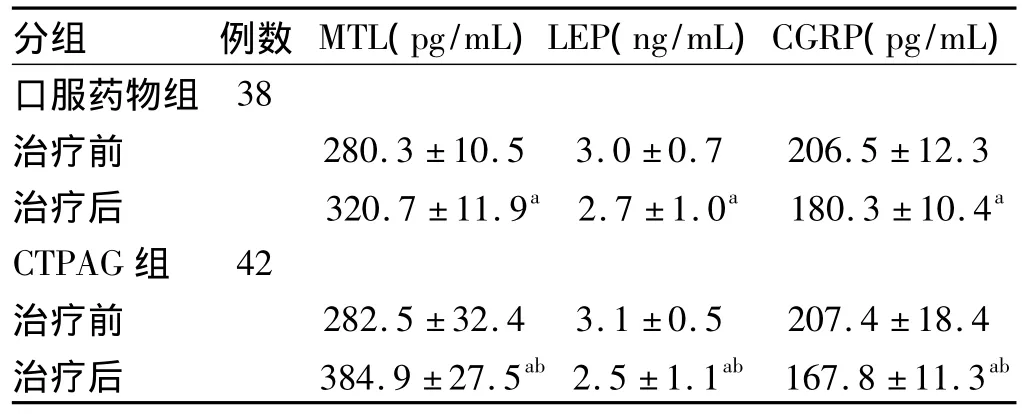
表3 两组治疗前后血浆MTL、LEP、CGRP浓度的比较(±s)Tab 3 Comparison of plasma concentrations of MTL,LEP,and CGRP before and after treatment(±s)
与本组治疗前比较,aP<0.05,与口服药物组治疗后比较,bP<0.05
分组 例数 MTL(pg/mL)LEP(ng/mL)CGRP(pg/mL)口服药物组38治疗前 280.3 ±10.5 3.0 ±0.7 206.5 ±12.3治疗后 320.7 ±11.9a 2.7 ±1.0a 180.3 ±10.4aCTPAG组 42治疗前 282.5 ±32.4 3.1 ±0.5 207.4 ±18.4治疗后 384.9 ±27.5ab2.5 ±1.1ab 167.8 ±11.3ab
3 讨论
FD(functional dyspepsia,功能性消化不良)的发病机制尚未完全阐明,可能与胃肠动力下降、内脏敏感性增高、精神心理、H.pylori感染、胃肠激素、胃酸分泌、环境等因素相关,而胃肠激素分泌紊乱在其发病机制中的重要性越来越受到人们的重视[3]。
在FD的治疗方案中,促胃肠动力药联合抑酸药是目前临床比较常用且疗效公认的方法之一。促动力药多潘立酮,是一种选择性多巴胺-2(DA2)受体阻断剂,DA2受体是胃肠道的主要受体,因此多潘立酮可减少多巴胺介导的胃平滑肌松弛,能增加消化道的动力。抑酸药法莫替丁,是一种组织胺H2受体拮抗剂,对胃酸分泌具有明显的抑制作用。因此,我们采用随机对照研究,通过比较CTPAG组与口服药物组在治疗难治性 FD的临床疗效,同时检测两组 MTL、LEP、CGRP血浆浓度的变化,旨在进一步揭示CTPAG治疗难治性FD的可能分子机制。
胃肠激素又称脑肠肽,是产生于胃肠道内分泌细胞与神经细胞的一种小分子肽类活性物质。以往研究表明,FD与胃动素(motilin,MTL)、瘦素(leptin,LEP)和降钙素基因相关肽(calcitonin gene-related peptide,CGRP)均密切相关。
MTL是上世纪七十年代国外学者Brown等发现的一种由22个氨基酸组成的直链多肽。MTL的生理作用有:促进胃肠运动,提高胃肠道、胆管、Oddi括约肌的收缩力和张力,并能减轻进食带来的饱胀不适症状[4],起着肠道清道夫的作用。关于 MTL在 FD发病机制中的作用尚不确定,有部分学者[5]研究报道认为,FD患者血浆 MTL含量低于正常对照组,FD患者胃排空延长、收缩减弱或移行性复合运动(MMC)Ⅲ相收缩缺乏均与MTL分泌下降有关。
LEP是一种主要由白色脂肪细胞合成和分泌的、由肥胖基因编码的、含有167个氨基酸残基的多肽类激素,具有调节能量代谢平衡,抑制摄食,延迟胃排空的作用[6]。国内学者发现,瘦素通过作用于下丘脑区而抑制胃体及胃窦MMCⅠ相收缩运动,从而抑制胃排空。王礼建等[7]研究表明,大鼠空腹 MMC与餐后胃运动模式的转换,是由MTL与LEP相互控制,形成饥饿—进食—饱感—饥饿的循环。FD与LEP关系的研究较少,且结论不一。
CGRP是一种含有37个氨基酸的神经肽,广泛分布于中枢和外周神经系统。现代研究无论是中枢还是外周CGRP的释放均参与了内脏敏感性变化[8]。内脏高敏感性一直被认为是功能性胃肠道疾病发生的主要机制之一[9]。有研究证明,FD患者胃黏膜CGRP及P物质(SP)阳性纤维中合成和释放CGRP及SP增加,可能与胃机械感觉过敏有关[10]。
本研究发现,两组治疗后与治疗前比较,血浆MTL均升高。与口服药物组(对照组)治疗后相比,CTPAG组血浆MTL浓度升高得更为显著,差异有统计学意义;并且,在CTPAG组中,上消化道的症状缓解程度也较对照组更为显著。可见,随着MTL浓度的升高,胃肠动力会增强,胃排空会加快,这可能是CTPAG明显改善FD患者上腹饱胀的重要机制之一。
本研究还发现,经两组治疗的FD患者,LEP和CGRP均比治疗前明显降低,而CTPAG组降低得更为显著,差异有统计学意义。这一结果表明,与口服药物组相比,CTPAG组在治疗FD的过程中,明显下调了LEP和CGRP的血浆浓度,从而使延迟胃排空和减少食欲的作用减弱,使胃的高敏感性降低,这可能是CTPAG改善FD患者早饱、上腹痛,从而增进食欲的机制之一。
已有研究[11]表明,FD患者容易出现精神过度紧张,对压力性事件呈现出一种夸大的反应,容易受外界的暗示和影响,干扰中枢神经的正常活动,并通过植物神经系统和内分泌系统引起胃肠功能障碍如胃排空延长等。故有人推测某些FD就是一种以躯体症状为主要表现的特殊类型的抑郁症,这类患者有较明显将情绪方面的问题不自觉地转化为躯体症状的倾向。针对这种情况,我们研发的CTPAG方法将精神心理因素作为治疗FD患者的靶点之一,在治疗过程中,通过心理语言的诱导,使患者进入一个非常放松的状态,抑郁和焦虑情绪得到缓解,增加了穴位刺激、胃电起搏的疗效,穴位刺激、胃电起搏治疗时患者躯体紧张得到缓解,也增加了其对心理语言的顺从性;而同时,穴位刺激能够通过手阳明大肠经及足阳明胃经的级联调节作用,促进胃功能的恢复,加强了胃电起搏的作用,这样三者相互作用、相辅相成,增加了单项治疗带来的疗效叠加,更大程度地缓解了患者的上消化道不适症状。而仅仅靠口服药物,则很难达到这样的综合疗效。我们从两组的症状缓解程度和脑肠肽水平改善程度对比来看,CTPAG组的治疗效果更加显著。而同时在针对该80例患者的治疗后随访中发现,72例(90%)患者在治疗后半年内未再出现原有症状或原有症状未再加重,提示本方法的治疗效果稳定性较高。
总之,本研究表明,CTPAG组在改善FD临床症状上明显优于口服药物组;同时,与口服药物组比较,经CTPAG组治疗的患者血浆MTL水平显著升高,LEP与CGRP的水平显著下降,这些变化与临床疗效的提高是同步的。这一结果使我们有理由认为,我们研发的CTPAG治疗难治性FD效果更优的原因,可能是更显著地调整了某些脑肠肽(如MTL、LEP、CGRP)的分泌紊乱而实现的,具体的作用环节还需要更深入地研究。
[1] Ghoshal UC,Singh R,Chang FY,et al.Epidemiology of uninvestigated and functional dyspepsia in Asia:facts and fiction[J].J Neurogastroenterol Motil,2011,17(3):235-244.
[2] Brun R,Kuo B.Functional dyspepsia[J].Therap Adv Gastroenterol,2010,3(3):145-164.
[3] Hernando-Harder AC,Franke A,Singer MV,et al.Functional dyspepsia.Newpathophysiologic knowledge with therapeutic implications[J].Medicina(B Aires),2007,67(4):379-388.
[4] Cuomo R,Vandaele P,Coulie B,et al.Influence of motilin on gastric fundus tone and on meal-induced satiety in man:role of cholinergic pathways[J].Am J Gastroenterol,2006,101(4):804-811.
[5] Galligan JJ,Vanner S.Basic and clinical pharmacology of new motility promoting agents [J].Neurogastroenterol Motil,2005,17(5):643-653.
[6] Nakahara T,Harada T,Yasuhara D,et al.Plasma obestatin concentrations are negatively correlated with body mass index,insulin resistance index,and plasma leptin concentrations in obesity and anorexia nervosa[J].Biol Psychiatry,2008,64(3):252-255.
[7] Wang LJ,Zhou L,Yuan B,et al.Regulative effect of leptin on gastric motility:experiment with conscious rats [J].Natl Med J China,2006,86(32):2266-2270.
王礼建,周吕,袁勃,等.瘦素对大鼠胃运动的调节运动[J].中华医学杂志,2006,86(32):2266-2270.
[8] Zhang FF,Mo JZ.Effect of calcitonin gene related peptide on sensitivity alteration of visceral nervous system[J].Chin J Gastroenterol Hepatol,2005,14(2):200-202.
章菲菲,莫剑忠.降钙素基因相关肽在内脏敏感性改变机制中的作用[J].胃肠病学和肝病学杂志,2005,14(2):200-202.
[9] Şimşek I.Irritable bowel syndrome and other functional gastrointestinal disorders[J].J Clin Gastroenterol,2011,45 Suppl:S86-S88.
[10] Li QX,Zhu LZ,Hou XH.Role of Gastric Mucosal CGRP-and SP-immnoreactive Positive Nerve Fiber on Gastric Hypersensitivity in Patients with Non-ulcer Dyspepsia [J].Journal of Hubei Institufe for Nationalities.Medical Edition,2003,20(4):1-4.
李启祥,朱良知,侯晓华.功能性消化不良病人胃粘膜CGRP、SP免疫阳性纤维与胃机械感觉过敏的关系[J].湖北民族学院学报.医学版,2003,20(4):1-4.
[11] Tang YP,Yao HC,Li FR,et al.Clinical research of the mind and physique combined therapy for the functional dyspepsia patients[J].Chin J Dig,2002,22(4):247-249.
唐艳萍,姚宏昌,李方儒,等.功能性消化不良患者心身综合治疗的临床研究[J].中华消化杂志,2002,22(4):247-249.
Effects of coordinated treatment of psychological language,acupuncture point stimulation and gastric pacing on the brain gut peptides of the functional dyspepsia patients
YANG Chunmin,CHEN Ying,FAN Qin,ZHANG Hongling,TANG Helan,DU Bin,JIA Min,HAN Quanli,LI Jing
Department of Gastroenterology,the General Hospital of the Air Force,Beijing 100142,China
ObjectiveTo investigate the clinical effects and the potential mechanism about brain gut peptides for treating refractory functional dyspepsia(FD)with coordinated treatment of psychological language,acupuncture point stimulation and gastric pacing(CTPAG).MethodsEighty refractory FD patients were enrolled and divided into two groups randomly:oral application group(n=38)and CTPAG group(n=42).The scores of clinical symptom and plasma concentrations of motilin(MTL),leptin(LEP)and CGRP were evaluated and analyzed.ResultsIn the CTPAG group,the scores of clinical symptom were descended,the ratios of therapeutic effect were elevated significantly.The plasma level of MTL was elevated,and the plasma levels of LEP and CGRP were descended significantly compared with the oral application group(P <0.05).ConclusionCTPAG,a new non-drug choice for treating refractory functional dyspepsia is effective and reliable.The curative effect surpasses the traditionary method of oral application.This effect may be attributed to the up-regulation of MTL as well as down-regulation of LEP and CGRP.
Functional dyspepsia(FD);Coordinated treatment of Psychological language,Acupuncture point stimulation and Gastric pacing(CTPAG);Motilin;Leptin;CGRP
R576.3
A
1006-5709(2012)08-0754-04
2012-02-01
10.3969/j.issn.1006-5709.2012.08.020
首都医学发展科研基金项目(2009-3088)
杨春敏,主任医师。E-mail:chunmyang@sina.com
