Dyrk1A经ASF调控CaMKⅡδ可变剪接在肾血管性高血压大鼠心肌肥厚中的作用*
2012-09-14朱健华陆尽亚秦晓同于小红盛红专
姚 健, 朱健华, 陆尽亚,3, 秦晓同, 于小红, 盛红专△
(南通大学1附属医院心内科,2医学院组胚教研室,3南通市第一人民医院老年医学科,江苏南通226001)
心肌肥厚是心肌细胞对多种心血管刺激的代偿性反应,可由压力超负荷、损伤和神经激素活化引起[1]。心肌肥厚可导致多种心血管意外如心肌梗死、心律失常、心衰等的发生率显著增加,预防心肌肥厚可以明显改善心脏病患者的预后。
钙/钙调素依赖蛋白激酶Ⅱ(calcium/calmodulin-dependent protein kinaseⅡ,CaMKⅡ)是介导心肌肥厚的重要激酶[2]。心脏组织中主要表达CaMKⅡ的δ亚型[3],由于外显子14、15或者16的可变剪接,CaMKⅡδ可表达A、B、C 3种亚型,正常机体内CaMKⅡδ的可变剪接受着严格的调控。可变剪接因子(alternative splicing factor,ASF)在心肌CaMKⅡδ可变剪接的调控中发挥关键作用[4]。ASF是受磷酸化高度调控的蛋白,前期本课题组通过转基因细胞研究的方法发现,双特异性酪氨酸磷酸化调节激酶1A(dual-specificity tyrosine phosphorylation-regulated kinase 1A,Dyrk1A)可磷酸化 ASF,从而使其移位,失去对可变剪接的调控作用[5],提示存在Dyrk1A经ASF调控CaMKⅡδ可变剪接的信号通路,但该通路在心肌肥厚中的作用尚未见研究报道。
本实验利用两肾一夹(two-kidney one-clip,2K1C)的大鼠心肌肥厚模型,通过检测大鼠心肌肥厚过程中CaMKⅡδ亚型可变剪接的改变及Dyrk1A、ASF表达的变化,并分别应用Dyrk1A抑制剂——表没食子儿茶素没食子酸酯(epigallocatechin gallate,EGCG)和哈尔碱(harmine)干预,探讨EGCG和哈尔碱对心肌肥厚、CaMKⅡδ可变剪接和ASF、Dyrk1A蛋白表达的影响,阐明心肌中 Dyrk1A经 ASF对CaMKⅡδ可变剪接的调控在肾血管性高血压大鼠心肌肥厚中的作用。
材料和方法
1 动物
采用健康、雄性Sprague-Dawley(SD)大鼠32只,清洁级,体重(174±9)g,购于上海西普尔-必凯实验动物有限公司,动物生产许可证号为SCXK(沪)2008-0016。
2 方法
2.1 动物心肌肥厚模型的制备与分组 大鼠随机分为4组:假手术组(sham组)、两肾一夹组(2K1C组)、EGCG组和哈尔碱组,每组8只。大鼠以2%戊巴比妥钠(2 mL/kg)腹腔注射麻醉,从腹部正中切口,分离左肾动脉,以直径0.2 mm的U型银夹钳夹左肾动脉,右肾动脉不触及。假手术组不夹左肾动脉,其余步骤同手术组。EGCG组及哈尔碱组大鼠在两肾一夹基础上分别喂以EGCG 100 mg·kg-1·d-1和哈尔碱 15 mg·kg-1·d-1,假手术组和2K1C 组大鼠喂以等量生理盐水,共8周。
2.2 大鼠血压、心肌标本采集与重量测定 术后8周,称取大鼠体重(body weight,BW),2%戊巴比妥钠2 mL/kg腹腔注射麻醉后分离左侧颈总动脉,插入内充有肝素及生理盐水的导管,记录动脉收缩压(systolic blood pressure,SBP)和舒张压(diastolic blood pressure,DBP),随后处死大鼠,称取左心室重量(left ventricular weight,LVW),计算左室重与体重比值(LVW/BW);取左室游离壁心肌组织,立即置入10%甲醛中,石蜡包埋切片,Masson染色,以Leica Q550 IW图像分析仪计算横截面跨核的心肌细胞面积。余左室组织经液氮冷冻后于-80℃冰箱保存备用。
2.3 免疫印迹法检测Dyrk1A和ASF蛋白质表达取大鼠左室心肌组织100 mg,提取心肌胞浆蛋白,BCA法测定蛋白浓度,经聚丙烯酰胺变性凝胶电泳分离蛋白,用湿转法将蛋白转移到聚氟乙烯膜,5%脱脂牛奶封闭,加Ⅰ抗,4℃过夜,加辣根过氧化物酶标记的Ⅱ抗,显色,凝胶成像系统分析结果,以磷酸甘油醛脱氢酶(glyceraldehyde phosphate dehydrogenase,GAPDH)为内参照,以目的条带与GAPDH的吸光度比值表示蛋白表达水平。小鼠抗大鼠Dyrk1A单克隆抗体由南通大学神经再生重点实验室刘飞教授惠赠;小鼠抗大鼠ASF单克隆抗体、小鼠抗大鼠GAPDH单克隆抗体及共同的羊抗小鼠Ⅱ抗均购自Santa Cruz。
2.4 逆转录-多聚酶链反应法检测CaMKⅡδ可变剪接 取大鼠左室心肌组织50~100 mg,用Trizol法提取RNA,在紫外分光光度计260 nm处测样品RNA浓度。取样品 RNA 5 μg逆转录为 cDNA,取cDNA 1 μg行PCR扩增。25 μL PCR 反应体系:2×PCR MasterMix(北京天根)12.5 μL 、cDNA 1 μg、20 μmol/L 双向引物各1 μL ,ddH2O 补足至25 μL。凝胶成像系统分析结果,以GAPDH为内参照,以目的条带与GAPDH的吸光度比值表示mRNA表达水平。反应条件为:98℃预变性5 min,98℃ 30 s,62℃ 45 s,72℃ 45 s,共35 个循环,72℃延伸 5 min。引物序列分别为:GAPDH[14]上游引物 5'-ATTGCATCCTGCACCACCAACTGC-3',下游引物 5'-GGAGGCCATGTAGGCCATGAGGTC-3';CaMKⅡδ上游引物[4]5'-CGAGAAATTTTTCAGCAGCC-3',下游引物 A[4]5'-ACAGTAGTTTGGGGCTCCAG-3',下游引物 B[4]5'-GCTCTCAGTTGACTCCATCATC-3',下游引物 C[4]5'-CTCAGTTGACTCCTTTACCCC-3'。
3 统计学处理
采用SPSS Statistics 17.0统计软件分析,数据以均数±标准差(±s)表示,均数比较采用单因素方差分析及q检验,以P<0.05为差异有统计学意义。
结 果
1 大鼠心肌肥厚程度及血压的变化
两肾一夹术后8周,2K1C组大鼠收缩压和舒张压较假手术组分别升高了51%和56%(P<0.05),提示大鼠高血压模型制备成功;同时2K1C组大鼠LVW和LVW/BW较假手术组升高(P<0.05),大鼠心肌病理切片观察发现手术组大鼠心肌细胞面积较假手术组增大(P<0.05),上述结果均表明该组大鼠发生心肌肥厚。与2K1C组相比,EGCG组及哈尔碱组大鼠LVW、LVW/BW及心肌细胞面积均显著下降(P<0.05),与假手术组相比无明显差异,提示EGCG及哈尔碱可以防止肾血管性高血压大鼠心肌肥厚的发生;同时发现EGCG及哈尔碱组大鼠血压与2K1C组相似,显著高于假手术组(P<0.05),提示EGCG和哈尔碱预防心肌肥厚与血压无关,见图1、表1。
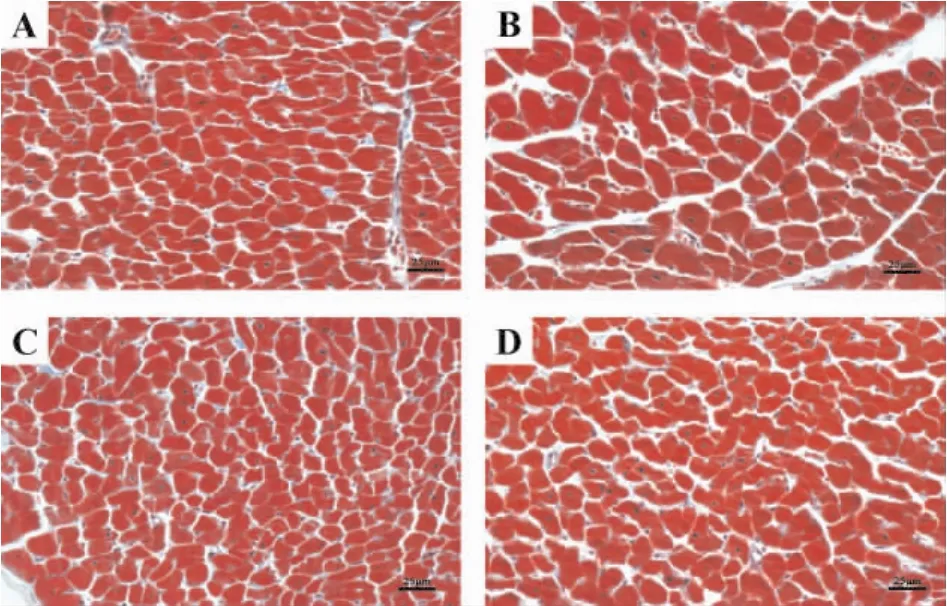
Figure 1.Masson trichrome staining of rat myocardium in different groups.Bar=25 μm.A:sham;B:2K1C;C:EGCG;D:harmine.图1 各组大鼠心肌Masson染色结果
表1 大鼠心肌肥厚程度与血压的变化Table 1.The changes of cardiac hypertrophy and blood pressure in rats(±s.n=8)

表1 大鼠心肌肥厚程度与血压的变化Table 1.The changes of cardiac hypertrophy and blood pressure in rats(±s.n=8)
*P<0.05 vs sham group;#P<0.05 vs 2K1C group.
Group Sham 2K1C EGCG Harmine SBP(mmHg) 119.9 ±21.3 180.8±23.5* 172.0 ±21.6* 174.4±19.7*DBP(mmHg) 75.9±20.1 119.5±17.0* 115.2 ±15.1* 112.4±14.1*LVW(mg) 839.4 ±48.01 062.9 ±71.1* 844.5±57.6# 872.2 ±114.6#LVW/BW(mg/g)2.19±0.22 2.49±0.11* 2.21±0.04# 2.23±0.11#Area(μm2) 153.6±75.7 368.8±73.0* 168.3±50.0# 187.6±36.9#
2 CaMKⅡδ可变剪接的改变
两肾一夹术后8周,2K1C组大鼠心肌CaMKⅡδ可变剪接表现为A、B亚型mRNA表达与假手术组相比升高,分别为假手术组的2倍和2.5倍(P<0.05),CaMKⅡδC亚型mRNA表达显著下降,为假手术组的53%(P<0.05);与2K1C组相比,EGCG组CaMKⅡδA、B亚型mRNA表达下降,分别为2K1C组的48%和43%(P<0.05),CaMKⅡδC亚型 mRNA表达升高,为2K1C组的1.7倍(P<0.05);哈尔碱组大鼠与2K1C组相比,CaMKⅡδA、B亚型mRNA表达下降,分别为2K1C组的51%和45%(P<0.05),CaMKⅡδC亚型mRNA表达升高,为2K1C组的1.8倍(P<0.05);与假手术组相比,EGCG和哈尔碱组CaMKⅡδA、B、C 3种亚型mRNA表达均无显著差异(P >0.05),见图2、表2。
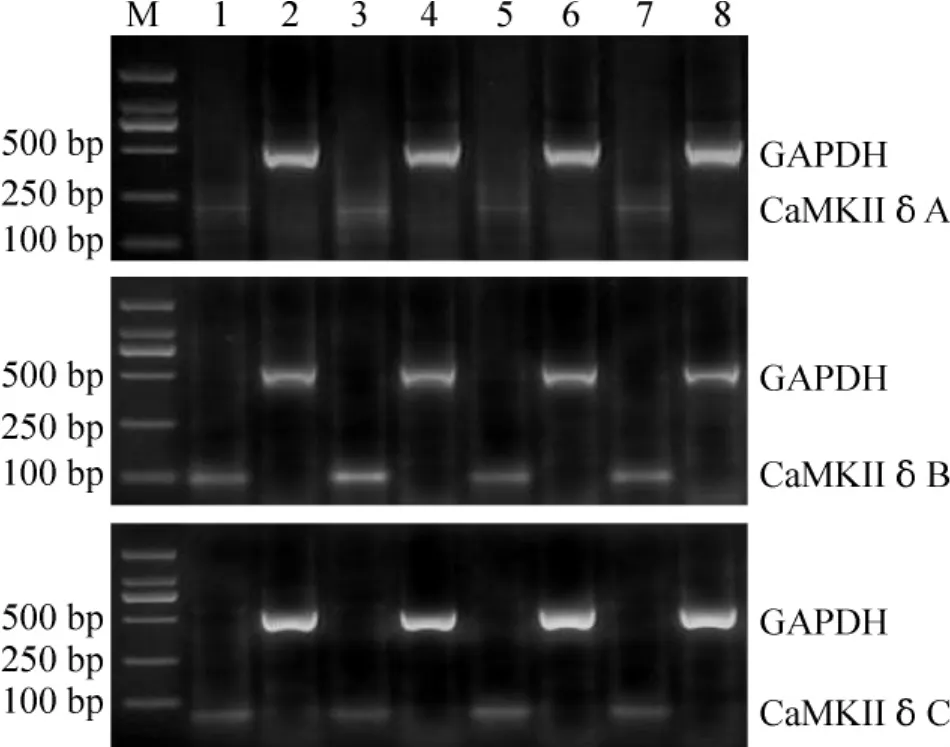
Figure 2.Changes of CaMK II δA,B and C mRNA expression in the myocardium of rats.M:marker;1,2:sham;3,4:2K1C;5,6:EGCG;7,8:harmine.图2 大鼠心肌CaMK II δA、B、C亚型mRNA表达变化
表2 不同组别大鼠CaMK II δA、B、C亚型mRNA表达的比较Table 2.The comparison of CaMK II δA,B,C mRNA expression in different groups(±s.n=8)

表2 不同组别大鼠CaMK II δA、B、C亚型mRNA表达的比较Table 2.The comparison of CaMK II δA,B,C mRNA expression in different groups(±s.n=8)
*P<0.05 vs sham group;#P<0.05 vs 2K1C group.
Group CaMK II δA CaMK II δB CaMK II δC Sham 0.051 ±0.014 0.174 ±0.028 0.143 ±0.019 2K1C 0.106 ±0.011* 0.447 ±0.050* 0.076 ±0.009*EGCG 0.051 ±0.007# 0.194 ±0.023# 0.131 ±0.012#Harmine 0.054 ±0.008# 0.203 ±0.022# 0.136 ±0.025#
3 大鼠心肌Dyrk1A蛋白质表达的变化
大鼠心肌Dyrk1A蛋白质表达以Dyrk1A蛋白与GAPDH蛋白条带的吸光度比值表示。2K1C组大鼠左室心肌Dyrk1A蛋白表达为1.651±0.282,较假手术组(0.585±0.108)升高1.8倍(P<0.05);EGCG组Dyrk1A蛋白表达为0.828±0.147,较2K1C组下降50%(P<0.05);哈尔碱组Dyrk1A蛋白表达为0.909±0.099,较2K1C组显著下降,为2K1C组的55%(P <0.05),见图3。

Figure 3.The changes of Dyrk1A protein expression in the myocardium of rats.±s.n=8.*P<0.05 vs sham group;#P <0.05 vs 2K1C group.图3 大鼠心肌Dyrk1A蛋白质表达的变化
4 大鼠心肌ASF蛋白质表达的变化
大鼠心肌ASF蛋白质表达以ASF蛋白与GAPDH蛋白条带的吸光度比值表示。2K1C组大鼠左室心肌ASF蛋白表达为0.150±0.022,较假手术组下降,表达量是假手术组 ASF蛋白表达(0.310±0.023)的48%(P<0.05);EGCG组为0.304±0.041,较2K1C显著升高,表达量为2K1C组的2.0倍;哈尔碱组 ASF蛋白表达为 0.318±0.036,为2K1C组的2.1倍(P<0.05),见图4。
讨 论
本实验利用两肾一夹的大鼠模型发现:术后8周,2K1C组大鼠收缩压、舒张压、LVW、LVW/BW和心肌细胞面积较假手术组显著升高,提示模型制备成功,大鼠血压升高并发生了心肌肥厚。实验同时发现在肥厚心肌中存在CaMKⅡδ的可变剪接调控紊乱,表现为CaMKⅡδA、B亚型mRNA表达升高,CaMKⅡδC亚型mRNA表达下调;Dryk1A抑制剂EGCG、哈尔碱在预防心肌肥厚同时,可改善CaMKⅡδ的可变剪接调控紊乱,表现为下调CaMKⅡδA、B亚型mRNA表达,并使CaMKⅡδC亚型mRNA表达升高。上述结果提示CaMKⅡδ的可变剪接调控紊乱参与了肾血管性高血压大鼠的心肌肥厚过程,也证实 CaMKⅡδ 是介导心肌肥厚的重要激酶[2,6-9]。

Figure 4.The changes of ASF protein expression in the myocardium of rats.±s.n=8.*P<0.05 vs sham group;#P <0.05 vs 2K1C group.图4 大鼠心肌ASF蛋白质表达的变化
ASF是一种富含精氨酸和丝氨酸的剪接体,参与多种前体mRNA分子的可变剪接[10]。在ASF基因心脏靶向敲除的小鼠中发现,CaMKⅡδ的剪接产物发生了变化,CaMKⅡδB表达增加,而CaMKⅡδC的表达下降,引起心脏心肌兴奋偶联机制失调,心肌肥厚,进而引起扩张性心肌病和心力衰竭[4],提示ASF参与了CaMKⅡδ的可变剪接。前期我们利用已构建的CaMKⅡδ minigene和ASF共转染COS-7或H293T细胞,发现ASF可促进 CaMKⅡδC表达,而δA和δB表达均下降,也证实了ASF对CaMKⅡδ可变剪接的调控作用[11]。ASF是受磷酸化高度调控的蛋白,不同的磷酸化水平可影响其细胞内定位和功能。Dyrk1A是一种丝/苏氨酸蛋白激酶,位于人类21号染色体的关键区域[12]。本课题组最近的研究显示Dyrk1A可磷酸化ASF,促进它转位到无活性丝氨酸/精氨酸丰富蛋白存储部位——核斑,从而抑制ASF结合到新生转录体,失去对可变剪接基因的调节作用[5],提示存在Dyrk1A经 ASF调控 CaMKⅡδ可变剪接的信号通路。
本实验发现:与假手术组相比,2K1C组大鼠在心肌发生肥厚时,心肌中Dyrk1A蛋白表达上调,ASF蛋白表达下降(胞浆 ASF蛋白表达下调考虑与Dyrk1A致ASF磷酸化后移位至核斑有关),同时心肌中CaMKⅡδ可变剪接调控紊乱。哈尔碱是目前发现的最具特异性和高效的Dyrk1A抑制剂[12-13],两肾一夹大鼠在给予哈尔碱干预后,大鼠LVW、LVW/BW及心肌细胞面积显著下降,心肌肥厚程度减轻,同时心肌中存在Dyrk1A蛋白表达下降,胞浆ASF蛋白表达上调和CaMKⅡδ可变剪接调控改善,提示Dyrk1A经ASF调控CaMKⅡδ可变剪接调控的信号通路参与了肾血管性高血压大鼠心肌肥厚的过程。
EGCG提取自绿茶,是茶多酚生物活性的主要成份,近年研究认为EGCG是特异且安全的Dyrk1A抑制剂,可以保护由于Dyrk1A过表达引起的脑损伤[14]和减轻腹主动脉缩窄所致的大鼠心肌肥厚,进一步研究发现EGCG抑制心肌肥厚的机制部分与调节丝裂素活化蛋白激酶信号通路相关[15]。本实验中,EGCG组大鼠LVW、LVW/BW及心肌细胞面积均显著低于2K1C组,提示EGCG可预防肾血管性高血压大鼠心肌肥厚;EGCG在抑制心肌肥厚同时,大鼠心肌中Dyrk1A表达上调、胞浆ASF蛋白质表达下降及CaMKⅡδ可变剪接调控改善,提示EGCG抑制肾血管性高血压大鼠心肌肥厚与其对心肌中Dyrk1A-ASF-CaMKⅡδ可变剪接信号通路的抑制有关。
[1] Colomer JM,Mao L,Rockman HA,et al.Pressure overload selectively up-regulates Ca2+/calmodulin-dependent protein kinase II in vivo[J].Mol Endocrinol,2003,17(2):183-192.
[2] Maier LS.Role of CaMKII for signaling and regulation in the heart[J].Front Biosci,2009,14:486-496.
[3] Braun AP,Schulman H.The multifunctional calcium/calmodulin-dependent protein kinase:from form to function[J].Annu Rev Physiol,1995,57(3):417-445.
[4] Xu X,Yang D,Ding JH,et al.ASF/SF2-regulated CaMKIIdelta alternative splicing temporally reprograms excitation-contraction coupling in cardiac muscle[J].Cell,2005,120(1):59-72.
[5] Shi J,Zhang T,Zhou C,et al.Increased dosage of Dyrk1A alters alternative splicing factor(ASF)-regulated alternative splicing of tau in Down syndrome[J].J Biol Chem,2008,283(42):28660-28669.
[6] Backs J,Backs T,Neef S,et al.The delta isoform of CaM kinase II is required for pathological cardiac hypertrophy and remodeling after pressure overload[J].Proc Natl Acad Sci USA,2009,106(7):2342-2347.
[7] Mishra S,Ling H,Grimm M,et al.Cardiac hypertrophy and heart failure development through Gq and CaM kinase II signaling[J].J Cardiovasc Pharmacol,2010,56(6):598-603.
[8] Li C,Cai X,Sun H,et al.The δA isoform of calmodulin kinase II mediates pathological cardiac hypertrophy by interfering with the HDAC4-MEF2 signaling pathway[J].Biochem Biophys Res Commun,2011,409(1):125-130.
[9] 李 超,刘善红,张家明,等.长期甲状腺素刺激对大鼠心肌Ca2+/钙调蛋白依赖性蛋白激酶Ⅱ的影响[J].中国病理生理杂志,2012,28(1):147-151.
[10] Dreyfuss G,Kim VN,Kataoka N.Messenger-RNA-binding proteins and the messages they carry[J].Nat Rev Mol Cell Biol,2002,3(3):195-205.
[11] Gu Q,Jin N,Sheng H,et al.Cyclic AMP-dependent protein kinase A regulates the alternative splicing of CaMKIIδ[J].PLoS One,2012,6(11):e25745.
[12] Becker W,Sippl W.Activation,regulation,and inhibition of DYRK1A[J].FEBS J,2011,278(2):246-256.
[13] Adayev T,Wegiel J,Hwang YW.Harmine is an ATP-competitive inhibitor for dual-specificity tyrosine phosphorylation-regulated kinase 1A(Dyrk1A)[J].Arch Biochem Biophys,2011,507(2):212-218.
[14] Guedj F,Sebrie C,Rivals I,et al.Green tea polyphenols rescue of brain defects induced by overexpression of DYRK1A[J].PLoS One,2009,4(2):e4606.
[15] Chen DD,Dong YG,Liu D,et al.Epigallocatechin-3-gallate attenuates cardiac hypertrophy in hypertensive rats in part by modulation of mitogen-activated protein kinase signals[J].Clin Exp Pharmacol Physiol,2009,36(9):925-932.
