半乳糖—L-赖氨酸美拉德反应产物的抗氧化活性
2012-09-05郭丽萍王凤舞唐娟
郭丽萍,王凤舞,唐娟
(青岛农业大学食品科学与工程学院,山东青岛 266109)
美拉德反应被称为非酶褐变,是食品原料中氨基化合物(氨基酸,肽和蛋白质)和羰基化合物(糖类)在食品加工和储藏过程中自然发生的反应[1]。美拉德反应历程、产物组成及其性质是氨基化合物和羰基化合物的种类、性质、以及它们的反应比例、pH、温度、反应时间、水分活度、缓冲液浓度等多种因素共同作用的结果[2]。
美拉德反应产物的抗氧化活性是由Franzke和Iwainsky[3]于1954年首次发现的,他们对加入甘氨酸-葡萄糖反应产物的人造奶油的氧化稳定性进行了相关报道。直至上世纪八十年代,关于美拉德产物抗氧化活性研究才逐渐增多,并成为当今食品营养学和食品化学的热门课题[4]。因为美拉德反应产物是食品原料在加工和贮藏中自然产生的物质,所以美拉德反应产物被认为是天然的具有抗氧化活性的物质,其中某些物质的抗氧化能力可以与食品中常用的抗氧化剂相媲美[5-7]。
本文研究了pH和加热时间对半乳糖-L-赖氨酸美拉德反应的影响,并对产物的还原能力和清除DPPH·的能力进行了检测,为美拉德反应产物的应用提供了一定的参考。
1 材料与方法
1.1 材料与试剂
无水半乳糖;L-赖氨酸盐酸盐;磷酸钠缓冲液;六亚甲基四胺缓冲液;柠檬酸;无水碳酸钠;铁氰化钾;三氯乙酸;三氯化铁;无水乙醇;DPPH·;双氧水;紫尿酸胺(TMM)指示剂;超纯水等。
1.2 仪器与设备
YY-1恒温油浴锅:天津市欧诺仪器仪表有限公司;GT-8涡轮振荡器:宁波飞驰科技有限公司;UV-2100PC紫外可见分光光度计:尤尼柯(上海)仪器有限公司;F-2500型荧光分光光度计:日本日立公司;ETTLer AE100电子天平:上海天达仪器有限公司;PHS-3C精密pH计:上海雷磁仪器厂;KQ-500B型超声波清洗器:昆仑市超声仪器有限公司。
1.3 方法
1.3.1 美拉德反应产物的制备
室温下,配制等摩尔浓度的半乳糖-L-赖氨酸溶液:浓度为0.03 mol/mL的半乳糖和0.03 mol/mL的赖氨酸盐酸盐等体积于100 mL乳盐(乳清的超滤渗透物在一定浓度、温度、pH条件下,经过一定的时间沉淀,便得到了乳盐,主要成分是磷酸钙。)溶液,磁力搅拌至晶体全部溶解。将溶液均分为3份,分别用柠檬酸和无水碳酸钠调节其pH为5、7和9;取约7 mL各pH样品分装至10 mL安培瓶中,充氮气1 min,酒精喷灯封口。将封口后的安培瓶至于120℃的恒温油浴锅,加热并不断振荡,至预订时间(5 min,10 min,15 min,20 min,30 min,1 h,2 h,3 h,4 h,6 h,8 h 和 12 h),取出样品,并放于冰水浴中快速冷却。待样品制备完全并平衡至室温,测定pH。
1.3.2 美拉德反应产物的光谱行为分析
1.3.2.1 样品的紫外-可见光(UV-Vis)扫描
将pH5和pH7的所有样品用超纯水进行100倍稀释(体积比),pH9样品为200倍稀释。利用UNICOPC-2012型分光光度计将稀释后的样品进行198 nm~501 nm的扫描,以未加热样品为对照,建立基线,记录特定波长下的光密度用于分析美拉德反应进度及产物形成情况。
1.3.2.2 样品的荧光分光光度测定
利用日立F-2500型荧光分光光度计测定347 nm波长激发下样品的350 nm~550 nm的发射光谱,记录最大发射波长下的荧光强度,用以分析美拉德反应进程及荧光性中间产物的产生与积累。
1.3.3 抗氧化能力的测定
1.3.3.1 还原能力的测定[8]
取1 mL 1.3.1中稀释后的美拉德反应产物于5 mL离心管中,加入1 mL的磷酸钠缓冲液 (0.2 mol/mL,pH6.6)和铁氰化钾(1 mL,1%)。利用涡轮振荡器将混合液振荡均匀后,将离心管至于50℃的恒温水浴中,水浴20 min后取出,加入1 mL、10%的三氯乙酸,振荡均匀。取此混合液1 mL于干燥的5 mL离心管中,加入1 mL水和0.2 mL、0.1%三氯化铁,迅速混匀。室温下静置10 min后,以未加热样品为对照,调零,测定700 nm下的吸光值,此吸光值的大小反应了样品还原能力。
1.3.3.2 DPPH·清除能力的测定[9-10]
取0.4 mL 1.3.1中稀释后的美拉德反应产物于5 mL离心管中,加入2 mL、0.1 mol/L的DPPH·无水乙醇溶液混匀,室温下于暗处放置30 min,放置过程中不断振荡;以未加热样品为对照,同条件下无水乙醇与未加热样品的混合物调零,30 min后测定反应混合液517 nm下的吸光值。因为美拉德反应产物在517 nm下有光吸收,所以同时准备样品空白,进行测定结果修正。
2 结果与分析
2.1 体系pH测定结果及分析
2.1.1 pH5体系pH测定结果
室温下在不同的加热时间段内,pH变化强度不同,如图1所示。
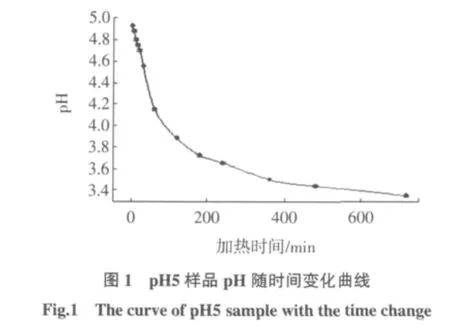
在最初的60 min加热时间内,样品pH下降了0.8个单位,但是在随后的660 min内,pH也是下降了0.8个单位。
2.1.2 pH7体系pH测定结果
pH7样品随加热时间的延长,pH也出现逐渐降低的趋势。而且在不同的加热时间段内,pH变化强度不同。pH随时间变化曲线见图2。
如图2所示,在最初的60 min加热内,样品pH下降了2.8个单位,但是在随后的660 min内,pH仅仅下降了0.8个单位。
2.1.3 pH9体系pH测定结果
任何初始pH条件下,美拉德反应进入高级阶段后都会经历降解反应,所以随着美拉德反应的进行都会有小分子的有机酸积累,从而体系pH降低,结果见图3。

如图3所示,在初始pH为9的体系中,随着加热时间的延长,样品pH也是逐渐降低的,而且不同加热时间内,降低强度不同。在最初的60 min加热内,样品pH下降了3.6个单位,在随后的660 min内,pH下降了1.1个单位。
2.1.4 体系pH变化分析
对于3个pH不同样品来讲,在反应初始的一段时间内,pH下降速度较快,而且与时间存在较好的线性关系;但是随加热时间的延长,pH下降趋于缓慢,且与时间的线性关系很差,说明羰-氨在热处理比较温和的条件下(加热时间不长),参与反应的物质较少,反应途径比较简单,降解产物如甲酸和乙酸等进行简单的积累,致使体系pH可以与反应进程呈现良好的线性关系,如表1所示。
但是,随着处理条件的加剧(加热时间持续延长),美拉德反应进入终级阶段,中间产物作为反应物参与到高级与终级阶段的降解、缩合、聚合、环化合等反应中;还有研究表明,Amadori产物和它们的二羰基降解产物在相对较高的pH下易于降解,产生低分子有机酸,所以体系在开始的时间内pH下降较快,而且在相同的pH环境中,pH变化相同。比较3个pH样品变化关系,相同时间内pH9样品变化最大。表明,美拉德反应速率随pH的增加而增加,已有大量研究证实了这个观点[11]。

表1 不同加热时间段内pH变化与时间的线性关系Table 1 The linear relationship of pH and time in different heating period
2.2 体系光度行为分析
2.2.1 体系的紫外-可见分光光度扫描结果
以各pH模型加热8 h的样品为例,研究各个模型体系美拉德反应产物的光度行为,如图4所示。从扫描结果可以看出,半乳糖-赖氨酸模型体系加热后,都在294 nm处产生了明显的光吸收,而且210 nm处也有较强的吸收峰,但是对于可见光波段处的光吸收,模型体系的表现非常不同。pH5和pH7模型在360 nm处有吸收峰,在400 nm~470 nm之间没有较强的光吸收;pH9模型在360 nm~470 nm之间没有吸收峰,物质的可见光吸收是物质结构中含有发色团,能够吸收特定波长下的光能量,所以,反应介质的初始pH能够影响终级产物-类黑素的发色团结构。

2.2.2 样品荧光测定结果
研究表明,美拉德反应可以产生具有荧光性的物质,且反应产生的荧光性先于褐色聚合物,所以认为荧光性是反应中产生的小分子中间体所具有的,从而用样品在一定激发和发射波长下荧光强度的变化来表征另一类美拉德反应小分子中间体的产生速率和积累情况[12-13],这类小分子中间体与210 nm和294 nm吸光值所指示的无色小分子中间体不同,被称为荧光中间体。3模型体系在EX/EM为347/415波长下的荧光强度随加热时间的变化如图5所示。

从图5中可以看出,美拉德反应产生荧光没有诱导期,与同体系的紫外-可见光吸收相比,在加热开始的时间内,随时间变化较为剧烈,表明荧光中间体更易于产生。各模型体系中荧光强度在加热一段时间后都达到了最大值,然后降低,表明荧光中间体比无色中间体更易于参与到美拉德反应的终级阶段,生成褐色聚合物。但是,三模型体系荧光强度到达最大值的时间不同,pH9体系在加热30 min后就达到了最大值,而pH5和pH7体系分别加热180 min和120 min后才达到最大值。这也表明随pH增加,美拉德反应速率增大。
2.3 美拉德反应产物抗氧化结果及分析
2.3.1 美拉德反应产物还原能力测定结果
测定结果如图6所示。

对于初始pH5和pH7的模型体系,其产物的抗氧化能力随时间的延长而不断增强,且在60 min时间内增长速度较快。但是,pH9模型体系中产物的还原能力随加热时间的延长,出现了极不规律的变化,即在加热15 min时达到了一个较大值,然后降低,后又逐渐增大,在加热120min到180min之间出现最大值,然后产物还原能力表现出逐渐下降的趋势。就组间比较而言,pH5和pH7样品还原能力相差不多,此两模型的产物在较低浓度下(还原能力测试浓度1.089 mg/mL)表现出较好的还原能力;pH9样品还原能力很强,在非常低的浓度下(样品测试浓度为0.544 5 mg/mL)表现出了很强的还原能力。但是500 min后,pH9的样品还原能力有所下降,可能是美拉德反应中间体——还原酮类物质及类化合物生成,这些产物也具有抗氧化等活性[14]。
2.3.2 美拉德反应产物DPPH·清除能力测定结果
美拉德反应产物自由基清除能力是通过其对DPPH·的清除能力来表征的,3个模型体系的美拉德反应产物均表现了较强的自由基清除能力。pH5和pH7体系中产物的自由基清除能力随时间而不断增加;pH9体系加热60 min后的产物对DPPH·的清除能力就已达到87%,随加热时间延长,产物的自由基清除能力基本不变。组间产物的自由基清除能力比较可以看出,pH9体系产物的自由基清除能力非常强,在0.5445mg/mL的测试浓度下,清除能力最高为92.07%。
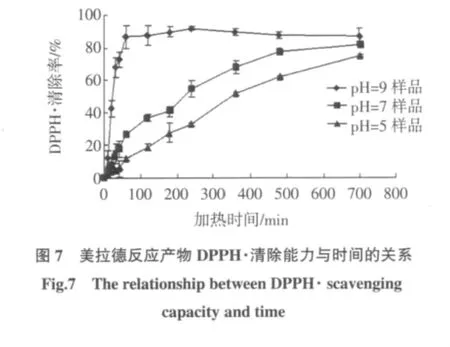
从图6和图7可以看出,3个体系在加热6 h后,美拉德反应产物的抗氧化能力趋向一致,甚至pH5和pH7样品要强于pH9,从这一方面来讲,褐色聚合物的大量积累不一定能够表现出较好的抗氧化能力,但是很多研究认为类黑素类物质是美拉德反应产物中具有抗氧化作用的主要成分。这需要进一步研究半乳糖-赖氨酸美拉德反应类黑素类物质的抗氧化作用。
3 结论
由实验结果可知,美拉德反应在碱性环境中反应速率较快,随加热时间的延长,无色中间体和荧光中间体都参与到美拉德反应的终级阶段,生成褐色聚合物,且荧光中间体参与到终级阶段的反应速度更快。
美拉德反应在碱性环境中不但反应速率较快,在反应初期反应产物的抗氧化活性也明显强于酸性和中性环境;加热600 min后,美拉德反应产物的抗氧化能力趋向一致,甚至pH5和pH7样品要强于pH9。但是pH9模型中美拉德反应最终产物-类黑素类物质生成量要远远高于pH5和pH7,从这一方面来讲,褐色聚合物的大量积累不一定能够表现出较好的抗氧化能力,但是很多研究认为类黑素类物质是美拉德反应产物中具有抗氧化作用的主要成分。所以这需要进一步研究半乳糖-赖氨酸美拉德反应类黑素类物质的抗氧化作用,而这也是研究美拉德反应产物抗氧化活性的难点所在。
:
[1]付莉,李铁刚.简述美拉德反应[J].食品科技2006(12):1-3
[2]龚巧玲,张建友,刘书来,等.食品中的美拉德反应及其影响[J].食品工业科技,2009(2):330-338
[3]Franzke C,Iwainsky H.Antioxidant capacity of melanoidin[J].Dtsch lebensm rundsch.1954(50):251-254
[4]JING H,KITTS D D.Chemical and biochemical properties of casein-sugar Maillard reaction products[J].Food and chemical toxicology,2002(40):1007-1015
[5]王惠英,孙涛,周冬香,等.美拉德反应产物抗氧化性能研究进展[J].食品科技,2007(8):12-16
[6]赵希荣.壳聚糖与葡萄糖发生美拉德反应的条件及产物的抗氧化性能[J].食品科学,2004,25(6):61-63
[7]龚平,阚建全.美拉德反应产物性质的研究进展[J].食品与发酵工业,2009,35(4):141-146
[8]Sun-Neo Lee,Nam-Sun Kim,Dong-Sun Lee.Comparative study of extraction techniques for determination of garlic flavor components by gas chromatography-mass spectrometry[J].Analytical and bioanalytical chemistry[J].2003,377(4):749-756
[9]Javier Vioque,Raul Sánchez-Vioque,Alfonso Clemente,et al.Partially hydrolyzed rapeseed protein isolates with improved functional properties[J].Journal of the American oil chemists'society,2000,77(4):447-450
[10]王惠英,孙涛,周冬香,等.L-赖氨酸和D-核糖的模式美拉德反应及其产物抗氧化性能研究[J].食品科学,2008,29(5):112-115
[11]尹姿,孙倩,景浩.木糖—甘氨酸美拉德反应蓝色产物的生成及其抗氧化性能[J].食品工业科技,2009,30(6):131-134
[12]Silvia B Matiacevich,M Pilar Buera.A critical evaluation of flurescence as a potential marker for the Maillardreation[J].Food chemistry,2006,95:423-430
[13]刘红,欧仕益,黄才欢.抗氧化剂对美拉德反应产物中荧光物质的影响[J].食品科技,2007(7):83-86
[14]马志玲,王延平,吴京洪.模式美拉德反应产物抗氧化性能的研究[J].中国油脂,2002,27(4):68-71
