水杨醛类希夫碱的合成及其光谱性能的研究
2012-08-29刘会涛周子彦
刘会涛,周子彦
(山东理工大学 化学工程学院,山东 淄博 255091)
水杨醛及其衍生物是有机合成中重要的中间体,由水杨醛及其衍生物与胺类化合物反应所生成的希夫碱在医药合成[1],分析化学[2],光致变色领域[3],有着重要的作用,还可应用于光信息存储、防护与装饰、防伪和鉴伪及光控磁性变色等功能材料[4].水杨醛类希夫碱是水杨醛的衍生物,故还有抑菌、抗病毒活性等特点[5].因此现在合成和研究水杨醛类衍生物是一大热点.
本文通过一系列反应得到了5-氯甲基水杨醛,三苯基膦盐,5-苯乙烯基水杨醛和两种水杨醛希夫碱(图1).并通过测定紫外光谱分析不同取代基对苯环吸收波长的影响.并对有些合成方法进行了一些改进,使它们的合成、纯化工艺简化,提高了产率.
1 实验部分
1.1 试剂和仪器
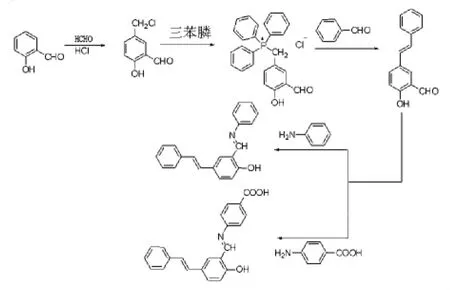
图1 反应路线图
低温冷却液循环泵(DLSD1郑州长城科技工贸有限公司) 紫外可见红外光谱仪(UV-5301PC日本岛津)核磁共振仪(AV-400德国布鲁克)数字熔点仪(RF-5301PC武汉格莱莫检测设备有限公司)调温电热套(KDM中国山东)电热鼓风干燥箱(101A-1ET中国上海).
水杨醛;三苯基膦;苯胺(使用之前减压蒸馏);对氨基苯甲酸;苯甲醛均为国内市售分析纯试剂,其他试剂和溶剂均为分析纯试剂,甲醇使用前进行了重新蒸馏,四氢呋喃使用前用金属钠干燥,苯使用前用4A分子筛干燥.其它的化学药品没有进行处理,买来直接使用.
1.2 水杨醛类衍生物的合成
1.2.1 5-氯甲基水杨醛的合成
根据文献[6],改进的实验方法为:在250mL的三口瓶中加入21mL(0.21mol)水杨醛、16mL 36%(0.21mol)甲醛水溶液和135mL浓盐酸,冰水浴搅拌下,通入干燥的HCl(g),保持反应温度在15~20℃,约1h出现白色固体,继续通HCl(g)8h,停止反应.将三口瓶用塞子密封,放置36h.抽滤,然后将粗产物用乙醚溶解,用10%碳酸氢钠溶液洗涤,并用蒸馏水洗至中性.分水后,乙醚层用无水硫酸镁干燥,干燥过夜.滤出干燥剂硫酸镁,蒸馏乙醚至近干.稍冷,加入石油醚(30~60℃)重结晶,可得白色针状结晶,真空干燥箱干燥称重为26.4g,产率为74.1%,熔点:83~85℃.(文献[6]值:产率为65%,熔点为84~86℃).
1.2.2 三苯基膦盐的合成
在100mL三口瓶中加入4.5g 5-氯甲基水杨醛,加入50mL干燥的苯,打开搅拌装置,待5-氯甲基水杨醛全部溶解之后,向三口瓶中加入7.0g三苯基膦,溶液呈淡黄色透明溶液,然后加热至回流,反应0.5h后有白色沉淀析出,继续反应4h,停止反应,抽滤出白色沉淀,所得沉淀用无水乙醇洗涤两次.烘干,称重为10.2g,产率为89.5%.
1.2.3 5-苯乙烯基水杨醛的合成
合成5-苯乙烯水杨醛用的是典型的witting反应,就是用三苯基膦盐与醛反应生成双键.具体步骤为:向250mL的三口瓶中加入40mL DMSO和10mL蒸馏水,再加入2.1g苯甲醛,打开搅拌装置.取5g三苯基膦盐溶于30mL DMSO中(溶液为乳白色),倒入恒压漏斗中,准备向三口瓶中滴定,再用一个恒压漏斗滴定12.5mL 2mol/L的NaOH溶液,两个恒压漏斗同时滴定,滴定过程大约用3h,反应温度保持在35~37℃,滴定完之后继续反应5h.
反应完毕之后,将反应混合物倒入含有155mL 0.5mol/L NaOH溶液的烧杯中,溶液中立刻有大量黄色沉淀析出,过滤出沉淀,用苯(20mL×3)萃取滤液.再用10%的HCl调节滤液的pH到3,此时析出大量的淡黄色沉淀,抽滤,并用蒸馏水洗涤沉淀三次,真空干燥箱干燥,称重为0.59g,产率:45%.
1.2.4 2-(苯亚胺基)-4-苯乙烯基苯酚(希夫碱1)的合成
将2g 5-苯乙烯基水杨醛放入100mL三口瓶中,加入35mL甲醇,打开搅拌装置,待其全部溶解,然后用恒压漏斗滴加含有0.92g苯胺的15mL甲醇溶液,滴加45min,溶液成淡黄色,继续搅拌,30min后出现橘红色沉淀,继续反应2h,抽滤,真空干燥箱干燥,称 重 为2.2g,产 率 为:75%.1H NRM(400MHz,DMSO):δ7.885(s,H),δ8.966(s,H),δ7.141(d,2H,J=16),δ6.999(d,H,J=8.0),δ7.425(d,2H,J=8.0),δ7.575(d,2H,J=8.0),δ7.698(d,H,J=8.0),δ7.378(dd,2H,J=16.0),δ7.468(dd,2H,J=16.0).
1.2.5 4-(2-羟基-5-(苯乙烯基)氨基)苯甲酸(希夫碱2)的合成
将1.5g 5-苯乙烯基水杨醛放入100mL三口瓶中,加入30mL甲醇,打开搅拌装置,待其全部溶解,然后用恒压漏斗滴加含有0.92g对氨基苯甲酸的20mL甲醇溶液,滴加1h,溶液成淡黄色,继续搅拌,45min之后有少量沉淀析出,继续反应2.5h,抽滤,真空干燥箱干燥,称重为1.8g,产率:73%.1H NRM(400MHz,DMSO):δ7.920(s,H),δ8.989(s,H),δ7.145(d,2H,J=16.0),δ7.016(d,H,J=8.0),δ7.492(d,2H,J=8.0),δ7.577(d,2H,J=8.0),δ8.025(d,2H,J=8.0),δ7.377(dd,2H,J=16.0).
2 结果与分析
2.1 5-氯甲基水杨醛合成条件的讨论
文献[6]中,出现沉淀之后再通HCl 2.5h,密封24h,而本文通过大量的实验研究,我们得到了生成5-氯甲基水杨醛最优的条件为出现沉淀继续通HCl 8h,密封放置36h,使其产率从文献的65.0%提高到了74.1%.
2.2 物料配比对三苯基膦盐生成的影响
本文做了几组三苯基膦和5-氯甲基水杨醛的反应,研究物料配比对产率的影响,图2是反应物的配比对产率的影响,从图2中可以发现当n(三苯基膦):n(5-氯甲基水杨醛)=1.1时,产率已经最大,是这个反应的最佳物料配比.因为当物质的配比为1.1时,5-氯甲基水杨醛已经达到了最大的转化率,此时,再增加三苯基膦的用量对反应已经没有影响.

图2 物料配比对三苯基膦盐产率的影响
2.3 生成5-苯乙烯基水杨醛的讨论
生成5-苯乙烯基水杨醛是合成水杨醛衍生物中最关键的一步,刚开始得到的产率很低,是因为没有把三苯基膦盐往苯甲醛里滴加,而是直接把苯甲醛和三苯基膦盐混合在一起反应,这样做之所以产率低是因为5-氯甲基水杨醛的三苯基膦盐中本身就有一个醛基,所以有一部分膦盐自身就发生了反应,因次我们要把膦盐往苯甲醛中滴加,这样可以使醛基始终处在相对过量的状态.因此,我们就想到底让苯甲醛过量几倍才能使三苯基膦盐反应完全?因此,我们做了许多实验,探讨n(苯甲醛)∶n(三苯基膦盐)为何值时,三苯基膦盐反应最完全.从图3可以看出当苯甲醛为三苯基膦盐的1.5倍时,产率最高.
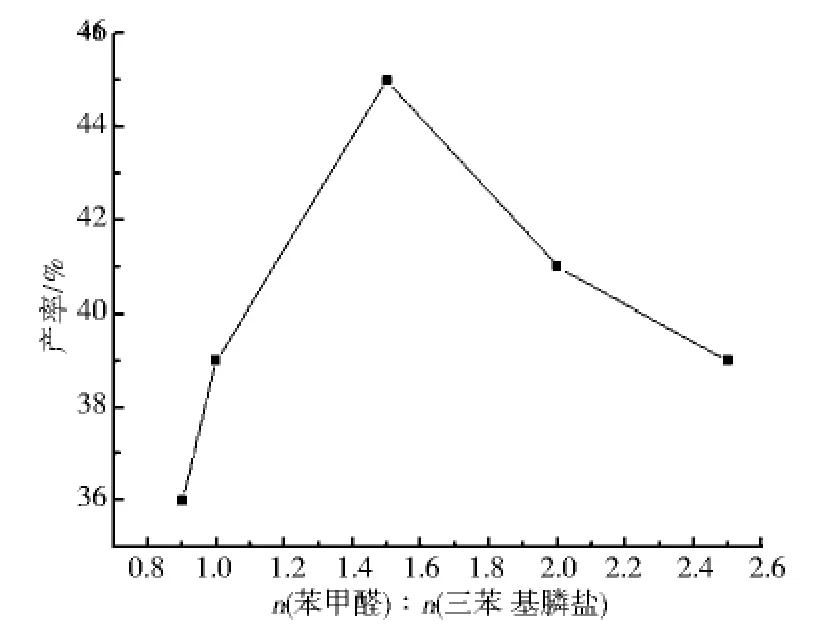
图3 物料配比对5-苯乙烯基水杨醛产率的影响
2.4 5-苯乙烯基水杨醛的紫外光谱
上图是5-苯乙烯基水杨醛溶解在THF中的紫外吸收光谱图,从图中我们可以看出,该化合物的紫外吸收光谱有三个吸收峰:261、307和370nm,261nm为苯环的特征吸收峰,为B吸收带,是由ππ*跃迁产生的;307nm处为C=C键的特征吸收;370nm为整个分子的吸收峰,是共轭体系的特征吸收峰.

图4 5-苯乙烯基水杨醛在THF中的紫外光谱
2.5 2-(苯亚胺基)-4-苯乙烯基苯酚(希夫碱1)的紫外光谱

图5 希夫碱1在THF和甲醇中的紫外光谱
从图5可以看出希夫碱1在THF和甲醇中都是有三个吸收峰,在THF中的吸收峰分别为:237、276和308nm,而在甲醇中的吸收峰分别为:226、252和280nm,我们可以发现在甲醇中的吸收峰比在THF中的吸收峰发生了明显的蓝移,分别蓝移了11、24和28nm,这是因为希夫碱的紫外吸收峰是由n-π*跃迁引起的,极性溶剂分子和溶质可能形成氢键,极性溶剂分子的偶极矩使溶质分子的极性增强,因而在极性溶剂中n-π*跃迁所需能量最大,吸收波长蓝移[7],因此看出希夫碱1具有明显的溶剂效应.
2.6 4-(2-羟基-5-(苯乙烯基)氨基)苯甲酸(希夫碱2)的紫外光谱

图6 希夫碱2在THF和甲醇中的的紫外光谱
图6是希夫碱2在THF和甲醇中的紫外光谱,从图中我们可以看出它在THF的吸收峰分别为238、285、317和386nm,而在甲醇中的吸收峰分别为223、317和374nm,由于希夫碱2在甲醇极性溶剂中受溶液极性的影响,使C=C键的吸收峰没有表现出来,希夫碱2和希夫碱1一样,紫外吸收峰也有一定程度的蓝移.同时比较图5和图6,我们可以发现希夫碱1和2的吸收峰也有变化,苯环的特征吸收峰变化不大,但是C=C的吸收峰红移达到了30nm,整个分子的吸收峰红移达到了70nm,这都是因为希夫碱2比希夫碱1多了一个羧基引起的,因为羧基是很强的吸电子基团.而在甲醇极性溶剂中,由于极性溶剂的作用,使得相应的峰值都发生了不同程度的蓝移.
3 结束语
本文通过大量实验得到了制备5-氯甲基水杨醛的最佳条件:通HCl 8h,静置36h;制备三苯基膦盐的最佳物料配比为n(三苯基膦):n(5-氯甲基水杨醛)=1.1;制备5-苯乙烯基水杨醛的最佳物料配比n(苯甲醛):n(三苯基膦盐)=1.5;测得了一系列化合物的紫外光谱,并讨论了目标化合物的紫外光谱受溶剂的极性影响.鉴于合成的这两种化合物的良好发光性能,预计在有机电致发光材料中有很好的应用前景.
[1]Desai S B,Desai P B,Desai K R.Synthesis of some Schiff bases thiazolidinones and azetidinones from 2,6-diaminobonzol[1,2-d:4,5-d]bisthiazole ane their anticancer activities[J].Hetercycl Commun,2001,7(1):83-90.
[2]Bastos M B R,Moreira J C,Farias P A M.Adsorptive stripping voltammetric behaviour of VO2(Ⅱ)complexed with the Schiff base N,N-prime-ethylenebis(salicylidenimine)in aqueous 4-(2-hydroxy-ethyl)-1-piperazine ethanesulfonic acid medium[J].Analytica,2000,408:83-88.
[3]赵建章,赵冰,徐蔚青,等.Schiff碱N,N,-双水杨醛缩-1,6己二胺的光致变色光谱的研究[J].高等学校化学学报,2001,22(6):971-975.
[4]吴锦明,汤艳峰,沈爱宝.硅胶负载H6PMo9V3O40催化合成5-硝基水杨醛 [J].应用化学,2012,29(5):545-550.
[5]耿建坡,王永辉,岳国义,等.变电站10kV电压互感器误差测试中的问题分析及对策[J].河北电力技术,2010,37(12):212-215.
[6]刘祥,何炜.几种取代水杨醛合成方法的改进[J].化学试剂,2001,23(4):237-238.
[7]郭仁.电子效应,空间效应,溶剂效应对紫外光谱的影响[J].玉溪师范高等专科学校学报,2000,16(3):55-57.
