葡萄糖在微生物燃料电池中的应用研究进展
2012-08-16徐金球王利军白建峰黄思超汤志涛
徐金球,梁 波,王利军,白建峰,黄思超,汤志涛
(上海第二工业大学城市建设与环境工程学院,上海 201209)
葡萄糖在微生物燃料电池中的应用研究进展
徐金球,梁 波,王利军,白建峰,黄思超,汤志涛
(上海第二工业大学城市建设与环境工程学院,上海 201209)
简要介绍了微生物燃料电池的特点、发展历史与工作原理,重点概括了近年来葡萄糖作为最常用的有机底物在MFC利用废水产电应用中的研究进展,最后展望了微生物燃料电池的应用前景。
微生物燃料电池;废水;产电;葡萄糖
0 引言
微生物燃料电池(microbial fuel cells,简称MFC)是利用微生物自身的代谢来实现有机物的降解和电子的转移而使化学能直接转化为电能的生物化学催化装置[1-2]。MFC技术不但可以用来处理废水,而且可以从废水的污染物中收获电能[3-4]。对MFC的研究开始于1910年英国植物学家Potter[3]以葡萄糖底物,以酵母和大肠杆菌为产电微生物,在MFC中获得了电压。Habermann等第一次将MFC用于处理废水进行了探索[5]。此后,MFC在空间科学研究领域取得了较大进展[6]。由于与常规燃料电池相比,MFC具有燃料来源多样化、操作条件温和、无污染、可实现零排放、无需能量的输入等方面的优点[7],用MFC技术来处理污水或废水成为近年来国内外的研究热点。20世纪80年代,电子传递中间体成为研究的热点,这类介体的广泛应用,使MFC的输出功率有了很大提高。90年代后,随着研究的进行,发现了不通过介体就能够进行电子传递的微生物,就此开始了对无介体MFC的研究[3]。在无介体MFC中,底物作为能量转化的来源,它的类型和利用效率影响着微生物群落的结构及生长速度,成为决定产电效率高低的重要因素之一,因此底物分析对提高MFC的产电能力具有重要的意义。
糖类是自然界中存在数量最多、分布最广且具有重要生物功能的有机化合物,其中既包括结构简单的单糖如葡萄糖,又包括双糖如蔗糖等,还包括结构复杂的多糖如纤维素、壳聚糖等。由于葡萄糖是微生物最好的碳源之一,因此,它成为MFC阳极室中最常用的有机底物。在MFC的研究发展过程中,葡萄糖作为主要的研究对象或者辅助的研究对象经常出现在MFC的各类研究论文中。本文主要介绍有关葡萄糖在MFC研究中的应用情况。
1 MFC的工作原理
以葡萄糖为底物的燃料电池为例,MFC通过在厌氧条件下氧化电子供体,并将电子传递到阳极上实现其功能[8]。当在阴极室中有氧气作为电子受体时,MFC一般由厌氧的阳极区和好氧的阴极区组成。阳极室内的微生物在厌氧条件下代谢水中的有机质(葡萄糖等),产生电子和质子。电子传递到阳极,再经由外电路到达阴极;质子则穿过质子交换膜或直接通过电解质到达阴极。在阴极室,质子、电子和氧气相结合生成水,从而完成整个生物电化学的电子转移过程[9]。阴阳两极之间存在电位差,最高电位可达0.5 V ~ 0.8 V。通过对反应器的集成,可以将这样的低电压转换成较高电压,从而获得可利用的电能[10]。
以葡萄糖作为底物为例,其阴阳两极反应如下式所示:
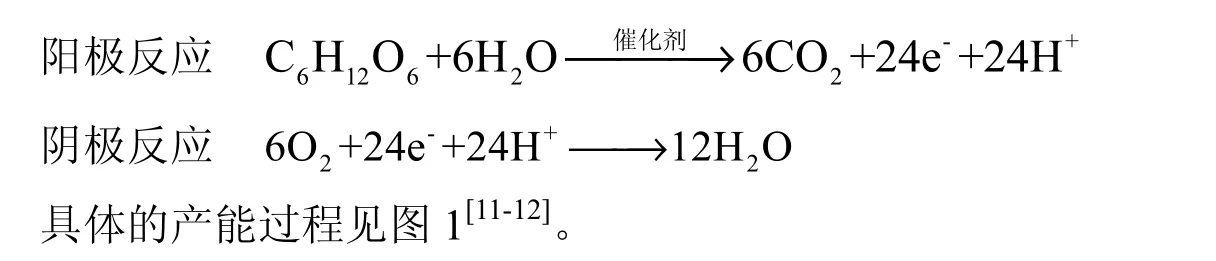

图1 微生物燃料电池工作原理示意图Fig. 1 Schematic diagram of working principle of microbial fuel cells
2 葡萄糖在MFC中的应用研究
2.1 以葡萄糖为底物对MFC产电微生物的研究
在MFC产电体系中,产电微生物对MFC输出功率有很大的影响,因此研究选择高活性微生物显得尤其重要。由于葡萄糖是微生物最好的碳源,因此在筛选产电微生物的过程中常被选为有机底物。
有一种新颖的微生物——铁还原红螺菌(Rhodoferax ferrireducens)能在MFC中将葡萄糖氧化成二氧化碳,并能够定量地将电子转移至石墨电极而无需传递电子的中介体,通过从电子传递过程所产生的能量可以获得长期的稳定的电能[14]。
有人以葡萄糖为燃料,以铁还原红螺菌(Rhodoferax ferrireducens)为产电微生物,对MFC的产电情况、产电原理进行研究。结果表明[15]:当外电阻为510 Ω时,常温下产生的电流密度为158 mA·m−2(平台电压为0.46 V,电极有效接触表面积为57 cm2),且循环性能良好。通过SEM观察发现,大量微生物吸附在石墨电极上,运行20 d后,用Bradford法测得悬浮细胞蛋白浓度为140 mg·L−1,吸附在电极上的生物量为1 180 mg·m−2。通过数据采集分析和细菌还原试验发现:吸附在电极上的微生物对电压的产生贡献最大,具有电化学和生物学活性;悬浮细胞对产电贡献很小,不具有电化学和生物学活性。
为了弄清MFC阳极生物膜内多种微生物群落与竞争和群落演替有关的生态学问题,有人采用厌氧污泥接种三室MFC与双室MFC,以乙酸、乳酸、葡萄糖为有机底物进行试验研究[16]。结果表明,所有的阳极微生物群落所包括的系列与硫还原地杆菌(Geobacter sulfurreducens)密切相关,相似度达到99 % 以上。与此同时,在大多数阳极的生物膜中也富集了许多其他与Geobacter相似序列的微生物。尽管分别采用上述三种底物在MFC中进行了试验,但是仅发现了在以葡萄糖为称底物的MFC中存在厚壁菌门微生物(Firmicutes),厚壁菌门微生物所起的作用是在MFC中将复杂有机碳转化为简单分子并清除在阳极区的氧气。
詹亚力等[17]考察了一个长期以葡萄糖为营养液的MFC对不同底物的适应性,通过形态学、生理生化特性和16SrDNA分析等手段对电池两极的优势微生物进行了分离与鉴定,并通过MFC方法确定了各微生物的电化学活性。结果显示:长期以葡萄糖为底物的MFC可以快速适应以其它单糖、二糖或糖类代谢产物为底物的环境;以代谢产物为底物时,电池输出最大电压、库仑效率均明显高于糖类物质;从电池阳极分离出三种微生物,经DNA分析可以确定它们分别为绿脓杆菌、地衣芽孢杆菌和肺炎克雷伯氏菌,经MFC进一步验证它们均为电化学活性微生物。
有研究结果显示[18],MFC阳极微生物菌群组成与MFC产电性能有重要关系。从稳定运行了210 d以上、以200 mg·L-1喹啉为燃料的MFC阳极室分离提纯出4株兼性厌氧菌Q1, b, c和d,分别代表原MFC中4类不同菌落形态的可培养菌。16 Sr DNA序列分析结果表明,菌株Q1, c和d属于假单胞菌属(Pseudomonas sp.),菌株b属于伯克霍尔德菌属(Burkholderia sp.)。通过构建双室 MFC,以200 mg·L−1喹啉和300 mg·L−1葡萄糖为混合燃料,以铁氰化钾为电子受体测定各菌株产电能力。结果表明,菌株b, c和d均为非产电菌。产电菌Q1与非产电菌b, c, d复合产电的电荷量依次为3.00 C, 3.57 C和5.13 C,库仑效率依次为3.85 % , 4.59 %和6.58 % 。GC/MS的测定结果表明,产电菌株Q1构建的纯菌MFC和原混合菌对喹啉代谢的产物均为2-羟基喹啉和苯酚。
2.2 以葡萄糖为底物对MFC影响因素的研究
在MFC产电体系中,除了产电微生物对MFCs的输出功率有影响以外,其它的因素如电池的结构、电极材料、电池的内阻与外阻、阳极室与阴极室缓冲溶液的组成等对MFC输出功率亦有不同程度的影响。葡萄糖作为微生物最好的碳源,以它为MFC的有机底物对MFC的影响因素进行研究并进行优化有利于使研究工作简化并取得预期的成果。
利用厌氧活性污泥为接种体,以葡萄糖作底物,当外电阻为1 000 Ω时,MFC产生了0.41 V的电压,最大功率密度为192.04 mW·m−2,葡萄糖的去除率为87 % 。但电子回收率仅为10 % 左右,主要原因是由于阴极对氧气分子的透过作用引起的微生物好氧呼吸导致了电子损失[19]。
Cheng等[20]的研究结果表明,在空气阴极单室MFC中,以葡萄糖为底物,如果反应器的操作是以连续平流的模式由阳极流向阴极,则可以通过降低电极间距而使功率输出得到增加。
为了减小氧气的输送对产电的不利影响,有人研究设计了具有挡板的无膜MFC。为了减少阴极附近的混合,对反应器进行了特殊的设计。通过添加厌氧生物/污泥(COD浓度为4 330 mg·L−1)来促进阴极上形成大于1 mm的厚生物膜。当以葡萄糖为底物时的COD浓度在96 mg·L−1~ 960 mg·L−1的范围内时,电池的总库仑效率超过30 % 。而作者前期所做的研究工作结果表明,在完全混合的无膜MFC中的库仑效率小于10 % 。这些研究结果表明,由生物质所提供的pH缓冲作用在将电子传输至阳极的过程中起着重要的作用,电力的产生主要与葡萄糖的降解相关,厌氧污泥本身能够提供的电子非常有限[21]。
Chung等[22]为了评价用MFC处理含有10 mM葡萄糖的模拟废水连续产电的可能性研制了一个无介体的三级双室MFC系统并使之连续运行了1.5年。当阳极的水力停留时间为4.5 h、磷酸盐缓冲液作为阴极电解液时,所获得的稳定功率密度为28 W·m−3,总的可溶性有机碳去除率约为85 % ,库仑效率约为46 % 。
有人以葡萄糖为底物,利用所构建的单室MFC研究了阴极板中铁离子浓度、阳极底物的浓度及阳极板面积对单室直接MFC性能的影响[23]。结果表明:随着阴极电极板中Fe3+含量的增加,电池负载输出电压随之提高;随着底物中所产生的电子和质子数的提高,电量随之增大,输出电压亦随底物浓度的增加而提高。增加阳极板数量可以使更多的微生物吸附在阳极电极上并传递电子,但电池的输出电压与阳极板的数量不成倍数关系。
陶虎春等[24]通过MFCs与传统厌氧消化(conventional anaerobic digestion, CAD)对比试验考察了对高浓度葡萄糖人工废水的处理效果。在以葡萄糖为碳源、初始TOC为2 100 mg·L−1、运行时间为144 h的条件下,MFCs获得了91.61 % 的TOC去除率,CAD获得了58.85 % 的TOC去除率。当NH3-N的初始浓度为500 mg/L时,MFC的NH3-N去除率为92.61 % ,CAD的NH3-N去除率为72.38 % 。
在一个经典的双室MFC中,在接种厌氧污泥的条件下,采用间歇运行的方式对葡萄糖模拟废水的产电性能研究结果显示[25],当外阻为100 Ω时,该电池在初始COD为1 000 mg·L−1时,以石墨为电极的运行条件下产电性能最好,最大电流密度为4.4 mA·m−2[25]。
孔载英等[26]研究了自行设计的MFC。在常温常压下,以厌氧污泥为接种源,以葡萄糖为底物,以不同溶液作为电子受体的条件下测试其稳定运行的影响因素与工艺条件。试验结果表明:该MFC可稳定运行约30 d ,在注入新的底物后,电压又快速回升至稳定电压。以铁氰化钾溶液为电子受体,输出电压可达0.75 V,输出功率为2 100m W·m−2;以高锰酸钾作为电子受体,输出电压为1.023 V,输出功率为2 638 mW·m−2。
有研究者以活性碳颗粒为阳极,空气电极为阴极,构建了上流式单室MFC,考察了电解质质量浓度和葡萄糖质量浓度等因素对MFC性能的影响[27]。结果表明:当电解质KCl的质量浓度由10 g·L−1增加到25 g·L−1时,MFC的内阻由19 Ω 降低到3 Ω ,最大输出功率密度由5 827 mW·m−3增加到18 021 mW·m−3;当KCl的质量浓度为25 g·L−1、葡萄糖的质量浓度从100 mg·L−1增加到1 000 mg·L−1时,MFC的最大输出功率密度由10.308 W·m−3提高到了19.371 W·m−3。
2.3 葡萄糖与其他有机底物在MFC中作用效果的比较
葡萄糖作为微生物最好的碳源而成为MFC阳极室中最常用的有机底物,也因此成为MFC对其它有机底物降解效果的参照物。
分别以醋酸、丁酸酯、丙酸酯和葡萄糖为MFC的底物,将它们接种厌氧污泥后运行了一年多的试验结果表明[28]:电池的库仑效率(CE)和输出功率随底物的不同而不同,而细菌的活力却相似。以醋酸为底物的MFC的库仑效率最高(CE 72.3 % ),其次是丁酸酯(43.0 % )、丙酸酯(36.0 % )和葡萄糖(15.0 % )。导致葡萄糖为底物时库仑效率最低的原因可能是其本身的可发酵性质。
骆海萍等[29]选取城市污水处理厂的好氧和厌氧混合污泥作为接种液,构建了双极室MFC,分别以单一葡萄糖、葡萄糖与苯酚混合物、单一苯酚为燃料的MFC进行了有机物降解和产电效果的试验研究。结果表明,以单一葡萄糖为燃料时MFC的启动时间最短,以单一苯酚为燃料时MFC的启动时间最长。MFC在不同燃料来源条件下对苯酚的去除率均大于85 % ,对COD的去除率超过80 % 。MFC的连续运行试验结果表明:在外电阻为1 000 Ω时,以单一葡萄糖为燃料的MFC运行周期最长,可达400 h ,最大输出电压为551 mV,功率密度为121 mW·m−2(阳极);以葡萄糖和苯酚为混合燃料的MFC运行周期约200 h ,最大输出电压为208 mV,功率密度为16 mW·m−2(阳极);而以单一苯酚为燃料的MFC运行周期仅约为100 h ,最大输出电压为121 mV,功率密度为6 mW·m−2(阳极)。这些结果为酚类难降解有机物的高效低耗处理提供了新的研究思路。
宋天顺等[30]以厌氧污泥作为初始接种体,分别以葡萄糖和丁二酸为底物,构建了一个直接MFC,将微生物经过160 h的驯化后,当外电阻为1 000 Ω时,所获得的最大电压为590 mV,同时考察了底物和催化剂对电池性能的影响。结果表明:葡萄糖的最大功率密度为669 mW·m−2,丁二酸的最大功率密度为235 mW·m−2,显然前者高于后者。
为了探讨污水中复杂有机质对MFC性能的影响,以浓度均为8 g/L的乙酸钠、葡萄糖、蔗糖、D-木糖、可溶淀粉为底物所进行的MFC产电性能的试验研究结果显示[31]:乙酸钠电池内阻为64 Ω ,最大体积功率密度达到3.7 W·m−3;葡萄糖的电池内阻为84 Ω,最大功率密度2.67 W·m−3;D-木糖的电池内阻为167 Ω,最大功率密度为1.37 W·m−3;蔗糖的电池内阻为68.3 Ω,最大功率密度为2.4 W·m−3;淀粉的电池内阻为236 Ω,最大功率密度1.36 W·m−3。这些结果表明,MFC可利用各种含糖有机物进行产电,在底物浓度相同的条件下,底物越简单,电池的启动时间越短,内阻越小,输出功率越大,库仑效率越大。
强琳等[32]采用空气阴极MFC,分别以葡萄糖、乙酸钠、蛋白胨和可溶性淀粉配制模拟生活污水,探讨了MFC处理模拟生活污水的特性。结果表明:不同的底物浓度对产电效率的影响差异不大,MFC最大输出功率为23.67 mW·m−2,COD最大去除率为88 % ;以不完全复合碳源和单一碳源为底物、接种混合菌的MFC对底物的选择性试验的结果表明, MFC处理复杂有机碳源(蛋白胨、淀粉)的产电效率优于处理简单分子有机碳源(葡萄糖、乙酸钠);讨论了硼砂缓冲液对产电的影响,50 mmol·L−1的硼砂缓冲液输出功率密度最大,最大功率为19.77 mW·m−2,COD最大处理率为72 % 。
2.4 多种底物存在时葡萄糖与其他底物的协同作用
葡萄糖作为基础的有机碳源和最常见的有机底物常常应用于MFC降解其它难降解有机底物的研究工作中,研究者这样做的目的在于,在微生物开始降解有毒难降解的有机底物之前给微生物提供一个基本的生存条件以及使微生物逐步适应不利的环境。
双陈冬等[33]利用淡水沉积物为接种源并以葡萄糖为底物构建了MFC,考查了苯酚对该MFC性能的影响。结果表明,电流的产生是由富集在电极表面的细菌引起的。当加入相同浓度的葡萄糖时,苯酚的加入降低了细菌消耗葡萄糖的速率,但同时延长了产电时间。
通过构建双室MFC,在葡萄糖存在的条件下,对MFC降解喹啉及产电性能进行研究的结果表明[34]:当喹啉初始浓度为500 mg·L−1,葡萄糖与喹啉浓度之比分别为11, 35, 15时,MFC的最大输出电压分别为558 mV, 469 mV, 328 mV,运行周期分别为56.4 h, 70 h, 82.5 h;最大功率密度分别为173 mW·m−2, 122 mW·m−2, 60 mW·m−2(按阳极截面积计算)或者35 W·m−3, 24 W·m−3, 12 W·m−3(按阳极室有效容积计算)。MFC可实现对喹啉的高效降解,但葡萄糖的浓度对喹啉的降解速率有较大影响。MFC以用喹啉和葡萄糖作为混合燃料时,可以在实现高效降解喹啉的同时稳定地向外输出电能,这为杂环芳烃类难降解有机物的高效低耗处理提供了新的途径。
毕哲等[35]构建了生物阴极型微生物燃料电池(BCMFC),研究了以葡萄糖与偶氮染料(活性艳红X3B)为共同底物时,BCMFC的产电性能及偶氮染料的降解特性。结果表明,电能的产生源于BCMFC对葡萄糖的降解,共代谢下活性艳红X3B的(ABRX3B)的生物降解是主要的脱色机理。当葡萄糖的初始浓度为500 mg·L−1(以COD计),ABRX3B浓度低于300 mg·L−1时,功率密度恒定为50.7 mW·m−2,最终脱色率在94.4 %以上。在共底物的条件下,BCMFC可成功地实现同步电能输出和高效脱色。
在以碳纸为阳极、空气电极为阴极、葡萄糖和对硝基苯酚为混合燃料的直接空气阴极单室MFC中,考察对硝基苯酚的降解及MFC的产电特性的研究结果表明[36]:MFC对废水中不同浓度的对硝基苯酚均有一定的去除效果,400 mg L−1的对硝基苯酚降解4 d的去除率为74.11 %,降解6 d的去除率为82.11 %。MFC的输出电压最高为0.293 V(外阻1 000 Ω),最大输出功率密度为56.5 mW m−3。
赵娟等[37]针对目前太湖流域存在大量蓝藻的情况,研究开发了从蓝藻水中回收电能、同时将其中的有机污染物降解的沉积型微生物燃料电池(Sediment Microbial Fuel Cell, SMFC)体系。主要考察了不同类型的底物对SMFC体系产电特性的影响。结果表明,底物的类型对所构建的SMFC体系的运行特性有较大的影响。功率密度峰值依蓝藻加乙酸钠、蓝藻、蓝藻加葡萄糖和空白体系的顺序递减,分别为15.59 mW·m−2, 12.72 mW·m−2, 10.52 mW·m−2, 8.35 mW·m−2。COD去除率则依蓝藻加乙酸钠、蓝藻加葡萄糖、蓝藻和空白体系的顺序递减,分别为60.1 %, 27.2 %, 19.6 %, 18.1 %。功率密度和COD去除率变化规律的区别,主要归因于发酵型底物葡萄糖的存在导致体系中去除的COD并非全部被产电微生物所利用。
通过构建填料型MFC,分别以葡萄糖和苯为单一燃料以及以葡萄糖加苯混合燃料对MFC的产电性能及苯的降解效果的研究结果表明[38]:以1 500 mg·L−1葡萄糖作为单一燃料时,MFC可获得的最高功率密度为228 mW·m−2(阳极),相应的体积功率密度为20.5 W·m−3(按阳极室有效体积计算),MFC的库仑效率为15.7 %;以1 000 mg·L−1苯作为单一燃料,外电阻为1 000 Ω时,最高功率密度为9.5 mW·m−2(阳极),体积功率密度为0.9 W·m−3;以1 000 mg·L−1葡萄糖加600 mg·L−1苯为混合燃料时,最高功率密度为288 mW·m−2(阳极),相应的体积功率密度为25.9 W·m−3,MFC在24 h内可将苯完全降解,产电周期结束时MFC的COD去除率在95 %以上,MFC的库仑效率为2.3 %。这些结果为苯类难降解有机物的高效低耗处理提供了新的研究思路。
通过构建双室MFC,以铁氰化钾溶液为阴极电子受体,以硝基苯(nitrobenzene,NB)和葡萄糖为混合燃料,对MFC的产电特性和NB降解的研究结果表明[39]:当外阻为1 000 Ω时,随着NB初始浓度的增加,双室MFC的产电特性明显受到抑制。当葡萄糖浓度为1 000 mg·L−1,NB初始浓度分别为0 mg·L−1, 50 mg·L−1, 150 mg·L−1, 250 mg·L−1时,MFC的运行周期逐渐缩短,分别为55.7 h, 51.6 h, 45.9 h, 32.2 h;最大输出电压分别为670 mV, 597 mV, 507 mV, 489 mV;最大体积功率密度分别为28.57 W·m−3, 20.42 W·m−3, 9.29 W·m−3, 8.47 W·m−3;电荷量分别为65.10 C, 43.50 C, 35.48 C, 30.32 C。当以NB和葡萄糖为混合燃料时,MFC可以在稳定地输出电能的同时,实现有机物高效降解,NB的去除率高达100 %,对COD的去除率达到87 % ~ 98 %。但以250 mg·L−1NB为单一燃料时,MFC无明显产电现象。DGGE图谱表明,NB的加入改变了MFC阳极电极上微生物的群落结构。
罗勇等[40]以铁氰化钾为电子受体,在两极阴阳室内使用碳毛刷纤维为电极材料构建了循环式MFC,研究了以吲哚为单一燃料和以吲哚加葡萄糖为混合燃料条件下MFC的产电特性以及对吲哚和COD的去除效果。结果表明:以1 000 mg·L−1葡萄糖加250 mg·L−1吲哚为混合燃料时,MFC的最高电压和最大功率密度分别为660 mV和51.2 W·m−3(阳极),MFC运行10 h对吲哚和COD的去除率分别为100 %和89.5 %;分别以250 mg·L−1和500 mg·L−1的吲哚为单一燃料时,MFC的平均最高电压分别为115 mV和118 mV,最大功率密度分别为2.1 W·m−3(阳极)和2.3 W·m−3(阳极)。在MFC中,250 mg·L−1和500 mg·L−1的吲哚被完全降解的时间分别为6 h和30 h。这些结果表明:MFC能够利用吲哚为燃料,在实现高效降解吲哚的同时对外产生电能,可用于处理含有毒且难降解有机物的焦化工业废水。
通过构建空气阴极型双室MFC,以苯胺和葡萄糖为燃料,对MFC降解苯胺的特性及产电性能的研究结果表明[41]:当外电阻为1 000 Ω时,以500 mg·L−1的葡萄糖为单一燃料时,MFC的最大输出电压为440 mV,最大输出功率密度为215 mW·m−2。当苯胺的初始浓度为500 mg·L−1,葡萄糖的浓度分别为500 mg·L−1, 300 mg·L−1和100 mg·L−1时,MFC的最大输出电压分别为430 mV, 402 mV和390 mV,最大输出功率密度分别为205 mW·m−2, 180 mW·m−2和169 mW·m−2(按阳极截面积计算)。高浓度苯胺对MFC利用葡萄糖进行产电有一定的影响。104 h内苯胺的降解率达到70 %以上,MFC在闭路状态下对苯胺的降解速率比开路厌氧状态下高约14 %。当以500 mg·L−1的苯胺为单一燃料时,MFC的最大输出电压为280 mV,最大输出功率密度为87 mW·m−2。MFC以苯胺和葡萄糖为混合燃料时,可在降解苯胺的同时稳定地向外输出电压。这些结果为难降解的苯胺类有机物的处理提供了一条新的思路。
2.5 以葡萄糖为底物对MFC的热力学研究
从热力学方面研究MFC的特性可以在试验研究的基础上探明影响MFC性能的因素,以及通过热力学理论对相应的试验结果进行解释,最终有利于MFC运行过程中工艺参数的优化。
窦涛等[42]主要从热力学方面研究了MFC的特性。研究结果显示,MFC中葡萄糖的氧化是一个放热的熵增反应,能够自发进行。在标准状态条件下,最大发电量为2 840 kJ·mol−1,可逆电压为1.227 V,其中阴极反应的可逆电压为1.229 V,阳极反应的可逆电压为−0.002 V。在压强不变的条件下,可逆电压与温度成线性变化关系,但变化幅度不大;浓度对可逆电压的影响由能斯特方程来描述。
2.6 以葡萄糖为底物对MFC反应动力学的研究
在MFC中,来自动力学方面的制约因素会造成底物在阳极上或者阴极上的反应速率较低,从而使MFC难以获得较高的输出功率,因此,对MFC反应动力学的研究也是研究者关注的热点之一。
在一个无介体无膜的MFC中,以生活污水为初始接种体,以葡萄糖水溶液为原料,对在MFC中微生物的生化反应动力学特征研究结果显示[43]:在低浓度范围内(< 500 mg·L−1),电池的电压输出与溶液浓度之间符合Monod方程。
陈夫进等[44]从反应动力学方面分析认为,在MFC中,葡萄糖在阳极的电化学反应是异相的,只能发生在阳极电极和阳极溶液的交界处。MFC的电压损失包括活化损失、欧姆损失和浓度损失。活化损失可通过降低溶液温度和提高交换电流密度的方法来减小。欧姆损失可通过采用高电导率的阳极溶液和阴极溶液、减小电极之间的距离和增大反应器截面面积的方法减小。浓度损失可通过采用降低溶液温度和增大极限电流密度的方法减小。
2.7 以葡萄糖为底物对MFC作用机理的研究
对MFC降解废水中有机物作用机理的研究属于MFC净化废水的基础理论研究范畴,其研究结果可以从较深的层次上解释MFC处理废水过程中的试验现象,最终可用于调节与优化MFC运行过程的工艺参数。
崔康平等[45]采用不锈钢金属丝阳极构建了管状单室无质子交换膜空气阴极MFC,并以葡萄糖为唯一电子供体,研究了该MFC的性能。分别用含葡萄糖、葡萄糖加硝酸钾、葡萄糖加硫酸钠、葡萄糖加氯化铁的培养液注入MFC。试验结果表明:MFC室内电子受体的氧化还原势越高,对固体电极接受和传输电子的影响越大,固体电极接受电子的能力介于之间,接近Fe3+。
陈姗姗等[46]研究了MFC阳极微生物的种类和作用机制对MFC的产电性能的影响。从稳定运行了210 d,以200 mg·L−1喹啉为燃料的MFC阳极室分离得到一株革兰氏阴性菌,命名为Q1,其16SrRNA基因序列与Pseudomonas citronellolis DSM 50332T的同源性为96.9 % ,属于假单胞菌属(Pseudomonas sp.)。循环伏安法及构建纯菌MFC方法的测定结果均表明,Q1具有电化学活性。菌株Q1能利用单一喹啉或喹啉和葡萄糖混合燃料产电。葡萄糖对菌株Q1降解喹啉有促进作用。以喹啉和葡萄糖为混合燃料时24 h对喹啉的去除率达99.53 % ,优于以单一喹啉为燃料的情况。循环伏安法检测结果表明,附着在电极上的菌株Q1对产电起主要作用,Q1的溶解态代谢产物对产电过程起电子介体的作用。
有人通过测试阳极液和阴极液的pH值和电导率的变化情况,对MFC的产电过程和能量利用情况进行了研究,研究结果表明[47]:随着MFC的运行,阳极液的pH值和电导率呈现下降的趋势,阴极液的pH值和电导率呈现上升的趋势,阴极液的pH值比阳极液的pH值大约高出了0.30 ~ 0.50,阳极液和阴极液的平均电导率变化不大。MFC稳定运行时,欧姆内阻为29.69 Ω,极限电流为2.69 mA,最大输出功率约为0.8 mW,对应的内阻约为95.72 Ω。铁氰化钾的质量传输是极限电流的限制性因素。通过能量分析发现,MFC阳极液中91.1 % 的葡萄糖被其他微生物消耗,仅有8.9 % 的葡萄糖用来发电;而用来发电的葡萄糖的88.5 % 的能量转化为了其他形式的能量,仅有11.5 % 的能量转化成电能。
3 结束语
最早研究报道的可被MFC利用获得电能的有机物主要为易降解物质。这些物质既包括纯物质如葡萄糖等[14]和乙酸[48]等,又包括各种有机混合物如食品废水[49]、畜禽养殖废水[50]、城市生活污水[51-52]等。随着研究工作的逐渐深入,许多传统的难降解物质如石油类污染物[53]、垃圾渗滤液[54]也可以作为MFC的燃料。此外,有研究表明,MFC还可以用来处理重金属废水[55-56]、脱盐[57]、脱氮[58-59]和脱硫[60-62]。MFC能够利用上述这些物质并产电,为MFC在污水处理中提供了实际应用的可能。
[1] LOGAN B E, REGAN J M. Microbial challenges and fuel cell applications[J]. Environmental Science & Technology, 2006, 40: 172-180.
[2] ALLEN R M, BENNETTO H P. Microbial fuel-cells electricity production from carbohydrates[J]. Applied Biochemstry and Biotechnology, 1993, 39/40: 27-40.
[3] RABAEY K, VERSTRAETE W. Microbial fuel cells: novel biotechnology for energy generation[J]. Trends in Biotechnology, 2005, 23(6): 1292-1298.
[4] FORNERO J J, ROSENBAUM M, ANGENENT L T. Electric power generation from municipal, food, and animal wastewaters using microbial fuel cells[J]. Electroanalysis, 2010, 22(7): 832-843.
[5] HABERMANN W, POMMER E H. Biological fuel cells with sulphide storage capacity[J]. Applied Microbiology and Biotechnology, 1991, 35: 128-133.
[6] STUARY W. Gastrobots-benefits and challenges of microbial fuel cells in food powered robot applications[J]. Autonomous Robots, 2000, 9: 9-111.
[7] ANGENENT L T, KARIM K A, DAHHAN M H, et al. Production of bioenergy and biochemicals from industrial and agricultural wastewater[J]. Trends in Biotechnology, 2004, 22(9): 477-485.
[8] LOVLEY D R. Microbial fuel cells: Novel microbial physiologies and engineering approaches[J]. Current Opinion in Biotechnology, 2006, 17: 327-332.
[9] BENNETTO H P, BOX J, DELANEY G M, et al. Redox mediated electrochemistry of whole microorganisms: from fuel cell to biosensors[M]// In: URNER A F T, KARUBE I, WILSON G S. Biosensors: Fundamentals and Applications[M]. Oxford: Oxford University Press, 1987: 291-314.
[10] KORNEEL R, WILLY V. Microbial fuel cells: novel biotechnology for energy generation[J]. Trends in Biotechnology, 2005, 23: 291-298.
[11] OH S E, MIN B, LOGAN B E. Cathode performance as a factor in electricity generation in microbial fuel cells[J]. Environ. Sci. Technol., 2004, 38: 4900-4904.
[12] 卢娜, 周顺桂, 倪晋仁. 微生物燃料电池的产电机制[J]. 化学进展, 2008, 20(7/8): 1233-1240.
[13] BENNETTO H P. Electricity generation by microorganisms[J]. Biotechnology Education, 1990, 1(4): 163-168.
[14] CHAUDHURI S K, LOVLEY D R. Electricity generation by direct oxidation of glucose in mediatorless microbial fuel cells[J]. Nature Biotechnology, 2003, 21 (10): 1229-1232.
[15] 刘志丹, 连静, 杜竹玮, 等. 利用异化金属还原菌构建含糖微生物燃料电池[J]. 生物工程学报, 2006, 22(1): 131-137.
[16] JUNG S, REGAN J M. Comparison of anode bacterial communities and performance in microbial fuel cells with different electron donors[J]. Applied Microbiology and Biotechnology, 2007, 77(2): 393-402.
[17] 詹亚力, 戚琳琳, 王琴, 等. 微生物燃料电池中的微生物分析[J]. 高校化学工程学报, 2009, 23(3): 445-449.
[18] 陈姗姗, 张翠萍, 刘广立, 等. 纯菌株与混合菌株在MFC中降解喹啉及产电性能的研究[J]. 环境科学, 2010, 31(9): 2148-2154.
[19] 尤世界, 赵庆良, 姜秋. 废水同步生物处理与生物燃料电池发电研究[J]. 环境科学, 2006, 27(9): 1786-1790.
[20] CHENG S, LIU H, LOGAN B E. Increased power generation in a continuous flow MFC with advective flow through the porous anode and reduced electrode spacing[J]. Environ. Sci. Technol., 2006, 40(7): 2426-2432.
[21] HU Z. Electricity generation by a baffle chamber membrane less microbial fuel cell[J]. Journal of Power Sources, 2008, 179(1): 27-33.
[22] CHUNG K, OKABE S. Continuous power generation and microbial community structure of the anode biofilms in a three-stage microbial fuel cell system[J]. Applied Microbiology Biotechnology, 2009, 83(5): 965-977.
[23] 冯雅丽, 李浩然, 祝学远. 单室直接微生物燃料电池性能影响因素分析[J]. 北京科技大学学报, 2007, 29(suppl. 2): 162-165.
[24] 陶虎春, 倪晋仁, 易丹, 等. 微生物燃料电池与传统厌氧消化处理人工废水的比较[J]. 应用基础与工程科学学报, 2008, 16(1): 23-27.
[25] 李毅, 胡翔, 王程远, 等. 微生物燃料电池在废水处理中的应用[J]. 工业水处理, 2008(9): 59-62.
[26] 孔载英, 孙永明, 李东, 等. 微生物燃料电池运行影响因素的研究[J]. 太阳能学报, 2010, 31(4): 469-472.
[27] 赵立新, 邹立军, 王宣, 等. 以葡萄糖为燃料的上流式单室微生物燃料电池[J]. 大庆石油学院学报, 2010, 34(1): 76-79.
[28] CHAE K J., CHOI M J, LEE J W, et al., Effect of different substrates on the performance, bacterial diversity, and bacterial viability in microbial fuel cells[J]. Bioresource Technology, 2009, 100(14): 3518-3525.
[29] 骆海萍, 刘广立, 张仁铎. 以苯酚为燃料的微生物燃料电池产电特性[J]. 环境科学学报, 2008, l28(7): 1279-1283.
[30] 宋天顺, 叶晔捷, 徐源, 等. 直接微生物燃料电池的影响因素[J]. 化学工程, 2009, 37(12): 51-54.
[31] 孔晓英, 孙永明, 李连华, 等. 不同底物对微生物燃料电池产电性能的影响[J]. 农业工程学报, 2011, 27(suppl. 1): 185-188.
[32] 强琳, 袁林江, 丁擎. 空气阴极微生物燃料电池处理生活污水产电特性研究[J]. 水处理技术, 2011, 37 (1): 76-79.
[33] 双陈冬, 张恩仁, 刁国旺, 等. 复合菌体及单一菌体催化的微生物燃料电池产电机理初步研究[J]. 电化学,2008, l14(3): 313-317.
[34] 张翠萍, 王志强, 刘广立, 等. 降解喹啉的微生物燃料电池的产电特性研究[J]. 环境科学学报, 2009, 29(4): 740-746.
[35] 毕哲, 胡勇有, 孙健. 生物阴极型微生物燃料电池同步降解偶氮染料与产电性能研究[J]. 环境科学学报, 2009, 29(8): 1635-1642.
[36] 温青, 孙茜, 赵立新, 等. 微生物燃料电池对废水中对硝基苯酚的去除[J]. 现代化工, 2009, 29(4): 40-42.
[37] 赵娟, 吴瑾妤, 李秀芬, 等. 基于底物类型的微生物燃料电池的产电特性[J]. 食品与生物技术学报, 2010, 29(4): 629-633.
[38] 骆海萍, 张翠萍, 宋海红, 等. 降解苯的微生物燃料电池产电性能研究[J]. 中山大学学报: 自然科学版, 2010, 49(1): 113-117.
[39] 李婕, 刘广立, 张仁铎, 等. 葡萄糖和硝基苯为混合燃料时 MFC 的产电特性研究[J]. 环境科学, 2010, 31(11): 2811-2817.
[40] 罗勇, 张仁铎, 李婕, 等. 以吲哚为燃料的微生物燃料电池降解和产电特性[J]. 中国环境科学, 2010, 30(6): 770-774.
[41] 武晨, 张嘉琪, 王晓丽, 等. 以苯胺和葡萄糖为燃料的微生物燃料电池的产电特性研究[J]. 环境科学学报, 2011, 31(6): 1227-1232.
[42] 窦涛, 陈夫进. 微生物燃料电池的热力学研究[J]. 河南科学, 2010, 28(6): 649-653.
[43] 詹亚力, 张佩佩, 闫光绪, 等. 无中间体无膜微生物燃料电池的构建与运行[J]. 高校化学工程学报, 2008, 22(1): 177-181.
[44] 陈夫进, 刘艳涛, 刘昌云. 微生物燃料电池的反应动力学探究[J]. 能源研究与管理, 2010(4): 40-43.
[45] 崔康平, 金松. 微生物燃料电池阳极室内电子受体竞争研究[J]. 环境科学研究, 2010, 23(1): 90-93.
[46] 赵立新, 邹立军, 王宣, 等. 以葡萄糖为燃料的上流式单室微生物燃料电池[J]. 大庆石油学院学报, 2010, 34(1):76-79.
[47] 张培远, 刘中良. 矩形微生物燃料电池性能的分析[J]. 微生物学通报, 2011, 38(6): 832-838.
[48] LIU H, CHENG S, LOGAN B E. Production of electricity from acetate or butyrate using a single-chamber microbial fuel cell[J]. Environmental Science & Technology, 2005, 39(2): 658-662.
[49] OH S E, LOGAN B E. Hydrogen and electricity production from a food processing wastewater using fermentation and microbial fuel cell technologies[J]. Water Research, 2005, 39(19): 4673-4682.
[50] MIN B, KIM J, OH S, et al. Electricity generation from swine wastewater using microbial fuel cells[J]. Water Research, 2005, 39(20): 4961-4968.
[51] ZUO Y, CHENG S, CALL D, et al. Tubular membrane cathodes for scalable power generation in microbial fuel cells[J]. Environmental Science & Technology, 2007, 41(9): 3347-3353.
[52] WANG X, FENG Y J, WANG H M, et al. Bioaugmentation for electricity generation from corn stover biomass using microbial fuel cells[J]. Environmental Science & Technology, 2009, 43(15): 6088-6093.
[53] MORRIS J M, JIN S, WANG J Q, et al. Lead dioxide as an alternative catalyst to platinum in microbial fuel cells[J]. Electrochemistry Communications, 2007, 9(7): 1730-1734.
[54] GREENMAN J, GÁLVEZ A, GIUSTI L, et al. Electricity from landfill leachate using microbial fuel cells: Comparison with a biological aerated filter[J]. Enzyme and Microbial Technology, 2009, 44(2): 112-119.
[55] HUANG L P, CHEN J W, QUAN X, et al. Enhancement of hexavalent chromium reduction and electricity production from a biocathode microbial fuel cell[J]. Bioprocess and Biosystems Engineering, 2010, 33(8): 937-945.
[56] HEIJNE A T, LIU F, WEIJDEN R V, et al. Copper recovery combined with electricity production in a microbial fuel cell[J]. Environmental Science & Technology, 2010, 44(11): 4376-4381.
[57] CAO X X, HUANG X, LIANG P, et al. A new method for water desalination using microbial desalination cells[J]. Environmental Science & Technology, 2009, 43(18): 7148-7152.
[58] GREGORY K B, BOND D R, LOVLEY D R. Graphite electrodes as electron donors for anaerobic respiration[J]. Environmental Microbiology, 2004, 6(6): 596-604.
[59] CLAUWAERT P, RABAEY K, AELTERMAN P, et al. Biological denitrification in microbial fuel cells[J]. Environmental Science & Technology, 2007, 41(9): 3354-3360.
[60] RABAEY K, VAN DE SOMPEL K, MAIQNIEN L, et al. Microbial fuel cells for sulfide removal[J]. Environmental Science & Technology, 2006, 40(17): 5218-5224.
[61] ZHANG B G, ZHOU S G, ZHAO H Z, et al. Factors affecting the performance of microbial fuel cells for sulfide and vandadium (V) treatment[J]. Bioprocess and Biosystems Engineering, 2010, 33(2): 187-194.
[62] ZHAO F, RAHUNEN N, VARCOE J R, et al. Factors affecting the performance of microbial fuel cells for sulfur pollutants removal[J]. Biosensors and Bioelectronics, 2009, 24(7): 1931-1936.
Progress of Application Research for Glucose in Microbial Fuel Cells
XU Jin-qiu, LIANG Bo, WANG Li-jun, BAI Jian-feng, HUANG Si-chao, TANG Zhi-tao
( School of Urban Development and Environmental Engineering, Shanghai Second Polytechnic University, Shanghai 201209, P. R. China )
The characteristics, development history and working principle of microbial fuel cells is briefly introduced. The progress of application research of glucose as the most common organic substrate in wastewater on production of electricity in microbial fuel cells in recent years is mainly summarized. Finally, it looks forward to the application prospect of microbial fuel cells.
microbial fuel cells; wastewater; production of electricity; glucose
X172
A
1001-4543(2012)04-0257-09
2012-09-07;
2012-10-16
徐金球(1965-),女,湖北省通城县人,教授,博士,主要研究方向为水处理技术以及电子废弃物资源化技术,电子邮箱jqxu@eed.sspu.cn。
上海市教育委员会重点学科建设项目(No. J51803);上海市教育委员会重点项目(No. 12ZZ194)
