新型PMNAP缩胺类席夫碱及其铜配合物的合成与表征
2012-07-28俞志东
俞志东,于 湘
(广东石油化工学院化工与环境工程学院,广东 茂名 525000)
酰基吡唑啉酮及其席夫碱是一类杂环β-二酮螯合剂。其活性的双酮配位基可以同各种金属或稀土离子形成大量的配合物,是金属和稀土离子良好的萃取剂和螯合剂[1~5],也是一类优良的荧光材料中间体,同时表现出一定的抗菌、抗病毒性能[6~11],在药理、生物活性试剂、冶金、染料、发光材料等领域得到了广泛的应用。由于芳环酰基吡唑啉酮席夫碱具有较强的抗菌、抗病毒、多点配位且易于传递电子的特性[10,12],使得该类化合物及其配合物在医药工业、催化化学、原子能、材料化学以及有机合成等领域有着广泛的应用前景。为进一步拓展其研究与应用范围,作者合成了3种基于1-苯基-3-甲基-4-萘乙酰基-5-吡唑啉酮(PMNAP)缩胺类新型席夫碱配体:PMNAP缩对溴苯胺(HL1)、PMNAP缩对甲氧苯胺(HL2)和PMNAP缩糠胺(HL3)及其相应铜配合物并进行了结构表征,为进一步研究该类化合物及其配合物的应用提供基础数据。
1 实验
1.1 试剂与仪器
PMNAP按文献[13]合成;对溴苯胺、对甲氧苯胺、糠胺、醋酸铜,北京化学试剂公司;所用试剂均为分析纯。
Flash EA 1112 型元素分析仪,意大利Carlo Erba公司;Agilent 1100型液-质联用仪,美国Agilent公司;AV 300型核磁共振仪,瑞士Bruker公司;TGA/SDTAe851型差热-热重分析仪,瑞士Mettler-Toledo公司;Avatar 370 FTIR型红外光谱仪(KBr压片),美国Thermo Nicolet公司;U-3010型紫外可见分光光度计,日本Hitachi公司;DDS-307型电导率仪,上海启威电子有限公司。
1.2 PMNAP缩胺类席夫碱的合成
在装有3.42 g(0.01 mol)PMNAP 的带冷凝管的150 mL三角瓶中加入4 mL无水乙醇,加热回流使其溶解。滴加含有等物质的量的对溴苯胺1.72 g(对甲氧苯胺1.23 g、糠胺0.97 g)的乙醇溶液,回流6 h,析出沉淀。经过滤、无水乙醇洗涤、丙酮重结晶2次、干燥,得有色沉淀PMNAP缩胺类席夫碱HL1(HL2、HL3)。
1.3 PMNAP缩胺类席夫碱铜配合物的合成

合成路线如下:
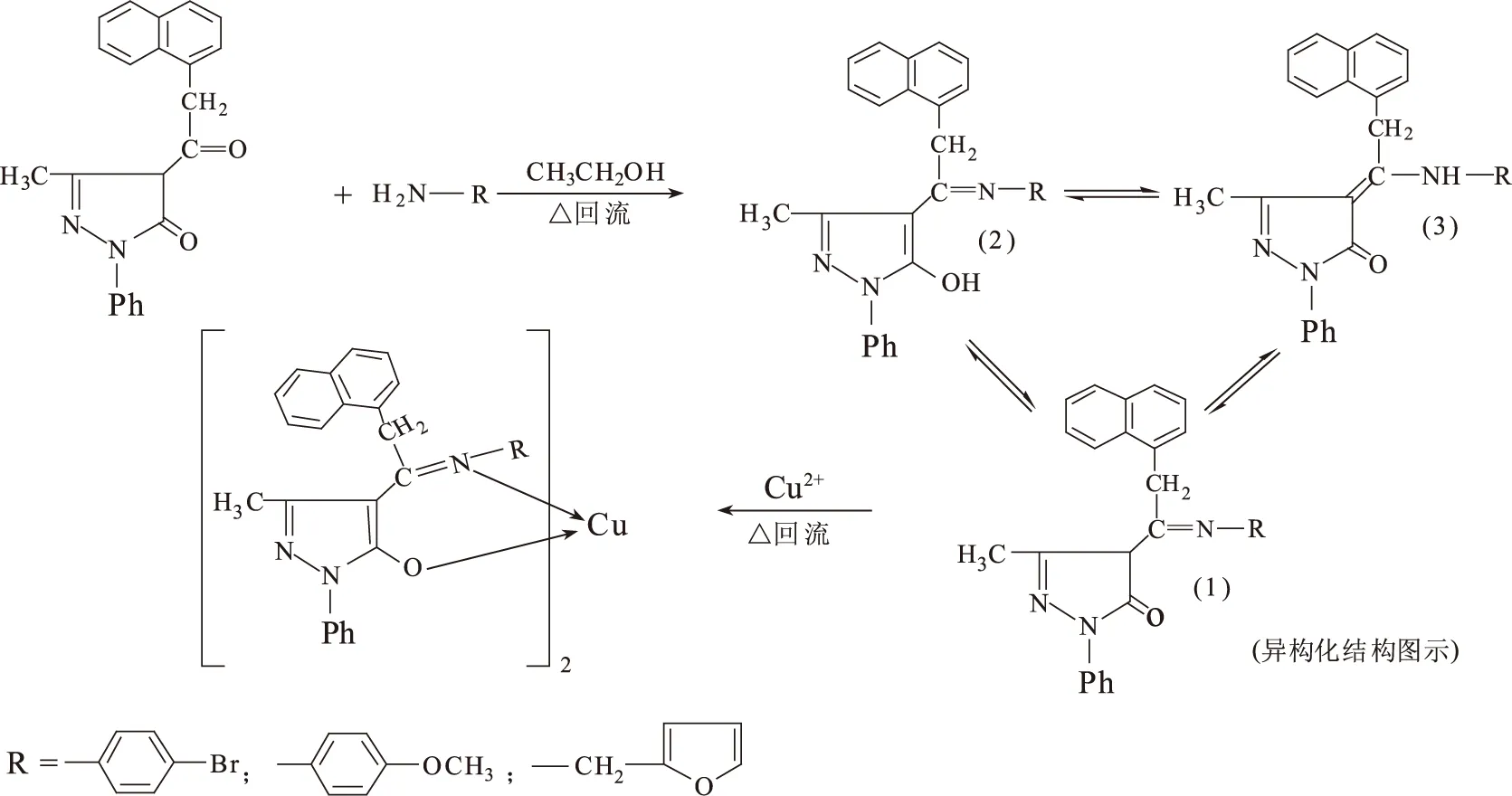
1.4 测试与表征
C、H、N用元素分析仪测定,Cu用EDTA络合滴定法测定。
质谱在液-质联用仪上测定,测试条件为:溶剂:10%DMF-90%甲醇;电离源:ESI;进样方式:注射泵连续进样;进样流速:0.4 mL·h-1;扫描模式:正(负)离子模式;雾化气压力:0.14 MPa;干燥气流速:10 L·min-1;干燥气温度:340 ℃。
紫外光谱在紫外可见分光光度计上测定。以甲醇为溶剂,配制1×10-5mol·L-1的溶液,在190~500 nm范围内测定。
红外光谱在红外光谱仪(KBr压片)上测定,测定范围400~4000 cm-1。
热重分析在差热-热重分析仪上测定。测试条件:参比物:Al2O3;气氛:静态空气;升温速率:20 ℃·min-1。
3种配体的1HNMR在核磁共振仪上测定。以CDCl3作溶剂,TMS作内标。
2 结果与讨论
2.1 元素分析结果及摩尔电导值(表1)
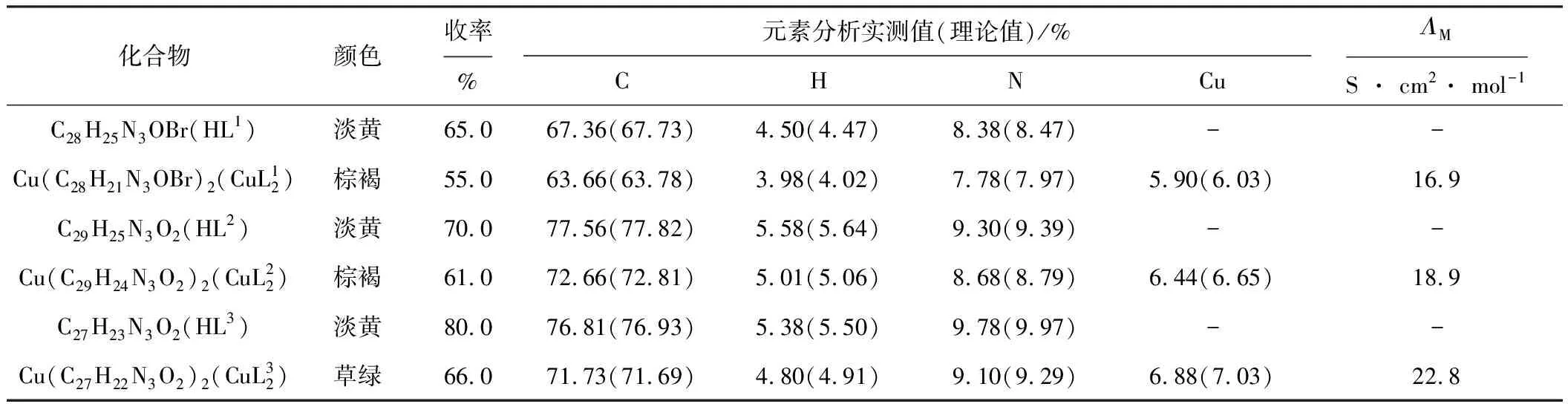
表1 配体及其铜配合物的元素分析数据及摩尔电导值
由表1可见,配体及其铜配合物的元素分析的实测值与理论值基本相符。摩尔电导值显示配合物属非电解质[14]。
2.2 质谱分析
配体及其铜配合物的一级质谱见图1。

图1 3种配体及其铜配合物的一级质谱
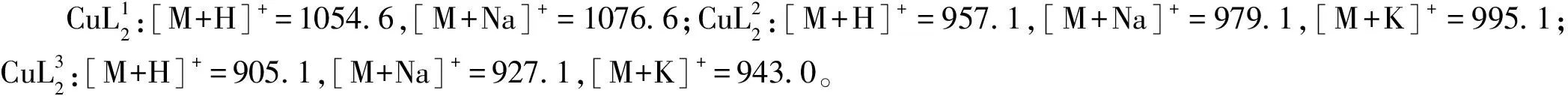
2.3 紫外光谱分析
配体及其铜配合物紫外光谱数据见表2。
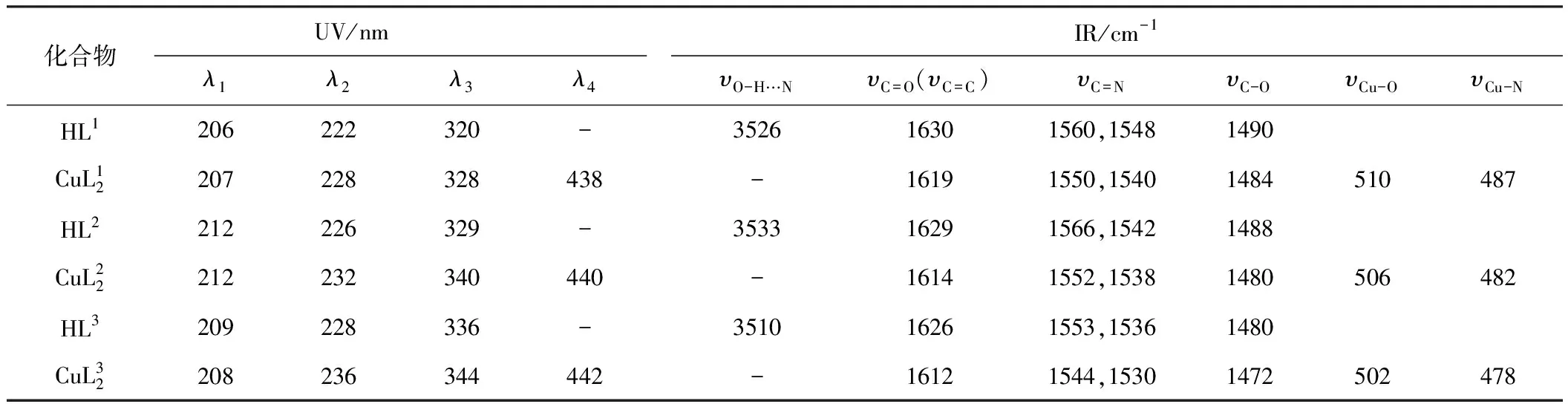
表2 配体及其铜配合物的紫外光谱和红外光谱数据
由表2可知,3种配体在紫外区均出现了3组吸收峰,分别位于206~212 nm、222~228 nm和320~336 nm,指认为芳环、亚胺基的π-π*跃迁和亚胺基的n-π*跃迁产生的吸收峰。与配体相比,形成配合物后,第一峰位基本不变,而第二、三峰位发生了程度各异的红移,可能是由于亚胺基上的N与铜中心离子发生配位作用,引起C=N键的极化并影响了相关共轭分子轨道的能级,配合物在440 nm左右出现了强度较弱的吸收峰,归属为铜离子的d-d跃迁吸收峰[10]。
2.4 红外光谱分析
配体及其铜配合物红外光谱数据见表2。
由表2可知,3种配体在3510~3533 cm-1处观察到了由烯醇式羟基与亚胺基上的N形成的υO-H…N宽缔合羟基峰,说明配体可能均以烯醇式和酮式结构共存,这与核磁共振氢谱测定结果吻合。与配体相比,形成配合物后,υC=O吸收峰由1626~1630 cm-1位移至1612~1619 cm-1,推测其可能发生了酮式结构向烯醇式结构的转化,且在502~510 cm-1出现υCu-O振动峰,说明烯醇羟基上的O原子参与配位;υC=N吸收峰分别由1553~1566 cm-1和1536~1548 cm-1位移至1544~1550 cm-1和1530~1540 cm-1,且在478~487 cm-1出现υCu-N振动峰,说明亚胺基上的N原子参与了配位。以上分析结合质谱数据表明,配位时配体可能发生了质子转移,由酮式结构向烯醇式结构转化,按去质子的方式通过烯醇负离子的O和亚胺基上的N与铜中心离子成键。
2.5 热重分析(表3)
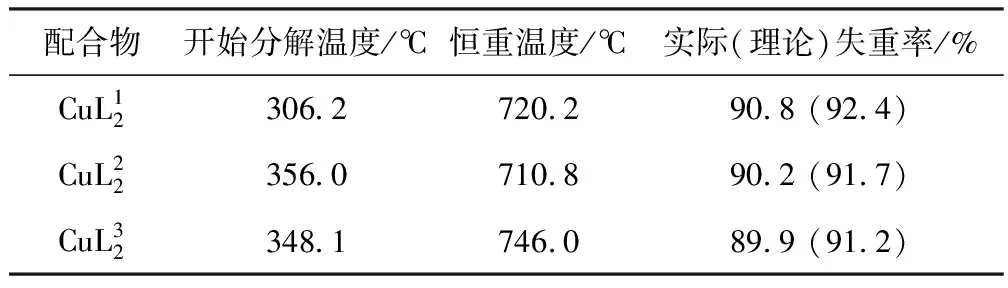
表3 3种配合物的热重数据
由表3可知,3种配合物在300 ℃以前均未观察到有失重发生,说明配合物中没有H2O参与配位,该推断与元素分析和红外光谱分析相吻合。升温至306.2~356.0 ℃时对应TG曲线开始明显下滑,这是配合物被氧化分解所致,体系加热至710.8~746.0 ℃达到恒重,最终分解产物为CuO,其实际失重率与理论值接近。
2.6 核磁共振氢谱分析
3种配体的各质子的化学位移δ及其归属如下:HL1:1.993(s,3H,-CH3),4.520(s,2H,-CH2-),7.122~8.078(m,16H,Ar-H),6.475(s)、13.587(bs)(1H,-CO-CH-CN-,-C=COH-);HL2:1.993(s,3H,-CH3),3.707(s,3H,-OCH3-),4.463(s,2H,-CH2-),6.696~8.082(m,16H,Ar-H),6.446(s)、13.403(bs)(1H,-CO-CH-CN-,-C=COH-);HL3:1.990(s,3H,-CH3),4.068(s,2H,-CH2-),4.417(s,2H,-CH2-CO-),6.924~8.115(m,15H,Ar-H),6.323(s)、11.990(bs)(1H,-CO-CH-CN-,-C=COH-)。配体在δ11.990~13.587处出现了一弱而宽的单峰,归属为-C=COH-质子峰[15],积分面积为0.773~0.808,同时在δ6.323~6.475处出现了积分面积为0.193~0.255更弱的小峰,两峰积分面积之和恰好相当于一个质子,说明δ6.323~6.475处出现的质子为-CO-CH-CN-。3种配体均未观察到-NH-质子峰。以上分析表明配体在测试条件下可能主要以酮式(1)和烯醇式(2)结构并存。该结论与红外光谱分析结果相一致。
综合上述分析,配合物的结构可初步推断为1.3中合成路线图所示结构。
3 结论
在非水溶剂中合成了3种基于1-苯基-3-甲基-4-萘乙酰基-5-吡唑啉酮(PMNAP)缩胺类新型席夫碱及其铜配合物。由元素分析、络合滴定法、质谱和摩尔电导值推测出配合物的组成为CuL2[L=L1,L2,L3],通过红外光谱、紫外光谱、热重分析和核磁共振氢谱对配体及其铜配合物进行了结构表征。结果表明:在测试条件下,3种新配体均以酮式和烯醇式结构共存,配位时酮式可能转化为烯醇式结构按去质子的方式以烯醇负离子的O和亚胺基上的N与铜中心离子配位,配合物的配位数均为4。
参考文献:
[1] Takeshi U,Sayuri A,Kunikazu I,et al.Effect of a modification site on the electron-transfer reaction of glucose oxidase hybrids modified with phenothiazine via a poly(ethylene oxide) spacer[J].Langmuir,2004,20(21):9177-9183.
[2] Shin-Ichiro I,Kazumichi B,Takeshi U,et al.Comparison of catalytic electrochemistry of glucose oxidase between covalently modified and freely diffusing phenothiazine-labeled poly(ethylene oxide) mediator systems[J].Journal of Physical Chemistry B,2003,107(34):8834-8839.
[3] 汪徐春,赵谦益,吴杰颖,等.N-异辛基吩噻嗪-3-乙烯基吡啶配体及其卤化亚铜配合物的合成与性质研究[J].功能材料,2008,39(7):1230-1233.
[4] Mukai H,Miyazaki S,Umetani S,et al.Synergic liquid/liquid extraction of lithium and sodium with 4-acyl-5-pyrazolones with bulky substituents and tri-n-octylphosphine oxide[J].Analytica Chimica Acta,1989,220:111-117.
[5] Sale M I,Ahmad M,Darus H.Solvent extraction of lanthanum(Ⅲ),europium(Ⅲ) and lutetium(Ⅲ) with fluorinated 1-phenyl-3-methyl-4-benzoyl-5-pyrazolones into chloroform[J].Talanta,1990,37(7):757-759.
[6] Zhou Dejian,Li Qin,Huang Chunhui,et al.Room-temperature fluoresecnce,phosphorescence and crystal structure of 4-acyl pyrazolone lanthanide complexes:Ln(L)3·2H2O[J].Polyhedron,1997,16(8):1381-1389.
[7] Li Jun,Zhang Li,Liu Lang,et al.A series of pyrazolone lanthanide(Ⅲ) complexes:Synthesis,crystal structures and fluorescence[J].Inorganica Chimica Acta,2007,360(6):1995-2001.
[8] Miguel F B,Ana G,Angel G O,et al.Synthesis and biological activity ofN,N-dialkyamino-alkyl-substituted bisindolyl and diphenyl pyrazolone derivatives[J].Bioorganic and Medicinal Chemistry,2006,14(1):9-16.
[9] 何其庄,马树芝,许东芳.稀土酰基吡唑啉酮邻菲咯啉配合物的合成、表征及其生物活性[J].无机化学学报,2007,23(10):1723-1728.
[10] 李锦州,张光林,沙靖全,等.呋喃甲酰基吡唑啉酮缩氨基硫脲配合物的合成、光谱表征及生物活性[J].光谱学与光谱分析,2005,25(2):216-218.
[11] 罗宗铭,余倩,杨迟,等.1-苯基-甲基-4-咔唑-N-丁基-4-苯甲酰基-吡唑啉-5-酮的合成及其光谱研究[J].化学试剂,2003,25(4):193-195.
[12] 张桂玲,戴柏青,李锦州.酰基吡唑啉酮双席夫碱配合物的电子结构、成键性与生物活性[J].无机化学学报,2003,19(12):1331-1334.
[13] 刘洲亚,俞志刚,竹学友,等.萘乙酰基吡唑啉酮及其席夫碱的合成与表征[J].化学试剂,2008,30(6):412-414.
[14] Geary W J.Use of conductivity measurements in organic solvents for the characterization of coordination compounds[J].Coordination Chemistry Reviews,1971,7(1):81-84.
[15] Emmanuel C O.A1H and13CNMR spectral study of some 4-acyl-3-methyl-1-phenylpyrazol-5-ones in chloroform[J].Spectrochimica Acta,Part A,1984,40(5):397-401.
