银苦黄白口服液的不同配伍对苦参碱和氧化苦参碱影响
2012-07-26李立顺钱晶晶时维静
李立顺, 钱晶晶, 时维静
(安徽科技学院,安徽凤阳233100)
银苦黄白口服液为临床经验方研制,由金银花、苦参、黄芪、白茅根按6∶7∶7∶10组成。具有清热祛湿,利水的功效,临床用于肾炎、肾盂肾炎、尿毒症等疗效显著。方中苦参系豆科植物苦参Sophora flavescens Air.的干燥根[1],具有清热燥湿,利水的功效,其主要活性成分是苦参碱、氧化苦参碱[2]。银苦黄白口服液采用的是水提醇沉制备工艺,为考察共煎对方中化学成分的影响,本试验采用L8(27)正交设计,考察不同配伍对苦参碱、氧化苦参碱含有量的影响,以探讨该方的配伍化学变化规律,为制备工艺的改进提供研究数据。
1 仪器与试药
1.1 仪器 CAMAG LINOMAT5半自动点样仪;CAMAG TLC Scanner 3薄层色谱扫描仪;winCATS软件,瑞士卡玛;CP225D准微量天平,德国赛多利斯;RE52-98旋转蒸发仪,上海亚荣生化仪器厂;LG10-24A离心机,北京医用离心机厂。
1.2 试药 黄芪 Astragalus membranaceua(Fisch.)Bge.var.mongholicus(Bge.)Hsiao.产地内蒙古;白茅根 Imperata cylindrical Beauv.Var.major C.E.Hubb.产地安徽;金银花Lonicera japonica Thunb.产地河南;苦参Sophora flavescens Ait.产地安徽。均购自安徽京皖中药饮片厂,药品生产许可证号:皖Y20020003批号20100319。经时维静教授鉴定为正品。
苦参碱 (110805-200306)、氧化苦参碱 (0780-200004),购自中国药品生物制品检定所;硅胶薄层板G,20 cm×10 cm,购自青岛海洋化工厂,批号20070724;试剂均为分析纯。
2 方法与结果
2.1 L8(27)配伍的正交设计 选黄芪、金银花、白茅根作为3个因素,选用药和不用药为2个水平,同时考虑两两交互作用,因素水平见表1。

表1 因素水平
2.2 供试溶液制备 按正交试验设计配比称取各味药材,加8倍量水浸30 min,煎提2次,每次1 h,合并滤液,静置12 h,取上清液。浓缩至每1 mL相当于1.5 g药材,加乙醇使含醇量达75%,静置,上清液回收乙醇,精滤,调整溶液量,使苦参含量均达35%,如法制备缺苦参样品 (见表2)。精密吸取各样品1 mL,过短中性氧化铝柱(100~200目2 g,内径1 cm),以50%甲醇洗脱约10 mL,洗脱液水浴蒸干后用甲醇溶解并定容至2 mL,冷藏备用。
2.3 对照品溶液的制备 精密称取苦参碱、氧化苦参碱适量,分别置10 mL量瓶中,甲醇溶解至刻度,制成质量浓度为0.2 mg/mL的溶液。
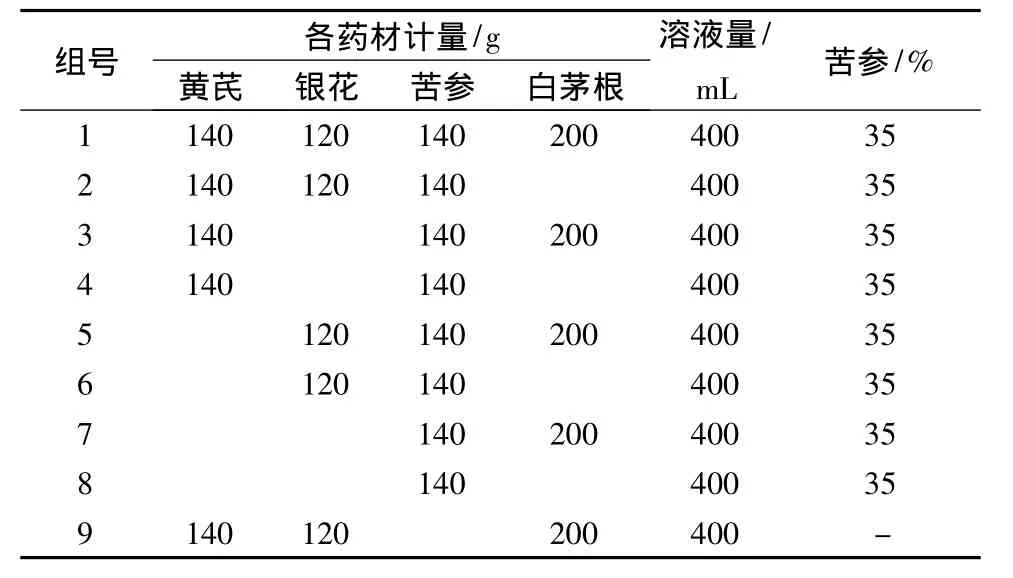
表2 苦参不同配伍的用药比例
2.4 薄层色谱条件 硅胶G板,板厚约0.3 mm;反复试验后,选定三氯甲烷-甲醇-浓氨试液 (10∶1.2∶0.2)为展开剂,置双槽展开缸,饱和20 min。取缺苦参、苦参药材、全方及苦参碱、氧化苦参碱溶液,半自动点样仪喷雾条带点样各2 μL,带宽6 mm,各2重复。置双槽展开缸的另侧预平衡15 min,上行展开8 cm,取出吹干,喷改良碘化铋钾试液 (碘化铋钾试液1 mL,加0.6 moL/L盐酸溶液2 mL,加水10 mL)显色剂,至显色清晰。室温15℃,相对湿度40%。此条件下,苦参碱、氧化苦参碱显橘黄色斑点,分离较好,可同板比较,缺苦参样品无干扰。见图1。
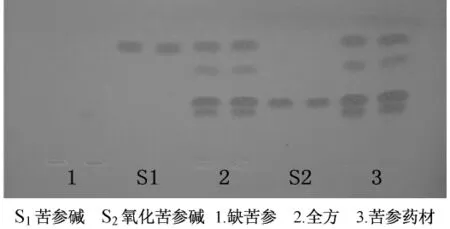
图1 苦参及全方薄层图谱
2.5 薄层扫描条件 使用薄层扫描仪,全光谱扫描,苦参碱、氧化苦参碱显色后,最佳检测波长λ=530 nm;采用吸收检测 (光源为钨灯),单波长反射直线扫描法,狭缝3.0 mm×0.45 mm,扫描速度20 mm/s。
2.6 线性关系考察 精密吸取苦参碱、氧化苦参碱对照品各1、2、3、4、5 μL,各重复2次,点于同一硅胶G薄层板上,按2.4项展开、显色,并按2.5项测定峰面积积分值,以对照品量为横坐标,相应的峰面积积分值为纵坐标,进行线性回归。二者的回归方程、相关系数及线性范围分别为:苦参碱的回归方程为 Y=56.801+1.409X,r=0.99867,苦参碱点样量在0.20~1.00 μg范围内呈良好的线性关系;氧化苦参碱的回归方程为Y=2374.410+13.580X,r=0.99996,氧化苦参碱点样量在0.20~1.00 μg范围内呈良好的线性关系。
2.7 稳定性考查 对一薄层板的同一斑点每间隔2h扫描测定1次,结果显示斑点在10 h内稳定,RSD为1.7%(n=5)。
2.8 精密度考查
2.8.1 同板精密度 精密吸取苦参碱、氧化苦参碱对照品溶液2 μL,于同一硅胶G薄层板上连续点5次,按2.4项展开、显色,并按2.5项测定峰面积积分值。结果苦参碱RSD为1.27%(n=5);氧化苦参碱RSD为0.51%(n=5)。
2.8.2 异板精密度 精密吸取苦参碱、氧化苦参碱对照品溶液2 μL,分别点于5块硅胶G薄层板上,按2.4项展开、显色,并按2.5项测定峰面积积分值。结果苦参碱RSD为2.19%(n=5);氧化苦参碱RSD为1.88%(n=5)。
结果表明该方法的同板精密度、异板精密度均较好。
2.9 加样回收率试验 精密称取已知含有量样品9份,分别精密加入适量苦参碱、氧化苦参碱对照品,按供试品溶液制备法制备,按上述薄层色谱条件及薄层扫描条件测定供试品溶液中苦参碱、氧化苦参碱的含有量。结果苦参碱平均加样回收率为98.67%,RSD为3.67%(n=9);氧化苦参碱的平均加样回收率为99.55%,RSD为1.94%(n=9)。2.10 配伍对苦参碱和氧化苦参碱含有量的影响 精密吸取表2中1-8号供试品溶液各2 μL,苦参碱1 μL、5 μL,氧化苦参碱1 μL、6 μL进样,各重复2次。按2.4项同板点样、展开、显色,并按2.5项测定峰面积积分值。采用线性回归二点法计算含有量。测定不同配伍样品苦参碱和氧化苦参碱的含有量见表3,方差分析见表4、表5。
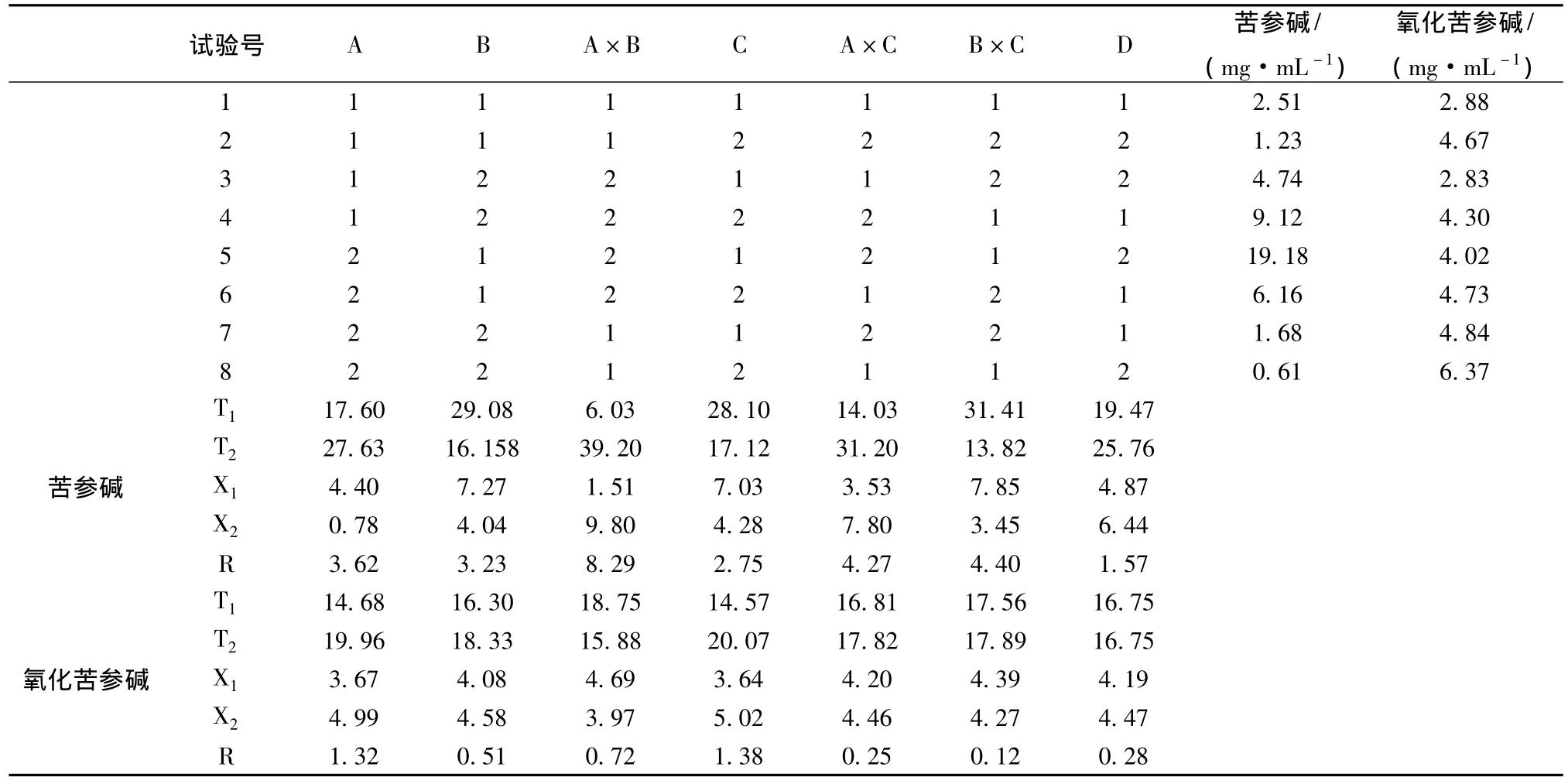
表3 L8(27)正交试验设计及结果
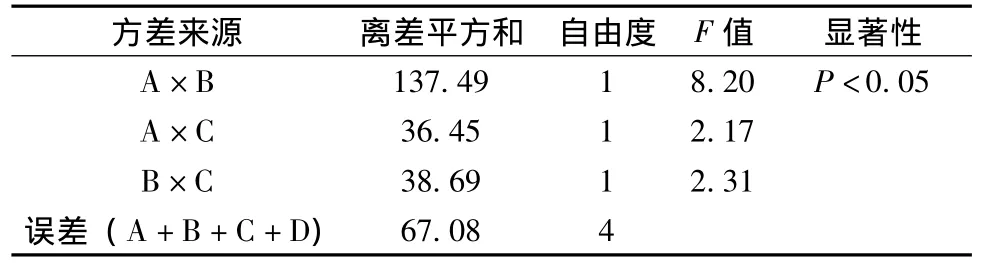
表4 苦参碱方差分析
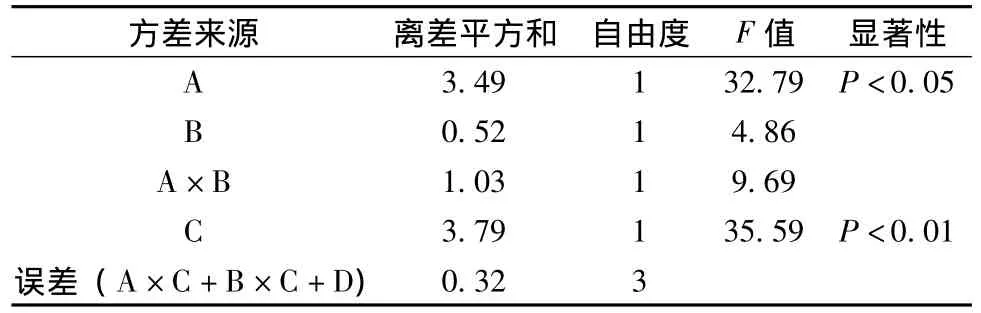
表5 氧化苦参碱方差分析
从表3、4、5可以看出,苦参单味药中苦参碱含有量最低,氧化苦参碱含有量最高。5号组 (金银花、白茅根、苦参)苦参碱含有量最高。方差分析表明,黄芪与金银花的交互作用对苦参碱含有量的影响具有显著性差异 (P<0.05),即黄芪与金银花共用或均不用苦参碱含有量较低;黄芪对氧化苦参碱含有量的影响具有显著性差异 (P<0.05),白茅根对氧化苦参碱含有量的影响具有极显著性差异 (P<0.01);但当白茅根与黄芪共同配伍苦参使用,明显降低了氧化苦参碱的含有量。
3 讨论
银苦黄白汤是临床治疗肾炎、肾盂肾炎、尿毒症的有效方。中药复方用药是中医临床治病的特色与灵魂[3]。方剂的药效并不是单味药效的简单加和,而是遵循“君臣佐使”原则。强调方证关联、病症结合,使各味药形成“有制之师”,针对相应的证或病,达到“整体综合调节”的效果[4]。中药复方治疗疾病的物质基础是其中的化学物质。在改剂型的过程中,只有明确其化学成分及其理化性质,明确中药有效成分的化学结构,才有可能明确其制备过程的动态变化,才有可能实现中药质量的稳定性和临床疗效的确切性,才能保证中药复方制剂等生产过程的质量控制和检测[5]。
本项试验研究了银苦黄白口服液不同配伍对苦参碱和氧化苦参碱含有量的影响。与配伍共煎相比苦参单味药中苦参碱含有量最低,氧化苦参碱含有量最高,表明共煎不仅是增加了苦参碱的提取率,也有氧化苦参碱转化为苦参碱可能[6]。3、4、5、6号共煎液中苦参碱和氧化苦参碱的总量高于单味苦参提取液的总量,其中5号 (苦参+银花+白茅根) >4号 (苦参+黄芪) >6号 (苦参+银花)>3号 (苦参+黄芪+白茅根),提示苦参与银花、白茅根共煎能显著增加苦参碱和氧化苦参碱的提取率;黄芪与金银花共用或均不用组苦参碱含有量较低,提示黄芪与金银花增加苦参碱提取率的途径不同,共用时反而互相抑制,影响了苦参碱的提取;白茅根与黄芪共同配伍苦参使用,明显降低了氧化苦参碱的含有量。从对苦参碱和氧化苦参碱含有量的影响角度,可以考虑黄芪不宜共煎。但对其他有效成分的影响及临床疗效的影响,还将进一步研究,另文报导。
试验对比了多种展开剂,如苯-丙酮-醋酸乙酯-浓氨(2∶3 ∶4 ∶0.2)[7],甲苯-丙酮-甲醇 (8 ∶3 ∶0.5),甲苯-乙酸乙酯-甲醇-水 (2 ∶4 ∶2 ∶1)[1,8],环己烷-乙酸乙酯-丙酮-浓试液 (4 ∶6 ∶8 ∶0.5)[9],三氯甲烷-甲醇-水 (7 ∶2 ∶1)和三氯甲烷-甲醇 (5 ∶0.2)[10],三氯甲烷-甲醇-浓氨试液 (5∶0.6∶0.3)等。因苦参碱和氧化苦参碱Rf值相差较大,有的对苦参碱展开效果较好,有的对氧化苦参碱展开效果较好,经调整选定三氯甲烷-甲醇-浓氨试液 (10∶1.2∶0.2)为展开剂,可同板检测两项指标。喷改良碘化铋钾试液为显色剂,显色稳定。因CAMAG薄层色谱扫描仪具有自动扣除背景的作用,故选用单波长反射直线扫描,简单、快速、准确。
[1]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010:188.
[2]李 毅,王 飞,吴 民.苦参药材质量标准研究[J].中成药,2011,33(2):363-364.
[3]贺福元,邓凯文,石继连,等.中药有效成分群组方技术研究若干基础瓶颈问题及数理特征化思路的提出[J].中药材,2009,32(1):1-7.
[4]贺福元,邓凯文,邹 欢,等.中药复方谱动学与谱效动力学差异性的研究[J].中国中药杂志,2011,36(2):136-141.
[5]王智民.中药药效物质基础的系统研究是中药现代化的关键[J].中国中药杂志,2003,28(12):1111-1113.
[6]万旭英,罗 明,贺 平,等.苦参碱和氧化苦参碱的提取鉴定和含量测定[J].中华中医药学刊,2009,27(10):2066-2068.
[7]姜志戎,李国柱,陈 明.妇洁洗剂的质量标准研究[J].中成药,2009,31(8):14-15.
[8]王惠娟,杨国亮,麻风华,等.苦参饮片质量标准研究[J].中国药房,2010,21(23):2151-2153.
[9]祁海宏,邬瑾丽,屈鹏舒,等.薄层色谱扫描法测定治带片中苦参碱含量[J].中国药业,2008,17(3):15-16.
[10]丁郁文.苦参薄层色谱法的改进[J].陕西中医,2008,29(8):1071-1072.
