低温胁迫对叶菜类观赏蔬菜抗寒性生理指标的影响
2012-07-16王文杰张国凤王华森
王文杰,张国凤,李 军,王华森*
(1、2、3.山东省东营市农业局,山东 东营 257091;1*.浙江农林大学,浙江 杭州 311300)
观赏蔬菜是一类既可食用又可观赏的新型蔬菜的总称,是集食用、观赏、绿化、美化于一体的多功能蔬菜。叶菜类观赏蔬菜作为观赏蔬菜中较大的一类,具有其独特的一面。叶菜类蔬菜其生长速度快,又可食用,作为观赏类蔬菜既可以美化生活,而且还能在种植的过程收获一定乐趣,减少人们的生活压力。冬季,叶菜类观赏蔬菜的栽培可在室内、封闭的阳台或温室中进行。温度是影响植物生长及植物观赏性的重要因素。低温会对其造成一定的伤害,低温不仅不利于植物的正常生长,也会对植物原有的一些生理指标产生影响。因此,研究低温对叶菜类蔬菜生长的影响,对明确叶菜类蔬菜适宜的生长环境具有重要的理论意义和应用价值。
1 材料与方法
1.1 试验材料
试验材料为大叶木耳菜、一点红苋菜、紫冠1号小白菜和紫罗兰生菜4种叶菜类蔬菜。
1.2 试验设计
采用温度处理法,在植株生长30 d后取外层第2、3片叶。采摘后,放入速封袋中,存在放有冰块的泡沫盒中,带回实验室,用去离子水冲洗两遍,然后用吸水纸吸干。将叶子混匀分成5份,置于速封袋中,放入程控冰箱内,所采的样品于0℃停留2.5 h后,取出第一组样品,再降温至-4℃停留2.5 h后,取出第二组样品,依次类推,直至温度降至-16℃。将低温处理过的样品置于0℃的冰箱内回温恢复2 h,然后进行相关指标的测定,每个处理重复3次。
1.3 测定方法
1.3.1 相对电导率 取0.1 g叶片于试管中,加入10 mL去离子水,在25℃环境下进行震荡,4 h后用电导仪测定初电导率(S1)。然后再将试管放入沸水中水浴15 min,经杀死植物组织。取出试管后冷却至室温,并在室温下平衡10 min,摇匀,测定终电导率(S2)[1]。
相对电导率的大小表示细胞受伤害的程度。
相对电导率=S1/S2
1.3.2 抗氧化酶活性测定 (1)抗氧化酶的提取和测定:参照朱祝军等[2]的方法。取0.3 g叶片,加2 mL 25 mmol·L-1HEPES 缓冲液(含0.2 mmo1·L-1EDTA,pH 7.8)和 2%不溶性 PVP。冰浴中匀浆,4℃12000 r·min-1离心20 min,上清液用于抗氧化酶活性测定。
(2)过氧化氢酶(CAT)活性的测定采用Cakmak和Marschner[3]的方法。取上清液100 μL,加25 mmol·L-1的磷酸缓冲液(pH7.0,含 0.1 mmol·L-1的 EDTA)1700 μL,10 mmol·L-1H2O2200 μL,25 ℃下反应。用岛津紫外可见分光光度仪(SHIMADZUUV-2550 PC)按kinetics程序测定OD240的动力学变化,取其中20 s的动力学变化计算酶促反应速率。吸光系数为39.4 mmol·L-1·cm-1。
(3)过氧化氢酶(POD)的测定。采用愈创木酚比色法参考郝再彬等[4]的方法。取25 mmol·L-1,磷酸缓冲液(pH7.0,含 0.1 mmol·L-1,的 EDTA)1700 μL,10 mmol·L-1H2O2100 μL,1% 愈创木酚 100 μL,加入上清液100 μL。用岛津紫外可见分光光度仪(SHIMADZUUV-2550 PC)按kinetics程序测定OD470的动力学变化,取其中20 s的动力学变化计算酶促反应速率。吸光系数为2.8 mmol·L-1·cm-1。
(4)超氧化岐化酶(SOD)活性的测定参照Rao和Sresty[5]的方法。取上清液0.05 mL,加3 mL反应液(含 15 mmol·L-1,甲硫氨酸,65 μmo1·L-1NBT,2.0 μmol·L-1,核黄素,0.1 mmol·L-1EDTA;用 50 mmol·L-1pH7.8 的磷酸缓冲液配制)。在 25 ℃ ,100 μmol·m2·s-1下照光 15 min 后,于黑暗下终止反应,立即在560 nm波长处测定吸光值,以缓冲液代替酶液作为空白。酶活性采用抑制NBT光化学反应50%为一个酶活性单位表示。
(5)丙二醛(MDA)含量测定参照王以柔等[6]的方法。取上清液1 mL,加3 mlL含2%TBA的30%三氯乙酸溶液,95℃水浴中保温30 min,立即置于冰浴中冷却,3000 r·min-1离心10 min测定 OD532、OD600,按消光系数155换算MDA含量。
(6)可溶性蛋白的含量;采取考马斯亮蓝法[7]:取0.1 mL的酶提取液,然后加入5 mL的考马斯亮蓝,于595 nm波长下测OD值,根据标准曲线计算蛋白质含量。
样品中蛋白质的含量(mg·g-1)=(C·VT)·(1000 Vs·WF)-1
式中:C-根据OD值,查标准曲线值(μg);VT-提取液的总体积(mL);
WF-样品鲜重(g);Vs-测定时加样量(mL)。
2 结果与分析
2.1 低温胁迫对细胞膜透性的影响
2.1.1 相对电导率 生物膜是低温伤害作用于植物细胞的原初部位,当植物遭受寒害时,其生物膜首先发生生物相变,生物膜的透性因此增大,细胞内的电解质外渗[8,9]。以电解质外渗率研究植物抗寒性是最有效手段之一[10],电解质外渗率结合Logistic曲线方程推导半致死低温能准确地反映植物耐受的低温极限,在园林植物抗寒性研究中得到验证并已广泛应用[11,12]。
随着处理温度的下降,细胞内相对电导率上升,相对电导率的上升是零下低温对叶片原生质膜透性破坏的效应。低温处理初期相对电导率上升缓慢,然后在一定低温范围内相对电导率急剧升高,随后又趋于缓慢,即相对电导率随着温度的下降呈S型曲线变化。
如图1所示,4种叶菜类观赏蔬菜的在低温胁迫下,细胞内相对电导率随温度降低呈S型线变化。

2.1.2 半致死温度 以电解质透出率达50%时为半致死温度(LT50),用Logistic方程y=K/(1+ae-bx)对相对电导率曲线进行拟合,可获得方程曲线拐点X=ln(a)/b,即为LT50。

表1 4种蔬菜叶片电导率的Logistic方程及半致死温度LT50Table 1 The Logistic and LT50 of five species leaves
由表可见通过计算得到了4种叶菜类的半致死温度,将4种叶菜的半致死温度由低到高排序为:一点红苋菜、紫叶生菜、大叶木耳菜、紫冠1号小白菜。一点红苋菜的半致死温度为-7.7℃是4种叶菜中最耐低温胁迫的,而紫冠1号小白菜的半致死温度为-5.8℃为最不耐低温胁迫的。
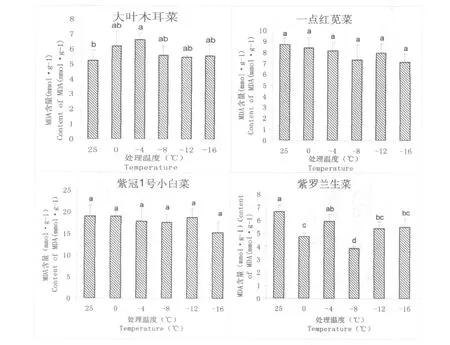
图3 低温胁迫下4种叶菜类观赏蔬菜MDA含量的变化Fig.3 The changes of MDA content in four species leaves under low temperature stress
2.2 低温胁迫对可溶性蛋白含量的影响
由图2,可见。在受到低温胁迫后。4种叶菜类蛋白含量的变化的表现各不相同。木耳有和紫冠1号小白菜的蛋白含量随着温度的降低有上升的趋势,大叶木耳菜在-16℃下的蛋白含量较对照增加了25.7%且差异显著(P<0.05),紫冠1号小白菜在-12和-16℃下的蛋白分别增加了24.1%、22.4%差异显著;而一点红苋菜和紫罗兰生菜的蛋白含量变化不明显与对照差异不显著。
2.3 低温胁迫对丙二醛(MDA)含量的影响
在植物在逆境胁迫或衰老过程中,活性氧超过正常水平时,产生积累,可导致膜脂过氧化、膜脂脱酣化、蛋白质变性、甚至DNA突变等一系列不良反应,对植物体造成伤害,膜脂过氧化的最终产物就是丙二醛。因此,丙二醛的含量已成为研究植物抗性常用的生理生化指标[13]。
由图3可知,4种叶菜类在低温胁迫的丙二醛含量的变化。大叶木耳菜各处理的含量略高于对照,有一个缓慢上升,而后又下降的趋势,在-4℃下达到最大值与对照相比差异显著(P<0.05);一点红苋菜和紫冠1号的各处理均低于对照且有下降的趋势,但与对照相比均无显著性差异;紫罗兰生菜各处理的丙二醛含量均低于对照,但变化规律不明显,在0℃和-8℃时下降较多分别为28.0%和42.1%,-12℃和-16下降较少分别为19.2%和17.5%与对照差异显著,-4℃含量与对照差异不显著。
2.4 低温对超氧化歧化酶(SOD)含量的影响
由图4可见,4种叶菜中SOD的在低温处理下的变化规律。大叶木耳菜中SOD含量随温度的降低先升高在-4℃是达到最高值,然后又下降的总趋势,其中0、-4、-8℃与对照相比上升了20.6%、44.3%和34.5%,差异显著(P<0.05),-12℃时下降了22.7%且差异显著;紫罗兰生菜在各温度处理下SOD的含量总体有所下降,其中0、-4、-8、-12、16 ℃下降也 32.2%、26.4%、41.8%、36.4%和 25.7%且差异显著,处理间无显著差异。一点红苋菜和紫冠1号小白菜的变化不明显SOD含量受温度影响不大。
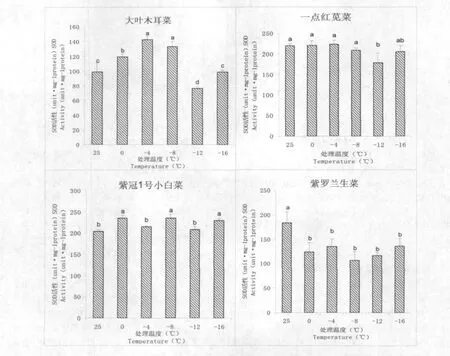
图4 低温胁迫下4种叶菜类观赏蔬菜SOD活性的变化Fig.4 The changes of SOD activity of four species leaves under low temperature stress
2.5 低温对过氧化物酶(POD)含量的影响

Fig.5 The changes of POD activity of three species leaves under low temperature stress
POD与SOD一样,也是植物对膜脂过氧化的酶促防御体系中重要的保护酶之一,它的主要功能起到酶促降解H2O2的作用,使植物受到低温胁迫时,免受伤害[14]。
实验过程中,未能测得大叶木耳菜的POD值,分析可能是因为,大叶木耳菜叶片中所含的粘液物质对POD造成了干扰。一点红苋菜的POD含量是先上升后下降再上升的一个过程,在0℃时较对照含量上升了30.9%,在-4℃时又下降到对照水平,在-8、-12和-16℃时分别较对照上升了56.0%、129%和139%且差异显著(P<0.05)。紫冠1号小白菜的POD含量也呈先下降后上升的趋势,但下降趋势不明显,从-4℃到-12℃有明显的上升趋势,各处理间差异显著;紫罗兰生菜的POD含量呈上升的趋势,-4、-8、-12和-16℃显著高于对照,含量分别上升了60.9%、60.8%、78.6%和73.1%且差异显著。
2.6 低温对过氧化氢酶(CAT)含量的影响
在活性氧代谢过程中,CAT可以使H2O2发生歧化生成水和氧分子发挥了重要作用[15]。大叶木耳菜各温℃处理下CAT的变化规律不明显,-8℃时含量显著高于对照和其它处理(P<0.05),-12℃时含量最低较对照低了29.6%且差异显著;一点红苋菜的CAT含量从0℃开始有一个先下降后上升的过程,-8℃时达到最高值,各处理与对照间的差异不显著;紫冠1号小白菜从0℃开始呈下降趋势在-8℃时达最小值,后又上升,-4、-8、-12和-16 ℃分别较对照下降了53.2%、69.8%、45.4%和38.4%;紫罗兰生菜从0℃开始CAT含量呈上升趋势到-8和-12℃达最大值,分别比对照上升了70.3%和75.0%差异显著,-16℃又下降到对照水平,下CAT含量显著低于对照和0℃下的含量。
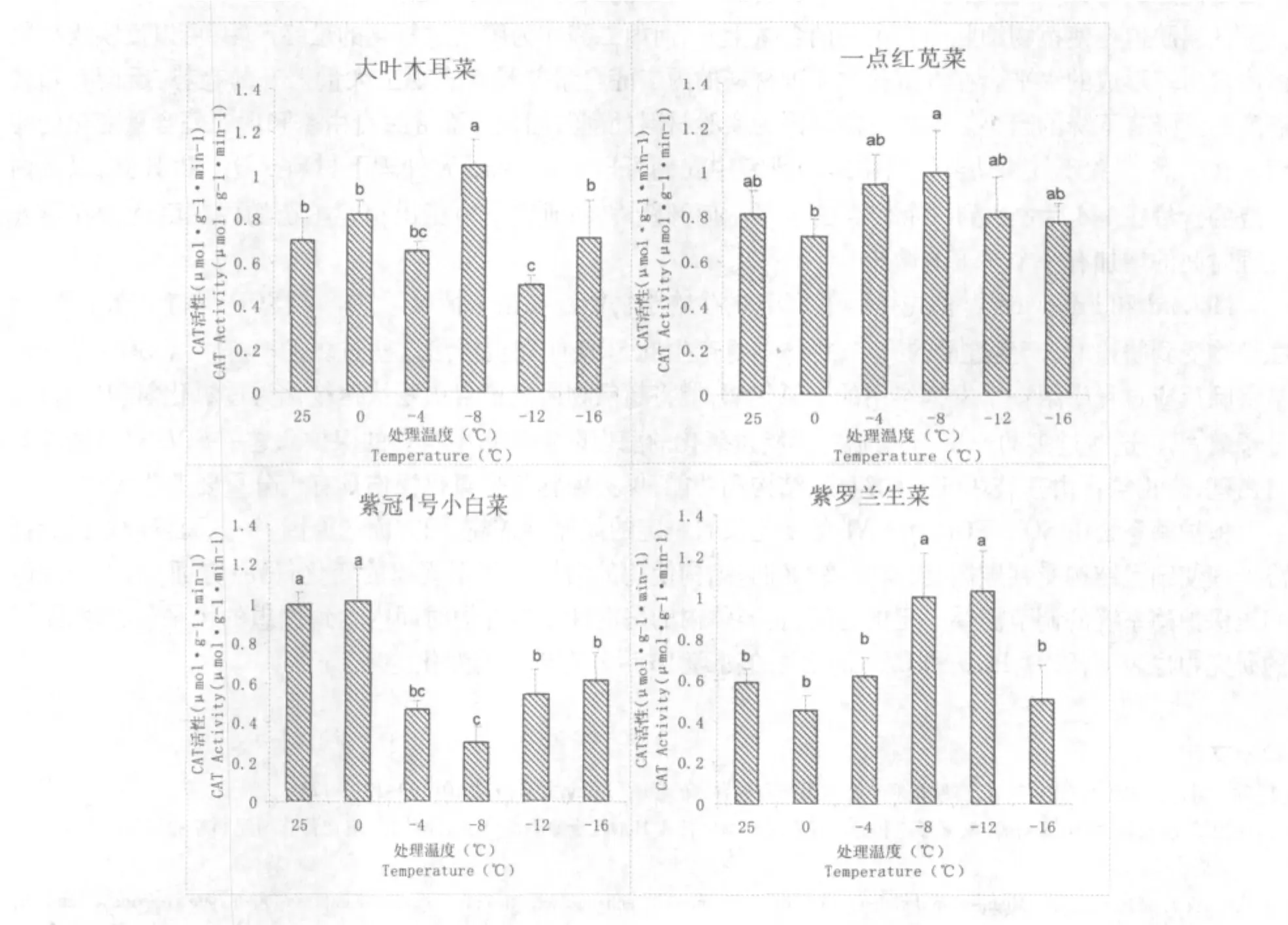
图6 低温胁迫下4种叶菜类观赏蔬菜CAT活性的变化Fig.6 The changes of CAT activity of four species leaves under low temperature stress
3 结论
观赏蔬菜。叶菜类观赏蔬菜是一类集食用、观赏、绿化、美化于一体的多功能蔬菜,温度是影响植物生长及植物观赏性的重要因素,研究低温对叶菜类蔬菜生长的影响对明确叶菜类蔬菜适宜的生长环境具有重要的理论意义和应用价值。本试验以4种叶菜类蔬菜为试材,通过低温处理来研究在不同低温下4种叶菜类蔬菜的相对电导率、半致死温度、可溶性蛋白等7个生理指标的变化。试验发现随着温度的降低4种叶菜类的膜通透性受到较大的破坏,4种叶菜类蔬菜的相对电导率随温度的降低而逐渐升高,通过对叶片相对电导率的测定,利用Logistic方程计算出其半致死温度,半致死温度(LT50)是评价一个物种抗寒性强弱比较准确的指标[16,11]。本试验中依据半致死温度来评价抗寒性高低的顺序依次是:一点红苋菜>紫叶生菜>大叶木耳菜>紫冠1号小白菜。
4 讨论
在植物抗低温研究中,对低温锻炼与蛋白质含量的关系一直存在着不同的看法。但有一点可以肯定,可溶性蛋白质的含量与植物的抗冷性之间有着密切的关系。大多数研究者认为细胞内可溶性蛋白质的含量与植物的抗冷性呈正相关。低温会导致植物细胞中可溶性蛋白含量的增加。可溶性蛋白的亲水胶体性质强,它能明显增强细胞的吃水力,可以束缚更多的水分,同时可以减少原生质因结冰而伤害致死的机会[17]。可溶性蛋白含量的提高可以提高植物的抗寒性,例如,低温胁迫下的植物合成抗冻蛋白,抑制冰晶生长,减轻冰晶对类囊体膜的伤害[18]。但在本实验中,发现4种叶菜类的蛋白含量,并没有较大幅度的提升,只是大叶木耳菜和紫冠1号小白菜有小幅上升,而一点红苋菜和紫叶生菜的蛋白含量基本没有变化。原因可能是因为,本实验低温处理时间较短,而植物未能及时合成抗冻蛋白。
低温胁迫会使植物细胞内自由基的含量上升,而丙二醛作为膜脂过氧化的最终产物,可以反映出植物体内自由基形成的水平。在本试验中4种材料的丙二醛含量并没有表现出大量上升的趋势,反而有随着温度的下降有下降的趋势。这也可能是因为实验材料处理时间较短而导致自由基和丙二醛含量变化的滞后。在李晶[19]关于红松幼苗低温胁迫的研究中我们可以发现,在低温处理下材料·O2-和H2O2以及丙二醛的含量在1 d后才达到一个较高的水平。何开跃[20]的研究中也指出福建柏苗的丙二醛含量在随着处理时间的增加有一个显著的增长。
McCord和Fridovich[21]首先揭示了SOD的生物学功能。在正常情况下,O2-与SOD保持动态平衡,但在植物受到胁迫时,产生过量的O2-,机体本身产生的SOD能完全清除这些过多的O2-[22]。SOD 是活性氧清除反应过程中第一个发挥作用的抗氧化酶,能将超氧物阴离子自由基快速歧化为过氧化氢(H2O2)和分子氧[23]。这些过多的SOD是植物对膜脂过氧化的酶促防御体系中重要的保护酶之一SOD对于清除氧自由基,防止氧自由基破坏细胞的组成、结构和功能,保护细胞免受氧化损伤具有十分重要的作用[24]。
保护酶系统中SOD、POD和CAT的变化没有一定的规律,可能有两方面的原因:一方面可能是因为低温处理使细胞结构受到破坏,没有完整的细胞结构使酶的活性出现不规律的变化;另一方面,由于处理时间短保护酶系统的调节需要一定的时间,材料体内的酶活性不能在短时间内达到理想的水平。在李晶[19]的研究中也表明,SOD、POD和CAT的活性在处理1d后才有较大的变化。
[1]陈 曦,张 婷,刘志洋,等.低温胁迫对十种宿根花卉电导率的影响[J].北方园艺,2010(10):121-122
[2]朱祝军,喻景权,Gerendas,等.氮素形态和光照强度对烟草生长和H2O2,清除酶活性的影响[J].植物营养与肥料学报,1998,4(4):379-385
[3]Cakmak I,Marschner H.Magnesium deficiency and high light intensity enhance activities ofsuperoxide dismutase,Ascrobate peroxidase,and glutathione reductase in bean leaves[J].PlantPhysiology,1992,98:1222-1227
[4]郝再彬,苍 晶,徐 仲.植物生理实验[M].哈尔滨:哈尔滨工业大学出版社,2004
[5]Rao KVM,Sresty TVS.Antioxidant parameters in the seedlings of pigonpea[Cajanus cajan(L.)MillspauQhl in response to Zn and Ni stresses[J].Plant Science,2000,157:113-128
[6]王以柔,曾韶西.低温诱导水稻幼苗的光氧化伤害[J].植物生理学报,1990,16(2):102-108
[7]高俊凤.植物生理学试验指导[M].北京:高等教育出版社,2006
[8]Jyons J M.Chilling injury in plants[J].Ann Rev Plant Physiol,1973,2(4):445-446
[9]董 丽,黄亦工,贾麦娥,等.北京园林主要常绿阔叶植物抗冻性及其测定方法[J].北京林业大学学报,2002,24(3):70-73
[10]张 钢.国外木本植物抗寒性测定方法综述[J].世界林业研究,2005,18(5):14-18
[11]徐 康,夏宜平,徐碧玉,等.以电导法配合Logistic方程确定茶梅'小玫瑰'的抗寒性[J].园艺学报,2005,32(1):148-150
[12]缴丽莉,路丙社,白志英,等.四种园林树木抗寒性的比较分析[J].园艺学报,2006,33(3):667-670
[13]杜永吉.兰引3号结缕草抗寒性的研究[D].石河子:石河子大学,2007
[14]田国忠,李怀方,裘维蕃.植物过氧化物酶研究进展[J].武汉植物学研究2001,19(4):332-344
[15]Frank V,Eva V,James F D,et al.The role of active oxygen species in plant signal transduction.Plant Science.2001,161:405 ~414
[16]罗正荣,章文才.应用Logistic方程测定柑桔抗冻力的探讨[J].果树科学,1994,4:100-102
[17]Krishna S.Nemali and M.W.van Iersel.Acclimation of Wax Begonia to light intensity:Changesin photosynthesis,respiration and chlorophyII concentration[J].Amer.Soc.Hort.Sci,2004,129(5):745-751
[18]潘瑞炽.植物生理学[M].北京:高等教育出版社,2008
[19]李 晶,阎秀峰,祖元刚.低温胁迫下红松幼苗活性氧的产生及保护酶的变化[J].植物学报,2000,42(2):148-152
[20]何开跃,李晓储,黄利斌,等.冷冻胁迫对福建柏苗可溶性糖和丙二醛(MDA)含量的影响[J].江苏林业科技,2000,6(12):6-8
[21]McCord J M,Fridovich I.Superoxide dismutase:an enzymaticfunction for erythrocuprein(hemocuprein)[J].J Biol Chem,1969,244:6049-6055
[22]李 勇,超氧化物歧化酶(SOD)的应用研究进展[J].攀枝花学院学报,2007,6(12):9-11
[23]马旭俊,朱大海.植物超氧化物歧化酶(SOD)的研究进展[J].遗传,2003,25(2):225-231
[24]王建华,刘鸿先,徐 同.超氧化物歧化酶(SOD)在植物逆境和衰老生理中的作用[J].植物生理学通讯,1989(l):1-7
