铀化合物与不同氟化剂反应的高温热力学
2012-06-30戴建兴张焕琦李晴暖吴国忠
戴建兴 张焕琦 李晴暖 吴国忠
(中国科学院上海应用物理研究所 上海 201800)
熔盐反应堆是六种第四代反应堆堆型之一,具有本征安全性高、放射性废物少、出口温度高、可实现钍增殖利用、防止核扩散等优点,近年来倍受国内外关注。其采用熔融氟化物盐作为燃料载体和冷却剂,由于氟化物熔融盐的特点,其乏燃料后处理工艺可使用干法技术,而非传统的水法技术。干法后处理过程中不用水作溶剂,其主要分离步骤在高温下进行。流程具有耐辐照、低临界风险、放射性废物少等优点,适宜处理高燃耗、短冷却期的乏燃料。
高温氟化物挥发法,是利用铀氟化物与裂变产物的氟化物的不同挥发性而实现分离的技术,可得到高纯度的UF6,回收率大于99%,去污系数可达108以上[1]。相对于其他干法(如高温电解、真空蒸馏等),高温氟化物挥发法具有工艺流程简单、铀分离效率高、去污效果好等优点,是具有良好发展前景的干法后处理工艺,可从金属元件、MOX元件、熔融盐等类型的燃料中高效地回收铀,适合快堆和熔盐堆等堆型乏燃料的处理,美国、日本、捷克等国相继开展了此类研究[2]。
但是,高温氟化的反应条件对设备材质的腐蚀性很强,该方法并未得到很好的发展。高温氟化挥发工艺使用F2作为氟化剂[1],F2与金属反应会生成致密的氟化物层具有钝化效果,可减少金属材质的进一步腐蚀。但熔融盐体系的熔融氟化物会溶解破坏钝化层,加剧腐蚀作用,使处理熔融盐燃料时的设备材料腐蚀问题尤为突出[3]。因此,有人提出使用常见的工业氟化剂(ClF3、BrF5、SF6等)作为替代[4−6],但此类氟化剂会在处理过程中引入化学反应,活性较高,难以去除Cl、Br、S等元素,不适用于以氟化物熔融盐为燃料载体的熔盐反应堆。美国太平洋西北国家实验室(Pacific Northwest National Laboratory, PNNL)提出,以 NF3作为氟化剂替代F2[7–9]。NF3是性质较为温和的气体氟化剂,无色、无毒、无味、不可燃,沸点为144.4 K,无腐蚀性,常温下不与水、酸和碱反应。对设备材料的腐蚀作用弱于F2,且氟化反应后N元素转化为N2;相比于其他氟化剂,熔融盐体系的残留影响较易控制。
评价一种氟化剂是否适合于熔盐燃料的高温氟化反应,须考虑多种因素:如反应活性、转化效率、材料腐蚀、使用安全性、副反应、残留影响、使用成本与经济性等。本文对不同氟化剂的氟化反应的反应热力学进行计算,比较它们对铀化合物的氟化反应热及反应平衡常数,判断反应的可行性,为熔融盐体系高温氟化挥发工艺设计与实验研究提供基础。
1 计算方法
1.1 反应热
化学反应的反应热,可根据反应物和生成物的生成焓计算:

式中,T是绝对温度,B代表反应式中的任一组分,P、R分别代表生成物和反应物的计量数,ΔrHm和ΔfHm分别表示一个反应的反应摩尔焓变和反应式中组分的摩尔生成焓,上标θ表示标准状态,在此公式指压强为 1 atm。已知铀化合物[10]以及常见的无机小分子等[11]的标准生成焓及熵值见表1。
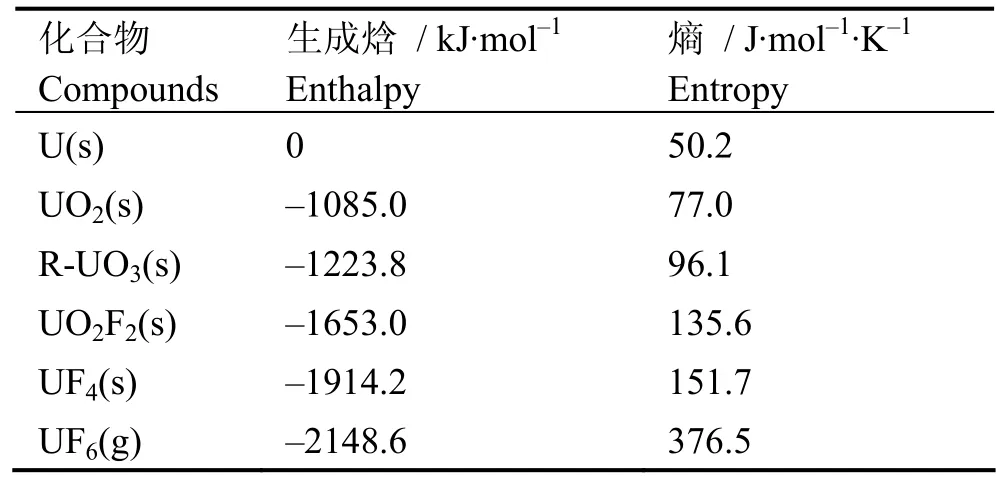
表1 在标准状态下,铀及其化合物的生成焓和熵[10]Table 1 The formation enthalpy and entropy of uranium and uranium compounds under standard state[10].
对于非标准状态下,反应焓可以根据基尔霍乎定律计算,化学反应在温度为 T时和标准状态下(298 K)的反应热关系由式(2)、(3)给出:
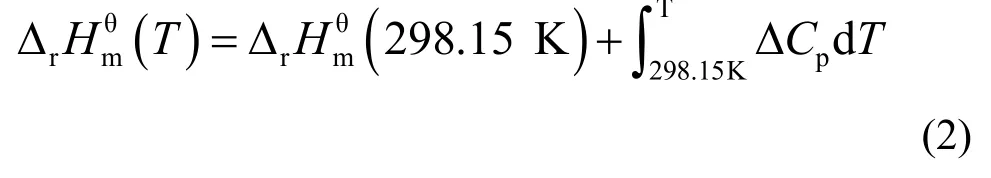

式中,Cp,m为化合物的摩尔热容,ΔCp为反应前后热容变化。由式(2)、(3),计算不同温度下某物质的生成焓,热容是关键,其随温度的变化是研究重点。一般而言,在较小温度区域内,热容的变化较小。根据文献[10,11],可知铀化合物以及常见的无机小分子等的热容与温度间的关系(表2)。

表2 铀及其化合物热容与温度关系Table 2 The temperature dependence of heat capacities for uranium and uranium compounds.
1.2 反应平衡常数
一个化学反应能达到的最高限度,可用反应平衡常数衡量。反应平衡常数若小于 1,表明此反应不能向正方向进行;平衡常数越大反应进行得越彻底。化学平衡常数与反应吉布斯自由能相关:
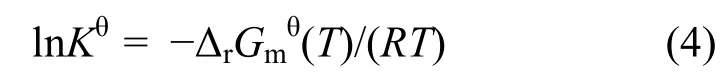
其中,Kθ为体系的热力学平衡常数,无量纲;ΔrGm表示摩尔吉布斯自由能,R为摩尔气体常数。
温度为T时,吉布斯自由能可由反应焓和反应的熵变(ΔrSm)计算得到:

热力学第三定律提供了物质熵变和热容的关系,可得到不同温度下的熵变值:
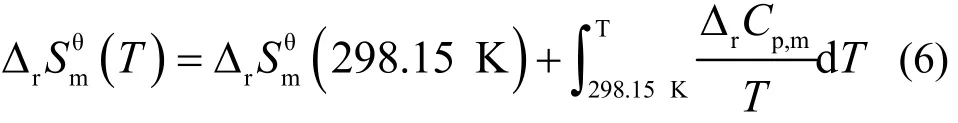
2 结果与讨论
2.1 铀化合物氟化反应热
由式(1)、(2)计算得到 F2、NF3、SF6、BrF5、ClF3等氟化剂氟化铀的氧化物和氟化物的反应热列于表 3。为比较常温、中温和高温条件下的氟化反应放热随温度的变化情况,选择温度为 298、573和800 K。铀具有多种价态,其氟化反应多数为复杂反应,即可能的产物不唯一,随氟化反应程度不同可能生成五价、六价或混合价态氟化物,本文以氟化反应充分、生成六价化合物为准。
由表3,除SF6氟化 UF4为吸热反应外,其余都属于放热反应。不同温度下,表3所列化学反应的放热变化不大。F2或NF3将不同铀化合物转化为UF6的反应热与铀化合物的化学形态和价态有关:氟化剂与铀氧化物反应的反应热明显大于与氟化物反应的反应热,且化合物中铀的价态越低,生成的反应热越多。这是因为氟化反应过程需要打破的键越少,消耗的能量就越少,最终的反应热就越多。例如铀单质的氟化反应热最高,因为它不需要先打破原有的键,再与F形成新的键。由于U-F键能大于U-O键能,打破U-F键所需能量要比打破U-O所需能量更大,因此UO2F2氟化反应热要多于UF4氟化反应热。
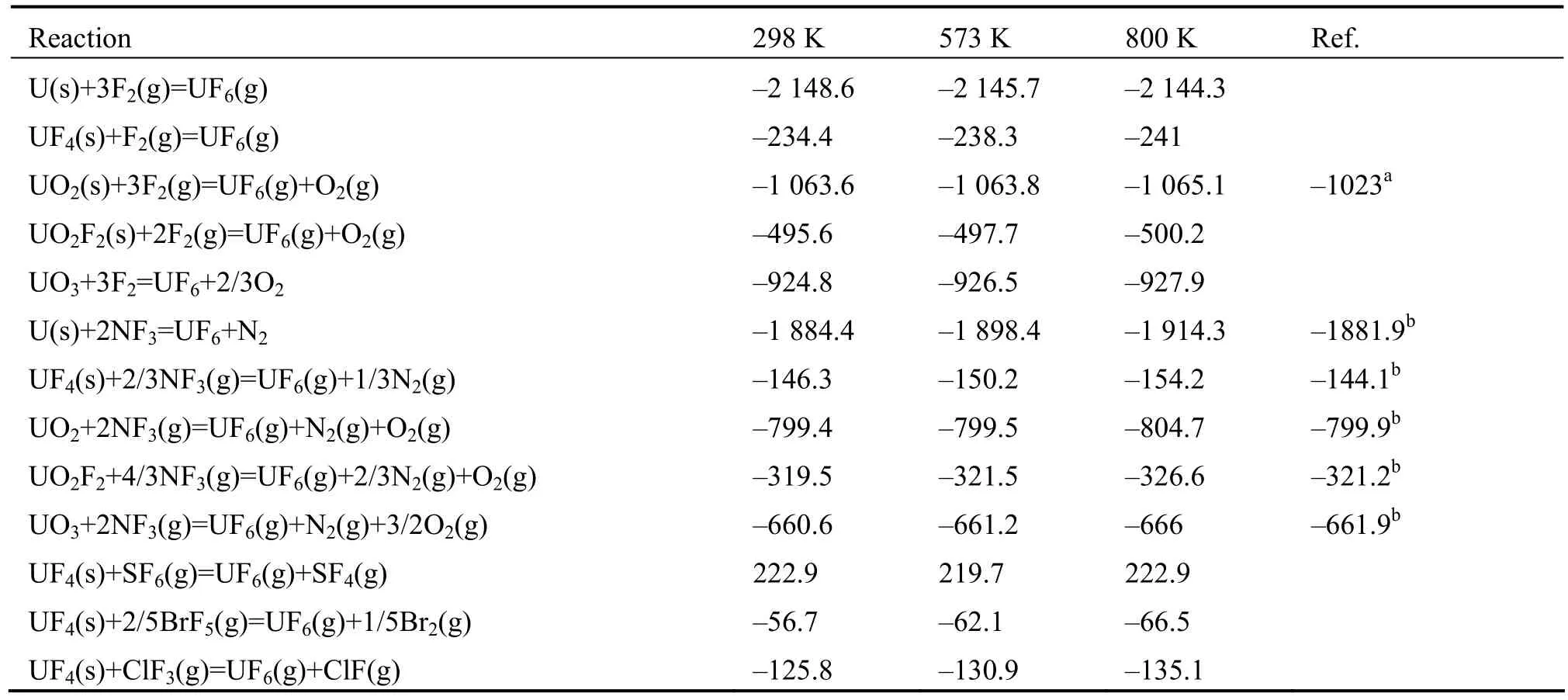
表3 298、573、800 K下铀及其化合物的氟化反应放热计算值Table 3 Enthalpies (in kJ/mol) for fluorinating uranium and uranium compounds at 298, 573 and 800 K.
为检验计算方法的可靠性,表3最后一列给出了文献[13]的实验值和文献[7]的计算值,本文计算值和文献值的偏差在 4%以内。文献[7]采用的计算软件为HSC Chemistry[12],其计算方法和本文一致。生成焓数据和热容数据根据文献来源不同会有一定的差距,因此认为本文计算结果与文献值的差异可能来源于生成焓或热容采用了不同的文献来源。
2.2 UF4氟化反应热及反应平衡常数
图 1为 F2、ClF3、BrF5、SF6和 NF3氟化 UF4的反应热和反应平衡常数与温度的关系。由图1(a),这些氟化剂的氟化反应热随温度变化不大,在298–1 000 K,反应热变化在10 kJ/mol内,温度影响并不明显;且除SF6外,其他氟化剂与固态UF4的氟化反应都属于放热反应,理论上反应易于进行。
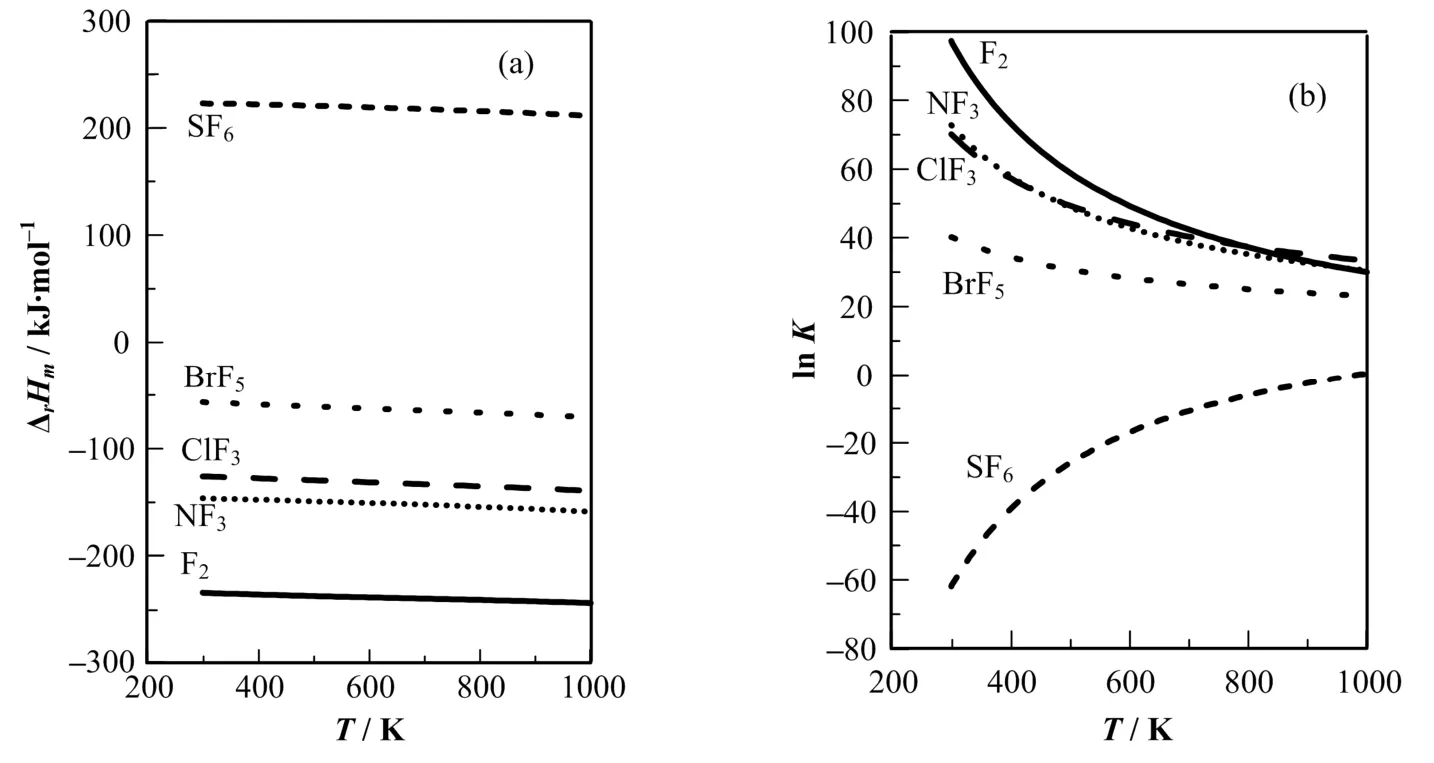
图1 不同氟化剂氟化UF4(固态)时的反应热(a)和反应平衡常数的对数(b)随温度的变化Fig.1 Temperature dependence of reaction enthalpies (a) and lnK (b) for UF4 fluorination using different fluorinating agents.
对图1(b)可作如下概述:(1) 1000 K时,SF6的反应平衡常数的对数变正,说明理论上SF6在1 000 K以下不能与固态 UF4进行氟化反应;(2) 除 SF6外,其余氟化剂在低于1000 K时的反应平衡常数对数都大于零,说明这几种氟化剂都能与UF4自发进行氟化反应;(3) F2、NF3、ClF3和BrF5作为氟化剂氟化UF4时,其反应平衡常数随温度升高而变小,说明随温度的升高,这几种氟化剂的氟化反应的平衡向逆方向进行;(4) 不同氟化剂的氟化反应程度不同,其从高到低依次为F2、NF3、ClF3、BrF5。
2.3 UF4氟化反应热对熔盐体系温度的影响
氟化反应是放热反应,会对熔盐体系的温度产生影响。若体系温度变化过于剧烈,则会对实验操作及安全带来严重影响。因此,氟化反应热对体系温度的影响,也是氟化挥发工艺实验研究中的重要问题。
根据上述计算的反应热数据,探讨了在LiF-NaF-KF(FLiNaK)、LiF-BeF2(FLiBe)和 LiF-BeF2-ThF4熔盐体系(氟化物熔融盐的物理化学参数[14,15]见表4)中,UF4的氟化反应热对熔盐体系温度的影响。假设熔融盐燃料体系中,UF4的含量在0.3%–1%(摩尔比),加入 UF4后,FLiNaK、FLiBe和 LiF-BeF2-ThF4熔盐的平均分子量分别为42.12–44.03、 34.84–35.81、 66.74–68.48。由于 UF4含量较低,假定其对熔盐体系比热容没有影响。由表2,温度对化学放热影响不会有巨大的变化,表5列出了573和800 K较为极端温度下,F2或NF3氟化UF4时熔盐体系的温度变化。
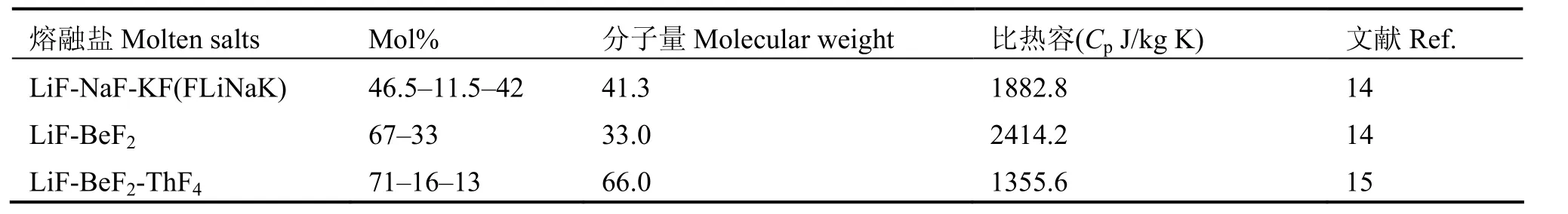
表4 氟化物熔盐的基本热物理性质Table 4 Basic thermophysical properties of fluoride molten salts.

表5 FLiNaK、FLiBe和LiF-BeF2-ThF4熔盐体系氟化反应热及温度变化Table 5 Reaction enthalpy and temperature variation (K) of fluorination in FLiNaK, FLiBe and LiF-BeF2-ThF4 systems.
计算结果显示,当UF4在熔盐中的摩尔含量为0.3%–1%时,氟化反应热不会对体系温度产生剧烈的影响。用F2进行氟化反应,假设熔盐中UF4摩尔分率为1%,且完全转化为UF6,则对于上述各体系,温度最多升高 29 K;如熔盐中 UF4摩尔分率为0.3%,则体系温度升高不超过9 K。
当以NF3作为氟化剂进行氟化反应时,相应的温度变化为6–19 K。由于反应热受温度变化影响较小,因此相同体系中不同反应温度(573和800 K)下氟化反应热导致的体系温度变化基本相同。
3 结语
本文通过反应热力学计算,比较了不同氟化剂氟化铀化合物的反应热及反应平衡常数。结果表明,F2、ClF3、BrF5和 NF3都可能与铀化合物自发进行氟化反应,但是 ClF3和 BrF5反应产生的 Cl和 Br具有较高的反应活性,无法彻底从熔盐体系中除去,不适合用作氟化物熔融盐燃料的氟化剂。
相比之下,NF3的反应产物能较易净化脱除,且其与UF4的反应平衡常数较高,氟化反应较容易进行,是一种潜在的F2替代氟化剂。
1 ORNL Reports: ORNL-TM-2578
2 刘学刚. 乏燃料干法后处理技术研究进展[J]. 核化学与放射化学, 2009, 31: 35–44 LIU Xuegang. Research on dry reprocessing technology of spent nuclear fuel[J]. Journal of Nuclear and Radiochemistry, 2009, 31: 35–44
3 ORNL Reports: ORNL -2832
4 Labaton V Y, Johnson K D B. The fluorides of uranium-IV Kinetic studies of the fluorination of uranium tetrafluoride by chlorine trifluoride[J]. Journal of Inorganic and Nuclear Chemistry, 1959, 10(1-2): 86–93
5 Jarry R L, Steindler M J. The reaction of gaseous bromine penta-fluoride with uranium compounds—I: The kinetics of the reactions with UF4and UO2F2[J]. Journal of Inorganic and Nuclear Chemistry, 1967, 29(7): 1591–1597
6 Johnson C E, Fischer J. Kinetics of the reaction of sulfur tetrafluoride with uranium trioxide and uranyl fluoride[J].Journal of Physical Chemistry, 1961, 65(10): 1849–1852 7 McNamara B, Scheele R, Kozelisky A,et al. Thermal reactions of uranium metal, UO2, U3O8, UF4and UO2F2with NF3to produce UF6[J]. Journal of Nuclear Materials,2009, 394(2-3): 166–173
8 Scheele R, Casella A. Assessment of the use of nitrogen
trifluoride for purifying coolant and heat transfer salts in the Fluoride Salt-Cooled High-temperature Reactor.Prepared for the U.S. Department of Energy 2010
9 McNamara B, Casella A, Scheele R,et al. Nitrogen trifluoride-based fluoride-volatility separations process:Initial studies. Prepared for U.S. Department of Energy 2011
10 Guillaumont R, Fanghänel T, Fuger J,et al. Update on the chemical thermodynamics of uranium, neptunium,plutonium, americium and technetium. North Holland Elsevier Science Publishers B. V., Amsterdam, The Netherlands, 2003
11 NIST Chemistry WebBook. NIST Standard Reference Database Number 69, National Institute of Standards and Technology, Gaithersburg, MD, June 2005,http://webbook.nist.gov
12 Roine A. Outokumpto HSC Chemistry Chemical Reaction and Equilibrium Software (HSC-5), Outokumpto Research Oy, ISBN 952-9507-08-9, 2002
13 Sazhin S S, Jeapes A P. Fluorination of uranium dioxide particles: a review of physical and chemical properties of the compounds involved[J]. Journal of Nuclear Materials,1999, 275(3): 231–245
14 Sohal M S, Ebner M A, Sabarwall P,et al. Engineering database of liquid salt thermophysical and thermochemical properties. Prepared for the U.S.Department of Energy 2010
15 ORNL Reports: ORNL-TM-2316
