活体珊瑚微量元素对硼同位素组成影响及硼掺入珊瑚的形式
2012-06-27肖应凯金章东刘丛强贺茂勇
肖 军, 肖应凯, 金章东, 刘丛强, 贺茂勇
活体珊瑚微量元素对硼同位素组成影响及硼掺入珊瑚的形式
肖 军1, 肖应凯2*, 金章东1, 刘丛强3, 贺茂勇1
(1. 中国科学院 地球环境研究所 黄土与第四纪地质国家重点实验室, 陕西 西安 710075; 2. 中国科学院 青海盐湖研究所 盐湖资源与化学重点实验室, 青海 西宁 810008; 3. 中国科学院 地球化学研究所 环境地球化学国家重点实验室, 贵州 贵阳 550002)

活体珊瑚; 微量元素; 硼同位素;11B-pH技术
0 引 言
近些年来,利用海洋生物碳酸盐的硼同位素组成重建古海水pH值, 计算当时大气CO2含量, 进而推测古气候的变化已成为国际硼同位素地球化学研究的热点[1–11], 被称为11B-pH技术。珊瑚因其快的生长速率和易于采集等自身优势成为研究的理想样品[2,5,11–13]。Vengosh[3]首次用负热电离法测定了现代珊瑚的硼同位素组成。Gaillardet.[5]首次用正热电离法分析了珊瑚中的硼同位素组成, 并建立了珊瑚的11B-pH值计。刘卫国等[13]用正热电离法分析了7000~300 a BP范围内南海滨珊瑚样品, 建立了南海珊瑚的11B-pH值计, 认为高海平面与低的珊瑚11B有关。Hemming.[14]的研究表明, 光照强度会对珊瑚硼同位素的季节变化产生影响, 但Hönisch[12]的研究表明, 除pH外, 光照强度、深度、食物供应对珊瑚的硼同位素不产生影响。
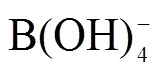
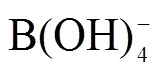
1 样品信息及分析方法
1.1 采样地点及样品信息
涠洲岛面积约34 km2, 属热带与亚热带气候相互影响的过渡区域, 该处珊瑚属浅水珊瑚类[33]; 灯楼角岬角位于雷州半岛的西南端, 地处热带北缘, 该海区海水温度、盐度、透明度和环境质量均适合造礁石珊瑚生长[34]; 鹿回头位于海南岛三亚东南, 属热带季风气候, 珊瑚生长繁茂, 属典型的珊瑚礁海岸, 该处珊瑚礁主要分布于三亚湾和小东海[35]。2006年10月在北海涠洲岛(109°8′51′′E, 21°03′40.9′′N)、雷州半岛的灯楼角(109°53′55′′E, 20°12′43′′N)和三亚湾(109°30′34′′E,18°11′3′′N)三地采集了52件活体珊瑚样品。对于每一海域, 尽量在小范围内采集珊瑚, 使得同一海域所采珊瑚生长海水的水化学条件基本相同, 因此每一海域只采1个海水样品。现场测定海水pH值, 涠洲岛、灯楼角和三亚湾海水pH值分别为8.06、8.07和8.30。所有珊瑚样品均采集于正在生长的珊瑚, 有关珊瑚样品信息见表1。
1.2 样品处理
先用去离子水反复冲洗以除去珊瑚样品表面大颗粒的泥污、可溶性盐以及残留海水, 然后在30% H2O2中浸泡4 h, 初步除去表面的有机杂质, 并用超声波进一步清洗。晾干后的珊瑚在玛瑙研钵中研磨成100~200目的粉末。粉末样品在净化恒温烘箱中于60 ℃恒重。称取约0.5 g恒重后的样品, 浸泡在30% H2O2中, 抽滤除去H2O2, 并用无硼水反复洗涤样品。用1.0 mol/L二次蒸馏 HCl溶解样品, 过滤除去少量残留物, 清液留作化学成分及硼同位素组成测定。
1.3 元素及硼同位素组成测定
样品的Ca、Mg、Sr、Na采用ICP-OES测定, 测定精度为3%。B浓度用甲亚胺-H法测定, 测定精度为2%。
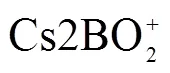
硼同位素组成用11B表示, 按下式计算:
11B(‰)=((11B/10B)样品/(11B/10B)标准−1)×1000
此处, 标准物质是NIST SRM 951, 其11B/10B推荐值为4.04362±0.00137[37], 而实测值为4.04763±0.00106 (2m,=8)。
2 结果与讨论
2.1 珊瑚和海水中元素浓度
CaCO3是珊瑚的主要化学成分, 以微晶方解石集合体形式存在。本研究测定的珊瑚Ca浓度变化范围为9.0~14.4 mol/L, 平均值为12.1 mol/L。在这5种元素中, Ca占到96.3%, 其他4种元素总和仅占3.7%。这表明珊瑚的主要成分为CaCO3, 其余的为微量元素或有机质。珊瑚中Mg、Sr、和Na浓度变化范围分别为22.9~65.4 mmol/L、66.8~106.1 mmol/L和296~668 mmol/L, 平均值分别为40.1 mmol/L、86.1 mmol/L和449 mmol/L(表2)。Ca、Sr、B和Na在珊瑚中富集, 其中Ca的富集程度最高,d平均达1186; 其次是Sr、B和Na,d平均值分别为1050、14.4和1.3。而Mg在珊瑚中却是贫化的,d只有0.8, 这与以前的研究结果一致[38]。
珊瑚中B浓度的变化范围为4.4~8.4 mmol/L, 平均值为5.9 mmol/L。鹿回头、涠洲岛和灯楼角海域海水的B浓度分别为0.41 mmol/L、0.40 mmol/L和0.40 mmol/L。珊瑚B浓度比海水的B浓度高得多, 表明珊瑚是海水中B的一个重要储库。Hemming.所测珊瑚B浓度变化范围为4.5~6.4 mmol/L[2]; Gaillardet.所测珊瑚的B浓度的变化范围为4.5~5.3 mmol/L[5]; Vengosh所测珊瑚B浓度的变化范围为5.8~7.2 mmol/L[3]; 刘卫国等所测珊瑚B浓度的变化范围为5.3~7.2 mmol/L[13]。本次所测珊瑚的B浓度的变化范围与前人的研究结果基本相同。
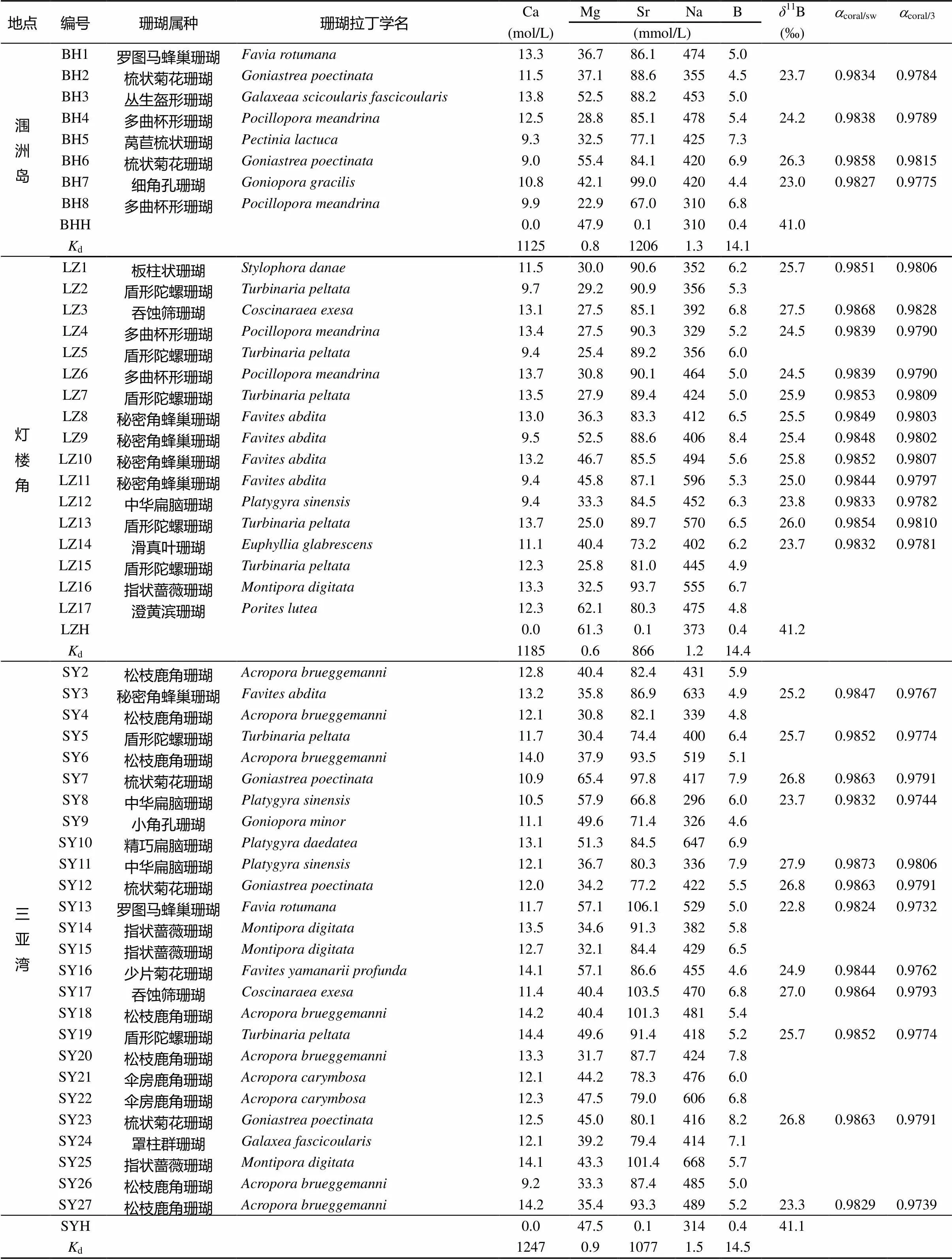
表1 珊瑚样品元素浓度及其硼同位素组成
注:d为分配系数,d=[E]珊瑚/[E]海水, [E]珊瑚和[E]海水分别为珊瑚和海水的元素浓度。LZH、BHH和SYH分别为雷州灯楼角、北海涠洲岛和三亚湾海水。
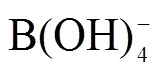

图1 海水中B的存在形式(采用pKb=8.597[39])及同位素组成与海水pH关系(采用α4-3=0.974[40])
2.2 珊瑚元素与B浓度及δ11B的关系
B如何掺入进珊瑚等生物碳酸盐的问题一直为人们所关注, 但对珊瑚中其他元素与B及硼同位素组成关系的研究则很少。珊瑚B浓度与其他化学成分的关系见图2。结果表明, 虽然珊瑚中Ca2+、Sr2+、Mg2+、Na+与B浓度呈现出正的或负的相关性, 但相关性不高(图2), 表明珊瑚的B浓度主要不是由这几种元素决定的。
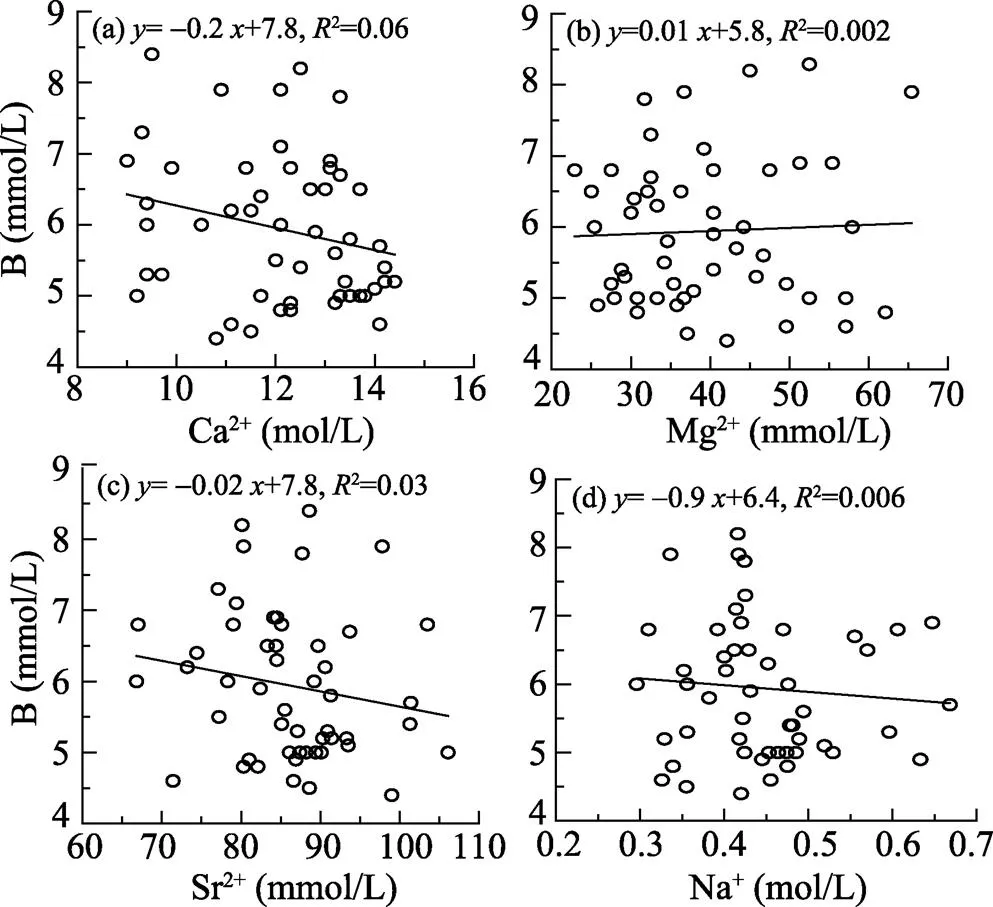
图2 珊瑚中B浓度与Ca、Mg、Sr、Na的关系
珊瑚中11B值的变化范围为22.8‰~27.9‰, 平均值为25.2‰。涠洲岛、灯楼角和三亚海水的11B值分别为41.0‰、41.2‰和41.1‰。Hemming.[2]所测珊瑚的11B为22.1‰±3‰; 刘卫国等[13]所测南海珊瑚礁11B的变化范围为22.7‰~24.8‰; Gaillardet.[5]所测现代珊瑚的11B为23.3‰~ 25.5‰, 珊瑚化石11B为23.5‰~27.3‰; Lécuyer.[11]所测珊瑚11B的变化范围为25.6‰~25.7‰; Vengosh[3]所测珊瑚11B的变化范围为26.7‰~ 31.9‰。我们的数据与以前研究的变化范围基本相同, 同时我们的数据表明不同属种珊瑚的11B值表现出一定的差异性。如多曲杯形珊瑚、滑真叶珊瑚、秘密角蜂巢珊瑚、盾形陀螺珊瑚和梳状菊花珊瑚的11B平均值分别为23.7‰、24.4‰、25.4‰、25.9‰和26.7‰。但不同采样点的同种珊瑚的11B值变化基本相同(表1)。如秘密角蜂巢珊瑚样品LZ8、LZ9、LZ10、LZ11和SY3的11B值分别为25.5‰、25.4‰、25.8‰、25.0‰和25.2‰。多曲杯形珊瑚样品BH4、LZ4和LZ6的11B值分别为24.2‰、24.5‰和24.5‰。分析表明(图3), 除与B浓度呈弱的正相关性外(2=0.39),11B与珊瑚的Mg、Ca、Sr和Na浓度不相关。据以前的研究[22,31,32], 珊瑚中若有Mg(OH)2存在, B(OH)3会优先掺入进Mg(OH)2, 使得珊瑚的11B值偏高, 进而使得用珊瑚硼同位素计算的古海水pH值升高, 给11B-pH技术带来不利影响。例如, 如果分别采用珊瑚的11B值23.7‰和26.7‰计算得到的海水pH值分别为8.36和8.57, 两者相差0.21。因此利用珊瑚硼同位素恢复古海水pH值时选择同属种珊瑚和判别是否有Mg(OH)2的存在是必要的。Rollion-Bard.[41]也建议在进行深海珊瑚的硼同位素测定时需仔细采样。珊瑚中11B与Mg/Ca的正相关性可作为珊瑚中Mg(OH)2存在的判别[32]。图3f显示11B与Mg/Ca无相关性, 这表明该区域珊瑚中虽有Mg存在, 但Mg不是以Mg(OH)2的形式存在, 不会影响到珊瑚的硼同位素组成。
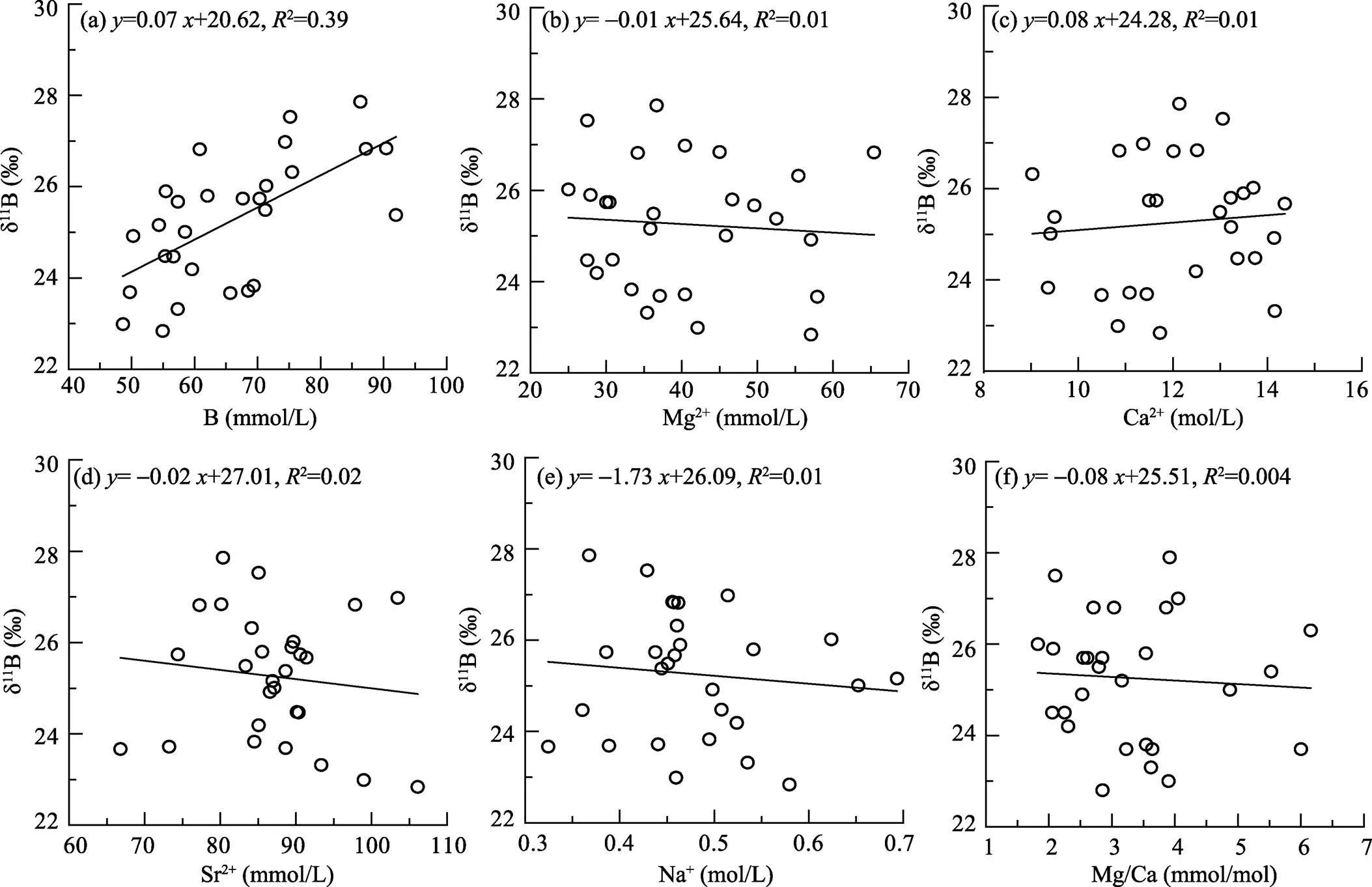
图3 珊瑚同位素组成(δ11B)与B、Mg2+、Ca2+、Sr2+、Na+浓度的关系
2.3 B(OH)4-与B(OH)3间的同位素分馏系数a4-3
Pagani.[20]报道了碳酸盐与海水B(OH)3间carb-3的计算公式:

整理后,4-3计算如下:

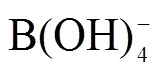
雷州灯楼角、北海涠洲岛和三亚鹿回头三地珊瑚与海水B(OH)3间分馏系数coral-3的变化范围分别为0.9781~0.9828、0.9775~0.9815和0.9732~0.9806, 平均值分别为0.9800、0.9791和0.9772。所有样品coral-3的平均值为0.9788, 该值与Kakihana.[42]得到的0.981较为接近。利用该分馏系数值和以下海水pH值的计算方程(3)可以得到珊瑚生长区海水的pH值。
pH=pa–lg((11Bsw-11B4)/(4-3-111B4-11Bsw+103(4-3-1-1))) (3)
此处, pa=8.597[39],11Bsw=41.1‰。
计算得到采样区海水pH值的变化范围为7.92~8.43, 平均值为8.20。当4-3分别取0.984[16]、0.981[42]和0.968[19]时, 据文献所发表的古代及现代有孔虫和珊瑚的11B值计算的海水的pH值分别为7.76±0.54、8.17±0.40和8.85±0.18。对于海水pH值的变化范围7.5~8.4[16]来讲, 采用4-3=0.984[16]和0.968[19]计算得到的pH值分别要低于和高于该变化范围, 表明0.984[16]和0.968[19]作为4-3值来计算古海水pH值是不合适的。采用Kakihana.[42]实验的4-3=0.981值计算得到的现代海水的pH值为8.17, 与现代海水基本相同。采用我们实验得到的4-3=0.9788值计算的现代海水的pH值为8.20, 与现代海水最为相近。这表明我们实验得到的a4-3值是可以接受的, 可用于11B-pH技术中反演古海水pH值。
2.4 硼掺入进珊瑚的形式
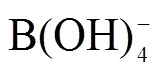
按照以下公式, 我们对掺入进珊瑚的B(OH)3的分数进行了计算。
B(OH)3(%)=(11Bcoral-11B4)/(11B3-11B4) (4)
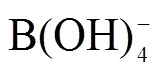
2.5 对δ11B-pH技术的影响
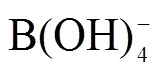
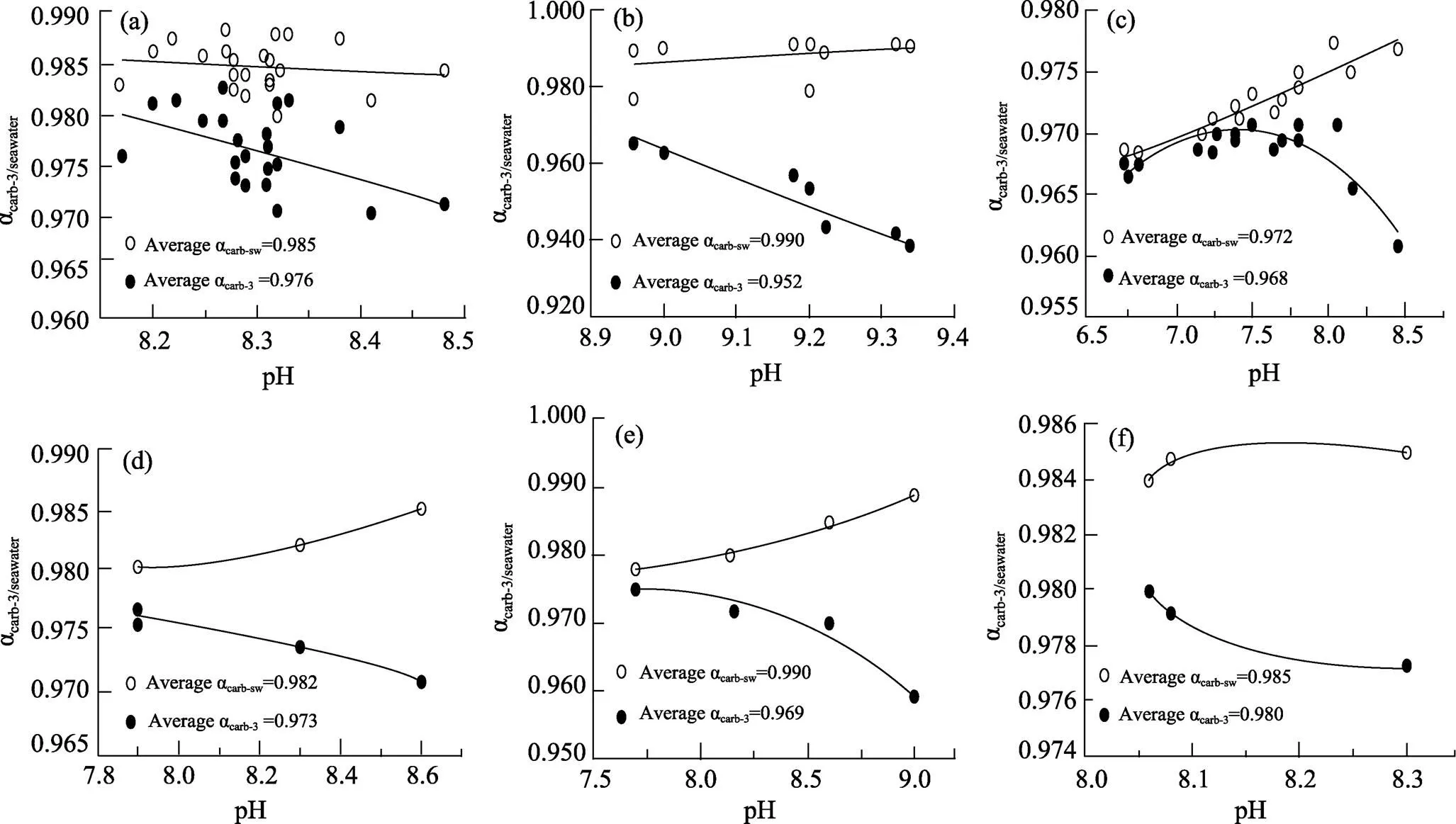
图4 acarb-3和acarb-sw随pH值的变化
(a) 珊瑚实验[38]; (b)无机碳酸盐沉积实验[22]; (c)吸附实验[19]; (d)无机方解石沉积实验[17]; (e)有孔虫养殖实验[18]; (f)本研究。
(a) coral experiment[38]; (b) precipitation experiment of inorganic carbonates[22]; (c) adsorption experiment[19]; (d) precipitation experiment of inorganic calcite[17]; (e)culture experiment of foraminifer[18]; (f) this study.
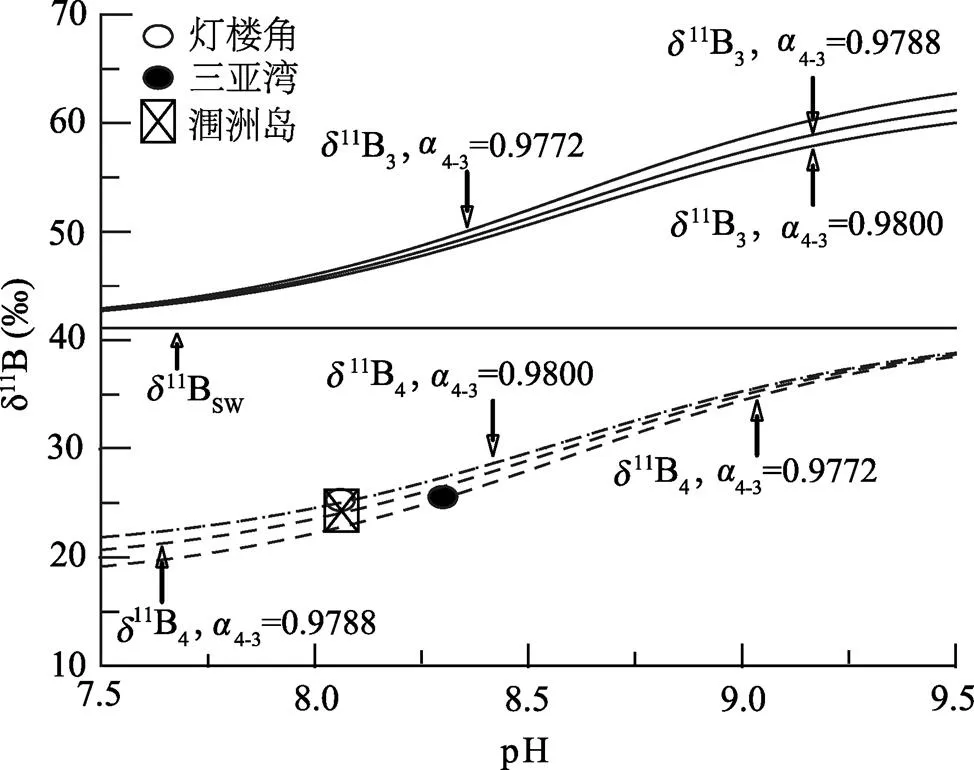
图5 珊瑚d11Bcoral和采用不同a4-3计算的原始海水B(OH)3和的硼同位素组成(d11B3和d11B4)随pH值的变化
3 结 论
(1)Ca和Sr在珊瑚中富集, 而Mg在珊瑚中贫化。
(2)珊瑚11B的变化范围为22.8‰~27.9‰, 平均为25.2‰。除与B浓度呈弱正相关关系外, 珊瑚11B与其他四种元素不相关。
(3)应用珊瑚11B恢复古海水pH值时选取同属种珊瑚和判别是否有Mg(OH)2的存在是必要的。
(4)本研究得到的新的4-3=0.9788可以用于11B-pH技术中反演古海水pH值。
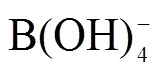
(6)今后根据无机碳酸盐沉积实验或有孔虫和珊瑚养殖实验(或者珊瑚野外观测实验)来建立一种通用的11B-pH经验方程对古海水pH值的重建是非常重要的。
[1] Ishikawa T, Nakamura E. Boron isotope systematic of marine sediments [J]. Earth Planet Sci Lett, 1993, 117(3/4): 567–580.
[2] Hemming N G, Hanson G N. Boron isotopic composition and concentration in modern marine carbonates [J]. Geochim Cosmochim Acta, 1992, 56(1): 537–543.
[3] Vengosh A. Coprecipitation and isotopic fractionation of boron in modern biogenic carbonates [J]. Geochim Cosmochim Acta, 1991, 55(10): 2901–2910.
[4] Spivack A J, You C F, Smith J. Foraminiferal boron isotopic ratios as a proxy for surface ocean pH over the past 21 Myr [J]. Nature, 1993, 363(6425): 149–151.
[5] Gaillardet J, Allègre C J. Boron isotopic compositions of coral: Seawater or diagenesis record? [J]. Earth Planet Sci Lett, 1995, 136(3/4): 665–676.
[6] Sanyal A, Hemming N G, Hanson G N, Broecker W S. Evidence for a higher pH in the glacial ocean from boron isotopes in foraminifera [J]. Nature, 1995, 373(6511): 234–236.
[7] Sanyal A, Hemming N G, Broecker W S, Hanson G N. Changes in pH in the eastern equatorial Pacific across stage 5-6 boundary based on boron isotopes in foraminifer[J]. Global Biogeochem Cycles, 1997, 11(1): 125–133.
[8] Palmer M R, Pearson P N, Cobb S J. Reconstructing past ocean pH-depth profiles [J]. Science, 1998, 282(5393): 1468–1471.
[9] Pearson P N, Palmer M R. Middle Eocene seawater pH and atmospheric carbon dioxide concentration [J]. Science, 1999, 284(5421): 1824–1826.
[10] Pearson P N, Palmer M R. Atmospheric carbon dioxide concentrations over the past 60 million years [J]. Nature, 2000, 406(6797): 695–699.
[11] Lécuyer C, Grandjean P, Reynard B, Albarède F, Telouk P.11B/10B analysis of geological materials by ICP-MS Plasma 54: Application to the boron fractionation between brachiopod calcite and seawater [J]. Chem Geol, 2002, 186(1/2): 45–55.
[12] Hönisch B, Hemming N G, Grottoli A G, Amat A, Hanson G N, Bijma J. Assessing scleratinian corals as recorders for paleo- pH: Empirical calibration and vital effects [J]. Geochim Cosmochim Acta, 2004, 68 (18): 3675–3685.
[13] 刘卫国, 彭子成, 肖应凯, 王兆荣, 聂宝符, 安芷生. 南海珊瑚礁硼同位素组成及其环境意义[J]. 地球化学, 1999, 28(6): 534–541. Liu Wei-guo, Peng Zi-cheng, Xiao Ying-kai, Wang Zhao-rong, Nie Bao-fu, An Zhi-sheng. Boron isotopic composition of corals from South China Sea and their environmental significance [J]. Geochimica, 1999, 28(6): 534–541 (in Chinese with English abstract).
[14] Hemming N G, Guilderson T P, Fairbanks R G. Seasonal variations in the boron isotopic composition of corals: A productivity signal? [J]. Global Biogeochemical Cycles, 1998, 12(4): 581–586.
[15] Sanyal A, Bijima J, Spero H, Lea D W. Empirical relationship between pH and boron isotope composition ofImplications for the boron isotope paleo-pH proxy [J]. Paleoceanography, 2001, 16(5): 515–519.
[16] Hemming N G, Reeder R J, Hanson G N. Mineral-fluid partitioning and isotopic fractionation of boron in synthetic calcium carbonate [J]. Geochim Cosmochim Acta, 1995, 59(2): 371–379.
[17] Sanyal A, Nugent M, Reeder R J, Bijima J. Seawater pH control on the boron isotopic composition of calcite: Evidence from inorganic calcite precipitation experiments [J]. Geochim Cosmochim Acta, 2000, 64(9): 1551–1555.
[18] Sanyal A, Hemming N G, Broecker W S, Lea D W, Spero H J, Hanson G N. Oceanic pH control on the boron isotopic composition of foraminifera: Evidence from culture experiments [J]. Paleoceanography, 1996, 11(5): 513–517.
[19] Palmer M R, Spivack A J, Edmond J M. Temperature and pH controls over isotopic fractionation during adsorption of boron on marine clay [J]. Geochim Cosmochim Acta, 1987, 51(9): 2319–2323.
[20] Pagani M, Lamarchand D, Spivack A, Gaillardet J. A critical evaluation of the boron isotope-pH proxy: The accuracy of ancient ocean pH estimates [J]. Geochim Cosmochim Acta, 2005, 69(4): 953–961.
[21] Klochko K, Cody G D , Tossell J A, Dera P, Kaufman A J. Re-evaluating boron speciation in biogenic calcite and aragonite using11B MAS NMR [J]. Geochim Cosmochim Acta, 2009, 73(7): 1890–1900.
[22] Xiao Y K, Li S Z, Wei H Z, Sun A D, Zhou W J, Liu W G. An unusual isotopic fractionation of boron in synthetic calcium carbonate precipitated from seawater and saline water [J].Sci China (B), 2006, 49(5): 454–465.
[23] Beck J W, Edwards L R, Ito E, Taylor F W, Recy J, Rougerie F, Joannot P, Henin C. Sea surface temperature from coral skeletal strontium/calcium ratios [J]. Science, 1992, 257(5070): 644–647.
[24] Wei G J, Sun M, Li X H, Nie B F. Mg/Ca, Sr/Ca and U/Ca ratios of a porites coral from Sanya Bay, Hainan Island, South China Sea and their relationships to sea surface temperature [J]. Palaeogeogr Palaeoclimatol Palaeoecol, 2000, 162(1/2): 59–74.
[25] 韦刚健, 余克服, 李献华, 赵建新, 孙亚莉, 孙敏, 聂宝符. 南海北部珊瑚Sr/Ca和Mg/Ca温度计及高分辨SST记录重建尝试[J]. 第四纪研究, 2004, 24(3): 325–331. Wei Gang-jian, Yu Ke-fu, Li Xian-hua, Zhao Jian-xin, Sun Ya-li, Sun Min, Nie Bao-fu. Coralline Sr/Ca and Mg/Ca thermometer for the northern South China Sea: Calibration and primary application on high-resolution SST reconstruction[J]. Quatern Sci, 2004, 24(3): 325–331 (in Chinese with English abstract).
[26] Yu K F, Zhao J X, Wei G J, Cheng X R, Chen T G, Felis T, Wang P X, Liu T S.18O, Sr/Ca and Mg/Ca records ofcorals from Leizhou Peninsula, northern South China Sea, and their applicability as paleoclimatic indicators[J]. Palaeogeogr Palaeoclimatol Palaeoecol, 2005, 218(1/2): 57–73.
[27] Alibert C, MCculloch M T. Strontium/calcium ratios in moderncorals from the Great Barrier Reef as a proxy for sea surface temperature: Calibration of the thermometer and monitoring of ENSO[J]. Paleoceanography, 1997, 12(3): 345–363.
[28] Kilbourne K H, Quinn T M, Taylor F W, Delcroix T, Gouriou Y. El Niño-Southern Oscillation-related salinity variations recorded in the skeletal geochemistry of acoral from Espiritu Santo, Vanuatu[J]. Paleoceanography, 2004, 19(4): 1029.
[29] Mitsuguchi T, Phong X D,Kitagawa H, Uchida T, Shibata Y. Coral Sr/Ca and Mg/Ca records in Con Dao Island off the Mekong Delta: Assessment of their potential for monitoring ENSO and East Asian monsoon[J]. Global Planet Change, 2008, 63(4): 341–352.
[30] Nothdurft L D, Webb G E, Buster N A, Buster N A, Holmes C W, Sorauf J E, Kloprogge J T.Brucite microbialites in living coral skeletons: Indicators of extreme microenvironments in shallow- marine settings[J]. Geology, 2005, 33(3): 169–172.
[31] Xiao J, Xiao Y K, Liu C Q, Zhao Z Q, Liang C S. Boron isotope fractionation during incorporation of boron into Mg(OH)2[J]. Chinese Sci Bull, 2009, 54(1): 3090–3100.
[32] Xiao J, Xiao Y K, Liu C Q, Jin Z D. Boron isotope fractionation during brucite deposition from artificial seawater[J]. Clim Past, 2011, 7: 693–706.
[33] 黎广钊, 梁文, 农华琼, 刘敬合. 涠洲岛珊瑚礁生态环境条件初步研究[J]. 广西科学, 2004, 11(4): 379–384. Li Guang-zhao, Liang Wen, Nong Hua-qiong, Liu Jing-he. Preliminary study on conditions of coral reef ecological environment along the coast of Weizhou Island [J]. Guangxi Sci, 2004, 11(4): 379–384 (in Chinese with English abstract).
[34] 赵焕庭, 王丽荣, 宋朝景, 余克服, 袁家义. 雷州半岛灯楼角珊瑚岸礁的特征[J]. 海洋地质与第四纪地质, 2002, 22(2): 35–40. Zhao Huan-ting, Wang Li-rong, Song Chao-jing, Yu Ke-fu, Yuan Jia-yi. Features of fringing reef at Dengloujiao, Leizhou Penisula[J]. Mar Geol Quatern Geol, 2002, 22(2): 35–40 (in Chinese with English abstract).
[35] 黄德银, 施祺, 余克服, 张叶春, 阎贫, 张乔民. 海南岛鹿回头珊瑚礁研究进展[J]. 海洋通报, 2004, 23(2): 56–64. Huang De-yin, Shi Qi, Yu Ke-fu, Zhang Ye-chun, Yan Pin, Zhang Qiao-min. Advances in the study on coral reef in region of Luhuitou, Hainan Island[J]. Mar Sci Bull, 2004, 23(2): 56–64 (in Chinese with English abstract).
[36] Xiao Y K, Beary E S, Fassett J D. An improved method for the high precision isotopic measurement of boron by thermal ionization mass spectrometry[J]. Int J Mass Spectrom Ion Proc, 1988, 85(2): 203–213.
[37] Catanzaro E J, Champion C E, Garner E L, Marinenko G, Sappenfield K M, Shield W R. Boric Acid: Isotopic and Assay Standard Reference Materials[M]. NBS Spec Publ, 1970, 260-17: 70.
[38] 李华玲, 肖应凯, 魏海珍, 杜秀月, 王秀芳, 陈玉锋. 三亚活体珊瑚的微量元素与硼同位素组成的进行初步研究[J]. 盐湖研究, 2006, 14(2): 35–41. Li Hua-ling, Xiao Ying-kai, Wei Hai-zhen, Du Xiu-yue, Wang Xiu-fang, Chen Yu-feng. Preliminary study for trace element and isotopic compositions of boron in growing corals from Sanya Bay, China [J]. J Salt Lake Res, 2006, 14(2): 35–41 (in Chinese with English abstract).
[39] Dickson A G. Thermodynamics of dissociation of boric acid in synthetic seawater from 273.15 to 318.15 K [J]. Deep Sea Res, 1990, 37(5): 755–766.
[40] Klochko K, Kaufman A J, Yao W S, Byrne R H, Tossell J A. Experimental measurements of boron isotope fractionation in seawater[J]. Earth Planet Sci Lett, 2006, 248(1/2): 276–285.
[41] Rollion-Bard C, Blamart D, Trebosc J, Tricot G, Mussi A, Cuif J P. Boron isotopes as pH proxy: A new look at boron speciation in deep-sea corals using11B MAS NMR and EELS [J]. Geochim Cosmochim Acta, 2011, 75(4): 1003–1012.
[42] Kakihana H, Kotaka M, Satoh S. Fundamental studies on the ion-exchange separation of boron isotopes [J]. Bull Chem Soc Japan, 1977, 50(1): 158–163.
[43] Xiao Y K, Li H L, Liu W G, Wang X F, Jiang S Y. Boron isotopic fractionation in laboratory inorganic carbonate precipitation: Evidence for the incorporation of B(OH)3into carbonate [J]. Sci China (D), 2008, 51(12): 1776–1785.
XIAO Jun1, XIAO Ying-kai2*, JIN Zhang-dong1, LIU Cong-qiang3and HE Mao-yong1
1. State Key Laboratory of Loess and Quaternary Geology, Institute of Earth Environment, Chinese Academy of Sciences, Xi’an 710075, China; 2. CAS Key Laboratory of Salt Lake Resources and Chemistry, Qinghai Institute of Salk Lakes, Chinese Academy of Sciences, Xining 810008, China;3. State Key Laboratory of Environmental Geochemistry, Institute of Geochemistry, Chinese Academy of Sciences, Guiyang 550002, China
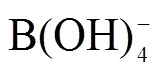
living coral; trace element; boron isotope;11B-pH proxy
P597
A
0379-1726(2012)05-0401-10
2012-02-08;
2012-04-28;
2012-05-16
国家自然科学基金(40776071, 41003012); 中国科学院“西部博士”项目
肖军(1980–), 男, 助理研究员, 同位素地球化学专业。E-mail: xiaojun@ieecas.cn
XIAO Ying-kai, E-mail: xiaoyk@isl.ac.cn; Tel: +86-971-6301684
