盐酸体系中二氧化锰浸出方铅矿的研究
2012-06-22湛雪辉李朝辉湛含辉李飞曹芬李侠周随安
湛雪辉,李朝辉,湛含辉,李飞,曹芬,李侠,周随安
(1. 长沙理工大学 化学与生物工程学院,湖南 长沙,410076;2. 中国矿业大学 环境与测绘学院,江苏 徐州,221116)
铅金属大部分来源于方铅矿,其提取方法主要有火法和湿法2种工艺[1]。火法炼铅可分为熔炼-鼓风炉还原熔炼[2]和直接熔炼 2种方法,产物是金属铅,具有技术成熟、生产能力强等优点,其缺点是劳动强度大,能耗高,产生的二氧化硫和含铅烟尘对环境的污染严重[3]。湿法炼铅[4]是近年来的研究热点之一,主要产物是铅盐,可避免二氧化硫及含铅烟尘的产生,对低品位及复杂铅精矿也有较强的适应性,根据氧化剂的不同,有三价铁法[5]、酸浸法[6]和通氯气浸出法[7];根据非氧化性介质浸出,有碱性介质[8]或硅氟酸介质[9]中的碳酸铵浸出法[10]和酸转化法[11]。然而,由于原料、设备和生产成本的限制,上述湿法炼铅的方法在工业上应用价值不大。近年来,一些研究者采取两矿法提取有色金属[12-13]。徐本军等[14]研究了两矿法浸出方铅矿的工艺研究,但是,想要实现其工业化应用,还需要对其进行更深入更系统的研究。在此,本文作者为避免软锰矿中其他成分对反应结果的影响,以二氧化锰代替软锰矿在盐酸体系中浸出方铅矿,对其浸出工艺进行研究,以期为两矿法浸出铅的工业化应用提供依据。
1 实验
1.1 实验原料和仪置
主要实验原料为方铅矿精矿,取自湖南郴州宜章矿,平均粒径小于0.074 μm,其主要成分如表1所示。实验用二氧化锰、35%盐酸以及氯化钠均为化学纯。
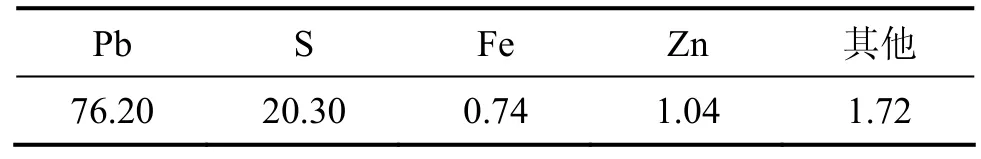
表1 方铅矿精矿中主要成分Table 1 Main chemical compositions of galena concentrate%
实验仪置主要包括反应釜、恒温加热器(DF-101S)、电子恒温搅拌机(JHS-1/90)、精密pH计(PHS-3C)、循环水式真空泵(SHB-Ⅲ)、高温抽滤设备和干燥箱等。
1.2 实验过程及原理
反应在500 mL反应釜中进行,用恒温加热器控制温度。在反应釜中加入一定体积的盐酸溶液后,按一定的总液体与总固体质量比同时加入一定比例的方铅矿、氯化钠和二氧化锰,然后,密封、搅拌,并升温到所需的反应温度。当反应完成后,高温抽滤去除浸出渣,滤液经降温沉淀、抽滤,得氯化铅固体。
浸出过程中涉及的主要反应如方程式为:
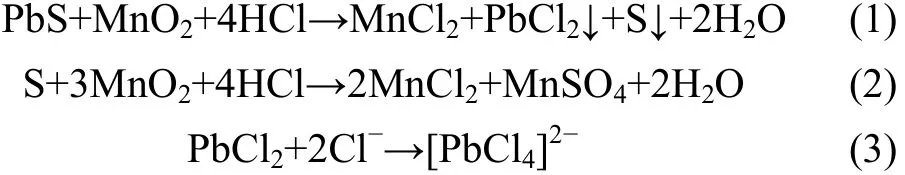
方铅矿、二氧化锰和盐酸反应生成锰盐、氯化铅和硫,其中硫可能被深度氧化成硫酸盐,而氯化铅与氯离子在较高温度时会生成易溶入水的络合物[PbCl4]2-。反应完成后,经过高温过滤可得到含锰盐和络合物[PbCl4]2-的溶液,而[PbCl4]2-在低温时会不断转化成PbCl2晶体析出[15],由此可得产物氯化铅。
将整个实验过程视为一个整体,认为只有得到的产品中的铅才算是从方铅矿中成功浸出来的,则铅的浸出率可按下式进行计算:
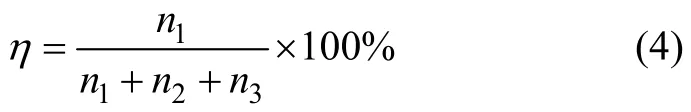
式中:η为铅的浸出率,%;n1为氯化铅的物质的量,mol;n2为滤渣中铅的物质的量,mol;n3为滤液中铅的物质的量,mol。
2 结果与讨论
2.1 操作条件对浸出率的影响
浸出过程在反应釜中进行。任何影响反应的因素都将改变最终铅的浸出率,为此,采用单因素条件优化法考察各种操作条件(包括搅拌速度、反应体系中总的液体与固体的质量比m总液:m总固、二氧化锰与方铅矿精矿的质量比m二氧化锰:m方铅矿、反应时间、反应温度、盐酸浓度、氯化钠浓度)对方铅矿精矿铅浸出率的影响,以期获得最佳的操作参数。
2.1.1 搅拌速度的影响
在 m总液:m总固=7,m二氧化锰:m方铅矿=1 以及反应时间为60 min,反应温度为60 ℃,盐酸浓度为1 mol/L,氯化钠质量浓度为250 g/L等反应条件下,考察搅拌速度对铅浸出率的影响,结果如图1所示。从图1可见:随着搅拌速率的增加,方铅矿中铅浸出率先迅速上升,然后基本保持不变。外扩散对多相催化反应的反应速率有很大的影响,对于此过程,生成的单质S和PbCl2可能会吸附在方铅矿颗粒的外表面,阻碍反应进一步进行,加快搅拌速率能使单质S和PbCl2迅速剥离而进入溶液;同时,加大氧化锰与方铅矿颗粒的碰撞反应概率;当搅拌速率大于500 r/min时,外扩散影响已基本消除,因此,合适的搅拌速率为500 r/min。
2.1.2 m总液:m总固的影响

图1 搅拌速率对铅浸出率的影响Fig.1 Effect of stirring rate on leaching rate of lead
在搅拌速率为 500 r/min,m二氧化锰:m方铅矿=1,反应时间为 60 min,反应温度为 60 ℃,盐酸浓度为 1 mol/L,氯化钠质量浓度为250 g/L等反应条件下,考察m总液:m总固的变化对铅浸出率的影响,结果如图2所示。从图2可见:随着m总液:m总固的增大,铅浸出率先迅速增大,达到最大值后再降低。其原因可能是该反应为固-液-固多相反应,在固定条件下,随着m总液: m总固的提高,体系的湍流程度提高,固体颗粒在相同时间内能接触到更多的反应液体,传质速率增加,反应效果提高;然而,当m总液:m总固大于10时,体系中固体颗粒碰撞的概率降低,导致铅浸出率降低。经综合考虑,液固比选10为宜。

图2 m总液:m总固对铅浸出率的影响Fig.2 Effect of mtotal liquid:mtotal solid on leaching rate of lead
2.1.3 m二氧化锰:m方铅矿的影响
在搅拌速率为500 r/min,m总液:m总固= 10,反应时间为 60 min,反应温度为 60 ℃,盐酸浓度为 1 mol/L,氯化钠质量浓度为250 g/L等反应条件下,考察m二氧化锰:m方铅矿的变化对铅浸出率的影响,结果如图3所示。从图3可见:随着m二氧化锰:m方铅矿的增大,铅浸出率先增大,然后基本保持不变。其原因是二氧化锰在反应体系作为氧化剂,将方铅矿中的硫元素转换为单质S,当二氧化锰的量过多时,会将单质S进一步氧化为硫酸盐。比较硫酸铅和氯化铅的溶度积发现会优先生成氯化铅,由于反应在盐酸体系中进行,且加入了氯化钠,体系中生成硫酸铅的概率很小,因此,本实验合适的 m二氧化锰:m方铅矿为 1.3。
2.1.4 反应时间的影响
在搅拌速率为 500 r/min,m总液:m总固=10,m二氧化锰:m方铅矿=1.3,反应温度为60 ℃,盐酸浓度为1 mol/L,氯化钠质量浓度为250 g/L等反应条件下,考察反应时间对铅浸出率的影响,结果如图4所示。从图4可见:随着反应时间的增加,铅浸出率先迅速增大,后缓慢增加,最后保持不变。说明在此反应条件下,过多地延长反应时间对提高铅浸出率没有效果。其可能的原因是反应体系中的盐酸浓度随着反应时间的延长而逐渐下降,导致反应速率也逐渐下降,铅浸出率恒定。经综合考虑,选反应时间为60 min。

图3 m二氧化锰:m方铅矿对铅浸出率的影响Fig.3 Effect of mmanganese dioxide:mgalena concentrate on leaching rate of lead
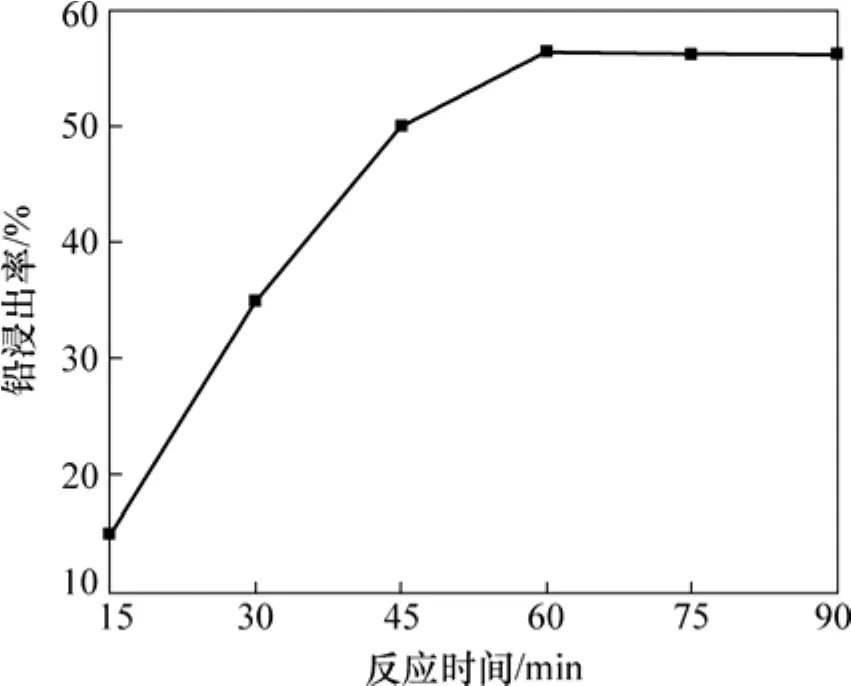
图4 反应时间对铅浸出率的影响Fig.4 Effect of reaction time on leaching rate of lead
2.1.5 反应温度的影响
在搅拌速率为 500 r/min,m总液:m总固=10,m二氧化锰:m方铅矿=1.3,反应时间为60 min,盐酸浓度为1 mol/L,氯化钠质量浓度为250 g/L等反应条件下,考察反应温度对铅浸出率的影响,结果如图5所示。从图5可见:随着反应温度的升高,铅的浸出率不断增大,最后趋于稳定。当温度升高时,分子的布朗运动逐渐加剧,反应速率随之增加[16],铅的浸出率增加,稳定后的铅浸出率也比图4中相应的值高。由此可见:温度是影响铅浸出率的重要因素。对于此反应体系,选择浸出温度为80 ℃。

图5 反应温度对铅浸出率的影响Fig.5 Effect of temperature on leaching rate of lead
2.1.6 盐酸浓度的影响
在搅拌速率为 500 r/min,m总液:m总固=10,m二氧化锰:m方铅矿=1.3,反应时间为60 min,反应温度为80 ℃,氯化钠质量浓度为250 g/L等反应条件下,考察盐酸浓度对铅浸出率的影响,结果如图6所示。从图6可见:随着盐酸浓度的升高,铅的浸出率不断增大,后基本保持不变。在此反应体系中,盐酸作为酸性反应介质,推动反应式(1)向正方向进行,其浓度的增加有利于铅浸出率的增加;当其浓度达3 mol/L时,铅浸出率达 99.5%,再提高盐酸浓度,铅浸出率不增加。因此,合适的盐酸浓度为3 mol/L。
2.1.7 氯化钠质量浓度的影响

图6 盐酸浓度对铅浸出率的影响Fig.6 Effect of concentration of hydrochloric acid on leaching rate of lead
在搅拌速率为 500 r/min,m总液:m总固=10,m二氧化锰:m方铅矿=1.3,反应时间为60 min,反应温度为80 ℃,盐酸浓度为3 mol/L等反应条件下,考察氯化钠质量浓度对铅浸出率的影响,结果如图7所示。从图7可见:随着氯化钠质量浓度的增大,铅的浸出率先不断增大,后基本保持不变。其原因是氯化钠在反应体系中提供氯离子,在较高温时与氯化铅反应生成溶于水的络合物[PbCl4]2-,如反应(3)所示;当氯化钠质量浓度达250 g/L时,提供的氯离子已足够,同时铅的浸出率也达到最大值 99.5%。因此,选择氯化钠质量浓度为250 g/L。

图7 氯化钠的质量浓度对铅浸出率的影响Fig.7 Effect of mass concentration of sodium chloride on leaching rate of lead
2.2 产品检测
对上述最优反应条件下制备得到的 PbCl2产物进行XRD分析,结果如图8所示。从图8可见:其衍射数据与JCPDS卡数据吻合较好,无杂质峰,表明此产物纯度很高。
将产物进行元素分析,其中主要的元素含量如表2所示。从表2可见:产物PbCl2的纯度在99.6%以上。
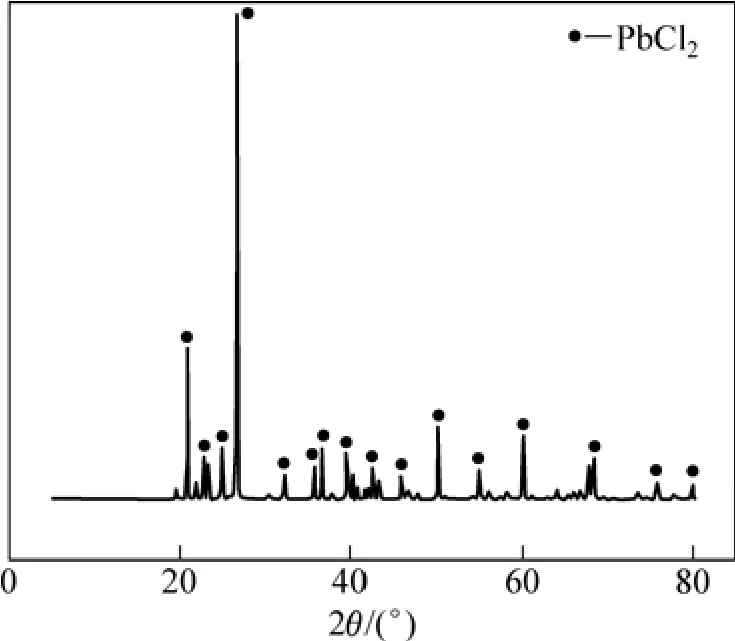
图8 氯化铅的XRD图谱Fig.8 XRD pattern of PbCl2

表2 氯化铅固体的元素成分分析(质量分数)Table 2 Element contents of lead chloride %
3 结论
(1) 通过单因素条件优化法,得到了盐酸体系中二氧化锰浸出方铅矿的最佳操作参数:搅拌速率为500 r/min,m总液:m总固=10,m二氧化锰:m方铅矿=1.3,反应时间为60 min,反应温度为80℃,盐酸浓度为3 mol/L,氯化钠质量浓度为250 g/L。
(2) 在最佳操作参数下,铅的浸出率在 99.5%以上,氯化铅产物纯度在99.6%以上。
[1] 胡全红, 许民. 三氯化铁浸出铅精矿研究[J]. 江西化工,2001(4): 30-33.HU Quan-hong, XU Min. Technical study on leaching galena concentration by ferric chloride[J]. Jiangxi Chemical, 2001(4):30-33.
[2] 蒋爱华, 杨双欢, 梅炽, 等. SKS炼铅氧气底吹炉的火用分析[J].中南大学学报: 自然科学版, 2010, 41(3): 1190-1195.JIANG Ai-hua, YANG Shuang-huan, MEI Chi, et al. Exergy analysis of oxygen bottom blown furnace in SKS lead smelting system[J]. Journal of Central South University: Science and Technology, 2010, 41(3): 1190-1195.
[3] 徐爱明, 宗复. 传统法炼铅技改方案的探讨[J]. 有色金属: 冶炼部分, 1997(1): 2-6.XU Ai-ming, ZONG Fu. A new scheme of technical modification about the tradition Pb-smelting[J]. Nonferrous Metals: Extractive Metallurgy, 1997(1): 2-6.
[4] 胡全红, 许民. 铅精矿全湿法工艺研究[J]. 有色金属: 冶炼部分, 2003(2): 5-7.HU Quan-hong, XU Min. Study on technical hydrometallurgy lead concentration[J]. Nonferrous Metals: Extractive Metallurgy,2003(2): 5-7.
[5] Balǎž P, Achimovičová M. Mechano-chemical leaching in hydrometallurgy of complex sulphides[J]. Hydrometallurgy,2006, 84(1/2): 60-68.
[6] Irma C, Mercedes T O, Ignacio G. An electrochemical study of galena concentrate in perchlorate medium at pH 2.0: The influence of chloride ions[J]. Electrochimica Acta, 2000, 45(17):2729-2741.
[7] 陈家越. 方铅矿湿法冶金探索[J]. 宁德师专学报: 自然科学版, 2000, 12(1): 47-49.CHEN Jia-yue. Exploration of galena hydrometallurgy[J].Journal of Ningde Teachers College: Natural Science, 2000,12(1): 47-49.
[8] 俞小花. 复杂铜、铅、锌、银多金属硫化精矿综合回收利用研究[D]. 昆明: 昆明理工大学材料与冶金学院, 2008: 14-34.YU Xiao-hua. Synthetic recovery of complexpolymetalli sulfide concentrate containing copper, lead, zinc and silver[D].Kunming: Kunming University of Science and Technology.School of Materials and Metallurgy, 2008: 14-34.
[9] 王俊中. 方铅矿及脆硫铅锑矿浸出新工艺研究[D]. 昆明: 昆理工大学材料与冶金学院, 2001: 22-67.WANG Jun-zhong. A study on new leaching process of Galena or Jamesonite concentrate[D]. Kunming: Kunming University of Science and Technology. School of Materials and Metallurgy,2001: 22-67.
[10] Lu K Y, Chen C Y. Conversion of galena to lead carbonate in ammonium carbonate solution: A new approach to lead hydrometallurgy[J]. Hydrometallurgy, 1986, 17(l): 73-83.
[11] 王淑萍, 王瑞芬. 硫化铅与盐酸的作用[J]. 石家庄大学学报,2000, 12(1): 36-37.WANG Shu-ping, WANG Rui-fen. Interaction of lead sulfide and hydrochloric acid[J]. Journal of Shijiazhang College, 2000,12(1): 36-37.
[12] 袁明亮, 梅贤功, 陈荩, 等. 两矿法浸出软锰矿的工艺与理论[J]. 中南工业大学学报: 自然科学版, 1997, 28(4): 329-332.YUAN Ming-liang, MEI Xian-gong, CHEN Jin, et al. Technique and theory of two ore method to leach manganese dioxide ore[J].Journal of Central South University of Technology: Natural Science, 1997, 28(4): 329-332.
[13] 卢宗柳, 都安治. 两矿法浸出氧化锰矿的几个工艺问题[J].中国锰业, 2006, 24(1): 39-42.LU Zong-liu, DU An-zhi. Some technical problems on soaking methods of MnO ore[J]. China’s Manganese Industry, 2006,24(1): 39-42.
[14] 徐本军,覃文庆,邱冠周.方铅矿和软锰矿两矿法浸出工艺的研究[J]. 矿产保护与利用, 2005(3): 29-34.XU Ben-jun, QIN Wen-qing, QIU Guan-zhou. Study on simultaneously leaching of pyrolusite and flotation galena concentrate[J]. Conservation and Utilization of Mineral Resources, 2005(3): 29-34.
[15] Holdich R G, Lawson G J. The solubility of aqueous lead chloride solutions[J]. Hydrometallurgy, 1987, 19(2): 199-208.
[16] LI Zhao-hui, CHEN Ri-zhi, XING Wei-hong, et al. Continuous acetone ammoximation over TS-1 in a tubular membrane reactor[J]. Industrial & Engineering Chemistry Research, 2010,49(14): 6309-6316.
