快淬Mg2Ni型合金的结构及贮氢动力学
2012-11-29张羊换张国芳李霞侯忠辉任慧平赵栋梁
张羊换,张国芳,李霞,侯忠辉,任慧平,赵栋梁
(1.钢铁研究总院功能材料研究所,北京,100081;2.内蒙古科技大学 省部共建国家重点实验室培育基地,内蒙古 包头,014010)
Mg及 Mg基合金由于具有高的贮氢能力和低的制备成本而被认为是最具应用前景的贮氢材料[1]。然而,由于这些材料的氢化物具有很高的热稳定性,导致其吸放氢动力学性能极差,从而极大地限制了这些材料的实际应用。因此,寻求改善Mg基贮氢材料吸放氢动力学的方法成为本领域研究者面临的主要挑战。各种方法,特别是机械合金化(MA)[2],熔体快淬[3]以及多元合金化[4]已经被用来改善合金的吸放氢性能。Yu等[5]用机械合金化制备Mg基合金,发现在压力为2 MPa、温度为200 ℃,合金在60 s内的最大吸氢量可达5.5% H。 Janot等[6]用机械球磨法对Mg2Ni进行表面改性,证明可以显著改善其放氢动力学。Kohno等[7]在Mg2Ni合金中加入Ni粉,通过机械球磨法进行表面改性,获得最大放电容量为750 mA·h/g。高能球磨是一种制备纳米晶/非晶Mg及Mg基合金非常有效的方法。然而,球磨Mg及Mg基合金的吸放氢循环稳定性很差,主要是由于球磨形成的亚稳态结构在多次吸放氢循环的过程中逐渐消失[8]。与球磨相比,熔体快淬是获得纳米晶/非晶结构的有效方法,并非常适合于批量化制备纳米晶/非晶Mg基合金。已经证实,快淬纳米晶/非晶Mg基合金在室温下具有优良的吸放氢性能,可与球磨制备的非晶合金的性能匹敌。Huang等[9]用快淬技术制备了非晶(Mg60Ni25)90Nd10合金,其最大吸氢量为 4.2%。Tanaka等[10]用快淬技术制备了纳米晶和非晶 Mg–Ni–RE (RE=La,Nd)合金,发现合金具有优良的吸氢动力学性能。Spassov和Köster[11]用熔体快淬技术制备了 Mg2(Ni,Y)型Mg63Ni30Y7贮氢合金,合金的最大吸氢量约为3.0%。Yamaura等[12]在 Mg-Ni基合金中添加第三组元 Pd,La和Ca等元素,用快淬的方法能获得非晶结构。因此,在本研究中La元素被作为第三组元加入到Mg2Ni型合金中,以便用快淬的方法获得非晶结构。本文作者用快淬技术制备Mg2−xLaxNi(x=0~0.6)合金,并研究La替代及快淬处理对合金结构及贮氢动力学的影响。
1 实验
试验合金的成分为 Mg2−xLaxNi(x=0,0.2,0.4,0.6),对应La的含量,合金编号为La0,La0.2,La0.4和La0.6。试验合金用1 kg真空中频感应电炉熔炼。将母合金重熔后,进行单辊快淬处理。淬速以铜辊表面线速度表示,本试验的淬速为15,20,25和30 m/s。
用 XRD(D/max/2400)分析合金的相结构;用SEM(Philips QUANTA 400)观察铸态合金的形貌,并用EDS分析微区成分。将快淬合金薄带用离子减薄法制备成薄膜样品,用 HRTEM(JEM−2100F)观察其形貌,并用电子衍射(ED)分析合金的晶态。
用自动控制的 Sieverts设备测试合金的吸放氢动力学,测试前,将合金先进行几次吸放氢循环,以使其完全活化。吸氢的初始氢压为1.5 MPa,放氢的初始压力为100 Pa,吸放氢过程均在200 ℃进行。
快淬态合金薄带经机械破碎后与镍粉以质量比1:4充分混合,在35 MPa压力下制成直径为15 mm的试验用电极片。用三电极模拟电池系统测试合金的电化学贮氢动力学。合金电极以恒定的电流密度充电,间隔 15 min后,以相同的电流密度放电至截止电压−0.500 V。测试环境温度保持在30 ℃。
用电化学工作站(PARSTAT 2273)测试合金的电化学交流阻抗谱(EIS),测试在50%放电深度DOD,频率范围为5.0 mHz~10 kHz,电位扰动幅度为5 mV。在电极满充状态测定500 mV电位阶跃后的阳极电流−时间响应曲线,持续时间为3 600 s。
2 结果与讨论
2.1 微观结构
铸态及快淬态 Mg2−xLaxNi(x=0~0.6)合金的 XRD衍射谱如图1所示,从图1(a)可以看出:快淬La0合金具有明显的晶态结构,而快淬 La替代合金具有明显非晶化倾向,表明La替代Mg可以提高Mg2Ni型合金的非晶形成能力。比较图1(a)及(b)可以看出:La0合金的主相为Mg2Ni型相,当x达到0.4时,铸态合金的主相转变为(La,Mg)Ni3+LaMg3相。从图1(a)可以看出:快淬态合金的非晶峰对应的衍射角2θ随La含量的增加而明显向左偏移,当La含量x=0.2,0.4和0.6时,非晶峰对应的衍射角 2θ分别为 39.9°,36.2°和35.2°。这进一步说明随x的增加,合金的主相发生了改变。
铸态La0和La0.4合金的SEM形貌如图2所示。从图2可以看出:La0合金为单相Mg2Ni组织,其形貌具有典型的粗大枝晶状特点。La替代导致合金的形貌发生显著变化,La0.4合金的形貌与 La0合金完全不同,具有明显的多相组织特征。EDS结合XRD分析可以判断合金的主相为(La,Mg)Ni3+LaMg3相。
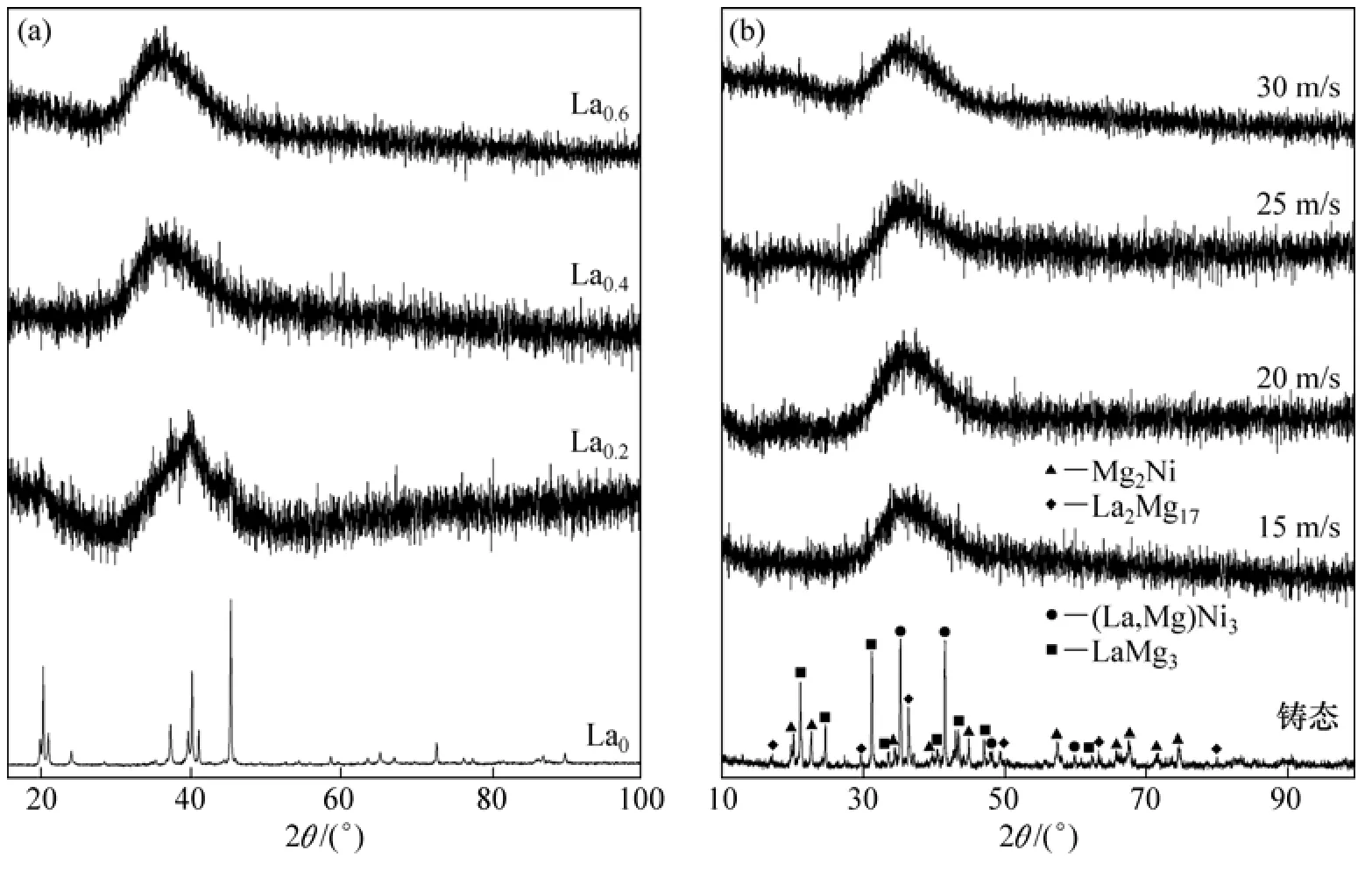
图1 铸态及快淬态合金的XRD衍射谱Fig.1 XRD profiles of as-cast and spun alloys

图2 铸态合金的SEM形貌Fig.2 SEM images of as-cast alloys
用HRTEM观察了15 m/s快淬Mg2xLaxNi(x=0~0.6)合金的形貌,如图3所示。从图3可以看出:La0具有典型的纳米晶结构,其ED衍射环也显示了晶体结构。合金的晶粒粒径在 20~30 nm之间,这与Friedlmeier等[13]报道的结果基本一致。而其余快淬态合金均显示了非晶化趋势,其ED衍射环明显宽化,证实了非晶相的存在。La替代Mg提高合金非晶形成能力主要归因于2个方面:首先,在Mg–Ni 或 Mg–Cu合金中添加第三组元能极大地提高其非晶形成能力[14];其次,合金的非晶形成能力与原子半径差密切相关,原子半径差越大,非晶形成能力越强[15]。La原子半径远大于Mg原子半径,所以,La替代Mg必然增加合金的非晶形成能力。
2.2 气态吸放氢动力学
合金的吸氢动力学用吸氢饱和度()来表示。吸氢饱和度被定义为给定时间的吸氢量与饱和吸氢量之比,计算公式为:×100%。其中:Ca和100分别为吸氢时间为100 min和时间t时的吸氢量。实验结果表明:所有合金的均大于其饱和吸氢量的95%。因此,将近似地作为合金的饱和吸氢量是合理的。显然,对于给定的时间t,越大,合金的吸氢动力学越好。类似地,用放氢率来评价合金的放氢动力学,以表示。放氢率被定义为给定时间的放氢量与饱和吸氢量的比,其计算公式为:
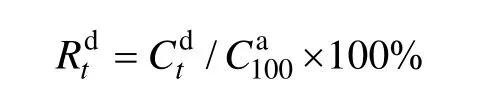

图3 快淬态(15 m/s)合金的HRTEM形貌及电子衍射花样Fig.3 HRTEM micrographs and ED patterns of as-spun (15 m/s)alloys
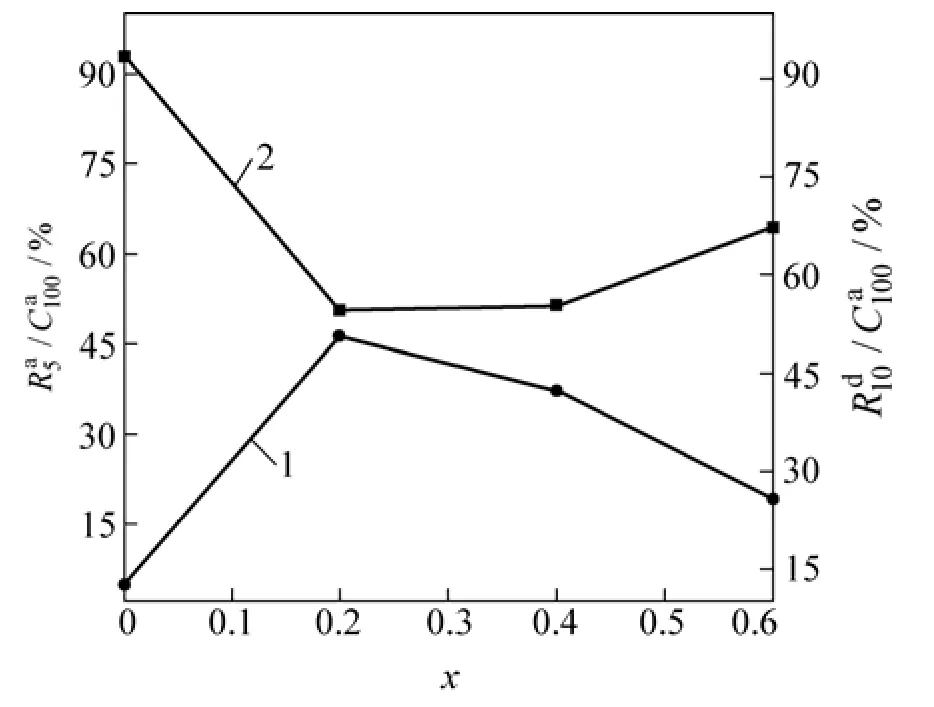
图4 15 m/s快淬合金的和与La含量x的关系Fig.4 Evolution of and values of as-spun (15 m/s)alloy with La content
图5所示为La0.4合金的(t=5)和(t=10)与淬速的关系。可以看出:随淬速的增加先降低后增加,而随淬速的增加而增加;当淬速从0 m/s(铸态被定义为淬速 0 m/s)增加到30 m/s时,La0.4合金的从81.9%下降到39%,然后增加到85.6%,从42.6%增大到58.6%。
氢在合金中的扩散能力是影响合金气态吸放氢动力学性能的重要因素,为了揭示La替代Mg及快淬对Mg2Ni型合金气态吸放氢动力学影响的机理,探究La替代及快淬处理对氢在合金中扩散能力的影响显然是非常必要的。图6所示为满充状态下,铸态及快淬态合金电极在+500 mV电位阶跃后的阳极电流−时间的响应曲线。氢在合金中的扩散系数可由式(1)和(2)计算[18]:
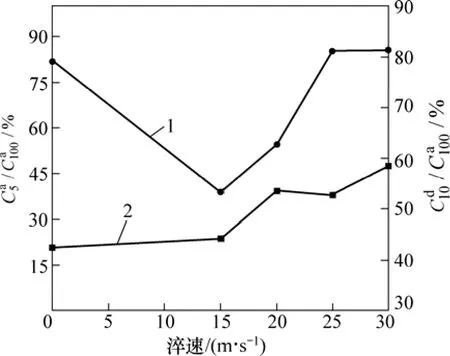
图5 La0.4合金的,值与淬速的关系Fig.5 Evolution of and values of La0.4 alloy with spinning rate

式中:i为扩散电流密度(mA/g);a为合金颗粒半径(cm);d为贮氢合金密度(g/cm3);F为法拉第常数;D为氢扩散系数(cm2/s);c0为合金电极中的初始氢浓度(mol/cm3);cs为合金颗粒表面的氢浓度(mol/cm3);t为放电时间。根据式(2)计算的氢扩散系数被列入图6。从图6(a)可以清楚地看到:15 m/s快淬态合金的扩散系数随 La含量的增加先降低后增加。图6(b)表明:La0.4合金的扩散系数随淬速的增加先减小后增加。合金的吸氢动力学随 La含量及淬速的变化与其扩散系数的变化趋势基本一致,说明氢在合金中的扩散是气态吸氢动力学的主要控制因素。
2.3 电化学贮氢动力学
合金的电化学动力学用其高倍率放电能力(DHR)来表征,其计算方法为:DHR=Ci,max/C20,max×100%。其中:Ci,max和C20,max分别为放电电流密度分别为i和20 mA/g时合金的最大放电容量。铸态及快淬态合金放电电流密度与时间的关系如图7所示。从图7可以看出:15 m/s快淬La0.4合金的高倍率放电性能优于其他合金的性能,但快淬对La0.4合金的高倍率放电能力影响比较复杂。为了清楚地显示La含量x及淬速与合金DHR的关系,图7所示为合金的高倍率放大能力DHR(i=90 mA/g)与La含量x及淬速的关系。从图7可以看出:DHR随x及淬速的变化均先增加后减少。比较图4,5和7可以看出:合金的气态及电化学贮氢动力学随La含量x及淬速的变化是不同的,这说明合金的电化学贮氢动力学与气态贮氢动力学具有不同的控制因素。

图6 铸态及快淬态合金在满充状态下的阳极电流与时间响应半对数曲线Fig.6 Semilogarithmic curves of anodic current vs time responses of alloys
合金的高倍率放电能力(HRD)象征着合金电化学吸放氢动力学性能,主要取决于合金与电解液界面的电荷转移及氢从合金电极内部到电极表面的扩散能力[19]。而合金与电解液界面的电荷转移由合金电极表面的电化学反应阻抗来表征。
图8所示为铸态及快淬态合金电极的电化学阻抗谱(EIS)。从图8可以看出:阻抗谱由2段半圆弧和1段斜线组成。根据 Kuriyama模型[20],高频区的半圆弧反映合金与集流体之间的接触电阻,低频区的半圆弧反映合金电极表面的电化学反应阻抗,主要与合金表面的电化学活性及氢的扩散相关;15 m/s快淬态合金的大圆弧半径随x的增大先减小后增大,La0.6合金具有最大的电化学反应阻抗,这与图7(a)的变化趋势一致。La0.4合金的大圆弧半径随淬速的增加先降低后增加,这种变化的趋势与图7(b)所示的基本一致,上述结果说明电极表面的电荷转移是合金电化学贮氢动力学的主要控制因素。

图7 合金的高倍率放电能力DHR与放电电流密度的关系Fig.7 Evolution of high rate discharge ability DHR of alloys with discharge current density
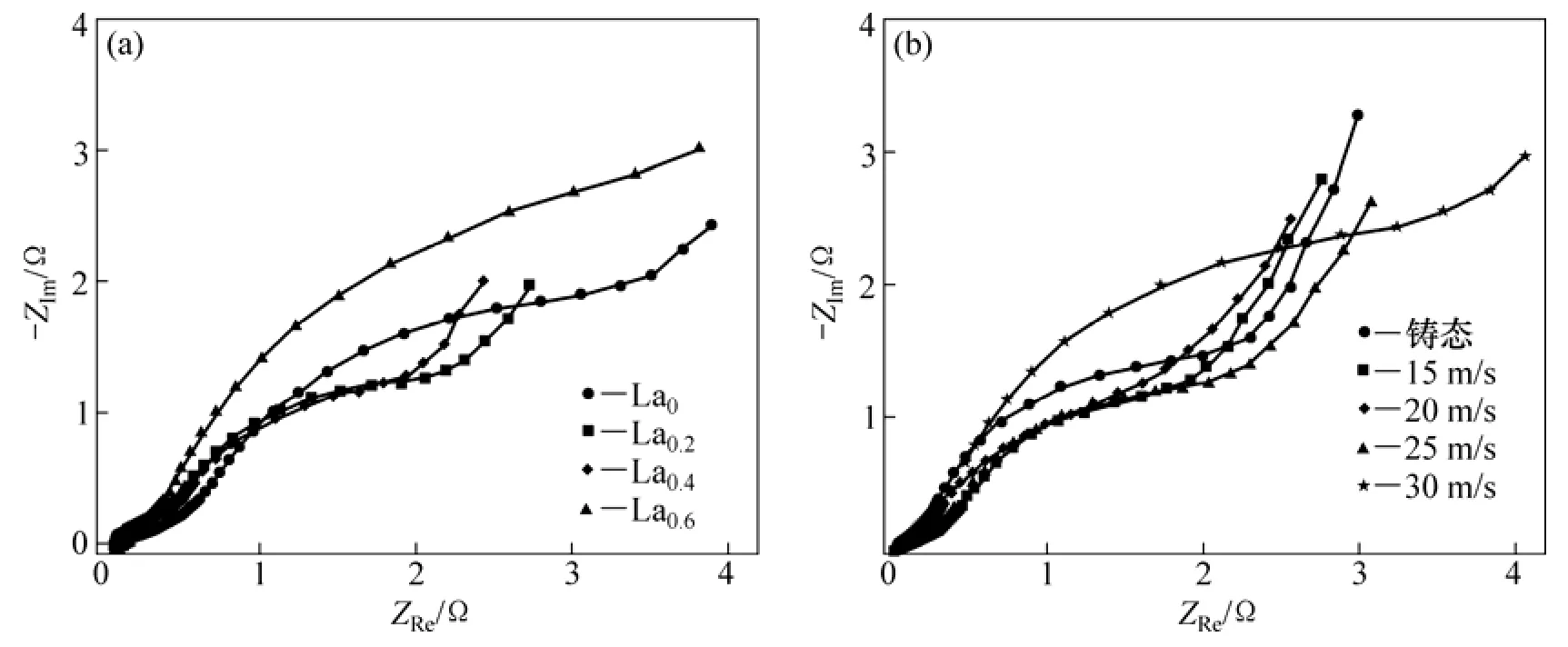
图8 在50%(DOD)放电深度下合金的交流阻抗谱Fig.8 Electrochemical impedance spectra (EIS)of alloy electrodes at 50% depth of discharge (DOD)
3 结论
(1)快淬 La0合金具有典型的纳米晶结构,快淬La替代合金中出现明显的非晶相,证实La替代Mg可提高 Mg2Ni型合金的非晶形成能力。La替代 Mg使 Mg2−xLaxNi(x=0~0.6)合金的相组成发生显著变化。当 La含量x≥0.4时,La替代 Mg使合金的主相由Mg2Ni相转变为(La,Mg)Ni3+LaMg3相。
(2)La替代Mg导致快淬Mg2Ni型合金的吸氢动力学性能下降,但适量的La替代(x≤0.4)可以显著提高合金的放氢动力学。快淬态合金的DHR随x增加先增加后降低,当淬速为15 m/s时,La0.4合金具有最佳的电化学贮氢动力学性能。
(3)La0.4合金的气态吸氢动力学随淬速的变化先降低后增加,但其放氢动力学随淬速的增加而增加。此外,La0.4合金的DHR随淬速的增加先增加后降低,导致这一不同变化趋势的主要原因是合金的气态及电化学贮氢动力学具有不同的控制因素。
[1]Jain I P,Lal C,Jain A.Hydrogen storage in Mg: A most promising material[J].International Journal of Hydrogen Energy,2010,35(10): 5133−5144.
[2]Woo J H,Lee K S.Electrode characteristics of nanostructured Mg2Ni-type alloys prepared by mechanical alloying[J].J Electrochemical Society,1999,146(3): 819−823.
[3]Palade P,Sartori S,Maddanena A,et al.Hydrogen storage in Mg-Ni-Fe compounds prepared by melt spinning and ball milling[J].Journal of Alloys and Compounds,2006,415(1/2):170−176.
[4]LIU Yong-ning,ZHANG Xian-ji.Effect of lanthanum additions on electrode properties of Mg2Ni[J].Journal of Alloys and Compounds,1998,267(1/2): 231−234.
[5]YU Zhen-xing,LIU Zu-yan,WANG Er-de.Hydrogen storage properties of nanocomposite Mg-Ni-Cu-CrCl3prepared by mechanical alloying[J].Materials Science and Engineering: A,2002,335(1/2): 43−48.
[6]Janot R,Darok X,Rougier A,et al.Hydrogen sorption properties for surface treated MgH2and Mg2Ni alloys[J].Journal of Alloys and Compounds,2005,404/405/406: 293−296.
[7]Kohno T,Kanda M.Effect of partial substitution on hydrogen storage properties of Mg2Ni alloy[J].Journal of the Electrochemical Society,1997,144(7): 2384−2388.
[8]Nohara S,Fujita N,ZHANG Shu-guo,et al.Electrochemical characteristics of a homogeneous amorphous alloy prepared by ball milling Mg2Ni with Ni[J].Journal of Alloys and Compounds,1998,267(1/2): 76−78.
[9]HUANG Lin-jun,LIANG Gong-ying,SUN Zhan-bo,et al.Electrode properties of melt-spun Mg-Ni-Nd amorphous alloys[J].Journal of Power Sources,2006,160(1): 684−687.
[10]Tanaka K,Kanda Y,Furuhashi M,et al.Improvement of hydrogen storage properties of melt-spun Mg-Ni-RE alloys by nanocrystallization[J].Journal of Alloys and Compounds,1999,293/294/295: 521−525.
[11]Spassov T,Köster U.Thermal stability and hydriding properties of nanocrystalline melt-spun Mg63Ni30Y7alloy[J].Journal of Alloys and Compounds,1998,279(2): 279−286.
[12]Yamaura S I,Kim H Y,Kimura H,et al.Thermal stabilities and discharge capacities of melt-spun Mg-Ni-based amorphous alloys[J].Journal of Alloys and Compounds,2002,339(1/2):230−235.
[13]Friedlmeier G,Arakawa M,Hirai T,et al.Preparation and structural,thermal and hydriding characteristics of melt-spun Mg-Ni alloys[J].Journal of Alloys and Compounds,1999,292(1/2): 107−117.
[14]Inoue A,Masumoto T.Mg-based amorphous alloys[J].Materials Science and Engineering: A,1993,173(1/2): 1−8.
[15]CHEN H S.Thermodynamic considerations on the formation and stability of metallic glasses[J].Acta Materialia,1974,22(12):1505−1511.
[16]OUYANG Liu-zhang,Yang Xu-sheng,DONG Han-wu,et al.Structure and hydrogen storage properties of Mg3Pr and Mg3PrNi0.1alloys[J].Scripta Materialia,2009,61(4): 339−342.
[17]Ouyang L Z,Wen Y J,Xu Y J,et al.The effect of Ni and Al addition on hydrogen generation of Mg3La hydrides via hydrolysis[J].International Journal of Hydrogen Energy,2010,35(15): 8161−8165.
[18]Zheng G,Popov B N,White R E.Electrochemical determination of the diffusion coefficient of hydrogen through a LaNi4.25Al0.75electrode in alkaline aqueous solution[J].Journal of the Electrochemical Society,1995,142(8): 2695−2698.
[19]Gasiorowski A,Iwasieczko W,Skoryna D,et al.Hydriding properties of nanocrystalline Mg2−xMxNi alloys synthesized by mechanical alloying (M=Mn,Al)[J].Journal of Alloys and Compounds,2004,364(1/2): 283−288.
[20]Kuriyama N,Sakai T,Miyamura H,et al.Electrochemical impedance and deterioration behavior of metal hydride electrodes[J].Journal of Alloys and Compounds,1993,202(1/2):183−197.
