单壁碳纳米管中受限水的热容及饱和含水量
2012-06-07梁晓凡曲媛媛黄定海
梁晓凡,曲媛媛,温 涛,黄定海
单壁碳纳米管中受限水的热容及饱和含水量
梁晓凡,曲媛媛,温 涛,黄定海
(天津大学材料科学与工程学院,天津 300072)
单壁碳纳米管纳米级的管径使其成为一种准一维的容器.用示差扫描量热的方法对受限于单壁碳纳米管中水的热容进行研究,结果显示,受限水的热容-温度曲线在所测量的温度范围内并未出现熔融峰,并且相比于同温度下的本体水,单壁碳纳米管中受限水的热容有反常的降低.红外光谱显示,单壁碳纳米管内水的氢键强度相对本体水变弱.结合红外结果可知,受限水热容反常降低的现象是因为氢键强度的下降,导致构象对热容的贡献减少.通过对溢出部分水的焓值计算可知,单壁碳纳米管内受限水含量质量分数上限为16,%.简化模型预测的单壁碳纳米管理论含水量比实际含水量质量分数高出2%左右.
单壁碳纳米管;受限水;热容;氢键
由于单壁碳纳米管(single-walled carbon nanotubes,SWNTs)纳米级的管径,可将其视为一种准一维的容器[1-2]或反应器[3],受限于单壁碳纳米管内的水,其性质与本体水相比,有很大差异.有人用分子动力学研究发现,单壁碳纳米管内的受限水在298,K呈现一种类似于固体的有序结构[4].Mashl等[5]认为,在100,kPa 和300,K的条件下,单壁碳纳米管中的受限水呈一种类似于结晶冰的状态,同时其氢键结构却类似于液态水.在较低的温度下,碳纳米管内的受限水会经历一种固-液相转变,在碳纳米管内形成一种“纳米冰管”状结构[6].由于单壁碳纳米管极小管径的限制效应,受限于其中的水的氢键结构会显著改变[7].Hanasaki等[8]发现单壁碳纳米管受限水的氢键比本体水更容易断裂,同时也更容易重新形成.Striolo[9]发现水在单壁碳纳米管内扩散时,属于哪种扩散机理取决于水分子和碳纳米管管壁的相互作用,以及碳纳米管的管径尺寸等.Wang等[10]认为单壁碳纳米管的尺寸会影响其内的水分子的扩散速率.
在以往的报道中,很少有关于受限水热容及SWNTs临界含水量方面的工作,笔者利用DSC和红外光谱对SWNTs中受限水的热容进行了研究,并根据测得的熔融焓计算了实验所用SWNTs的临界含水量上限,与1个简化的SWNTs含水模型的预测结果进行了比较.
1 实验方法
1.1原 料
实验所用SWNTs由南开大学陈永胜课题组提供,用电弧法制备,SWNTs外径为1.2~1.8,nm.
1.2碳纳米管的纯化与切割
粗制的碳纳米管用浓硝酸纯化,并用分散剂Triton X-10在超声中分散3,h,得到纯化的单壁碳纳米管.纯化后的单壁碳纳米管用质量比为3∶1的浓硫酸和浓硝酸的混合酸氧化切割,同样在超声中分散3,h,然后用蒸馏水洗去酸液,得到去除端帽的切割碳纳米管,并在氮气气氛下加热到200,℃,等温30,min以除去水分.
1.3碳纳米管填充水
取1份已经称得质量的干燥切割SWNTs,在大气压下置于水蒸气浴中1~2,h,然后迅速放入质量已知的DSC液体盘中,并压紧密封.对此样品进行加热直至其质量不再变化,并记录下质量.重复以上步骤,得到4份密封的加水单壁碳纳米管样品,其含水质量分数分别为7.41%、10.67%、12.40%和16.90%.
1.4热容测量
实验用于测量热容的仪器是Perkin Elmer公司生产的配有机械制冷系统的Diamond系列示差扫描量热仪(differential scanning calormetry,DSC).将4份加水碳纳米管样品连同1份干燥切割碳纳米管样品分别放入DSC炉中用阶梯扫描(step-scan)方法[11]进行扫描.扫描温度范围从-40,℃到25,℃,升温速率为5,℃/min,同时每个阶梯等温1.3,min.用同样的扫描程序对蓝宝石标准样品进行扫描,其结果用以校准实验样品的热容偏差.最终得到的是校准后的5个样品的热容值.
1.5红外光谱测试
实验用于扫描红外光谱的仪器是Perkin Elmer公司生产的带有衰减全反射附件的Spectrum,100傅里叶变换红外光谱仪.将一滴蒸馏水及干燥的SWNTs、水的质量分数分别为7.41%、10.67%、12.40%和16.90%的SWNTs各一份分别置于ATR附件样品台上进行红外扫描,获得红外光谱.扫描波数范围为650~4,000,cm-1,扫描分辨率为8,cm-1.
2 结果与讨论
2.1受限水的反常热容与氢键
由DSC得到的切割SWNTs的热容值cp经蓝宝石校准后,对温度作图,如图1所示.图1中另外4条曲线为4个不同含水量的(SWNTs+水)体系的较准热容对温度的曲线.从图1中可以看出,水的质量分数分别为7.41%、10.67%和12.40%的(SWNTs+水)体系的热容值cp,total随含水量的增加而升高.

图1 SWNTs与不同含水量的(SWNTs+水)体系热容Fig.1 Heat capacities of SWNTs and SWNTs in water with different water contents
由于SWNTs内壁为疏水性的,与水分子间无特殊相互作用,故将切割SWNTs的热容cp,SWNTs从cp,total中减去,可得到SWNTs中水的热容cp,pure-w,计算为

然后将cp,pure-w对温度作图,结果见图2.同时将本体水[12]和本体冰[13]的热容曲线也绘于图2中,以作对比.从图2中可以看到,水的质量分数分别为7.41%、10.67%和12.40%的(SWNTs+水)体系的纯水热容值cp,pure-w随温度上升近似地线性增加,并且在所测温度范围内并未出现熔融峰.说明与本体水相比SWNTs内的水的性质已经发生了很大的改变.此外,3个样品的cp,pure-w值明显要低于同温度下的本体水的.同时,尽管3个样品的含水量不同,其cp,pure-w值彼此间却很接近.
图3为2,000~4,000,cm-1波数范围内干燥SWNTs和水的质量分数分别为7.41%、10.67%、12.40%和16.90%的SWNTs,以及本体水的红外光谱.其中3,400~3,600,cm-1处的谱带对应着水中羟基的伸缩振动.如图3所示,干燥的SWNTs在这个波段范围内并无红外吸收,因此4个含水的SWNTs样品在这个波段处的红外吸收峰应该对应于其所含水分子的羟基的伸缩振动.从图3中可以看到本体水的伸缩振动峰位于3,408,cm-1,峰形很宽;而4个含水的SWNTs样品的峰均位于较高波数,且形状变得尖锐,这一结果说明受限水结构中的氢键强度变弱[14].3个含水质量分数分别为7.41%、10.67%和12.40%的样品的伸缩振动峰都位于约3,475,cm-1处,形状也没有明显差别,这表明3个样品中受限水的结构很接近.三者的cp,pure-w值彼此间很接近,也同样证明了这一点.同时16.90%的样品的该峰位于约3,469,cm-1处,相对其他3个含水量的样品,峰形变得略宽,这说明了该样品已经达到临界饱和含水量,并有部分水溢出管腔,这部分溢出水使得峰形变宽并造成了峰位向低波数移动.由于曲线5的峰形加宽效应和峰位的红移并不十分显著,这部分溢出水的比例应该较小.
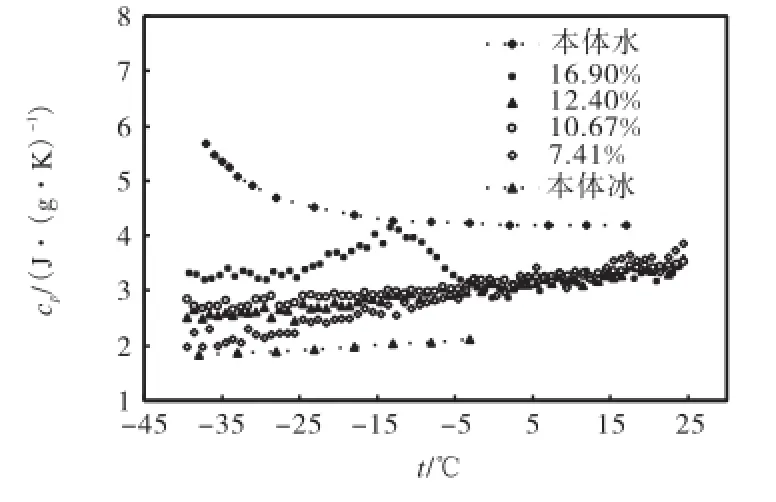
图2 不同含水量的(SWNTs+水)体系中受限水的热容及本体水和本体冰的热容Fig.2 Heat capacities of confined water in(SWNTs+water) with different water contents and heat capacities of bulk water and bulk ice
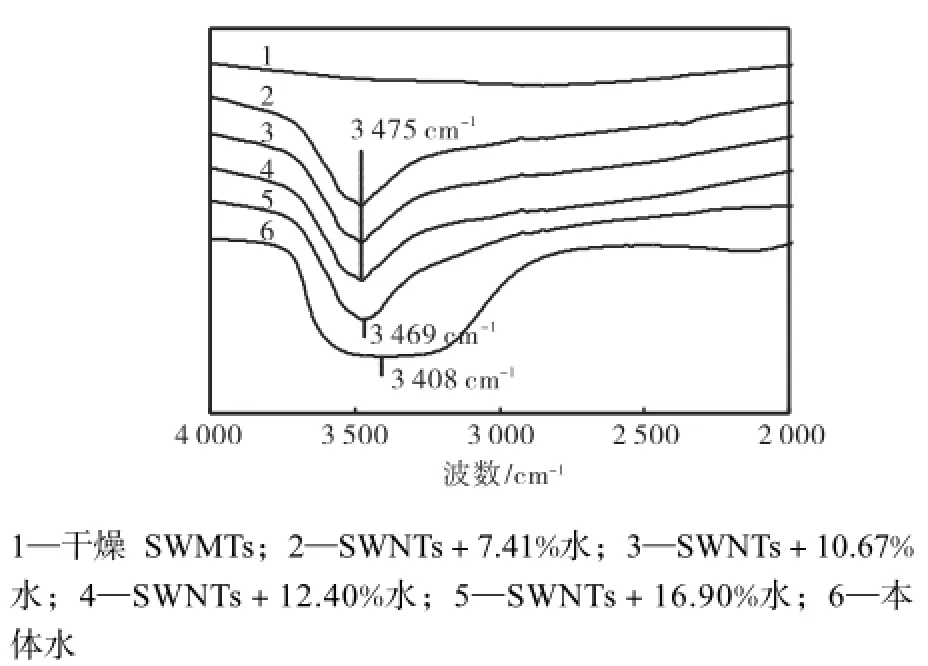
图3 各样品的红外光谱Fig.3 FTIR spectra of samples
2.2反常热容成因探讨
对于液态水,其热容主要由2种贡献构成:①振动贡献;②构象贡献.振动贡献会随机械自由度的激发而上升,而构象自由度会随水的结构变化而变化,如氢键的扭曲断裂等[15].即液态水温度升高1,℃所需要的能量cp由两部分组成:①激发振动;②改变水的结构.氢键的存在,使得水分子行为受到限制,因此要改变液态水的结构,需要更多的能量使氢键扭曲甚至断裂.这也正是液态水的热容值很高的原因.Oguni等[16]的工作也支持了这一观点.他们将水与不同比例的H2O2或N2H4分别混合,然后测量其热容.当混合液中第2组分H2O2或N2H4的比例高于20%时,混合液中水的氢键消失.这样用外推法得到了水作为“正常液体”(不含氢键)的热容,发现这个热容值要远低于本体水(含氢键)的热容.而当混合液中第2组分(H2O2或N2H4)的比例低于20%时,水的氢键影响将体现出来,导致外推得到的水的热容增加.Oguni等的实验充分说明了液态水中氢键的确会显著影响其热容.
结合在受限水氢键强度变弱的结论,正好解释了为何SWNTs中受限水热容会降低.SWNTs纳米级管径对水分子的限制效应,使得水分子结构相对本体水来说产生变化,氢键强度变弱.这样在温度升高时,改变水结构所需的能量减少,导致水的热容的构象贡献减少,从而使受限水的热容明显降低.
2.3SWNTs的临界含水量及其简化模型
从图1和图2中可以看出,含水的质量分数为16.90,%的样品在-13,℃附近时出现一个熔融峰.此时SWNTs中的水已经达到饱和,溢出部分的水吸附于SWNTs的外壁上,这部分溢出的水造成热容曲线上出现了熔融峰.溢出水占总含水量的比例为

式中:Q为熔融过程中吸收的热能;mtotal为碳纳米管和水的总质量;ΔHm为本体水的标准熔融焓(ΔHm= 333.5,J/g).Q/mtotal的值可由熔融峰面积的积分得到.考虑到表面吸附水的热容比本体水约高25%左右[17],最终得到Ww的值为5.77%.溢出SWNTs的水只占含水量的1/17左右,这也解释了为什么水的质量分数为16.90%的样品在较高温度(高于熔融区间)下其热容值并未明显高于其他样品.同时,也得到了实验所用的SWNTs的临界饱和含水质量分数为16.90%(1-5.77%)≈16%.
通过一个简化的SWNTs含水模型,从理论上对实验所用SWNTs的临界饱和含水量进行简单计算和预测.
对于本体水来说,密度ρ为1.0×106,g/m3,摩尔质量M为18,g/mol,阿弗加德罗常数为6.023×1023,据此得到单个水分子的有效体积为

计算得VH2O=2.99×10-29,m3.
实验所用的SWNTs外径为1.2~1.8,nm,为了简化计算,假设其服从参数为(μ,σ2)的正态分布,显然μ=1.5.充分考虑到此正态分布的峰度系数要适当,以使曲线尽量落到区间[1.2,1.8]内而又要尽量充满该区间,不妨令σ=0.1.则此分布的密度函数为(如图4所示)


图4 SWNTs外径的正态分布密度函数Fig.4 Density function of normal distribution of SWNTs diameters
而考虑到水分子填充碳纳米管的过程,碳管的直径实际是在截面的2个维度方向上起作用的,所以需要求得上述分布的二阶原点矩的平方根,即SWNTs的均方根直径.对于正态分布,二阶原点矩2μ′为

SWNTs的均方根直径为

解得D=1.503 nm.
图5(a)为SWNTs轴心方向示意,其中C原子直径dC=0.14,nm,SWNTs中C—C键平均键长bC—C= 0.143,nm[18].由于SWNTs中C原子之间形成正六边形结构,所以从平行轴心方向看去,相邻两C原子之间的投影距离应为(2)bC—C,也即0.866bC—C.由此可得SWNTs一个垂直于轴心方向上的锯齿状C原子环所含C原子数为

计算得N0≈35.图5(b)为SWNTs外壁示意.如图所示,每1.5,bC—C长度内就含有N0个C原子,所以长度为L的SWNTs含有C原子的个数为

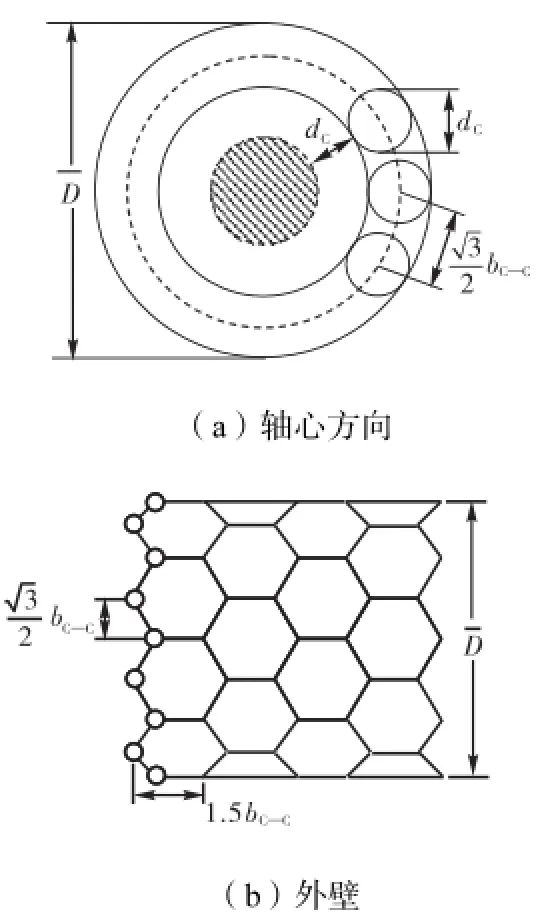
图5 SWNTs示意Fig.5 Sketches for SWNTs
事实上,Thomas等[19]研究得出,在SWNTs内,曲率效应会影响管壁附近的分子密度及分布,曲面会排斥形成于六角碳表面的低势能阱,因而迫使水分子脱离碳表面并降低液体密度.综合考虑这种分布及密度效应,将SWNTs内壁到距内壁表面一个C原子直径之间的区域视为势阱区,区域内不含有水分子,而区域外的水分子仍保持本体密度.图5(a)中阴影部分即为含水区.这样对于长度为L的SWNTs,其内部含有水的空间体积为

则长度为L的SWNTs内部容纳水分子个数为

所以,对于长度为L的SWNTs,其临界饱和含水量为

联立式(8)、式(10)和式(11),最终得到maxω′=18.1%.
对比实验得到的临界饱和含水量,可以看到理论含水质量分数要高出2%左右.说明该简化模型相对来说比较成功,另一方面也说明理论预期和实验值存在一定偏差.在实际情形中,SWNTs管径不可能完全服从正态分布,同时SWNTs管壁本身存在的诸如五元环或七元环的缺陷也会使受限水的分布情况更为复杂.此外,对低势能阱造成的受限水密度及分布的异常,该模型的处理方式也较为粗糙.有理由相信正是上述因素导致实际饱和含水量和理论值的偏差.
3 结 语
用DSC测量了受限于SWNTs中水的热容,发现在临界饱和含水量以下,受限水在所测的温度范围并未出现熔融峰.受限水的热容随温度上升近似呈线性增加,并且反常地低于同温度下的本体水.红外光谱研究表明,受限水中氢键强度明显变弱.热容的变化可归结为由于SWNTs的尺寸限制作用,受限水的氢键强度下降所致.根据溢出部分水的熔融焓计算得到,实验所用SWNTs的临界饱和水的质量分数为16%.通过理论模型得到的饱和水的质量分数比此值高出约2%,说明模型在某种程度上较为成功,此外也说明模型的精度尚嫌不足,没有充分反映SWNTs填充水这一现象的复杂性.
[1] Ye Y,Ahn C C,Witham C,et al. Hydrogen adsorption and cohesive energy of single-walled carbon nanotubes [J]. Appl Phys Lett,1999,74(16):2307-2309.
[2] Chen P,Wu X,Lin J,et al. High H2uptake by alkalidoped carbon nanotubes under ambient pressure and moderate temperatures[J]. Science,1999,285 (5424):91-93.
[3] Ugarte D,Châtelain A,de Heer W A. nanocapillarity and chemistry in carbon nanotubes [J]. Science,1996,274(5494):1897-1899.
[4] Liu Y C,Wang Q,Wu T,et al. Fluid structure and transport properties of water inside carbon nanotubes [J]. J Chem Phys,2005,123(23):234701.
[5] Mashl R J,Joseph S,Aluru N R,et al. Anomalously immobilized water:A new water phase induced by confinement in nanotubes[J]. Nano Lett,2003,3(5):589-592.
[6] Koga K,Gao G T,Tanaka H,et al. Formation of ordered ice nanotubes inside carbon nanotubes[J]. Nature,2001,412:802-805.
[7] Gordillo M C,Martí J. Hydrogen bond structure of liquid water confined in nanotubes[J]. Chem Phys Lett,2000,329(5/6):341-345.
[8] Hanasaki I,Nakatani A. Hydrogen bond dynamics and microscopic structure of confined water inside carbon nanotubes[J]. J Chem Phys,2006,124(17):174714.
[9] Striolo A. The mechanism of water diffusion in narrow carbon nanotubes[J]. Nano Lett,2006,6(4):633-639.
[10] Wang J,Zhu Y,Zhou J,et al. Diameter and helicity effects on static properties of water molecules confined in carbon nanotubes[J]. Phys Chem Chem Phys,2004,6(4):829-835.
[11] Huang D H,Simon S L,McKenna G B. Chain length dependence of the thermodynamic properties of linear and cyclic alkanes and polymers[J]. J Chem Phys,2005,122(8):084907.
[12] Angell C A,Ogunl M,Sichina W J. Heat capacity of water at extremes of supercooling and superheating [J]. J Phys Chem,1982,86(6):998-1002.
[13] Handa T P,Mishima O,Whalley E. High-density amorphous ice. Ⅲ:Thermal properties[J]. J Chem Phys,1986,84(5):2766-2770.
[14] 沈德言. 红外光谱法在高分子研究中的应用[M]. 北京:科学出版社,1982.
Shen Deyan. The Application of IR Spectrum Method in Polymer Research[M]. Beijing:Science Press,1982(in Chinese).
[15] Eisenberg D,Kauzmann W. The Structure and Properties of Water[M]. Oxford:Oxford University Press,1969.
[16] Oguni M,Angell C A. Heat capacities of H2O+H2O2,and H2O+N2H4,binary solutions:Isolation of a singular component for cpof supercooled water[J]. J Chem Phys,1980,73(4):1948-1954.
[17] Etzler F M. A statistical thermodynamic model for water near solid interfaces[J]. J Colloid Interface Sci,1983,92(1):43-56.
[18] 颜浩然,王利光,Tagami K,等. 石墨烯与关联单壁碳纳米管物理特性比较研究[J]. 黑龙江大学自然科学学报,2009,26(2):259-264.
Yan Haoran,Wang Liguang,Tagami K,et al. Comparison of physical properties between graphene and its related SWCNT[J]. Journal of Natural Science of Heilongjiang University,2009,26(2):259-264(in Chinese).
[19] Thomas J A,Mcgaughey A J H. Density,distribution,and orientation of water molecules inside and outside carbon nanotubes[J]. J Chem Phys,2008,128(8):084715.
Heat Capacity of Confined Water and Maximum Water Content of Single-Walled Carbon Nanotubes
LIANG Xiao-fan,QU Yuan-yuan,WEN tao,HUANG Ding-hai
(School of Materials Science and Engineering,Tianjin University,Tianjin 300072,China)
A single-walled carbon nanotube can be regarded as quasi one-dimension container owing to its nanoscale diameter. The specific heat capacities of water confined in single-walled carbon nanotubes were calculated with differential scanning calorimeter. The results showed that the confined water presented no melting peak in the heat capacity plot, and had an anomalous lower heat capacity than that of bulk water at the same temperature. Fourier transform infrared spectroscopy results showed the hydrogen bonding in confined water was weaker than that of the bulk water. The anomalous lower heat capacity could be ascribed to the weakening of the hydrogen bonding, which induced the decrease of the configurational contribution. An approximate 16% maximum water mass fraction of single-walled carbon nanotubes was obtained through enthalpy calculation. Asimplified model predicted a 2% higher maximum water mass fraction of single-walled carbon nanotubes, indicating that the model was successful to a certain extent.
single-walled carbon nanotubes;confined water;heat capacity;hydrogen bonding
O469
A
0493-2137(2012)03-263-05
2010-12-15;
2011-03-16.
天津大学-天津市青年教师留学回国人员启动基金资助项目.
梁晓凡(1983— ),男,博士研究生.
梁晓凡,xiaofanliang@tju.edu.cn.
