浮肿、发热、截瘫
2012-06-05刘琳,沈敏,张文
刘 琳,沈 敏,张 文
(中国医学科学院北京协和医院风湿免疫科,北京 100032)
浮肿、发热、截瘫
刘 琳,沈 敏,张 文
(中国医学科学院北京协和医院风湿免疫科,北京 100032)
患者女,34岁,因“浮肿1年余,发热3个月,双下肢瘫痪6天”入院。
1 病例摘要(第1部分)
1.1 病史
患者于1年余前无明显诱因出现颜面及双下肢浮肿,伴脱发。查血常规 WBC 3.2×109/L,Hb 101 g/L,PLT 89×109/L,尿常规:蛋白5.0 g/L,24 h尿蛋白定量4.03 g,血 Alb 25 g/L,Cr正常,ANA、抗dsDNA(+),肾穿病理:狼疮性肾炎Ⅳ-S(A)+Ⅴ型。诊断系统性红斑狼疮(SLE)给予泼尼松龙55 mg qd→每月减5 mg,25 mg qd之后每月减2.5 mg,来氟米特50 mg/d×3 d→20 mg qd维持。尿蛋白逐渐减少,浮肿、脱发逐渐减轻。1年前泼尼松龙减至40 mg qd时出现发热,多于上午出现,Tmax 39℃,下午自行降至正常,伴盗汗,中药治疗数日后体温正常。8个月前再次发热,性状同前,中药治疗约20 d后体温正常。3个月前泼尼松龙减至15 mg qd时第3次发热,Tmax 40℃,上午及夜间达峰值,可自行降至正常,伴盗汗、畏寒,偶有寒战,无咳嗽、咳痰。胸部CT提示“双肺结节,肺间质改变”。考虑SLE病情活动合并肺间质病变,泼尼松龙加至30 mg qd,并加用左氧氟沙星,3 d后体温正常。停抗生素后再次发热,将泼尼松龙改为早20 mg,晚10 mg,至今未再发热。1个月前感乏力,行走无力,8 d前双下肢无力明显加重,无法行走,伴感觉减退,大小便失禁,6 d前双下肢完全瘫痪。否认结核接触史。既往史、个人史、月经婚育史、家族史:无殊。
1.2 入院查体
生命体征平稳,神清,对答切题。心、肺、腹(-)。双下肢轻度水肿。脊柱无压痛、叩击痛。脑膜刺激征(-),双上肢肌力V级,双下肢肌力0级。脐下5cm平面以下痛温觉减退,深感觉迟钝。双侧腱反射略亢进,双下肢病理反射(+)。
2 讨论(第1部分)
2.1 沈敏医师(风湿免疫科)
患者为青年女性,病程1年余。起病时有肾脏、血液系统受累,伴脱发,ANA及抗dsDNA阳性,已确诊为SLE。外院给予了相对正规的治疗——泼尼松1 mg/kg·d+来氟米特,治疗后患者症状好转,尿蛋白量减少,提示治疗有效。但激素减量略微偏慢。病程中共3次发热,前2次时间较短,中药治疗后体温正常。本次发热持续时间较长,伴盗汗,无呼吸系统症状体征,但外院CT提示双肺内多发结节影。1个月前出现双下肢无力,仅1周就快速进展为截瘫。入院时诊断主要考虑:
1)SLE复发:因患者发热、截瘫症状出现在激素减量过程中,免疫抑制剂的应用又相对偏弱,因此需考虑SLE病情复发活动。神经精神狼疮(NPSLE)几乎可出现所有的神经系统症状体征,故患者截瘫高度怀疑系NPSLE所致。但如何解释患者新出现的双肺多发结节?总结我院SLE肺受累病例,最多见为胸膜炎,也可出现肺间质纤维化,但多表现为网格、索条影,另有少见的弥漫肺泡出血、急性狼疮性肺炎,还包括肺栓塞、肺高压等。多发结节影在SLE肺部受累中十分罕见。
2)感染:患者有免疫病基础,长期使用激素、免疫抑制剂,且激素减量偏慢,近期新出现发热、肺部病变,感染不能除外。SLE合并肺部感染发病率非常高,结合患者肺内结节、截瘫、发热、盗汗等表现,首先考虑结核感染。双肺结节弥漫分布,要警惕血行播散结核,需复查胸部HRCT。而中枢神经系统结核感染,多表现为神志障碍,脑膜刺激征阳性,截瘫多由于椎体结核压迫所致,但患者脊柱查体未见椎体病变的证据,所以截瘫用结核感染似乎不好解释。除结核感染外,双肺结节影还应考虑真菌感染。需进一步寻找病原学证据。
3)肿瘤:肺内多发大小不等结节可见于弥漫肺泡癌、肺内转移癌等。但SLE合并实体肿瘤报道不多,且肺内肿瘤转移或副癌综合征引起髓内病变均十分少见,不好解释患者病情全貌。
因此患者入院后需要重点排查SLE原发病复发和感染。新出现的截瘫是危急重症,需抓紧时间诊治,我们在患者入院后2天积极完善了大部分重要的相关检查。
3 病例摘要(第2部分)
3.1 辅助检查
3.1.1 常规检查:血常规、肝肾功基本正常,Alb 31 g/L。尿常规 PRO(-),RBC(-),24 h尿蛋白0.29 g。ESR 116 mm/h,CRP 18.19 mg/L。补体正常。IgG 19.1 g/L。腰穿:压力、常规、生化正常,病原学(-)。行CT引导下经皮肺穿,已送病理及病原学,病原学涂片萋尼法抗酸染色(-)。
3.1.2 免疫指标:ANA(+)斑点型1∶160,胞质型1∶320,抗 dsDNA-IF(+)1∶10/ELISA 239 IU/mL。抗 ENA:抗 Sm 原倍阳性/28,29,13.5 ku,抗 RNP原倍阳性/73,32,17.5 ku。
3.1.3 感染方面:血TB-SPOT 504SFCs/106PBMC,PPD试验 (+),TB-Ab(-)。血清蛋白电泳:γ球蛋白28%↑,A/G 0.7↓。G试验、GM试验(-)。血培养:需氧、厌氧(-),分枝杆菌培养结果未出。痰培养:抗酸染色、真菌涂片(-)。
3.1.4 肿瘤方面:肺癌筛查:Cyfra211 5.57 ng/mL,SCCAg 1.66 ng/mL,余正常,CSF抗 HU.YO.RI抗体(-),骨扫描(-)。
3.1.5 影像学:胸部HRCT:双肺弥漫多发结节影,双侧胸膜增厚。脊髓MRI平扫+增强:T10-11水平胸髓类圆形异常信号;T3椎体水平以下脊髓内弥漫稍长T2信号影;脊膜断续样强化;T6椎体异常信号;T7椎体楔形变。头颅MRI平扫+增强:右侧额叶皮层下环形强化灶,右侧额叶、颞叶点状强化。
3.2 治疗经过
患者入院后发热,Tmax 38.5℃,继续泼尼松20 mg qd,10 mg qn,加用拜复乐0.4 qd静点抗感染治疗后体温正常,左下肢远端肌力恢复至Ⅰ级。
4 讨论(第2部分)
4.1 高鑫医师(放射科)
分析患者影像学特点:胸腰椎平片见胸腰椎骨质疏松,T7椎体楔形变(图1)。将胸部HRCT设置成骨窗,矢、冠状位重建影像进一步明确椎体无明显骨质破坏,椎管无狭窄,因此无椎体占位性病变压迫脊髓的证据(图2)。胸部HRCT肺窗可见双肺弥漫结节影,偏背侧肺段分布比较集中,结节较大,密度较高,而腹侧肺段相对稀疏(图3);纵隔窗未见淋巴结肿大。头颅MRI可见右侧额叶类圆形等T1长T2信号,增强后呈环形强化(图4),并且右额叶前方另有一个小的点状异常强化灶。胸髓MRI:T10-T11类圆形等T1短T2异常信号,伴有环形强化,病变位置与体格检查定位相符(图5),此外,T8-T10节段脊膜增厚,增强后强化。
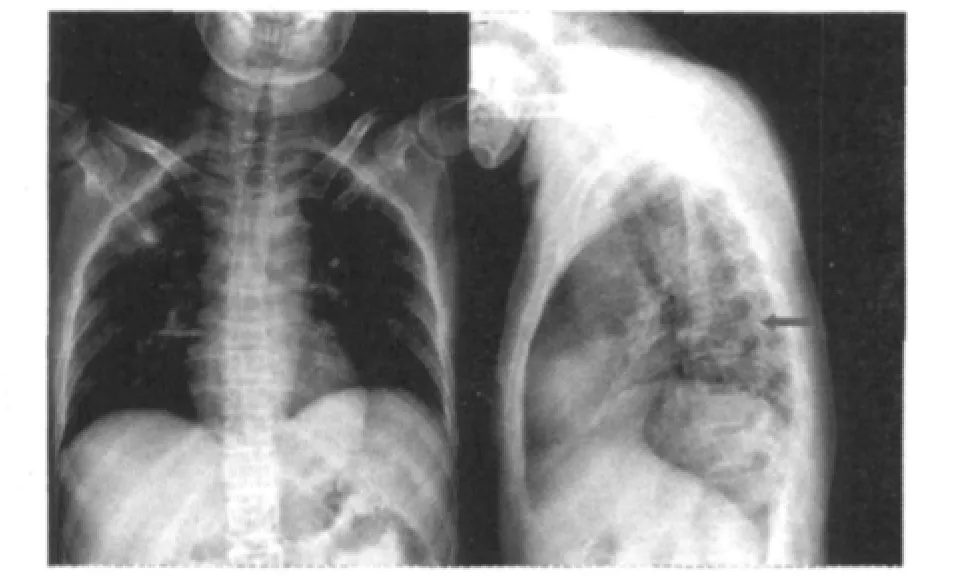
图1 胸腰椎平片Fig 1 Thoracic and lumbar vertebral X ray
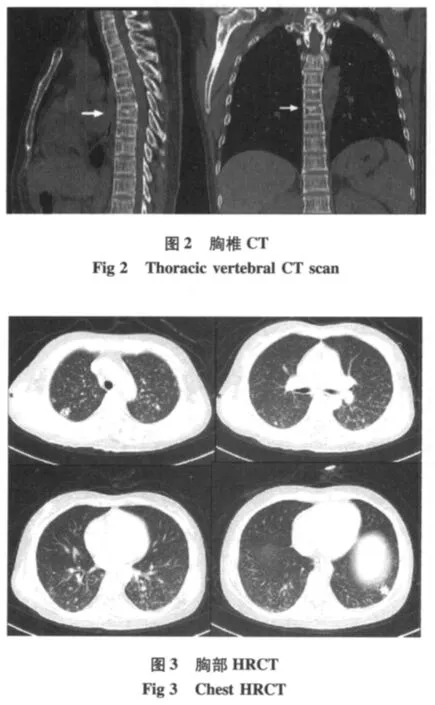
综合以上影像学特点,首先考虑诊断本患者为肺及中枢系统结核感染。患者肺部多发结节表现为大小、分布、密度都不均的“三不均”分布,符合亚急性血行播散性肺结核的典型表现。关于中枢神经系统结节状异常信号,结合文献报道,“靶征”(即T2WI示病变中心低信号周围高信号)及增强后周边环形强化,为中枢神经系统结核瘤的特征性表现(图4,5)。且T8-T10节段脊膜增厚,强化明显,符合脊膜炎表现。而胸椎的骨质疏松伴有个别椎体楔形变,考虑为长期服用激素引起的骨质流失引起,没有结核相关的影像学证据。

图4 头颅MRIFig 4 Head MRI
脊髓髓内结核非常少见,根据文献报道发病率仅百万分之二,胸髓结核占其中的3/4。髓内结核在病变初期表现为等T1、等T2信号,平扫不易发现;随病变进展,结核瘤逐渐形成,胶冻样物质增多,中心T2信号减低,形成“靶征”。“靶征”的信号可以不完整,与不同时期结核肉芽肿内的成分有关。
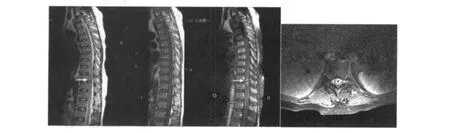
图5 胸髓MRIFig 5 Thoracic spinal cord MRI
4.2 沈敏医师(风湿免疫科)
入院后第2天,根据实验室检查及影像学结果,我们作出了修正诊断——高度怀疑结核感染。患者有发热、盗汗等结核中毒症状,但肺部症状体征轻,而影像表现重,影像学表现为双肺从肺尖到肺底弥漫大小不等结节(刚才放射科高大夫已经详细分析),并有多项炎性反应指标升高,TB-SPOT升高,符合血行播散粟粒性结核特点。患者的截瘫是否是结核中枢神经系统感染?比较令人意外的是患者的腰穿结果完全正常。中枢神经系统结核感染患者脑脊液大多数表现出蛋白、细胞数、糖、氯化物的变化,但脑脊液正常并不能完全除外结核。患者脊髓MRI显示脊髓横断面内环形强化的“葡萄样”病变占据了脊髓横截面2/3以上(图5)。虽然患者没有颅内受累表现,但因中枢神经系统结核感染仅累及脊髓者罕见,多数同时合并颅内感染,故为患者加做了头颅MRI,并找到了类似的环形强化“葡萄样”病灶(图4)。我们分析其脑脊液阴性结果可能与结核脓肿形成、炎症包裹有关。
同时,我们反思SLE原发病是否活动?SLE患者新发肺部阴影,需要首先考虑肺部感染。其他SLE肺部受累表现包括胸膜炎、急性狼疮性肺炎、弥漫肺泡出血、慢性间质性肺炎、肺动脉高压等。肺部结节影属于肺间质改变,但SLE并肺间质改变程度多较轻,并且在老年人多见,影像学多表现为中下肺纤维索条、小网格、小蜂窝影。所以该患者的肺部表现无法用SLE肺部受累解释。那么患者神经系统受累是否为SLE所致横贯性脊髓炎?SLE脊髓炎在MRI上多表现为长条形分布的异常信号,而非圆形病灶环形强化,从这一点上看也不符合NPSLE的表现。
因此,我们作出修正诊断:暂不考虑SLE原发病活动,中枢神经系统、肺部表现考虑为结核感染,需要抗痨治疗。但我们尚缺乏确凿的病原学证据,病原体也许可能为不典型结核分枝杆菌或者真菌。由于患者有免疫病基础,需长期服用激素、免疫抑制剂,病原学的明确对于患者未来的治疗十分重要。我们做了很多努力,但多次诱导排痰行抗酸染色均为阴性。而中枢神经系统组织活检危险性极高,脊髓活检可能造成永久截瘫,颅内病变位置又比较深,于是我们选择了CT引导下经皮肺穿,取肺内结节活检,分别送病理及病原学以明确病变性质。
4.3 赵静医师(呼吸科)
反复追问病史,患者病程中无呼吸道症状,既往亦无明确结核病史或接触史。肺部查体(-)。入院后评估系统性红斑狼疮处于相对稳定状态。结核方面证据:TB-SPOT 504SFCs/106PBMC,PPD(+),炎症指标很高。其他病原学检查:G试验、GM试验均(-)。肿瘤方面检查:Cyfra211、SCCAg轻度升高。胸部HRCT可见,双肺多发小结节影,有的小结节分布于胸膜下和叶间裂,有的小结节与次级肺小叶的肺动脉相连,似小结节“滋养动脉”,有的小结节与所有次级肺小叶结构无明显毗邻关系,右上肺尖段可见数个小结节融合形成稍大的病灶,纵隔淋巴结不大。因此,患者影像符合典型随机分布结节的HRCT表现。
2006 年Chest(Vol 129:805-815)曾发表一篇文章讲述肺部多发结节的HRCT诊断流程,该文章中讲述,这种随机分布的结节,其本质上体现的是沿淋巴血流播散的疾病,最常见的疾病为:转移性肿瘤、粟粒性感染(包括结核、真菌和病毒)。明确概念:次级肺小叶是肺的基本结构单元,包括细支气管至肺泡之间的部分,从HRCT上仅可分辨到与细支气管伴行的肺小动脉,而小叶间隔,肺小静脉,肺小淋巴管以及细支气管壁均无法显示。随机分布即结节与上述次级肺小叶结构(肺小动脉、小叶间隔、脏层胸膜等)均无明显毗邻关系,随机分布于双肺。
因此本例诊断方面:1)根据患者病史及辅助检查首先怀疑感染性疾病。根据HRCT上结节随机分布的特点,符合血行感染性疾病,结合PPD、TB-SPOT等结果,最可能为血行感染性结核。其他病原如真菌、病毒均无典型表现。2)转移瘤,结合中枢神经系统影像学表现以及病理予排除(CNS转移瘤往往多发,部位常见于灰白质交界处,这种表现为颅内单发,以及横贯脊髓的转移病变非常罕见)。3)狼疮性肺炎,其本质为血管炎,主要表现为沿支气管血管束分布的斑片影,严重时可合并肺泡出血等,患者往往呼吸系统症状非常重,患者表现与此不符,暂不考虑。
另复习我院张晓彤医师等总结的27例血行播散型肺结核临床特征[中华内科杂志,2004,43(1)],可见这类患者临床表现多不典型,呼吸道症状隐匿,以发热为主要表现,部分患者可有肝脾肿大,皮疹和血三系下降。胸部影像学以浸润性改变为主,空洞少见,粟粒性结节影出现较晚,结核菌素试验多阴性,病原学检测阳性率低。12例误诊,误诊率为44.4%,12例中11例(92%)因伴发或疑为结缔组织病、血液系统疾病或肿瘤而误诊。27例患者中17例(63%)长期应用激素或反复化疗导致结核播散。这些特征与本例患者有很多类似的地方。因此,临床医生应该加强对结核病的警惕性,特别是有结核病史,免疫缺陷(包括长期使用激素或化疗)病史,合并营养不良的患者,出现长期发热和(或)有多系统损害,尤需重视结核可能。
4.4 周宝桐医师(感染科)
本病例的诊断也是感染科经常面对的困难,当免疫病与感染同时存在时往往难以判断。当然,最直接的证据是组织病理或病原学,但常难以获得。本患者肺内表现典型,T-SPOT.TB强阳性,可以诊断亚急性血行播散性肺结核。但中枢神经系统病变性质仍需要进一步分析。我们知道,结核感染累及中枢大多表现为结核性脑膜炎,而结核瘤仅占中枢神经系统结核的1%。结核感染对于免疫力健全者,主要表现为浸润性肺结核、淋巴结结核等局限性炎症;免疫力严重受损者易表现为急性血播性结核,颅内病变可能出现类似于粟粒样结节的表现;本患者免疫力不健全,出现亚急性血播肺结核以及少见的中枢神经系统结核瘤,能够解释病情全貌。此外,颅内病变应注意与其他中枢神经系统占位,如肿瘤、寄生虫、其他感染包括细菌、真菌脑脓肿等鉴别。但细菌、真菌感染肺部表现常与症状平行,本患者肺部病变重,全身症状轻,不支持。无肿瘤、寄生虫相关证据。因此,结合患者全身表现,中枢神经系统病变也首先考虑结核感染。
CSF检查,结核性脑膜炎有特征性改变,可有TSPOT.TB(+),甚至分枝杆菌培养(+)。但CSF改变对诊断结核瘤意义不大。我院神经内科曾总结脑结核瘤的CSF改变,大多数结核瘤患者CSF完全正常,仅有一半以下患者出现非特异变化。MRI影像学环形强化病灶为结核瘤诊断支持点,但并非绝对可靠。临床诊断需多层次依据,包括结核接触史、其他部位结核病灶、临床表现如结核中毒症状,以及影像学支持。确诊依据主要有:1)组织病原学、病理证据。2)治疗随访,若治疗后病灶消失,病情改善,可确诊。
治疗方面,本患者应给予积极抗结核治疗。但中枢神经系统结核瘤在开始有效抗结核后,可能会从增殖性病变演变出现液化、坏死,炎症反应加剧,短期内症状加重,故在治疗初期建议加用激素。对于本患者与狼疮治疗刚好无矛盾。
本例引发的思考,结核感染与免疫力低下有关,各种原因引起免疫力低的患者若出现发热、盗汗、炎症指标明显升高等表现,需高度警惕结核感染。但明确诊断仍是巨大挑战,TB-SPOT.TB是一个重要参考,阳性、阴性预测值90%左右,但仍有不足,诊断需依靠对患者整体评估。
4.5 霍真医师(病理科)
该患者经皮肺穿病理结果:送检组织为灰粉组织2条,长0.6~0.7 cm,直径0.5 cm。HE染色(图6)可见明显上皮样结节及多核巨细胞反应,伴片状坏死,符合结核、真菌及结节病改变,暂时不考虑肿瘤。根据HE结果行特殊染色:抗酸染色(-),六铵银染色(-),PAS染色(-)。综合以上,首先考虑感染性疾病,结核、真菌均不能除外,明确诊断需结合临床及病原学培养综合考虑。
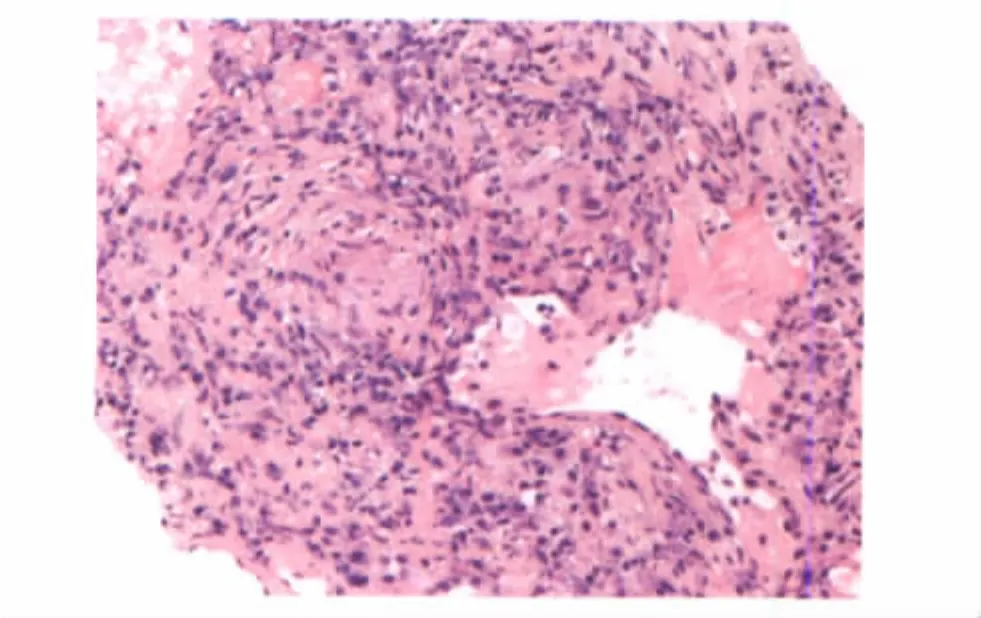
图6 肺组织活检病理(HE染色)Fig 6 Pathology of lung biopsy(×40)
4.6 沈敏医师(风湿免疫科)
经过多科积极努力,患者最终诊断为结核感染(亚急性血行播散性肺结核,脑脊髓结核脓肿),系统性红斑狼疮(狼疮性肾炎IV+V型)。本次发热和截瘫系结核感染所致。

图7 2007年1例内科大查房患者的胸HRCT及头颅和脊髓MRIFig 7 Chest HRCT,head and spinal cord MRI of another patient in 2007
2007 年内科大查房曾由呼吸科提供过类似结核性脑脊髓脓肿的病例。该患者肺部主要表现为磨玻璃影,以及下肺结节影部分融合。该患者因肢体无力,行头颅及脊髓MRI显示颅内及脊髓多发环形强化“葡萄样”病灶,符合结核脓肿(图7)。主治医师张弘大夫在当时总结了2000~2007年血行播散肺结核累及中枢神经系统共16例患者,发现所有患者均出现脑膜刺激征表现。神经科关鸿志大夫总结了2007年前共12例结核性脑脓肿患者,其中仅有1例合并出现脊髓脓肿。我们通过病案室资料检索了从北京协和医院建院至2011年3月住院病例,其中血行播散性肺结核合并中枢神经系统结核感染共50例,单纯颅内结核感染23例,合并脊髓结核感染者仅3例。由此可见脊髓结核非常罕见。
在风湿免疫科,SLE合并脑结核脓肿的情况又如何呢?北京协和医院风湿免疫科徐东、徐燕大夫曾总结1995~2001年北京协和医院收治4 130例狼疮患者中,脑脓肿共15例,其中10例(66.7%)最终诊断为结核,3例奴卡菌,1例非典型分枝杆菌,另1例可能为普通细菌。10例结核感染患者中有6例从痰或组织中获得确凿病原学证据。该15例SLE患者原发病均稳定,所有患者均出现脑脊液蛋白升高,MRI表现为环形强化病灶或脑膜强化。我们形象地将这种结核脓肿环形强化病灶称为颅内的“葡萄”。在此分享近期我们风湿免疫科收治的5例SLE合并结核性脑和(或)脊髓结核脓肿:病例1,20岁女性患者,新发中枢神经系统症状,曾疑诊NPSLE,但头颅MRI显示多发成串分布的“葡萄”样环形强化病灶,诊断结核感染,抗痨治疗有效;病例2为28岁女性,表现为神志障碍,一度怀疑NPSLE,后经头颅MRI发现颅内多发成串“葡萄”样环形强化灶(图8),给予抗痨治疗,回当地医院随诊;病例3,21岁女性,颅内多发“葡萄”样环形强化病灶,家属放弃治疗;病例4为24岁女性,曾被误诊为NPSLE,我院行MRI检查发现颅内多发“葡萄”样环形强化病灶并颅底脑膜强化,考虑结核感染,予抗痨并转结核病专科医院继续治疗;本次查房病例,较前4例更为特殊之处在于脊髓中也出现了“葡萄”,是非常罕见的脊髓结核脓肿。
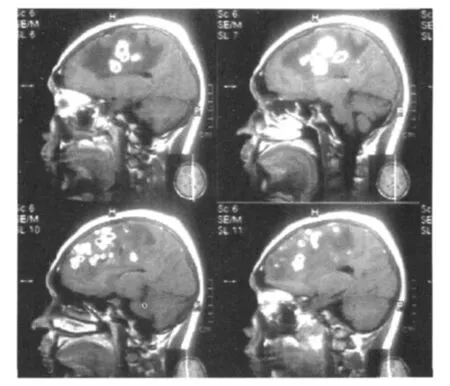
图8 1例28岁女性SLE患者的头颅MRIFig 8 Head MRI of a 28-year old woman with SLE
在临床工作中我们常常会遇见SLE患者出现神经系统症状体征,我们也在不断思考,如何鉴别SLE原发病活动与中枢神经系统感染。我们体会,尤其在SLE病情稳定时,如果新出现神经系统症状体征,更需十分警惕感染。结核感染临床表现变化多端,诊断手段有限,且病理、病原学证据不易取得,诊断十分困难,而结核感染的临床表现时常容易与结缔组织病尤其是SLE相混淆,也给鉴别诊断带来很大困难。更何况,免疫病患者由于长期服用激素、免疫抑制剂,当同时合并结核感染时,使得症状更加不典型,比如:1)我们常见的结核中毒症状午后低热、盗汗等可能变得并不明显;2)激素的应用可使得结核的临床谱发生很大改变,比如结核更容易局限和包裹,一旦结核活动会更多见血行播散;3)活动性结核在使用激素后很可能短期内有效,给诊断带来更多困惑。我们的体会是,对于SLE新出现中枢神经系统症状,需要及时完善腰穿检查及增强MRI,若后者显示环形强化灶则对结核诊断有很强提示意义。当然,并非全部环形强化灶都是结核感染,如脑囊虫等寄生虫感染也会引起类似改变,但通常病灶小,中心可见囊蚴头节引起的点状钙化。非典型结核分枝杆菌、奴卡菌感染等也可以出现环形强化病灶。因此,积极取得病原学、病理学证据对明确诊断非常重要!
我们对于肺内感染与SLE肺部受累鉴别诊断的体会是:1)HRCT有较大帮助价值;2)病原、病理学资料非常重要。特别在患者一般情况可耐受时,要积极获取病理、病原学证据,为后续治疗指明方向;3)结核在中国发病率仍然很高,需要引起高度重视。
本例患者目前已转入结核病专科医院继续治疗,应用6联抗痨治疗及激素治疗后,左下肢肌力已恢复至2级。根据结核病专科医院医生的经验,通过早期积极抗结核治疗,中枢神经系统结核脓肿多数能够痊愈。我们期待着本例患者能够康复,走进门诊诊室随诊。
4.7 张弘医师(呼吸科)
分享此前我经管的一个类似病例,也是前面沈大夫提到的那例内科大查房病例。患者是青年男性,既往体健,因发热2个月于07年5月入院。入院后查胸部CT示肺内磨玻璃影,给予莫西沙星治疗后,患者体温正常,肺内磨玻璃影有所吸收。但治疗1周后再次发热,伴下肢肌力下降、感觉异常,很快出现截瘫,大小便失禁。MRI示颅内多个T1长T2信号,内可见结节影,增强后强化,增强后呈环形强化(图7)。该患者经TBLB检查,肺组织内发现干酪样坏死灶,抗酸染色阳性,确诊为血行播散性结核。经抗结核药物及地塞米松10 mg qd治疗一段时间后体温正常,神经系统症状体征改善。出院后继续抗痨治疗,半年后复查症状完全消失,肺内及颅内病变完全吸收。
从这2个病例引发思考,结核感染表现的多形性值得重视。大多数中枢神经系统结核感染为结核性脑脊髓膜炎,CSF出现典型“三高”表现:压力、细胞数和蛋白升高。但临床可见诸多非典型表现,如结核瘤、结核脓肿、变态反应性血管炎等,其中结核瘤患者的CSF常无明显变化。因此,对于CSF检查正常者,仍应警惕结核感染。中枢神经系统病变预后与治疗时间有关,故怀疑结核后应尽快对体内病灶进行病理及病原学检查,尽快确诊,从而争取治疗时间。此外,对结核病灶穿刺应注意加做结核菌培养,有时病理无阳性发现,病原学很可能提供有力证据。
4.8 沈敏医师(风湿免疫科)
非常感谢张弘大夫的病例分享。也非常感谢各科医生在本患者诊治过程中所给予的帮助!该患者肺穿刺活检组织已经送结核菌培养,正在等待结果。
4.9 张文医师(风湿免疫科)
感谢沈敏大夫提供的精彩病例和各位兄弟科室的精彩分析!
浅谈今天我的两方面收获:1)分析病情要结合临床综合分析。一个狼疮患者突然出现截瘫,通常首先考虑到狼疮横贯性脊髓炎。但本例患者狼疮的治疗相对正规,且无其他狼疮病情活动表现,突然出现截瘫,需考虑有无原发病以外的原因。经过病房的积极检查证实为结核感染,患者得到了及时诊断,这对治疗和预后非常重要。2)感染问题。感染与免疫病关系密切。首先,感染造成分子模拟状态可以诱发自身免疫反应;同时,自身免疫病患者在治疗过程中常常合并感染,给判断原发病活动还是感染造成很多困难,此时应开阔思路,根据临床表现,借助影像学、病理、病原学等检查进行综合分析。
再谈一下我对免疫病患者合并结核感染的体会。自身免疫病患者本身免疫功能紊乱,经激素、免疫抑制剂治疗后更可能发生细胞和体液免疫功能低下,因此结核感染后肉芽肿形成的能力比较弱,故部分患者结核肉芽肿表现可不明显,影像学上可以不典型。此外,我们也观察到在细胞、体液免疫功能较低的结缔组织病患者,即使存在活动性结核感染,TB-SPOT的结果也可呈现阴性,所以需要结合临床综合判断。
5 随诊
转当地结核病院治疗20 d后,患者家属返我院门诊随诊,告知患者在经过抗痨治疗数天后已拔除尿管,现已下地行走,已经出院回家继续抗结核治疗。
R 593.24+1;R 521.4
A
1001-6325(2012)01-0106-07
2011-04-11
2011-09-01
