共价固定芘衍生物荧光载体制备呋喃妥因传感器
2012-05-15焦晨旭韩媛媛邢宝研
焦晨旭, 韩媛媛, 邢宝研
(中北大学 理学院 山西 太原 030051)
0 引言
芳香稠环化合物芘及其衍生物是一类性能特异的电子学材料,对它们的发光性质及其他物理性质的研究是一个异常活跃的课题[1-5].芘及其衍生物在激光染料、生物荧光探针分子、液晶显示材料及电致发光器件等方面已有广泛应用.同时,芘的稳定性好、量子产率高,适合于用作荧光载体制备光化学传感器.在制作光化学传感器过程中,将氨基芘分子中引入一个端基双键,此双键能使此荧光分子聚合在硅烷化修饰过的玻片上.氨基芘与甲基丙烯酰氯反应生成甲基丙烯酰胺基芘(methylacryloylamidepyrene, MAAP),并将它与甲基丙烯酸羟丙酯在紫外光照射下共聚在硅烷化处理过的玻片上.实验发现光极膜的荧光能被一化合物猝灭,此猝灭可以用来测定相应的化合物.
呋喃妥因(nitrofurantoin, NFN),是一种用于治疗泌尿系统感染的药物,口服后约40%~50%随尿排出.测定NFN的方法有HPLC法[6-8]、极谱法[9]和伏安法[10]等.郭炬亮等[11]在醋酸纤维素中包埋芘丁酸制成一种NFN光纤传感器,除荧光载体可能流失外,也没有提供此传感器详细的分析特性.作者制得的基于MAAP的荧光传感器可用于NFN的测定,并得到满意的结果.
1 实验部分
1.1 仪器和试剂
Hitachi F-4500荧光分光光度计(日本日立公司), PHS-3C型精密pH计(上海精密科学仪器有限公司).
氨基芘和3-(三甲氧基硅烷基)甲基丙烯酸丙酯(TSPM)购自百灵威公司.不同pH 值的B-R缓冲溶液由浓度分别为0.04 mol/L的磷酸、乙酸、硼酸混合液与不同体积的0.2 mol/L氢氧化钠溶液混合得到.NFN(山东济南制药厂)用DMF配制成2.0×10-2mol/L储备液,NFN工作液由B-R缓冲液(pH为7.0)稀释制得.其他试剂均为分析纯,未经纯化,实验用水均为二次蒸馏水.
1.2 甲基丙烯酰胺基芘(MAAP)的合成
MAAP的合成路线如图1所示.
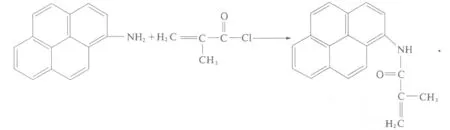
图1 甲基丙烯酰胺基芘的合成路线示意图Fig.1 Synthesis scheme of methylacryloylamidepyrene (MAAP)
具体合成步骤如下:称取1.0 g氨基芘,溶于15 mL无水DMF中,加入0.60 mL三乙胺.在剧烈搅拌下滴加0.40 mL甲基丙烯酰氯,滴完后,在室温下继续搅拌反应4 h.反应结束后过滤除去生成的沉淀,收集滤液,减压除去溶剂,得到灰褐色固体MAAP 1.10 g,产率为 72.6%,M+=285.
1.3 玻片的修饰
为了将MAAP通过共价键固定在玻片表面,在传感器载体玻片上应引入一个末端双键.通过文献[12]所述的硅烷化方法来修饰玻片,硅烷化步骤如下:将玻片依次浸入铬酸洗液中3 h,3%(体积分数)HF和10%(体积分数)H2O2中各20 min,用二次蒸馏水冲洗干净.在0.2 mL TSPM和2 mL 0.2 mol/L HAc-NaAc(pH为3.6)的缓冲溶液中,加入8 mL水并搅拌5 min,制成TSPM溶液.将玻片浸入此溶液3 h,再用二次蒸馏水冲洗,室温干燥备用.
1.4 光极膜的制备
MAAP光极膜的制备过程如下:将甲基丙烯酸羟丙酯(2.9 mL)、MAAP(10 mg)、安息香乙醚(400 mg)、丙烯酰胺(90 mg)、二苯甲酮(60 mg)和三乙醇胺(0.2 mL)在50 mL烧杯中混匀,用胶头滴管移取少量滴于干净的聚四氟乙烯板上.用硅烷化后的玻片盖于其上,紫外灯照射5 h后,分别用水和甲醇冲洗直至观察不到敏感物质的流失为止.
1.5 荧光测量
荧光测量在Hitachi F-4500荧光计上进行.光源为150 W氙灯,检测器为R918F红外敏感光电倍增管.激发和发射光谱狭缝均为2.5 nm.将制好的敏感膜放置在检测池中,用注射器将样品溶液注入检测池中,记录膜与样品溶液达到平衡时的荧光强度.每次测量后,用注射器注入空白溶液清洗MAAP光极膜,使它的荧光强度恢复到初始值,以备下一次测量.
2 结果与讨论
2.1 光谱特征
图2显示MAAP聚合膜与不同浓度(从上往下浓度依次为0, 4.0×10-5, 6.0×10-5, 8.0×10-5, 1.0×10-4,2.0×10-4mol/L)的NFN溶液(pH为7.0)接触时的荧光光谱.其发射光谱是将激发波长固定在366 nm处得到的.NFN能强烈猝灭MAAP聚合膜的荧光.用注射器将不同浓度的NFN溶液注入检测池中,记录膜与样品溶液达到平衡时的荧光强度.
2.2 猝灭机理和测量原理
若MAAP聚合物中的荧光载体与NFN形成n∶m型化合物,则有如下平衡:
mA (aq)+nB (membrane)=AmBn(membrane),
(1)
式中:A和B分别代表NFN和MAAP聚合物中的荧光载体.平衡常数表达式为
(2)
式中:K是复合物的表观形成常数.
由物料平衡可得:[B]0=[B]+n[AmBn] ,即
(3)
式中:[B]和[B]0分别是膜相中MAAP的游离浓度和总浓度.相对荧光强度比率(α)可定义为MAAP的游离浓度与总浓度的比值.实验中通过测量光极膜的相对荧光强度可测定α值,即
(4)
式中:F0是膜与空白液接触时的荧光强度;Fs是膜中MAAP完全被NFN络合时的荧光强度;F是膜与不同浓度的NFN接触时的相对荧光强度.
根据(2)~(4)式,K可表示为
(5)
α与样品溶液中NFN浓度的关系可表示为
(6)
(6)式可通过拟合曲线来估计复合物中MAAP和NFN的复合比.通过改变m∶n的比值和调整表观平衡常数K可使实验数据与拟合曲线相符合,拟合结果如图3中的曲线2所示.由图3可知,生成的NFN与MAAP光极膜应当形成了1∶1型复合物,即m=1,n=1,表观复合常数K值为1.1×104.

图2 MAAP膜传感器与不同浓度的NFN溶液接触时的发射光谱Fig.2 Fluorescence emission spectra of the MAAP sensor upon exposing to NFN solutions of different concentrations

图3 相对荧光强度比率与lg cNFN的关系Fig.3 Relative fluorescence intensity ratio as a function of lg cNFN
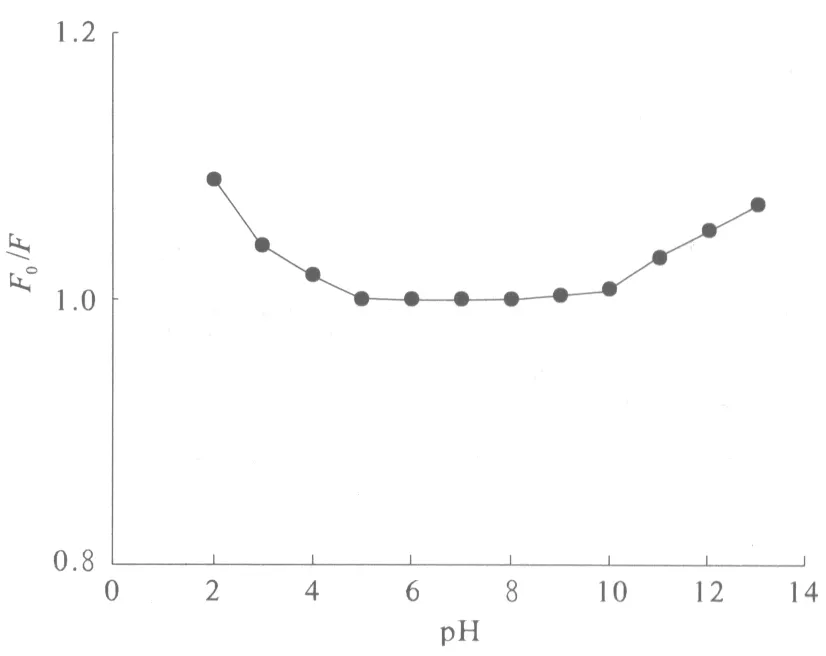
图4 酸度对光极膜荧光强度的影响Fig.4 Effect of pH on F0/F values
2.3 酸度影响
图4显示了酸度对光极膜荧光强度的影响.MAAP光极膜的荧光分子中含有羰基和亚氨基,易于极化且对酸性溶液敏感.为了使溶液的酸碱性对NFN的测定影响最小,实验选择pH为7的B-R 缓冲溶液为测试底液.
2.4 重现性、可逆性和响应时间
通过注射器注入1.0×10-5, 4.0×10-5,1.0×10-4mol/L的NFN溶液及空白B-R缓冲溶液,并记录其荧光强度来评估传感器的重现性与可逆性.对1.0×10-5,4.0×10-5,1.0×10-4mol/L的NFN溶液重复测定7次,荧光强度分别为270.6±0.5,227.1±0.6和162.2±0.4,空白溶液荧光强度为299.8±0.3(n=22,P=0.95),重现性和可逆性令人满意.洗回时间与浓度大小关系不大,无论浓度从低到高或从高到低变化,洗回恢复时间基本一样,约为60 s.由此可知,复合物的形成与离解是可逆的且无明显的滞后现象.
2.5 传感器的短期稳定性和寿命
为了研究此传感器的稳定性,将1.0×10-5mol/L的NFN溶液(pH为7)连续10 h通过传感器.每隔30 min记录一次光极膜的荧光强度,相对标准偏差为1.5%.光极膜的使用寿命可达2个月,活性组分共价固定在共聚物基质上能有效阻止其流失并延长传感器的寿命.
2.6 选择性
固定NFN浓度为1.0×10-5mol/L,加入0.001 mol/L各种无机物及有机物来研究干扰物对NFN荧光测定的影响,实验结果见表1.可以看出,一般的有机物和药物及无机盐所导致的荧光强度的相对偏差小于5%,但是当样品中存在硝基苯类化合物时,会在一定程度上猝灭光极膜的荧光信号而干扰测定.由于苦味酸和硝基苯类化合物一般不可能与NFN作为一种医用品在同一体系中共存,因此,此传感膜对NFN的测定有一定的选择性.

表1 干扰物对光极膜相对荧光强度的影响Tab.1 Effect of different interferents on the relative fluorescence intensity of the optode
2.7 定量基础和检测限
由于键合在光极膜上的MAAP与NFN之间形成的是1∶1型复合物,猝灭效率可通过Stern-Volmer方程得到:
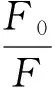
(7)
式中:F0和F分别是光极膜与空白溶液、NFN溶液接触时的荧光强度.将实验数据代入式(7),当NFN浓度在

表2 NFN在水样中的回收率Tab.2 The recovery test for NFN in water samples
8.0×10-7~1.0×10-4mol/L时,其校正方程为:F0/F=1.007+8 142.200cNFN(r=0.996 9),这可以作为传感器测定NFN的定量关系.用3倍于12次测定空白溶液的标准偏差来计算检测限,检测限约为6.0×10-7mol/L.NFN在水样中的回收率结果见表2,回收率为96.0%~104.0%,表明该传感器可用于水样中NFN的直接测定.
参考文献:
[1] Yamauchi A, Hayashita T, Nishizawa S, et al. Benzo-15-crown-5 fluoroionophore/γ-cyclodextrin complex with remarkably high potassium ion sensitivity and selectivity in water[J]. J Am Chem Soc, 1999, 121(10): 2319-2320.
[2] Yang J S, Lin C S, Hwang C Y. Cu2+-induced blue shift of the pyrene excimer emission: a new signal transduction mode of pyrene probes[J]. Org Lett, 2001, 3(6): 889-892.
[3] Nishizawa S, Kato Y, Teramae N. Fluorescence sensing of anions via intramolecular excimer formation in a pyrophosphate-induced self-assembly of a pyrene-functionalized guanidinium receptor[J]. J Am Chem Soc, 1999, 121(10): 9463-9464.
[4] Sahoo D, Narayanaswami V, Kay C M, et al. Pyrene excimer fluorescence: a spatially sensitive probe to monitor lipid-induced helical rearrangement of apolipophorin III[J]. Biochemistry, 2000, 39(22): 6594-6601.
[5] Crippa P R, Fornes J A, Ito A S. Photophysical properties of pyrene in interaction with the surface of melanin particles[J]. Colloids and Surfaces B: Biointerfaces, 2004,35(2): 137-141.
[6] Diaz T G, Martinez L L, Galera M M, et al. Rapid determination of nitrofurantoin, furazolidone and furaltadone in formulations, feed and milk by high performance liquid chromatography[J]. J Liquid Chromatography, 1994, 17(2): 457-475.
[7] Muth P, Metz R, Siems B, et al. Sensitive determination of nitrofurantoin in human plasma and urine by high-performance liquid chromatography[J]. J Chromatography A, 1996, 729(1/2): 251-258.
[8] Diaz T G, Cabanillas A G, Valenzuela M I A, et al. Determination of nitrofurantoin, furazolidone and furaltadone in milk by high-performance liquid chromatography with electrochemical detection[J]. J Chromatography A, 1997, 764(2): 243-248.
[9] Khodari M, Mansour H, El-Din H S, et al. Cathodic stripping voltammetry of the antibacterial drug (nitrofurantoin)[J]. Anal Lett, 1998, 31(2): 251-262.
[10] 王桂芬,朴元哲. 呋喃妥因的伏安法测定[J]. 厦门大学学报:自然科学版, 2000, 39(5): 653-656.
[11] 郭炬亮,陈坚. 用光纤化学传感器连续在线监测呋喃妥因肠溶片的体外溶出度[J]. 药物分析杂志,1997, 17(4): 228-231.
[12] Munkholm C, Walt D R, Milanovich F P, et al. Polymer modification of fiber optic chemical sensors as a method of enhancing fluorescence signal for pH measurement[J]. Anal Chem, 1986, 58(7): 1427-1430.
