氧化法处理含砷饮用水的研究进展
2012-05-07周文庆朱友利
周文庆,冯 燕,朱友利,邴 帅,齐 欣
(昆明理工大学建筑工程学院,云南 昆明 650500)
砷广泛分布于水、土壤和空气中,大多以硫化物形式夹杂在铜、铅、锡、镍、钴、锌、金等矿石中。在环境污染物中,砷是最毒的元素之一,美国疾病控制中心(CDC)和国际癌症研究机构(LARC)已经将砷确定为第一类致癌物质[1~4]。迄今为止,我国已发现多个饮水型地方性砷病区或高砷区,包括新疆、山西、内蒙古、宁夏、青海、安徽、北京、山东、四川、吉林、黑龙江、河南等[5]。
1993年世界卫生组织(WHO)率先将饮用水中砷标准限值由0.05 mg·L-1提高到0.01 mg·L-1。随后,欧盟、日本、美国也分别将各自的饮用水砷标准限值定为0.01 mg·L-1。我国的新标准《生活饮用水卫生标准》(GB 5749-2006)自2007年7月1日实施,将砷的标准限值从0.05 mg·L-1提高到不超过0.01 mg·L-1[6]。因此,常规水处理方法已不能有效满足除砷的要求,有必要采取更安全、有效的方法,最大程度地降低砷的危害,以保证饮用水安全。
1 水体中砷的存在形式和毒性
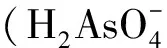
砷是一种有害物质,砷及其化合物的毒性与其存在形式和价态有很大的关系。砷的单质几乎无毒,As(Ⅲ)的毒性比As(Ⅴ)要大得多,砷及其化合物的毒性大小依次为:砷化三氢(As3-)>有机砷化物三氢衍生物(As3-)>无机亚砷酸盐(As3+)>有机砷化物(As3+)>氧化砷(As3+)>无机砷酸盐(As5+)>有机砷化物(As5+)>金属砷(As0)[10,11]。
虽然科研工作者对含砷饮用水的处理做了大量的研究,但依然还有很多问题需要改进,如工艺流程复杂、成本较高、易造成二次污染等。因此,研究含砷饮用水的处理方法及除砷材料,对含砷饮用水净化有着重大的现实意义,也是防治地方性砷中毒的关键。
2 含砷饮用水的处理方法
由于砷在水体中的主要存在形态是As(Ⅲ)和As(Ⅴ),所以饮用水除砷包括两种不同价态砷的去除。除砷方法可分为混凝沉淀法、吸附法、离子交换法、膜处理法、氧化法[9~18]。在水体处于中性范围(pH=7.0)时,As(Ⅲ)以中性分子形式存在,表现出电中性。因此,那些对As(Ⅴ)具有很好去除效果的方法,如混凝沉淀法、吸附法、离子交换法等对As(Ⅲ)的去除效果却较差。各种处理方法的原理、应用、优缺点如表1所示。

表1 含砷饮用水的处理方法
由表1可以看出,氧化法与其它处理方法相比,去除As(Ⅲ)的效果特别明显,是最具发展前景的含砷饮用水的处理方法。
3 氧化法处理含砷饮用水
3.1 原理
研究证实,As(Ⅴ)的毒性、流动性、溶解性远小于As(Ⅲ),因此利用氧化剂或微生物将As(Ⅲ)氧化成As(Ⅴ)是去除As(Ⅲ)的关键步骤,既可以提高去除效果,又可以降低毒性[19]。
氧化法分为单纯预氧化法、氧化吸附同步新技术、生物氧化法等。单纯预氧化法,尤其是高级氧化技术具有很好的氧化性,但是氧化后砷并不能得到有效去除且造价高;氧化吸附同步新技术由于零价铁[Fe(0)]分布广、价廉易得、对人体无毒害,且无需投加药剂,尤其适合于经济不富裕的广大农村地区;生物氧化法具有一般物化法无法比拟的优势,不仅环保,而且不需要添加任何化学药剂、能耗低、无二次污染,被公认为是最具发展前景的除砷方法。常见的化学氧化剂有Cl2、HClO、KMnO4、O3、·OH、H2O2等,由于不同氧化剂的氧化还原电位以及氧化反应机理不同(表2),因此,其对As(Ⅲ)的氧化速率和程度也各不相同。

表2 饮用水处理常用氧化剂的标准氧化还原电位
氧化吸附同步新技术是利用Fe(0)将As(Ⅲ)的氧化与去除结合起来的除砷方法。Fe(0)对As(Ⅲ)的氧化机理为:Fe(0)在水中与溶解氧反应生成中间产物[包括Fe(Ⅱ)、Fe(Ⅲ)、H2O2、·OH等],这些中间产物能将As(Ⅲ)氧化为As(Ⅴ),As(Ⅲ)、As(Ⅴ)再与Fe(Ⅲ)聚合体、水合氧化铁(HFO)产生共沉淀以达到去除目的[20~22]。反应式如下:
Fe(0)+1/2O2+2H2O-(RI)→Fe(Ⅱ)+H2O+2OH-
Fe(Ⅱ)+1/4O2+H2O-(RI)→Fe(Ⅲ)+ 1/2H2O+OH-
As(Ⅲ)+RI→As(V)
Fe(Ⅲ)+3H2O→Fe(OH)3+3H+
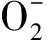
生物氧化法是利用生物表面存在的功能键(如羟基、氨基、羧基、硫基等)能够氧化、甲基化并与砷共价结合[13],使砷在生物体表面富集浓缩而达到除砷的目的。
3.2 研究进展
Pettine等[23]用H2O2对As(Ⅲ)进行氧化,发现pH值在7.5~10.3范围内,氧化率随着pH值的增大而升高。反应式如下:

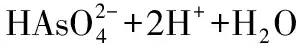
黄梓博等[24]研究了次氯酸钠预氧化与氯化铁混凝相结合的除砷效果。实验配制了0.05 mg·L-1、0.1 mg·L-1、0.5 mg·L-1等3种浓度的砷溶液,以氯化铁为混凝剂,投加量为12 mg·L-1,以次氯酸钠为氧化剂,氧化时间为1 min,投加量(mg有效氯·L-1)分别为0.1、0.2、0.5、1.0、1.5、2.0。结果发现,预氧化时间对除砷效果影响不大,砷去除率随次氯酸钠投加量的增加先急剧升高而后趋缓。
研究表明,当pH=6.3~8.3时,Cl2和KMnO4都能在40 s内将As(Ⅲ)迅速氧化为As(Ⅴ);即使水中存在的溶解性Mn2+、Fe2+、硫化物以及TOC会略微减缓氧化速率,完全氧化也能在1 min内完成。ClO2对As(Ⅲ)的氧化十分有限。O3在15 s内即能完成对As(Ⅲ)快速氧化,它是依靠水解产生·OH间接氧化As(Ⅲ);但·OH会因水中天然有机物的捕获而极大地减缓氧化反应的速率,因此O3不适于有机物污染严重的水体中As(Ⅲ)的氧化[25]。
苑宝玲等[26]研究了多功能高铁酸盐对饮用水中砷的去除效果。 当高铁酸盐(主要成分为K2FeO4)与砷浓度比为15∶1、pH值为5.5~7.5、氧化时间为10 min、絮凝时间为30 min时,水样中砷残留量可达国家饮用水卫生标准。
Driehaus等[27]以MnO2作为氧化剂,对As(Ⅲ)进行氧化。MnO2在环境中具有相当强的氧化性,并且能控制自然界和人体内铁、钴、铬和砷的移动性及其毒性。As(Ⅲ)与Mn(Ⅲ)、Mn(Ⅳ)在pH=7时的氧化还原反应式如下:
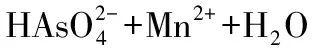
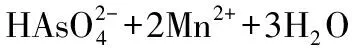
Kim等[28]分别用臭氧、纯氧(99.9%)和空气对As(Ⅲ)进行了氧化。结果表明,臭氧对As(Ⅲ)的氧化效果很好,能够在20 min内完成氧化,10 min内96%的As(Ⅲ)被氧化为As(Ⅴ);而纯氧和空气对As(Ⅲ)的氧化效果较差。
近年来,各种高级氧化技术(UV/自然光-TiO2[29]、Fenton试剂[30]、紫外光等)已成为As(Ⅲ)氧化的研究热点。Ementt等[31]采用紫外光照射,能很好地将As(Ⅲ)氧化为As(Ⅴ)。
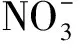
Leupin等[32]研究了Fe(0)对孟加拉国地下水中As(Ⅲ)的氧化和去除效果。实验用水为人工模拟地下水配水,As(Ⅲ)浓度为500 μg·L-1,pH=7.0。结果表明,出水中总砷浓度降至50 μg·L-1。
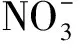
Bang等[34]研究发现,DO和pH值对Fe(0)除砷影响较大。在有氧条件下,Fe(0)对As(V)的去除速率大于As(Ⅲ),在pH=6.0、混合9 h时的As(V)去除率大于99.8%,As(Ⅲ)去除率为82.6%。当溶液中充入N2去除DO后As(Ⅲ)和As(V)的去除率都低于10%。这是由于高DO和低pH值都能加快Fe(0)的腐蚀速率,Fe(0)腐蚀产生的水合氢氧化铁与砷产生吸附共沉淀作用而去除水中的砷。
用于饮用水中过量砷去除的微生物菌种有:无色杆菌(Achromobacter)、假单胞菌(Pseudomonas)、棒状杆菌[35](Microbacteriumlacticum)、嗜酸硫杆菌(Thiobacillusacidophilus)、氧化亚铁硫杆菌(Thiobacillusferrooxydan)、模式种[36]Gallionella(Microbacteriumlactium)、锈色嘉利翁氏菌(Ferruginea)、砷氧化杆菌(Bacillusarsenoxidans)、赭色纤发菌(Leptothrixochracea)、赭曲霉菌(Leptothrix)和铁细菌[37](Gallionella)。
早在1918年,Green就从牲畜浸浴水中筛选出了一株砷氧化杆菌,能将As(Ⅲ)氧化为As(Ⅴ)。
Mokashi等[35]成功地将棒状杆菌固定化后氧化含As(Ⅲ)的地下水,然后用活性炭进行吸附,能有效地去除地下水中的As(Ⅲ)。Katsoyiannis等[17]研究了地下水中常见的微生物(如铁细菌和赭曲霉菌)对水中As(Ⅲ)的氧化能力,当水体中As(Ⅲ)含量为150~200 μg·L-1时,这些微生物能同时氧化Fe2+和As(Ⅲ),生成的铁氧化物能通过吸附共沉淀作用有效地去除水中的砷,去除率高达95%。Zouboulis等[38]通过X-ray光谱仪,进一步分析出As(Ⅲ)被铁细菌去除的机理是As(Ⅲ)被氧化成As(Ⅴ)后得以降解。Suhendrayatna等[37]用小球藻对砷的生物转化进行了研究,测得细胞对砷的富集最高可达610 μg·g-1。美国伊利诺伊大学(University of Illinois)的研究人员建立了一种通过细菌检测预防砷污染的简易方法。其原理是细菌能将水中的硫酸盐还原为硫化物,使硫酸盐含量减少,利用硫化物对砷的沉淀作用,从而有效地去除水中的砷;而水样中硫酸盐含量与砷浓度成反比,因此,通过检测水中硫酸盐的含量可以间接地反映水中的砷含量。Leblanc等[39]发现氧化亚铁硫杆菌和乳酸硫杆菌能有效地将As(Ⅲ)氧化为As(V)。郑凤英等[40]研究了超富集植物蜈蚣草对水中As(Ⅲ)的吸附实验。以50 mg经2 mol·L-1HCl洗脱处理后的蜈蚣草粉末为吸附剂,在吸附时间为15 min、pH=2时,蜈蚣草对50 mL 20 g·L-1As(Ⅲ)溶液的As(Ⅲ)去除率为86.1%。
4 展望
随着社会的不断发展,人们对饮用水水质也提出了更高的要求,这就给饮用水除砷方法带来了新的挑战。不同除砷方法都有各自的优缺点,因此在选择除砷方法时要综合考虑原水水质、处理成本、地域差异、经济发展水平及环保性等因素。传统的各种物理化学法对As(Ⅲ)的去除效果较差;氧化法无需投加药剂、对As(Ⅲ)的氧化效率高、去除效果好,虽然单纯预氧化法需要额外投加氧化剂、处理流程长,但生物法节能、环保。今后,氧化法处理含砷饮用水的研究重点应放在以下几方面:研发廉价、高效、无毒的氧化剂;进行具有氧化能力的菌种的研究与生物除砷技术的开发;研发廉价、易于取得或制备、吸附容量大、再生能力强的新型除砷吸附剂;各种除砷方法与氧化法的联合使用等。
参考文献:
[1] WHO.Arsenic in drinking water[S].2001.
[2] 杨振林,丘宝国.砷元素与砷污染[J].化学教学,1999,(6):27-28.
[3] 陈敬军,蒋柏泉,王伟.除砷技术现状与进展[J].江西化工,2004,(2):1-4.
[4] 刘姣,孟庆强,易青.水源水中三价砷的去除实验研究[J].广东化工,2009,36(6):141-142.
[5] 沈雁峰,孙殿军,赵新华,等.中国饮水型地方性砷中毒病区和高砷区水砷筛查报告[J].中国地方病学杂志,2005,24(2):172-175.
[6] GB 5749-2006,生活饮用水卫生标准[S].
[7] 方宇,江桂斌,何滨,等.砷形态分析中的样品前处理方法[J].环境污染治理技术与设备,2002,3(2):46-52.
[8] 杨宏,尹瑞,张杰.生物除锰滤池对砷(Ⅲ)的去除效果研究[J].中国给水排水,2006,22(7):85-88.
[9] 黄鑫,高乃云,刘成,等.饮用水除砷工艺研究进展[J].净水技术,2007,26(5):37-41.
[10] 王薇,徐炎华.水体中砷污染和治理概况[J].微量元素与健康研究,2005,22(5):59-61.
[11] 梁美娜.铁、铝及其复合氢氧化物去除水中砷(Ⅴ)的吸附研究[D].桂林:桂林工学院,2006.
[12] Gu Zhi-mang,Fang Jun,Deng Bao-ling.Preparation and evaluation of GAC-based iron-containing adsorbents for arsenic removal[J].Environmental Science & Technology,2005,39(10):3833-3843.
[13] 李大成.国家饮用水标准与砷、镉去除技术[J].污染防治技术,2009,22(2):74-76.
[14] 陈雪梅,胡锋平.含砷饮用水处理技术综述[J].江西化工,2009,(4):42-45.
[15] Korngold E,Belayev N,Aronov L.Removal of arsenic from dr-inking water by anion exchangers[J].Desalination,2001,141(1):81-84.
[16] 李晓波.饮用水除砷技术研究进展[J].环境工程学报,2009,3(5):777-781.
[17] Katsoyiannis I A,Zouboulis A I.Application of biological processes for the removal of arsenic from groundwater[J].Water Research,2004,38(1):17-26.
[18] 王华,吕锡武.饮用水处理技术现状及研究进展[J].江苏环境科技,2004,17(2):41-45.
[19] Ferguson J F,Gavis J.A review of the arsenic cycle in natural waters[J].Water Research,1972,6(11):1259-1274.
[20] 张伟.零价铁去除原水中砷的研究[D].昆明:昆明理工大学,2010.
[21] Leupin O X,Hug S J,Badruzzaman A B.Arsenic removal from Bangladesh tube well water with filter columns containing zero-valent iron filings and sand[J].Environmental Science & Technology,2005,39(20):8032-8037.
[22] Kanel S R,Manning B,Charlet L,et al.Removal of arsenic(Ⅲ) from groundwater by nanoscale zero-valent iron[J].Environmental Science & Technology,2005,39(5):1291-1298.
[23] Pettine M,Campanella L,Millero F J.Arsenic oxidation by H2O2in aqueous solutions[J].Geochimica et Cosmochimica Acta,1999,63(18):2727-2735.
[24] 黄梓博,林洁玲.次氯酸钠预氧化与氯化铁混凝相结合除砷效果研究[J].净水技术,2007,26(2):25-27.
[25] 姚娟娟,高乃云,夏圣骥,等.饮用水除砷技术研究新进展[J].工业用水与废水,2007,38(4):1-5.
[26] 苑宝玲,李坤林,邓临莉,等.多功能高铁盐去除饮用水中砷的研究[J].环境科学,2006,27(2):281-284.
[27] Driehaus W,Seith R,Jekel M.Oxidation of arsenate(Ⅲ) with manganese oxides in water treatment[J].Water Research,1995,29(1):297-305.
[28] Kim M J,Nriagu J.Oxidation of arsenite in groundwater using ozone and oxygen[J].Sci Total Environ,2000,247(1):71-79.
[29] Ferguson M A,Hering J G.TiO2-Photocatalyzed As(Ⅲ) oxidation in a fixed-bed,flow-through reactor[J].Environmental Science & Technology,2006,40(13):4261-4267.
[30] Krishna M V B,Chandrasekaran K,Karunasagar D,et al.A combined treatment approach using Fenton′s reagent and zero valent iron for the removal of arsenic from drinking water[J].Journal of Hazardous Materials,2001,84(2-3):229-240.
[31] Ementt M T,Khoe G H.Photochemical oxidation of arsenic by oxygen and iron in acidic solutions[J].Water Research,2001,35(3):649-656.
[32] Leupin O X,Hug S J.Oxidation and removal of arsenic(Ⅲ) from aerated groundwater by filtration through sand and zero-valent iron[J].Water Research,2005,39(9):1729-1740.
[33] Tyrovola K,Nikolaidis N P,Veranis N,et al.Arsenic removal fr-om geothermal waters with zero-valent iron——Effect of temperature,phosphate and nitrate[J].Water Research,2006,40(12):2375-2386.
[34] Bang S,Korfiatis G P,Meng X G.Removal of arsenic from water by zero-valent iron[J].Journal of Hazardous Materials,2005,121(1-3):61-67.
[35] Mokashi S A,Paknikar K M.Arsenic(Ⅲ) oxidizing microbacterium lacticum and its use in the treatment of arsenic contaminated groundwater[J].Letters in Applied Microbiology,2002,34(4):258-262.
[36] Weeger W,Lievremont D,Perrret M,et al.Oxidation of arsenite to arsenate by a bacterium isolated from an aquatic environment[J].Biometals,1999,12(2):141-149.
[37] Suhendrayatna,Ohki Akira,Kuroiwa Takayoshi,et al.Arsenic compounds in the freshwater green microalgaChlorellavulgarisafter exposure to arsenite[J].Applied Organometallic Chemistry,1999,13(2):127-133.
[38] Zouboulis A I,Katsoyiannis I A.Recent advances in the bioremediation of arsenic-groundwaters[J].Environment International,2005,31(2):213-219.
[39] Leblanc M,Achard B,Personne J-Ch.Arsenic-rich bacterial mats from acidic mine waters[A].In:Pasava,Kribek and Zak eds.Mineral Deposits:From their origin to their environmental impacts[C].Carnoules,France,1995:127-130.
[40] 郑凤英,李顺兴,韩爱琴,等.超富集植物蜈蚣草对水中As(Ⅲ)吸附行为的研究[J].分析科学学报,2006,22(4):401-405.
