重组人粒细胞巨噬细胞刺激因子栓在大鼠和Beagle犬中的免疫原性
2012-04-28蔡永明张春云申文晋张宗鹏
蔡永明 张春云 申文晋 李 铭 姜 凌 张宗鹏*
(1.天津药物研究院天津市新药安全评价研究中心,天津 300301;2.天津中医药大学研究生院药物分析学专业,天津 300193;3.天津药物研究院释药技术与药代动力学国家重点实验室,天津 300193)
重组人粒细胞巨噬细胞集落刺激因子(recombi-nant human granulocyte-macrophage colony-stimulating factor,rhGM-CSF)作用于造血祖细胞,促进其增生和分化[1],增强单核细胞抗原递呈能力[2],提高粒细胞和单核细胞抗体依赖细胞的细胞毒[3]。rhGM-CSF临床用于治疗肿瘤病人因放射治疗或化学治疗引起的白细胞减少症[4];单独或与抗真菌药联合使用可增强抗菌作用[5];具有提高免疫、抗炎和促进创面愈合功能[6-7]。rhGM-CSF栓经阴道局部给药,拟治疗宫颈糜烂。为非临床安全性评价的确切性提供依据,本课题组进行了大鼠和Beagle犬的免疫原性试验。
1 材料和方法
1.1 试验药物
重组人粒细胞巨噬细胞刺激因子栓,长春金赛药业股份有限公司提供。规格:①1.5 g/栓(药物含量分别为0、0.87、3.46 和13.84 mg/g),批号20060401,用于大鼠给药;②8.0 g/栓(药物含量分别为0、0.7、2.8和11.2 mg/g),批号:20060510,用于 Beagle犬给药。4℃保存。
1.2 检测抗rhGM-CSF抗体的试剂
包被抗原为rhGM-CSF(HPLC纯度:99.4%,浓度:1 mg/mL,批号:CG20050901)长春金赛药业股份责任公司提供。大鼠免疫球蛋白(immunoglobulin G,IgG)和犬IgG由军事医学科学院微生物流行病研究所提供。辣根过氧化物酶标记的羊抗大鼠IgG,美国SBA公司产品;辣根过氧化物酶标记的羊抗犬IgG,美国Rockland Immunochemicals公司产品。酶反应底物3,3',5,5'-四甲基联苯胺(3,3',5,5'-tetramethylbenzidine,TMB)和噻唑蓝(MTT)为Sigma产品。TF-1(人红白血病细胞)由中国药品生物制品检定所提供。RPMI 1640培养液为美国Gibco产品。96孔酶标板和细胞培养板,均为美国Costar产品。
1.3 试验用主要仪器
550型酶标微板读数仪,美国Bio-red公司产品。Columbus洗板机,奥地利TECAN公司产品。Thermo Scientific Sorvall ST 16R低温离心机,美国Thermo公司产品。DKB-501A型恒温水槽,上海精宏实验设备有限公司产品。
1.4 实验动物
①雌性SD大鼠(试验开始体质量125~145 g)20只,北京维通利华实验动物技术有限公司提供,实验动物许可证号:SCXK(京)2002-0003,饲养环境为屏障系统。②雌性Beagle犬(6~8 kg)24只,安徽阜阳市维光实验动物中心提供,实验动物许可证号:SCXK(皖)06-001,全封闭观察室,单笼饲养。本试验在优良规范(good laboratory practice,GLP)实验室完成。
1.5 受检血清样本
1.5.1 大鼠血清
rhGM-CSF栓大鼠长期毒性试验设0(赋形剂对照组)、0.24、0.96及3.84 mg/kg 4个组,本试验是对长期毒性试验中每组的5只大鼠定期跟踪监测抗体,包括给药1、2、3个月和恢复1个月血清样本。大鼠眼静脉丛取血约0.8 mL,制备血清,-20℃保存。
1.5.2 Beagle犬血清
rhGM-CSF栓Beagle犬长期毒性试验设0(赋形剂对照组)、rhGM-CSF栓 0.07、0.28和1.12 mg/kg 4个组,每组6只动物。于给药前、给药期1个月、3个月及恢复期1个月从前肢隐静脉采血约2 mL,制备血清,-20℃保存。
1.6 间接ELISA法测定抗rhGM-CSF抗体
将rhGM-CSF(抗原)用 pH 9.6的 Na2CO3-NaHCO3溶液稀释成10 μg/mL浓度,包被于96孔酶标板上,每孔100 μL,4℃过夜。用2% 牛血清白蛋白(bovine serum albumin,BSA)封闭液37℃封闭2 h后,各孔加入100 μL经10倍系列稀释的待检血清样品;同时设阳性和阴性对照孔,37℃孵育1 h。洗涤后每孔加100 μL辣根过氧化物酶标记的羊抗大鼠IgG(1:10万)或羊抗犬IgG(1:30万),37℃再孵育1 h。洗涤后各孔加100 μL酶反应底物TMB,37℃反应20~25 min。用2 mol/L硫酸50 μL终止反应,在酶标微板读数仪上读取各孔450 nm处的吸光值。
1.7 体外测活法鉴定抗体的中和活性
采用TF-1细胞(人红白血病细胞)/MTT(噻唑蓝)比色法检测抗体的中和活性。TF-1细胞系为rh-GM-CSF依赖型细胞,只有在rhGM-CSF存在情况下才可存活,若血清产生抗rhGM-CSF的中和抗体,中和了rhGM-CSF活性,则TF-1细胞不能存活。据此原理检测血清产生抗rhGM-CSF抗体的中和活性。在96孔细胞培养板中,每孔分别加入用基础培养液稀释浓度至2 ng/mL rhGM-CSF(50 μL),分别取经系列稀释后的血清样品50 μL,加入上述含有2 ng/mL rhGMCSF 96孔板培养板中,振荡混合,37℃,作用1 h。然后各孔加入50 μL TF-1细胞悬液(4.0×105/mL),37℃,5%CO2培养 40~48 h。每孔再加入 20 μL MTT溶液,继续培养4 h。最后加入100 μL裂解液,混匀后,在酶标微板读数仪上读取各孔570 nm处的吸光度(参比波长为630 nm)。
1.8 阳性结果的判断标准及统计学方法
以同期赋形剂对照组动物血清标本所测得吸光值的2.1倍作为产生抗体的阈值,凡给药后血清标本测得的吸光值大于或等于阈值者,判定为阳性。各剂量组动物血清中所测的结合抗体和中和抗体的试验数据均以抗体滴度对数的均数±标准差()表示,满足正态性分布数据用单因素方差分析法进行组间比较,同时进行方差齐性检验(若方差齐性,用LSD法;方差不齐性,用Tamhane's T2法)。不满足正态性的数据用非参数检验中的多组秩和检验(Kruskal-Wallis H法)。计数资料采用交叉表χ2检验,Fisher单侧精确检验(总频数N<40)。采用SPSS 17.0统计软件进行统计学分析。
2 结果
2.1 ELISA法检测结果
2.1.1 大鼠血清样本测定结果
抗体监测试验结果表明,在大鼠重复阴道给予rhGM-CSF栓3个月的长期毒性试验中,从给药1个月(以下简称M1)起一直持续到恢复期结束(以下简称rM1),0.24、0.96和3.84 mg/kg 3个剂量组动物血清中均能检测到抗rhGM-CSF的抗体。在给药2个月(以下简称M2)后抗体强度有逐渐增强的趋势,并在给药期3个月(以下简称M3)至恢复期内抗体强度变化不大。在给药的第1个月和第2个月时,高剂量组动物血清所检测到的抗体滴度明显高于低剂量组和中剂量组,差异有统计学意义(P<0.05),低、中剂量组差异无统计学意义。结果详见表1、表2和图1。

表1 大鼠重复阴道给予rhGM-CSF栓后产生抗体的动物比例(产生抗体动物数/总动物数)Tab.1 The incidence of anti-rhGM-CSF antibodies in rats vaginally administered rhGM-CSF suppository(ratio of positive to total animals)
表2 ELISA法测定大鼠重复阴道给予rhGM-CSF栓后抗rhGM-CSF结合抗体的形成Tab.2 The titer of anti-rhGM-CSF binding antibodies in the sera of the rats were determined during the treatment and recovery periods by ELISA method (,n=5)

表2 ELISA法测定大鼠重复阴道给予rhGM-CSF栓后抗rhGM-CSF结合抗体的形成Tab.2 The titer of anti-rhGM-CSF binding antibodies in the sera of the rats were determined during the treatment and recovery periods by ELISA method (,n=5)
*P <0.05 vs group of 3.84 mg/kg;M1:treated with rhGM-CSF for one month;M2:treated with rhGM-CSF for two months;M3:treated with rhGM-CSF for three months;rM1:recovery period for one month;rhGMCSF:recombinant human granulocyte-macrophage colony-stimulating factor.
Doses(mg·kg_-1)_____________Log titer of treatment M1 M2 M3____Log titer of recovery rM1 0————0.24 2.00 ±0.00* 2.60 ±0.55 2.60 ±0.55 2.40 ±0.89 0.96 1.80 ±0.84* 2.20 ±1.10*2.40 ±0.89 2.60 ±0.55___3.84______3.00 ±0.00____3.60 ±0.55___3.40 ±0.8____________9_3.00±0.00
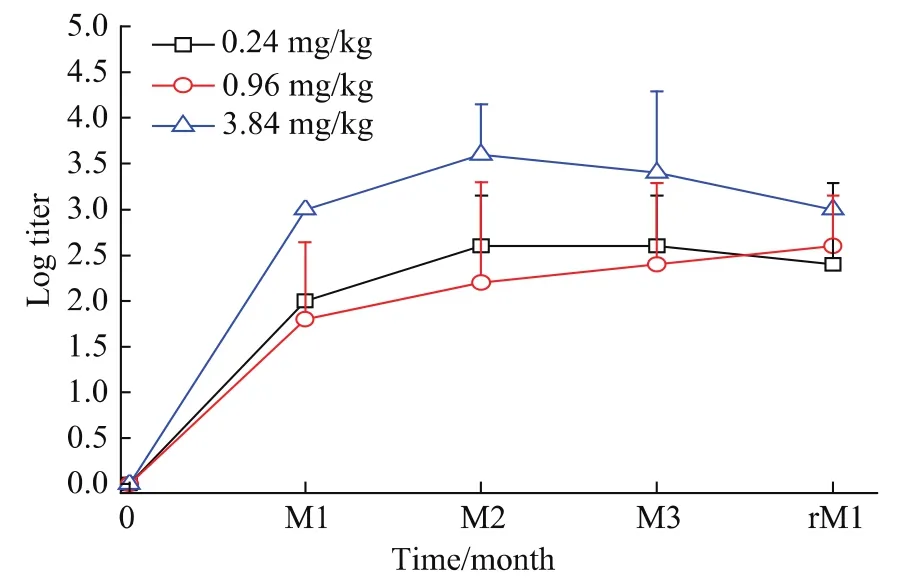
图1 ELISA法测定大鼠阴道给药血清中产生抗rhGM-CSF结合抗体滴度(,n=5)Fig.1 The titer of anti-rhGM-CSF binding antibodies in the sera of the rats were determined during the treatment and recovery periods using ELISA(,n=5)
2.1.2 Beagle犬血清样本测定结果
Beagle犬各剂量组在给药前、给药后1个月和3个月(停药次日)及恢复期1个月,各剂量组动物血清采用ELISA方法所测得的吸光值均低于同期赋形剂对照组抗体的阈值,表明血清中没有检测到抗rhGMCSF的结合抗体。
2.2 中和抗体检测结果
对采用ELISA方法检测出产生结合抗体的血清样品,进行抗体中和活性测定,以观察所产生的结合抗体是否为中和抗体。体外活性测定结果显示,各剂量组在给药1个月开始就有部分动物产生中和抗体;高剂量组在给药2个月开始全部动物都产生中和抗体,一直持续到恢复期结束,中和活性滴度(滴度的对数)在1.80~2.05间(滴度的对数);低、中剂量组则在恢复期结束才全部产生中和抗体;恢复期结束三个剂量组中和抗体滴度(滴度的对数)范围在1.02~2.05间。结果详见表3、表4和图2。

表3 大鼠重复阴道给予rhGM-CSF栓血清中产生中和抗体的比例(产生中和抗体动物数/总动物数)Tab.3 The incidence of neutralizing antibodies in rats vaginally administered rhGM-CSF suppository(ratio of positive to total animals)
M1:treated with rhGM-CSF for one month;M2:treated with rhGMCSF for two months;M3:treated with rhGM-CSF for three months;rM1:recovery period for one month;rhGM-CSF:recombinant human granulocyte-macrophage colony-stimulating factor.
表4 rhGM-CSF栓大鼠给药不同时期血清中抗体的中和活性滴度Tab.4 The titer of neutralizing antibodies in the sera of the rats were determined during the treatment and recovery periods(,n=5)

表4 rhGM-CSF栓大鼠给药不同时期血清中抗体的中和活性滴度Tab.4 The titer of neutralizing antibodies in the sera of the rats were determined during the treatment and recovery periods(,n=5)
*P <0.05 vs group of 0.96 mg/kg;#:P <0.05 vs group of vs 0.24 mg/kg;M1:treated with rhGM-CSF for one month;M2:treated with rh-GM-CSF for two months;M3:treated with rhGM-CSF for three months;rM1:recovery period for one month;rhGM-CSF:recombinant human granulocyte-macrophage colony-stimulating factor.
Doses/(mg·kg_-1)Log titer of treatment M1 M2 M3 Log titer of recovery rM1 0 0 0 0 0 0.24 0.421 ±0.404 1.806 ±1.021 1.445 ±0.252 1.024 ±0.457 0.96 0.120 ±0.269 0.843 ±0.779 0.843 ±0.779 1.626 ±0.269#_3.84___0.602 ±0.476 2.047 ±0.495*1.806 ±0.476*2.047 ±0.5__38#
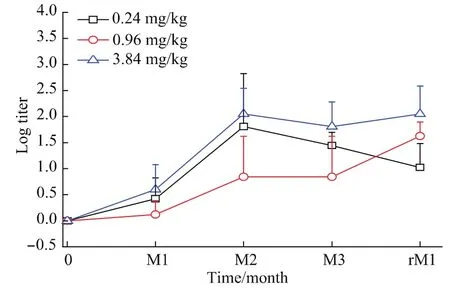
图2 rhGM-CSF栓大鼠给药不同时期血清中和抗体滴度Fig.2 The titer of neutralizing antibodies in the sera of the rats were determined during the treatment and recovery periods using bioassay method(,n=5)
3 讨论
rhGM-CSF是一种基因工程药物,其主要作用是刺激粒细胞和单核巨噬细胞的成熟,促进成熟细胞向外周血释放[8],rhGM-CSF可增加机体免疫力,对抗炎性反应[9]。rhGM-CSF作为重组蛋白或多肽类生物技术药物对非同源的动物而言具有免疫原性,所产生的抗体是否有中和活性视药物和动物而异[10]。在重复给药的毒性试验中,如果出现具有中和活性的抗体会减弱药物的药理作用,干扰毒性反应;而抗原抗体复合物的产生又可能会出现新的毒性反应[11-12]。因此监测抗体的产生和中和活性的强弱十分重要。大鼠重复阴道给予rhGM-CSF栓3个月的试验中,血清中能检测到抗rhGM-CSF的抗体,并且所检测到的抗体具有中和活性,表明rhGM-CSF对大鼠具有较强的免疫原性。该免疫原性会减弱药物的活性以及与活性相关的毒性,可能会影响rhGM-CSF毒性的判断。所产生的抗原抗体免疫复合物是否会在肾脏产生沉积,宜进一步用免疫组化方法来证实[13]。在Beagle犬体内未检测到抗rhGM-CSF的抗体产生,采用Beagle犬作为实验动物模型进行长期毒性试验以评价rhGMCSF栓重复给药毒性,会更能反映药物毒性暴露,为临床合理用药提供依据。
[1]Tarr P E,Lin R,Mueller E A,et al.Evaluation of tolerability and antibody response after recombinant human granulocyte-macrophage colony-stimulating factor(rhGM-CSF)and a single dose of recombinant hepatitis B[J].Vaccine,1996,14(13):1199-1204.
[2]Hu X,Sun H,Han C,et al.Topically applied rhGM-CSF for the wound healing:a systematic review [J].Burns,2011,37(5):729-741.
[3]Jaschke E,Zabernigg A,Gattringer C.Recombinant human granulocyte-macrophage colony-stimulating factor applied locally in low doses enhances healing and prevents recurrence of chronic venous ulcers [J].Int J Dermatol,1999,38(5):380-386.
[4]Zhang X R,Zheng Y,Jin T,et al.Formulation of sustained-release microspheres of granulocyte macrophage colony stimulating factor by freezing-induced phase separation with dextran and encapsulation with blended polymers[J].J Microencapsul,2011,28(8):743-751.
[5]Cianfarani F,Tommasi R,Failla C M,et al.Granulocyte/macrophage colony-stimulating factor treatment of human chronic ulcers promotes angiogenesis associated with de novo vascular endothelial growth factor transcription in the ulcer bed [J].Br J Dermatol,2006,154(1):34-41.
[6]Spitler L E,Weber R W,Allen R E,et al.Recombinant human granulocyte-macrophage colony-stimulating factor(GM-CSF,sargramostim)administered for 3 years as adjuvant therapy of stagesⅡ (T4),Ⅲ,and IV melanoma[J].J Immunother,2009,32(6):632-637.
[7]Wadhwa M,Skog A L,Bird C,et al.Immunogenicity of granulocyte-macrophage colony-stimulating factor(GM-CSF)products in patients undergoing combination therapy with GM-CSF[J].Clin Cancer Res,1999,5(6):1353-1361.
[8]Leal D P,Souto R B,Schutkoski R,et al.Granulocyte-macrophage colony stimulating factor:Evaluation of biopharmaceutical formulations by stability-indicating RP-LC method and bioassay[J].Biologicals,2011,39(4):211-216.
[9]Grossberg S E,Kawade Y.The expression of potency ofneutralizing antibodies for interferons and other cytokines[J].Biotherapy,1997,10(1):93-98.
[10]Wadhwa M,Bird C,Fagerberg J,et al.Production of neutralizing granulocyte-macrophage colony-stimulating factor(GM-CSF)antibodies in carcinoma patients following GMCSF combination therapy [J].Clin Exp Immunol,1996,104(2):351-358.
[11]吕秋军,高月,陶来宝,等.重组人碱性成纤维细胞生长因子在猕猴和大鼠中中和抗体的产生及其在肾脏沉积[J].军事医学科学院院刊,1999,23(3):168-171.
[12]吴春叶,齐文成,李力,等.系统性红斑狼疮患者血清GM-CSF及其抗体的变化及意义[J].华北国防医药,2009,21(1):11-14.
[13]Ragnhammar P,Wadhwa M.Neutralising antibodies to granulocyte-macrophage colony stimulating factor(GMCSF)in carcinoma patients following GM-CSF combination therapy[J].Med Oncol,1996,13(3):161-166.
