抗精神病药致急性静坐不能的研究现状
2012-04-17于相芬孙振晓孙波
于相芬 孙振晓 孙波
(山东省临沂市精神卫生中心精神科,山东 临沂 276005)
抗精神病药致急性静坐不能的研究现状
于相芬 孙振晓 孙波
(山东省临沂市精神卫生中心精神科,山东 临沂 276005)
【摘要】抗精神病药致静坐不能是急性锥体外系副反应的一种类型。本文对抗精神病药所致急性静坐不能的发生率、危险因素、病理机制、临床表现、诊断标准、鉴别诊断、治疗等作一综述,以提高临床认识。
【关键词】抗精神病药;治疗应用/副作用;急性静坐不能
静坐不能这一术语首先由Haskove于1902年用来描述2例伴有不安宁及不能静坐症状的病人,直到50年代,静坐不能才被用于描述抗精神病药引起的运动性不安宁[1]。抗精神病药所致静坐不能是急性锥体外系副反应的一种类型,以主观上想活动和客观上不停息的运动状态为特征[2]。常给病人造成极大痛苦,严重者可发生暴力行为及自杀等意外,它有时与精神症状加剧难以鉴别,若被误认为是精神症状恶化,盲目加大抗精神病药剂量,可导致不安症状恶化,甚至出现自杀意外,也可导致病人对治疗的依从性差,从而引起病情复发[3]。因此,正确识别和处理抗精神病药所致急性静坐不能至关重要。为了提高临床医师的认识,现对抗精神病药致急性静坐不能的研究近况作一综述。
1 抗精神病药所致急性静坐不能的发生率
抗精神病药致急性静坐不能的发生率,不同研究差异很大。文献报道,典型抗精神病药的发生率从 8% ~76%不等,Braude等报道发生率为25%,Ayd报道发生率为 21.2%[4]。Lindström等[5]进行的多中心、双盲、瑞莫必利与氟哌啶醇对照研究中发现瑞莫必利所致静坐不能的发生率为36%,而氟哌啶醇为 57%。Claghorn等[6]在氯氮平与氯丙嗪双盲对照研究中发现氯氮平发生率为 6.7%,而氯丙嗪为 5.3%。Cohen等[7]进行的氯氮平与典型抗精神病药对照研究中,以Chouinard锥体外系副反应评定量表得分≥3分作为诊断标准,氯氮平组静坐不能发生率为39%,而对照组为 45%,但重度静坐不能者(量表得分≥6分)氯氮平组为9%,对照组为 14%。Halstead等[8]报道在抗精神病药急性期及维持治疗中,发生率为 20% ~25%。孙振晓等[9]对 242例精神分裂症患者应用抗精神病药治疗期间静坐不能的发生率进行研究,以修订的Simpson锥体外系反应量表进行评定,结果发现发生率为21.49%。在 CATIE(The clinical antipsychotic trials of intervention effectiveness)试验中,应用Barnes静坐不能评定量表(BAS)评定急性静坐不能的发生率,结果显示,第二代抗精神病药(奥氮平、喹硫平、利培酮、齐拉西酮)静坐不能的发生率为26%~35%,而中等效价的第一代抗精神病药奋乃静发生率为 35%[10]。在欧洲首发精神分裂症试验中,急性静坐不能的发生率分别为:氨磺必利 16%,奥氮平 10%,喹硫平 13%,齐拉西酮 28%[11]。造成发生率差异的原因可能与调查人群、评定方法、药物种类、剂量及加药速度不同等因素有关。
2 抗精神病药所致急性静坐不能的危险因素
2.1 年龄
有关年龄与静坐不能发生的关系结果不一。Aguilar等[12]报道年龄小发生静坐不能的危险性大。朱少毅等[13]研究发现在首次发病服用利培酮的精神分裂症患者中,发生静坐不能组年龄(22.35±2.64)岁,明显小于未发生组 (31.82± 4.26)岁。孙振晓等[9]的研究也得出同样结论。而Braude等[14]、Sachdev等[15]发现发生组与未发生组年龄无显著性差异。
2.2 精神疾病诊断
Gardos等[16]报道抑郁症患者即使在应用小剂量抗精神病药时,静坐不能评分也较躁狂症及精神分裂症患者高,提示抑郁症患者发生静坐不能的可能性大。
2.3 精神疾病的严重程度
Aguilar等[12]报道病情严重者发生静坐不能的危险性大。朱少毅等[13]研究发现,发生静坐不能组应用药物治疗前功能大体评定量表(GAS)分值明显低于未发生组,而阳性和阴性症状量表(PANSS)分值高于未发生组,支持Aguilar等的观点。而Halstead等[8]、孙振晓等[9]未发现静坐不能的发生与疾病严重程度有关。
2.4 药物相关因素
2.4.1 药物效价高效价药物发生率高。Ayd[17]认为随着效价的增高,在用药早期及低剂量时便可发生静坐不能。孙振晓等[9]研究也发现高效价抗精神病药发生静坐不能的危险性大。
2.4.2 药物剂量药物剂量是静坐不能发生的重要影响因素。McClelland等[18]研究发现,在高剂量时发生率为22%,而标准剂量时为 9%。van Putten等[19]、孙振晓等[9]的研究也得出同样结论。
2.4.3 增加剂量的速度增加剂量的速度是静坐不能发生的又一重要因素。Braude等[14]研究发现在入院10天内加药剂量大者,静坐不能发生率明显增加。Sachdev等[15]也有类似发现。
2.4.4 非口服给药临床经验提示非口服给药更可能引起静坐不能。可能与下列因素有关:非口服给药通常为高效价药物;非口服给药常用于急性期处理,血药浓度从零或低水平快速增加;非口服给药不经过肝脏首过效应导致血药浓度快速增加[4]。
2.4.5 药物的血浆浓度有报道,氟奋乃静血浆浓度与副反应量表评分显著相关 (P=0.000 8),而副反应量表评分与静坐不能(r=0.6)及运动不能(r=0.44)显著相关,提示血药浓度增加与药物副反应尤其是静坐不能及运动不能相关[4]。
2.4.6 既往应用抗精神病药及应用时间首次用药者更可能发生静坐不能,重复用药或慢性长期用药可能减少静坐不能的发生。Sachdev等[15]的研究支持这一点,但效应较小。
2.4.7 其他锥体外系副反应许多研究发现药源性帕金森综合征与静坐不能相关,在Sachdev等[15]的研究中药源性帕金森综合征与静坐不能评分的相关系数为0.4(P<0.01),提示这两种副反应可能同时发生。
2.5 其他因素
2.5.1 铁缺乏研究发现铁缺乏在静坐不能的发病中起作用[20]。Barton等[21]对血清铁水平与静坐不能的关系进行研究,结果发现静坐不能组血清铁、转铁蛋白及转铁蛋白饱和度均降低。Horiguchi等[22]研究揭示,伴有静坐不能者血清铁水平显著低于无静坐不能者(P<0.05)。
2.5.2 脑器质性疾病静坐不能与许多神经系统疾病有关,如累及下丘脑和基底神经节的昏睡性脑炎、帕金森病、脑外伤、脑脓肿等。存在这些疾病的患者可增加药物所致静坐不能的可能性[15]。
2.5.3 酒精病例报道显示,对正在服用抗精神病药的患者摄入酒精可暂时增加静坐不能的发生[23]。
2.5.4 吸烟Menza等[24]报道慢性精神病患者中,女性吸烟者静坐不能发生率高,但这些吸烟者血药浓度较高,对此尚待进一步研究。
2.5.5 糖尿病Sandyk等[25]对68例慢性精神分裂症患者进行研究,发现伴有糖尿病者(16例)静坐不能评分较不伴糖尿病组高2倍。
2.5.6 原发性运动障碍家族史Lencer等[26]研究发现原发性运动障碍家族史是抗精神病药导致静坐不能的预测因素。
3 抗精神病药所致急性静坐不能的病理机制
3.1 多巴胺(DA)能假说
Marsden等[27]认为,急性静坐不能是由于抗精神病药阻断中脑DA通路上突触后D2受体所致。动物实验显示,当损伤啮齿动物的上述通路后,可引起运动活力增高,并可使注意范围缩小,被认为是静坐不能的一种动物模型。此外,也有人认为,一些抗精神病药所致静坐不能可能与脊髓DA通路受影响有关。
3.2 肾上腺素能假说
Bartels等[28]提出,静坐不能可能是由于抗精神病药引起脊髓去甲肾上腺素(NE)能受体过度敏感所致。他们发现静坐不能患者夜间尿3-甲氧-4羟基苯基乙二醇排泄量显著减少。肾上腺素能活力增高的机理可能是抗精神病药阻断了DA通路上突触前DA受体,而使NE活力相对增高。治疗学支持这一假说。β肾上腺素受体拮抗药治疗静坐不能有效,提示肾上腺素能系统亢进可造成静坐不能。
3.3 5-羟色胺(5-HT)能假说
临床和实验研究提示5-HT在抗精神病药导致静坐不能的发生中起着非常重要的作用。第一代抗精神病药,尤其是高效价药物,对 D2受体的阻断作用较强,而对5-HT2受体的作用较弱,静坐不能的发生率高。第二代抗精神病药相对于D2受体而言,对5-HT2受体具有优先阻断作用,其静坐不能的发生率较低[29]。另外,选择性5-HT再摄取抑制剂(SSRIs)可引起锥体外系反应,包括“静坐不能”样症状,可能是通过5-HT介导的DA阻断[30]。普萘洛尔通过突触前5-HT1A受体阻断作用发挥抗静坐不能效应。阻断5-HT2A/5-HT2C受体的药物如赛庚啶、曲唑酮、利坦色林及米安色林治疗静坐不能有效,进一步证实了这一假说[29]。
3.4 缺铁假说
文献报道,血清低铁状态与静坐不能的发生有关[21-22]。Horiguchi等[22]认为血清铁降低与中脑DA通路上突触后D2受体阻断假说密切相关。因为脑组织缺铁可降低D2受体的数量及活性,导致D2受体功能降低,使抗精神病药易致静坐不能。
4 抗精神病药所致急性静坐不能的临床表现
静坐不能的临床表现主要包括主观感觉和客观表现两个方面。
主观感觉:轻症病人仅诉有一种心神不宁及尤与腿部有关的躯体不安宁感觉,重症病人则诉有一种强迫性运动。病人通常描述为不舒服、烦躁不安、忧虑或内心紧张感,如一些典型的主诉为:感到不安宁,不能静坐,神经在跳动,腿总想动等。少见的表现有强烈的恐吓、恐怖、燥热感或精神症状恶化和痛苦的性体验,有的病人可表现为激越、冲动性自杀行为[31]。
客观表现:可有各种运动形式,但以腿和脚的不安宁运动最为常见,可以表现为复杂的重复运动,如交叉或不交叉的腿部运动、人体负重从一脚转移到另一脚、脚趾在地面上轻打、躯体持续摇摆、不停地踱步等;可见不能静坐、手臂及手的不安宁运动、摩擦地面及扭曲状躯体运动。有报告可有腿及脚趾的肌阵挛性反射、低频性或广泛性脚趾震颤等[31-32]。
5 抗精神病药所致急性静坐不能的诊断标准
《美国精神疾病诊断与统计手册第4版(DSM-Ⅳ)》有关抗精神病药所致急性静坐不能的诊断标准为[33]:①在应用抗精神病药后主诉坐立不安。②至少可观察到下列4项中的1项:不安宁运动或腿部摇摆;在站立时,身体负重从一脚转移到另一脚;踱来踱去以缓解坐立不安;不能坐着或站着不动。③在开始用抗精神病药或增加剂量4周内(或减少用于治疗锥体外系症状的药物后)发生。④症状不能用某一精神障碍来解释。⑤症状不是由于躯体疾病或其他非抗精神病药所引起。
6 抗精神病药所致急性静坐不能的鉴别诊断
6.1 不宁腿综合征
该综合征通常与服用抗精神病药无关,多数症状只限于腿,可伴有针刺、蚁走感、冷感或热感,常伴有睡眠中周期性肢体动作,夜间症状加重或消除,可资鉴别[34]。
6.2 焦虑障碍或与精神病有关的激越
静坐不能往往同时伴有情绪异常,如惊恐不安、烦躁等,应与焦虑障碍、重性抑郁或与精神病有关的激越相鉴别。静坐不能的一些特征性症状,如腿的不安宁、不能静坐、站立时双腿交替运动等可资鉴别[32]。另外,静坐不能的主观和客观检查所见的不安宁具有“非自愿性”也有助于鉴别[31]。与精神病有关的激越随着抗精神病药的增量而缓解;而静坐不能随着抗精神病药的增量而恶化。
6.3 脑器质性疾病
许多脑器质性疾病,如累及下丘脑和基底神经节的昏睡性脑炎、帕金森病、脑外伤、脑脓肿等,可出现静坐不能的症状,但还伴有相应的神经系统阳性体征。
7 抗精神病药所致急性静坐不能的治疗
7.1 减药或换药
急性静坐不能的发生与药物剂量有关,传统的治疗为减少抗精神病药剂量,或停用致病药物,或换用低效价的抗精神病药。
7.2 药物治疗
7.2.1 肾上腺素能药物β肾上腺素受体拮抗药普萘洛尔通过阻断肾上腺素能及促进腹侧大脑脚盖区DA神经传递而发挥抗静坐不能作用[31]。既往多个研究证实了普萘洛尔对抗精神病药所致静坐不能的疗效,曾作为一线用药。但Poyurovsky等[35]研究发现,普萘洛尔耐受性差,20%的患者出现有临床意义的体位性低血压和心动过缓,不得不中断治疗。另外,普萘洛尔与抗精神病药有复杂的药物相互作用,如普萘洛尔与氟哌啶醇合用可导致致死性心律失常;由于其非心脏选择性,明显增加对支气管平滑肌的影响和不良反应的发生[36]。
α2受体激动剂可乐定可减少中枢NE的传导,改善抗精神病药所致静坐不能。Adler等[37]应用可乐定(最大日剂量0.15~0.4 mg/d)治疗6例,治疗后静坐不能的自我评定、客观评定以及对焦虑的评定均显著改善。但常有镇静及低血压等副反应[2]。
7.2.2 抗胆碱能药物尽管抗胆碱能药物治疗药源性帕金森综合征及肌张力障碍有效,但对静坐不能疗效不肯定。Baskak等[38]的双盲、安慰剂对照研究发现,肌注比哌立登治疗第一代抗精神病药所致静坐不能疗效与安慰剂组无差异。而且抗胆碱能药物的不良反应(如认知损害、视物模糊、便秘、尿潴留等)限制其临床使用。Barnes等[39]建议仅用于与帕金森综合征有关的静坐不能。
7.2.3 苯二氮 类药物苯二氮 类药物(如氯硝西泮、劳拉西泮、地西泮等)通过其非特异性抗焦虑效应及镇静作用而发挥抗静坐不能效应[40]。路英智等[41]应用氯硝西泮治疗静坐不能33例,应用修订的Simpson锥体外系副反应量表评定疗效,结果发现治疗 10天后,24例(72.73%)患者完全缓解,其中16例服药2天后静坐不能症状即完全消失。
7.2.4 5-HT2受体拮抗剂利坦色林:具有5-HT2A及5-HT2C受体拮抗作用。Miller等[42]首先应用利坦色林(5~20 mg/d)治疗10例抗精神病药所致静坐不能,6例患者静坐不能量表减分超过50%,2例接近50%,2例无效,其起效快,疗效好,没有明显的不良反应。
赛庚啶:具有较强的5-HT2A及5-HT2C受体拮抗作用,还具有抗组胺及抗胆碱能作用。Weiss等[43]应用赛庚啶(16 mg/d)治疗抗精神病药所致静坐不能17例,应用BAS评定疗效,在治疗第2天就出现疗效,至第4天,17例病人均有不同程度的改善,15例BAS评分减少≥50%,6例病人完全缓解。孙振晓等[44]应用赛庚啶(12 mg/d)治疗抗精神病药所致静坐不能30例,并与普萘洛尔治疗30例对照,疗程10天,应用修订的 Simpson锥体外系副反应量表评定疗效,结果发现赛庚啶组总有效率为87%,而普萘洛尔组为83%,两组比较差异无显著性。
米安色林:是一种具有明显5-HT2A及5-HT2C受体拮抗作用,以及抗组胺及α2受体拮抗作用的四环类抗抑郁药,没有抗胆碱能特性。Poyurovsky等[45]应用米安色林(15 mg/d)治疗抗精神病药所致静坐不能16例,在治疗第3天,14例病人明显改善,且耐受性好,仅5例病人有短暂轻微的镇静作用。此后,Poyurovsky等[46]对米安色林治疗抗精神病药所致静坐不能的疗效进行双盲、安慰剂对照研究,应用米安色林(15 mg/d)治疗15例,安慰剂组15例,疗程5天,应用BAS评定疗效,以BAS分量表分至少降低1分作为有效的标准,结果发现,米安色林组 14例有效(93.3%),而安慰剂组完成试验的11例中,5例有效(45.6%)。当采用更严格的疗效标准 (BAS分量表分至少降低2分)时,米安色林组有效率为40%,而安慰剂组为9.1%。米安色林组有4例(26.6%)完全缓解,而安慰剂组无1例完全缓解。
小剂量米氮平:米氮平通过其较强的突触前α2肾上腺素受体拮抗作用而发挥抗抑郁效应,同时,具有明显的5-HT2A受体拮抗作用,这种作用在低剂量时占优势,而发挥抗静坐不能作用[40]。Poyurovsky等[35]进行的双盲、小剂量米氮平(15 mg/d)、普萘洛尔(80 mg/d)、安慰剂对照试验中,每组30例,应用BAS评定疗效,疗程7天,结果发现研究结束时,小剂量米氮平组、普萘洛尔组BAS减分均较安慰剂组明显,但小剂量米氮平组、普萘洛尔组比较无显著性差异。以BAS减分≥2分作为有效标准,米氮平组有效率为43.3%,普萘洛尔组为 30.0%,安慰剂组为6.7%。Hieber等[29]对米氮平治疗抗精神病药所致静坐不能的文献进行评价,其中3篇病例报告(9例)、1篇安慰剂对照研究(26例)、1篇安慰剂-普萘洛尔对照研究 (90例),结果发现米氮平有效率 (以BAS减分≥2分为标准)为53.8%,而安慰剂组为7.7%。提示米氮平治疗抗精神病药所致静坐不能有效。
7.2.5其他Fleischhacker等[47]报道应用DA再摄取抑制剂金刚烷胺治疗静坐不能有效。Danel等[48]报道阿米替林对静坐不能有效,并认为其作用机理可能是使β肾上腺素能突触后膜处于失敏感状态,从而提高抗胆碱能作用而产生治疗效果。
7.3 抗精神病药所致急性静坐不能的治疗流程
Poyurovsky等[40]回顾文献后,提出的抗精神病药所致急性静坐不能的治疗流程见图1。
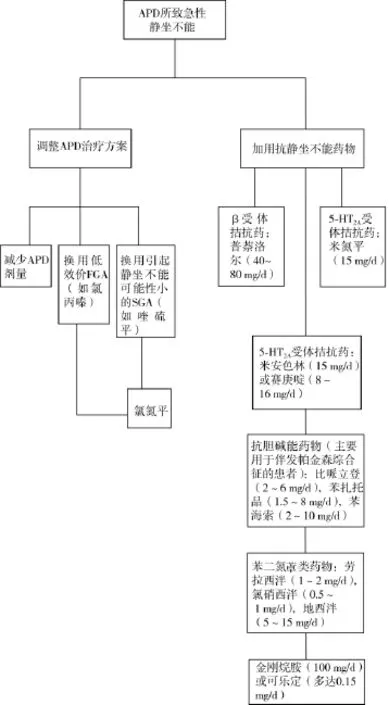
图1 APD所致急性静坐不能的治疗流程
参考文献:
[1] Adler LA,Angrist B,Reiter S,et al.Neuroleptic-induced akathisia:a review[J].Psychopharmacology,1989,97(1):1-11.
[2] Poyurovsky M,Weizman A.Serotonin-based pharmacotherapy for acute neuroleptic-induced akathisia:a new approach to an old problem[J].Br J Psychiatry,2001,179:4-8.
[3] Hirose S.The causes of underdiagnosing akathisia[J].Schizophr Bull,2003,29(3):547-558.
[4] Sachdev P.The epidemiology of drug-induced akathisia:PartⅠ. acute akathisia[J].Schizophr Bull,1995,21(3):431-449.
[5] Lindström LH,Wieselaren IM,Struwe G,et al.A double-blind comparative multicentre study of remoxipride and haloperidol in schizophrenia[J].Acta Psychiatr Scand Suppl,1990,358:130-135.
[6] Claghorn J,Honigfeld G,Abuzzahab FS,et al.The risks and benefits of clozapine versus chlorpromazine[J].J Clin Psychopharmacol,1987,7(6):377-384.
[7] Cohen BM,Keck PE,Satlin A,et al.Prevalence and severity of akathisis in patients on clozapine[J].Biol Psychiatry,1991,29(12):1215-1219.
[8] Halstead SM,Barnes TR,Speller JC.Akathisia:prevalence and associated dystonia in an in-patient population with chronic schizophrenia[J].Br J Psychaitry,1994,164(2):177-183.
[9] 孙振晓,崔义才,刘方礼,等.抗精神病药物治疗精神分裂症导致静坐不能的预测[J].山东精神医学,1997,10(1):27-29.
[10] Miller DD,Caroff SN,Davis SM,et al.Extrapyramidal side-effects of antipsychotics in a randomized trail[J].Br J Psychaitry,2008,193(4):279-288.
[11] Kahn RS,Fleischhacker WW,Boter H,et al.Effectiveness of antipsychotic drugs in first-episode schizophrenia and schizophreniform disorder:an open randomized clinical trial[J]. Lancet,2008,371(9618):1085-1097.
[12] Aguilar EJ,Keshavann MS,Martinez-Quiles MD,et al.Predictors of acute dystonia in first-episode psychotic patients[J].Am J Psychaitry,1994,151(12):1819-1821.
[13] 朱少毅,蚁丽芬.维思通所致静坐不能的研究[J].山东精神医学,2001,14(2):132-134.
[14] Braude WM,Barnes TR,Gore SM.Clinical characteristics of akathisia:a systematic investigation of acute psychiatric inpatient admissions[J].Br J Psychaitry,1983,143:139-150.
[15] Sachdev P,Kruk S.Clinical characteristics and predisposing factors in acute drug-induced akathisis[J].Arch Gen Psychiatry,1994,51(12):963-974.
[16] Gardos G,Teicher MH,Lipinski JF Jr,et al.Quantitative assessment of psychomotor activity in patients with neuroleptic-induced akathisis[J].Prog Neuropsychopharmacol Biol Psychiatry,1992,16(1):27-37.
[17] Ayd FJ Jr.A survey of drug-induced extrapyramidal reactions[J]. JAMA,1961,175(12):1054-1060.
[18] McClelland HA,Farquharson RG,Leyburn P,et al.Very high dose fluphenazine decanoate:a controlled trialin chronic schizophrenia[J].Arch Gen Psychaitry,1976,33(12):1435-1439.
[19] van Putten T,Marder SR,Mintz J.A controlled dose comparison of haloperidol in newly admitted schizophrenic patients[J]. Arch Gen Psychaitry,1990,47(8):754-758.
[20] Sachdev P.The neuropsychiatry of brain iron[J].J Neuropsychatry Clin Neurosci,1993,5(1):18-29.
[21] Barton A,Bowie J,Ebmeier K.Low plasma iron status and akathisia[J].J Neurol Neurosurg Psychaitry,1990,53(8):671-674.
[22] Horiguchi J.Low serum iron in patients with neuroleptic-induced akathisia and dystonia under antipsychotic drug treatment[J].Acta Psychiatr Scand,1991,84(3):301-303.
[23] Lutz EG.Neuroleptic-induced akathisia and dystonia triggered by alcohol[J].JAMA,1976,236(21):2422-2423.
[24] Menza MA,Grossman N,van Horn M,et al.Smoking and movement disorders in psychiatric patients[J].Biol Psychiatry,1991,30(2):109-115.
[25] Sandyk R,Kay SR,Awerbuch GI,et al.Risk factors for neuroleptic-induced movement disorders[J].Int J Neurosci,1991,61(3-4):149-188.
[26] Lencer R,Eismann G,Kasten M,et al.Family history of primary movement disorders as a predictor for neuroleptic-induced extrapyramidalsymptoms[J].BrJPsychiatry,2004,185:465-471.
[27] Marsden CD,Jenner P.The pathophysiology of extrapyramidal side-effects of neuroleptic drug[J].Psychol Med,1980,10(1): 55-72.
[28] Bartels M,Gaertner HJ,Golfinopoulos G.Acathisia-syndrome: involvement of noradrenergic mechanisms[J].J Neural Transm,1981,52(1-2):33-39.
[29] Hieber R,Dellenbaugh T,Nelson LA.Role of mirtazapine in the treatment of antipsychotic-induced akathisia[J].Ann Pharmacother,2008,42(6):841-846.
[30] Lane RM.SSRI-induced extrapyramidal side-effects and akathisia:implications for treatment[J].J Psychopharmacol,1998,12(2):192-214.
[31] 余海鹰.神经阻滞剂所致静坐不能的研究现状[J].中华精神科杂志,1996,29(2):120-122.
[32] 俞俊洪.抗精神病药物所致静坐不能研究进展[J].四川精神卫生,1994,7(3):205-208.
[33] American Psychaitric Association.Neuroleptic-induced acute akathisia.In:Diagnosti and statistical manual of mental disorders [M].4thed.Washington DC:APA,2000:800-802.
[34] Avecillas JF,Golish JA,Giannini C,et al.Restless legs syndrome:keys to recognition and treatment[J].Cleve Clin J Med,2005,72(9):769-787.
[35] Poyurovsky M,Rashinian A,Weizman R,et al.Low-dose mirtazapine:a new option in the treatment of antipsychotic-induced akathisia.Arandomized,double-blind,placebo-andpropranolol-controlled trial[J].Biol Psychaitry,2006,59(11):1071-1077.
[36] Kramer MS,Gorkin RA,Dijohnson C,et al.Propranolol in the treatment of neuroleptic-induced akathisia(NIA)in schizophrenia:a double-blind,placebo-controlled study[J].Biol Psychaitry,1988,24(7):823-827.
[37] Adler LA,Angrist B,Peselow E,et al.Clonidine in neuroleptic-inducedakathisia[J].AmJPsychiatry,1987,144(2):235-236.
[38] Baskak B,Atbasoglu EC,Ozguven HD,et al.The effectiveness of intramuscular biperiden in acute akathisia:a double-blind,randomized,placebo-controlled study[J].J Clin Psychopharmacol,2007,27(3):289-294.
[39] Barnes TR,McPhillips MA.Critical analysis and comparison of the side-effect and safty profiles of the new antipsychotics[J].Br J Psychiatry Suppl,1999,(38):34-43.
[40] Poyurovsky M.Acute antipsychotic-induced akathisia revisited [J].Br J Psychaitry,2010,196(2):89-91.
[41] 路英智,王法鑫,田明萍.氯硝安定与安坦治疗静坐不能的对照研究[J].中国神经精神疾病杂志,2000,26(4):253-254.
[42] Miller GH,Fleischhacker WW,Ehrman H,et al.Treatment of neuroleptic-induced akathisia with the 5-HT2 antagonist ritanserin[J].Psychopharmacol Bull,1990,26(3):373-376.
[43] Weiss D,Aizenberg D,Hermesh H,et al.Cyproheptadine treatment in neuroleptic-induced akathisia[J].Br J Psychiatry,1995,167(4):483-486.
[44] 孙振晓,王玉红,于相芬.赛庚啶与普萘洛尔治疗抗精神病药物所致静坐不能的比较[J].中国新药与临床杂志,1998,17(4):205-206.
[45] Poyurovsky M,Fuchs C,Weizman A.Low-dose mianserin in the treatment of acute neuroleptic-induced akathisia[J].J Clin Psychopharmacol,1998,18(3):253-254.
[46] Poyurovsky M,Shardorodsky M,Fuchs C,et al.Treatment of neuroleptic-induced akathisia with the 5-HT2 antagonist mianserin.Double-blind,placebo-controlled study[J].Br J Psychaitry,1999,174:238-242.
[47] Fleischhacker WW,Roth SD,Kane JM.The pharmacologic treatment of neuroleptic-induced akathisia[J].J Clin Psychopharmacol,1990,10(1):12-21.
[48] Danel T,Servant D,Goudemand M.Amitriptyline in the treatmentofneuroleptic-inducedakathisia[J].BiolPsychiatry,1988,23(2):186-188.
孙振晓,男,主任医师。研究方向:临床精神医学。通讯作者E-mail:szx.ywk@163.com
doi:10.3969/j.issn.1672-5433.2012.04.008
收稿日期:(2011-12-22)
作者简介:于相芬,女,副主任护师。研究方向:精神科护理学。
The Current Status of the Research on Acute Antipsychotics-induced Akathisia
Yu Xiangfen,Sun Zhenxiao,Sun Bo(Department of Psychiatry of Linyi Municipal Mental Health Center of Shandong Province,Shandong Linyi 276005,China)
ABSTRACTAcute antipsychotics-induced akathisia is a type of acute extrapyramidal symptom.In order to make a better understanding of acute antipsychotics-induced akathisia,this article presented a review on the application ofantipsychotic drugs such asthe incidence ofacute akathisia, risk factors,pathomechanism,clinical manifestation,diagnostic criteria,differential diagnosis and treatment.
KEY WORDSAntipsychotic Drugs;Therapeutic Use/Adverse Effects;Acute Akathisia
