工业清洗过程分类新方法
2012-04-05FryerAsteriadou化学工程学院配方工程中心英国伯明翰大学伯明翰英国
P.J. Fryer*, K. Asteriadou(化学工程学院配方工程中心,英国伯明翰大学,伯明翰,英国)
工业清洗过程分类新方法
P.J. Fryer*, K. Asteriadou(化学工程学院配方工程中心,英国伯明翰大学,伯明翰,英国)
清洗工艺设备在食品行业是无处不在的,但人们对它仍然是知之甚少。通过简化的分类机制,食品污染的研究得以推进。本文中,我们回顾了当前食品和个人产品清洁工作的现状,并提出对于清洗问题的两种分类,一种基于污垢的类型,另一种基于清洗机制。该分类的目的是使不同的清洗操作的结果便于比较以及帮助完善在工业清洗领域中已经行之有效的清洗方法。

清洗问题
在工业上,常用的设备如罐体、管道及换热器操作界面上形成的表面沉积物(污垢)是需要解决的一个重要问题,也是工业清洗领域一个重要的研究课题[1]。在食品和个人护理行业,清洗过程也很常见,这是因为:
1)对于一些工业设备固体颗粒物的沉积会造成性能的下降,并往往引发压降升高及换热效率降低的问题;
2)设备内部可能形成有机物并对设备造成损坏;
3)需要清理不同产品之间转换器上的污染物以避免交叉污染。当同一条生产线上同时生产一定数量不同的产品时,这一点尤为重要。
清洁过程通常是高度自动化,预先设定流量和时间的原位清洗技术(CIP)已经司空见惯[2]。然而,对于给定的条件设计一个合适的清洗程序还是半经验性的。
有很多重要的生产商、化学品清洁公司或组织在研究工业清洗。如欧洲卫生工程设计集团(EHEDG;http://www.ehedg.org),该集团制定了为数众多的清洗指南,说明清洗表面的类型和易于清洗的设备。保证产品安全性及纯度的必要性,意味着工业清洗的方案在设计上都要留有很大的余地,但因产品污染并被召回对品牌造成的严重负面影响使得人们没有动力去试探安全的临界线。
然而,人们越来越重视清洗过程对环境的影响并试图将其最小化。清洗过程会产生大量的污水,并且如果在清洗过程中分别使用碱性或酸性的清洗试剂,污水的pH值可能会非常高或者非常低。能源成本日益增加且清理用水的短缺,使得在清洗过程中降低清洗时间和成本受到重视。一个有效的衡量标准是生产1升产品所需的水的体积。一种方法是将污水净化并再利用[3],但最有效的还是降低清洗水用量。最大限度地减少清洗成本所面临的其他重大问题还有:
1、存在比较不同清洗方法的困难,例如不能通过清洗一种污物的时间来准确预测清理另一种污物的时间。
2、缺乏有效的在线测量方法来确定某种清洗工艺的有效性并确定清洗终点。当然,拆开设备通过擦拭和化验,可以发现残留的沉积物以及任何的生物[4],这往往是在制药工业中检查清洗效果的唯一途径[5]。这样的检测方法不可能做到在线监测。一般而言,清洗标准的建立是在工厂开始,有些擦拭也是质量保证的必要程序。
3、放大实验或中试的数据很难获得,因为在没有明晰清洗机理的情况下,放大实验规模也只能是一个半经验性的过程。
以上原因造成的实际后果就是:(1)清洗某种污物的最有效的工艺往往是单独开发出来的,所以在工艺开发过程中所掌握的信息并不适用于其他类型污物的清洗。(2)CIP程序的制定和运作缺乏有效的判断清洗终点的手段。
在结垢研究中,按照结垢过程涉及的机械设备进行分类是一大进步。Taborek 等[6]认为,结垢是换热器最后一个尚未解决的问题,但Epstein[7-9]已经开发了一种使用广泛分类方法。尽管人们已经做出了一些尝试来概括清洗行为[10,11],但迄今为止尚没有提出系统的分类方法。目前已经提出了一些优化方法[12-16],这些方法发展了热过程,以改善质量和减少结垢,但它们不包括清洁本身。
清洗研究的长期目标是减少清洗成本并辅助清洗设备的设计。Asteriadou等[17,18]和Jensen等[19]论述了计算流体动力学(CFD)应用于设备的设计,有利于改善设备的可清洗性。这种研究方法对于优化机械设备的设计是十分必要的。对于清洗过程的认识还需要进一步的深入。本文中,参考了Epstein的按照机械设备分类的方法尝试对清洗问题进行了分类。所做的工作在目前的阶段有一部分还是不确定的,不过对于将来的工作提出了一系列的建议。
结垢机理的分类
表面结垢的研究因遵循Epstein[7]的分类变得更加容易。最关键的一点是将清洗作业不以行业而是以沉积物的形成机理进行分类,这样才有可能对清洗作业进行归类并对不同行业的清洗结果进行比较。结垢机理叙述如下:
(1)反应污垢:这种污垢是由于流体中某些组分的反应造成的沉积物。不同行业的结垢如乳品结垢(蛋白质变性造成)[20]以及原油结垢[21]都属于这一类情况;
(2)生物污垢:生物污垢的尺度不一,从单个的生命体的相互附着的聚集体到自主生长的生物膜[22,23]、藤壶和海藻;
(3)结晶或沉淀污垢:这种污垢的形成是由于某些本来溶于流体的组分由于其溶解度降低导致析出沉积,例如沸水中析出的碳酸钙或磷酸钙(其溶解度随着温度的增加而降低)。固化结垢也是这种结垢的一种,指的是流体或流体中的某些组分在表面上结垢[24,25]。这种固化结垢包括水结成冰,食物流体中析出淀粉等。在个人护理产品加工过程中牙膏沉积物,化妆品中析出的蜡质都属于这类范畴。
(4)微粒污垢:颗粒黏附在一起并从流体中沉积到表面上,如冷却水中的磁性颗粒的聚集沉积,空气中的灰尘,或者蛋白质的聚集沉积[26]。
(5)腐蚀污垢:指的是由于表面腐蚀造成的结垢。通常腐蚀产物会通过流体被输送至设备的其他位置,输送过程遵从微粒结垢机理。
污垢的形成可能会遵从不止一个机理,例如蛋白质与磷酸钙相互作用形成乳垢[27,28],蛋白质聚集沉积的过程就包括反应结垢和颗粒结垢两种机理。
沉积过程被进一步划分为5×5的矩阵[9],即五种机理以及每种机理分为五个阶段:
1)起始阶段: 在出现明显的结垢之前会有一段时间,这个阶段通常被认为是准备阶段;
2)运输阶段:结垢成分转移到设备的表面;
3)附着阶段:结垢材料附着到设备的表面;
4)移除阶段:结垢过程通常被认为是污垢形成和污垢移除过程的平衡[29];
5)老化阶段:在这个阶段, 吸附在设备上的污垢在性质和结构上都发生了变化,例如食品结垢变为褐色并硬化。这一步是最难进行预测并建模的;但有一点很明确,即随着结垢反复暴露在空气中以及重复的清洗过程会使得设备的表面以及结垢/清洗的性能发生变化[30]。
清洗问题分类
虽然人们已经就清洗问题开展了一定的学术研究,但这些研究既没有对结垢过程的机理有深入的认识也不能指导工业实践。以一个工厂为试点或进行大规模的研究是有价值的,但价格昂贵;而规模较小的实验往往受到质疑因为:
1) 实验室采用的沉积物经常并不能代表工业污垢。要制造出可重复的污垢是非常的困难,并且目前对于污垢老化过程的了解并不十分透彻,所以真实沉积物的生成条件很难模拟出来。例如利用乳清蛋白模拟巴氏杀菌的行为得到的结果就与真实污垢不一样[31,32]。
2) 实验规模由于太小,因此其结果很难进行工业放大,并且如何来进行工业放大也不明确;不同规模情况下清洗频率和强度的关系也不清楚(如由实验或实验室数据来预测工业清洗时间)。
为了辅助理解结垢过程,我们提出了一个两阶段方法。第一步是对要清除的污垢进行分类,然后考察移除污垢的机理。
通过污垢类型和清洗方法分类
污垢的类型十分广泛,根据污垢类型及结垢程度应选择适合的清洗流体。图1是通过一个二维的示意图对清洗问题进行的分类,图中的橫、纵坐标轴分别代表:
橫坐标:污垢材料性能
污垢由于沉积材料的性质不同,其结垢程度各异:
1. 低黏度流体:该种流体形成的“沉积物”往往是水或具有接近水的性质;例如:
排空管道和储罐时残留的牛奶或啤酒。
2. 高黏度流体:这种沉积物是具有高度黏性(有时是黏弹性或粘塑性)的流体,如个人卫生用品加工过程中残留在设备壁上的一层层的牙膏或香波或者生产食品调味料时残留的淀粉。这些流体的表观黏度可能是水的几千倍。
3. 凝聚固体:这种积垢表面看起来和固体一样;不同的沉积物的性质迥异,有牛奶或其他流质食物形成的柔软的蛋白凝胶薄膜,也有由于矿物沉积形成的十分坚固的固体(如在牛奶超高温杀菌过程中形成的沉积物)。
纵坐标:清洗流体
沉积物的性质决定了应当采取何种清洗流体。
1. 冷水:有些污垢与设备表面的结合力很弱,通过冷水漂洗就可除去。在清洗过程中需要打破的键只有物理键及流体间相互作用力。
基于污垢类型和采用的清洗化学剂对清洗问题进行的分类。共分为三类:第一类包括个人产品(牙膏,香波等)和一些食品形成的薄膜(淀粉和其他凝胶):第二类是生物膜;第三类包括大部分的食物污垢如制奶(低温下析出蛋白质,高温下析出矿物质),酿酒和制糖行业。
2. 热水:在个人卫生产品加工过程中,使用循环热水进行清洗很常见,被清除的产品可以回收。热水能够增加大部分结垢组分的溶解度并且有可能促进相转变。
3. 热清洗液:有很多的沉积污垢单独用水难以清洗或者耗时太长,在这种情况下应加入化学试剂(酸性或碱性),使污垢能够按照要求被清洗下来。但这种清洗流体对环境的影响要大大超过其他的清洗液。
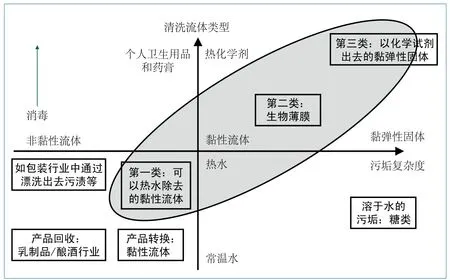
图1 工业清洗示意图
图1显示的是从食品行业到个人卫生用品行业所遇到的一系列清洗课题,证明清洗问题可以被归成几类。阴影区域显示的三种类型污垢是最难清洗的:
第一类:用水清洗高黏度或黏弹性或黏塑性的流体。
在个人护理产品中,污垢薄膜(如牙膏,香波,霜剂)的成分与产品流体是相同的,通过固化生成。对于黏性食品如淀粉为主要原料的调味汁和制糖行业也存在类似的问题。这些污垢单独通过水洗还是可以清除的。
第二类:清洗和杀死有机生物形成的污垢膜。
虽然单独通过水清洗也可以除去某些生物污垢膜[33,34],但通常的做法是加入杀菌剂以消灭粘附的有机生命体。添加杀菌剂可以改变污垢清洗剂的性质[35]。
第三类:通过化学剂清除固体结垢。
这里所指的固体结垢是通过一种或多种结垢机理形成的。这种结垢单独通过水难以清除,必须加入化学助剂。加入化学助剂能够改变污垢的存在形式,要么变得易于溶解,要么变得易于清除。使用化学助剂的种类取决于污垢本身的性质,如氢氧化钠可以用来清除有机结膜污垢,而酸可以用来清除矿物结垢。
通过清洗机制进行的分类
上面所定义的三种污垢可以通过清洗的机制进一步分类。CIP通常涉及流过结垢的流体(如通过分散形成的喷射流或管道中形成的流体),因此同时涉及物理和化学作用。清洗过程必须克服(1)污垢分子之间的结合力以及(2)污垢与设备表面之间的黏合力。有时通过清洗流体或清洗流体与化学助剂共同作用才能克服这两种力。
图2显示的是污垢不同组分的示意图。
流体机械清除
有些污垢(第一类)可以通过流体的流动行为本身来清除,即流体机械清除。
对于流体机械清除的控制因素是结垢的流变性能以及清洗流体的流变和流动性能(如施加到污垢的剪切力)。通过了解两相流体动力学可以预测清洗机制[36]。虽然对油/水两相的相互作用研究很多,但关于黏度迥异的两相流体的数据总体较少[37]。Henningsson等[38]利用CFD(计算流体动力学)模拟了水冲洗管路中残留酸奶的过程,在清洗的最后阶段只剩下很薄的一层酸奶残留在管壁上,这一阶段是最难模拟和计算的。
污垢的流变性能可能会随时间发生变化,原因有以下几个方面:(1)老化,污垢黏附在器壁上被高温蒸煮或暴露在空气中干燥;或(2)水扩散到污垢中。扩散的过程相对缓慢但可以降低污垢的黏度使之更容易除去,像清洗管路时缓慢清洗比喷射快速清洗更有效。清除过程因此取决于两个时间常数:
1. “纯”污垢的清除速率,清洗流体向污垢中扩散的速率可以忽略。
2. 清洗流体扩散到污垢中使污垢变得易于清除的速率。
如果单独用水清洗污垢的去除速率十分缓慢,那么就应使用化学助剂,清洗的机制也将随之改变。
扩散-反应去除
通常需要使用化学助剂而不是单单用水来清洗。这种情况下,清洗过程就包括化学助剂扩散到或扩散进污垢并与污垢反应将其变得易于清除。例如,脂肪皂化,乳化,熔化过程[39]。污垢清除过程可能遵从不同的机制:
1. 溶解:如矿物盐溶解于酸中,蛋白质溶解于碱,糖溶解于水。上述过程有可能通过表面传质控制或者通过溶解动力学控制。如果涉及到污垢熔化过程则还有可能通过传热控制。
2. 破坏污垢聚集:破坏污垢分子间的结合力,虽然污垢还停留在表面但已变得更易于除去;
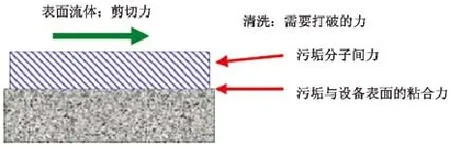
图2 清洗过程中需要克服的力示意图
3. 破坏表面黏结力:破坏污垢与器壁之间的黏结力,并进一步去除从设备表面脱落下来的污垢块体。
在某些情况下,污垢去除过程中一种机制占主导地位。例如,图3所示的淀粉膜去除(烤番茄糊)过程,就是通过破坏设备表面与污垢间的黏合力来去除污垢。在实际操作中,不同的机制在不同的条件下起控制作用。除了流体的剪切力,清洗效果还取决于:
1. 化学助剂到污垢/清洗流体界面或以清除下来的污垢传到界面以及从界面传到清洗流体的传质过程。
2. 活性组分对污垢的渗透;Mercade'-Prieto 等[40]研究了乳清蛋白的渗透过程。
3. 反应速率;关于污垢清除过程所涉及化学反应速率的研究很少,不过Yoo等[41]研究了奶制品的结垢,给出了碱与乳清蛋白作用的大量数据,结果显示温度效应占据主导地位。
4. 污垢与设备表面的物理反应。在蛋白质的清洗过程中,这种物理反应的作用是使污垢的体积增大,更易于溶解,也更易于作为块体被清除。但对于有些污垢来说,如果碱液的浓度过大反而会是蛋白污垢萎缩变硬,更加难以清除[42]。
基于商业重要性考虑,大部分的扩散-反应研究都使用牛奶或模拟牛奶形成的污垢膜。奶蛋白与碱液(在很高的pH条件下)接触后膨胀,然后被除去。Gillham等[43,44]研究了利用碱性清洗液清洗不锈钢表面乳清蛋白的过程,发现在清洗的不同阶段,不同的机制起控制作用。例如在清洗最后的污垢膜时,通过反向冲洗可以明显改善清洗效果,表明剪切力在很大程度上起控制作用。Christian等[45]按照蛋白污垢在化学助剂的冲击下被冲离设备表面的量来评估反应的效果。他们还发现(如图4所示),污垢去除和膨胀过程是同时进行的。Mercade'-Prieto等[46,47]对蛋白质块体的行为进行了卓有成效的研究。他们研究了乳清蛋白和β-乳球蛋白凝胶及其高pH溶液,并在蛋白质被分解的过程中观察到一系列的作用。他们还发现的溶解速率取决于在结垢条件下蛋白质的聚集结构。
清洗流体 (NaOH)流过污垢的时段如阴影部分所示。在清洗过程中,流体被水所替代时,因为污垢的膨胀压降首先增加,但清洗速率降低,清洗不彻底,如图所示,再以化学清洗液代替水的时候压降又出现了升高。
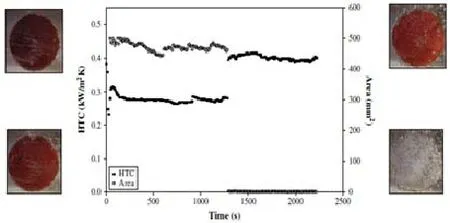
图3 传热破坏分子间力去除西红柿沉积物,通过光学显微镜测量去除效果
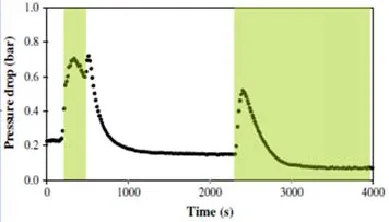
图4 清洗过程中的压降变化
黏合力和污垢分子间凝聚力的平衡可以通过改变表面能来调节。众所周知,通过这种方法可以最大限度地降低细菌间的黏连作用[48],通过表面改性来控制海洋生物污垢的污染已经做了很多卓有成效的工作,重大工作已经完成控制并表面改性[49]。通过改变表面能也可以减少矿物结垢[50]。对于一系列表面处理技术的研究也很广泛[51]。有一个欧盟大型科研项目[52,53],系统研究了奶垢在不同表面的粘合能力。Liu等[54]和Saikhwan等[55]使用动态测量和显微操作探针技术研究了污垢的清除过程,得到的结果是类似的[56,57]。污垢与表面之间的表面能在一定范围内时(22~28 mN/m)不能黏结在一起,这个时候表面结合力最低。Liu等[58-60]利用显微操作探针技术研究了多种污垢,包括奶垢,淀粉污垢等,并确定破坏其分子间结合力及与设备表面黏合力的模式,以此来作为一些变量如污垢厚度,界面能的函数。他们的研究结果显示,分子间结合力在高温及强碱性条件下会被破坏,因为这时的反应速率比较高。因此,对于污垢移除的过程很明显存在不同的模式,特别是在分子间结合力和污垢与设备表面间黏合力都有可能发生的条件下,动力学研究必不可少。
结论和展望
本文综述了现存的工业清洗研究工作,提出了两种新的清洗机理分类,其中一种是示意性的,另一种是机理性的。就像Epstein提出的积垢矩阵模型一样,上述工作可能将有助于增进人们对工业清洗机制的了解。相比创建针对特定污垢的复杂模型而言,构建针对不同机理的模型可能是更好的方法,因为这样有助于将不同清洗体系得到的数据进行对比,使之得到最有效的利用。很明显,将图1中的分类矩阵扩展到其他工业部门也十分有意义,同时可以确定这种分类方法在除了食品和消费品的其他行业是否有效。该图是特意简化的示意图,我们并没有把每个坐标轴对应的物理含义严格量化。
工业清洗遵从的机制不一样,则清洗过程中的原则也不同:
1. 溶解控制意味着流体的流速不是一个重要的因素:溶解速率将取决于局部反应速率或溶解度;
2. 流体机械去除将取决于流过污垢的流体性质。这种情况下,知道污垢的流变性能就可以预测出清洗时间,并且如果知道一种污垢在清洗条件下的流变性能,则可以预测其他污垢在该种条件下的清洗时间。如果没有有效的CFD模型,那么计算机建模的困难之处就在于使CFD模型能够和相应的流体相匹配。
3. 同时具有分子间结合力和污垢与设备表面黏结力的污垢是最难以清除的,相应的清除机制也不一样;很可能在清洗的不同阶段,清洗的控制因素不一样,这就会使实际情况很难和CFD模拟结果相符。
我们所提出的这种方法的长期目标是建立起可以预测的工业清洗模型以及计算模型,以方便清洗设备以及CIP工艺设计的更好。在实际生产中,不可能做到了解整个工厂所有类型污垢的结垢程度以及组成,因此将上述模型工业化时(如在过程控制方面)不得不考虑到这一点,清洗的方法可能得随机选择而不是能够完全确定。
(南海明译)
[1] Muller-Steinhagen, H., Reza Malayeri, R., & Watkinson, A. P. (2007). Heat exchanger fouling and cleaning VII, July 1-6, 2007-Tomar, Portugal.
[2] Tamime, A. V. (Ed.). (2008). Cleaning-inplace: Dairy, food and beverage operations. Society of dairy technology series. London:Wiley-Blackwell.
[3] Vourch, M., Balannec, B., Chaufer, B., & Dorange, G. (2008). Treatment of dairy industry wastewater by reverse osmosis for water reuse. Desalination, 19, 190-202.
[4] Vilar, M. J., Rodr'guez-Otero, J. L., Die'guez, F. J., Sanjua'n, M. L., & Yus, E. (2008). Application of ATP bioluminescence for evaluation of surface cleanliness of milking equipment. International Journal of Food Microbiology, 125, 357-361.
[5] Liu, L., & Pack, B. W. (2007). Cleaning verification assays for highly potent compounds by high performance liquid chromatography mass spectrometry:strategy, validation, and long-term performance. Journal of Pharmaceutical and Biomedical Analysis, 43, 1206-1212.
[6] Taborek, J., Aoki, T., Ritter, R. B., Palen, J. W., & Knudsen, J. G. (1972). Fouling: the major unresolved problem in heat transfer. Chemical Engineering Progress, 68, 59-68.
[7] Epstein, N. (1978). Fouling in heat exchangers. In: Proc. of the 6th Int. heat transfer conference (pp. 235-253).
[8] Epstein, N. (1981). Technical aspects (afterword to ‘Fouling in heat exchangers’). (pp. 31-53)
[9] Epstein, N. (1983). Thinking about heat transfer fouling: a 5 ×5 matrix. Heat Transfer Engineering, 4, 43-56.
[10] Fryer, P. J., Christian, G. K., & Liu, W. (2006). How hygiene happens: the physics and chemistry of cleaning. International Journal of Dairy Technology, 59, 76-84.
[11] Wilson, D. I. (2005). Challenges in cleaning: recent developments and future prospects. Heat Transfer Engineering, 26, 51-57.
[12] Benning, R., Petermeier, H., Delgado, A., Hinrichs, J., Kulozik, U., & Becker, T. (2003). Process design for improved fouling behaviour in dairy heat exchangers using a hybrid modelling approach. Food and Bioproducts Processing, 81, 266-274.
[13] De Jong, P., te Giffel, M. C., & Kiezenbrink, M. C. (2002). Prediction of the adherence, growth and release of microorganisms in production chains. International Journal of Food Microbiology, 74,13-25.
[14] De Jong, P., te Giffel, M. C., Straatsma, J., & Vissers, M. M. M. (2002). Reduction of fouling and contamination by predictive kinetic models. International Dairy Journal, 12, 285-292.
[15] Petermeier, H., Benning, R., Delgado, A., Kulozik, U., Hinrichs, J., & Becker, T. (2002). Hybrid model of the fouling process in tubular heat exchangers for the dairy industry. Journal of Food Engineering, 55, 9-17.
[16] Schutyser, M. A. I., Straatsma, J., Keijzer, P. M., Verschueren, M., & De Jong, P. (2008). A new web-based modelling tool (Websim-MILQ) aimed at optimisation of thermal treatments in the dairy industry. International Journal of Food Microbiology, 128, 153-157.
[17] Asteriadou, K., Hasting, A. P. M., Bird, M. R., & Melrose, J. (2006). Computational fluid dynamics for the prediction of temperature profiles and hygienic design in the food industry. Food and Bioproducts Processing, 84, 157-163.
[18] Asteriadou, K., Hasting, A. P. M., Bird, M. R., & Melrose, J. (2007). Predicting cleaning of equipment using computational fluid dynamics. Journal of Food Process Engineering, 30, 88-105.
[19] Jensen, B. B. B., Friis, A., Be'ne'zech, Th, Legentilhomme, P., & Lelie`vre, C. (2005). Local wall shear stress variations predicted by computational fluid dynamics for hygienic design. Food and Bioproducts Processing, 83, 53-60.
[20] Changani, S. D., Belmar-Beiny, M. T., & Fryer, P. J. (1997). Engineering and chemical factors associated with fouling and cleaning in milk processing. Experimental Thermal and Fluid Science, 14, 392-406.
[21] Watkinson, A. P. (2007). Deposition from crude oils in heat exchangers. Heat Transfer Engineering, 28, 177-184.
[22] Boulange'-Petermann, L. (2006). Processes of bioadhesion on stainless steel surfaces and cleanability: a review with special reference to the food industry. Biofouling, 10, 275-300.
[23] Verran, J. (2002). Biofouling in food processing: biofilm or biotransfer potential? Food and Bioproducts Processing, 80, 292-298.
[24] Fernandez-Torres, M. J., Fitzgerald, A. M., Paterson, W. R., & Wilson, D. I. (2001). A theoretical study of freezing fouling:limiting behaviour based on a heat and mass transfer analysis. Chemical Engineering and Processing, 40, 335-344.
[25] Sharma, A., Garg, D., & Gupta, J. P. (1982). Solidification fouling of paraffin wax from hydrocarbons. Letters in Heat and Mass Transfer, 9, 209-219.
[26] Simmons, M. J. H., Jayaraman, P., & Fryer, P. J. (2007). The effect of temperature and shear rate upon the aggregation of whey protein and its implications for milk fouling. Journal of Food Engineering, 79, 517-528.
[27] Rosmaninho, R., & Melo, L. F. (2008). Proteinecalcium phosphate interactions in fouling of modified stainless-steel surfaces by simulated milk. International Dairy Journal, 18, 72-80.
[28] Rosmaninho, R., Rizzo, G., Mu¨ ller-Steinhagen, H., & Melo, L. F. (2008). Deposition from a milk mineral solution on novel heat transfer surfaces under turbulent flow conditions. Journal of Food Engineering, 85, 29-41.
[29] Kern, D. Q., & Seaton, R. E. (1959). A theoretical analysis of thermal surface fouling. British Chemical Engineering, 4, 258-262.
[30] Jullien, C., Benezech, T., Le Gentil, C., Boulange-Petermann, L., Dubois, P. E., Tissier, J. P., et al. (2008). Physico-chemical and hygienic property modifications of stainless steel surfaces induced by conditioning with food and detergent. Biofouling, 24, 163-172.
[31] Christian, G. K., Changani, S. D., & Fryer, P. J. (2002). The effect of adding minerals on fouling from whey protein concentrate:development of a model fouling fluid for a plate heat exchanger. Food and Bioproducts Processing, 80, 231-239.
[32] Hooper, R. J., Paterson, W. R., & Wilson, D. I. (2006). Comparison of whey protein model foulants for studying cleaning of milk fouling deposits. Food and Bioproducts Processing, 84, 329-337.
[33] Blel, W., Legentilhomme, P., Be'ne'zech, T., Legrand, J., & Le Gentil-Lelie`vre, C. (2009a). Application of turbulent pulsating flows to the bacterial removal during a cleaning in place procedure. Part 1: experimental analysis of wall shear stress in a cylindrical pipe. Journal of Food Engineering, 90, 422-432.
[34] Blel, W., Legentilhomme, P., Be'ne'zech, T., Legrand, J., & Le Gentil-Lelie`vre, C. (2009b). Application of turbulent pulsating flows to the bacterial removal during a cleaning in place procedure Part 2: effects on cleaning efficiency. Journal of Food Engineering, 90, 433-440.
[35] Burfoot, D., & Middleton, K. (2009). Effects of operating conditions of high pressure washing on the removal of biofilms from stainless steel surfaces. Journal of Food Engineering, 90, 350-357
[36] Sahu, K. C., Valluri, P., Spelt, P. D. M., & Matar, O. K. (2007). Linear instability of pressure-driven channel flow of a Newtonian and a Herschel-Bulkley fluid. Physics of Fluids, 19, 122101.
[37] Grassi, B., Strazza, D., & Poesio, P. (2008). Experimental validation of theoretical models in two-phase high-viscosity ratio liquid-liquid flows in horizontal and slightly inclined pipes. International Journal of Multiphase Flow, 34, 950-965.
[38] Henningsson, M., Regner, M., O¨ stergren, K., Tra¨ga°rdh, T., & Dejmek, P. (2007). CFD simulation and ERT visualization of the displacement of yoghurt by water on industrial scale. Journal of Food Engineering, 80, 166-175.
[39] Plett, E. A. (1985). Cleaning of fouled surfaces. In D. B. Lund (Ed.), Proceedings of fouling and cleaning in food processing (pp. 286-311).
[40] Mercade-Prieto, R. J., Falconer,W. R., Paterson, & Wilson, D. I. (2007). Swelling and dissolution of beta-lactoglobulin gels in alkali. Biomacromolecules, 8, 469-476.
[41] Yoo, J. I., Chen, X. D., Mercade'-Prieto, R., & Wilson, D. I. (2007). Dissolving heat-induced protein gel cubes in alkaline solutions under natural and forcedconvection conditions. Journal of Food Engineering, 79, 1315-1321.
[42] Bird, M. R., & Fryer, P. J. (1991). An experimental study of the cleaning of surfaces fouled by whey proteins. Food and Bioproducts Processing, 69, 13-21.
[43] Gillham, C. R., Fryer, P. J., Hasting, A. P. M., & Wilson, D. I. (1999). Cleaningin-place of protein fouling deposits:mechanisms controlling cleaning. Food and Bioproducts Processing, 77, 127-136.
[44] Gillham, C. R., Fryer, P. J., Hasting, A. P. M., & Wilson, D. I. (2000). Enhanced cleaning of whey protein soils using pulsed flows. Journal of Food Engineering, 46, 199-209.
[45] Christian, G. K., & Fryer, P. J. (2006). The effect of pulsing cleaning chemicals on the cleaning of whey protein deposits. Food and Bioproducts Processing, 84, 320-328.
[46] Mercade-Prieto, R. J., Falconer,W. R., Paterson, & Wilson, D. I. (2007). Swelling and dissolution of beta-lactoglobulin gels in alkali. Biomacromolecules, 8, 469-476.
[47] Mercade-Prieto, R., Paterson, W. R., Chen, X. D., & Wilson, D. I. (2008). Diffusion of NaOH into a protein gel. Chemical Engineering Science, 63, 2763-2772.
[48] Baier, R. E. (1980). Substrate influences on adhesion of microorganisms and their resultant new surface properties. In G. Bitton, & K. C. Marshall (Eds.), Adsorption of microorganisms to surfaces (pp. 59-104). NY: John Wiley.
[49] Rosenhahn, A., Ederth, T., & Pettitt, M. E. (2008). Advanced nanostructures for the control of biofouling: the FP6 EU 0t AMBIO. Biointerphases, 3, IR1-IR6.
[50] Zhao, Q., Liu, Y.,Wang, C.,Wang, S., & Mu¨ ller-Steinhagen, H. (2005). Effect of surface free energy on the adhesion of biofouling and crystalline fouling. Chemical Engineering Science, 60, 4858-4865.
[51] Mauermann, M., Eschenhagen, U., Bley, Th, & Majscha, J.-P. (2009). Surface modifications application potential for the reduction of cleaning costs in the food processing industry. Trends in Food Science and Technology, 20, S9-S15.
[52] Rosmaninho, R., & Melo, L. F. (2008). Proteinecalcium phosphate interactions in fouling of modified stainless-steel surfaces by simulated milk. International Dairy Journal, 18, 72-80.
[53] Rosmaninho, R., Santos, O., Nylander, T., Paulsson, M., Beuf, M., Benezech, T., et al. (2007). Modified stainless steel surfaces targeted to reduce fouling e evaluation of fouling by milk components. Journal of Food Engineering, 80, 1176-1187.
[54] Liu,W., Fryer, P. J., Zhang, Z., Zhao, Q., & Liu, Y. (2006). Identification of cohesive and adhesive effects in the cleaning of food fouling deposits. Innovative Food Science and Emerging Technologies, 7, 263-269.
[55] Saikhwan, P., Geddert, T., Augustin, W., Scholl, S., Paterson, W. R., & Wilson, D.. (2006). Effect of surface treatment on cleaning of a model food soil. Surface and Coatings Technology, 201, 943-951.
[56] Hooper, R. J., Liu, W., Fryer, P. J., Paterson, W. R., Wilson, D. I., & Zhang, Z. (2006). Comparative studies of fluid dynamic gauging and a micromanipulation probe for strength measurements. Food and Bioproducts Processing, 84, 353-358.
[57] Hooper, R. J., Paterson, W. R., & Wilson, D. I. (2006). Comparison of whey protein model foulants for studying cleaning of milk fouling deposits. Food and Bioproducts Processing, 84, 329-337.
[58] Liu, W., Christian, G. K., Zhang, Z., & Fryer, P. J. (2002). Development and use of a micromanipulation technique for measuring the force required to disrupt and remove fouling deposits. Food and Bioproducts Processing, 80, 286-291.
[59] Liu, W., Christian, G. K., Zhang, Z., & Fryer, P. J. (2006). Direct measurement of the force required to disrupt and remove fouling deposits of whey protein concentrate. International Dairy Journal, 16, 164-172.
[60] Liu, W., Zhang, Z., & Fryer, P. J. (2006). Identification and modelling of different removal modes in the cleaning of model food deposits. Chemical Engineering Science, 61, 7528-7534.

