羧氨基葡聚多糖钠生物胶体液无菌检查法的建立
2012-03-26贵州省药品检验所贵阳550004
陈 玲(贵州省药品检验所,贵阳 550004)
羧氨基葡聚多糖钠生物胶体液属于壳聚糖类衍生物,为无色或微黄、澄明、略有黏性的灭菌液体,用于人体皮肤及创面的修复,具有保护组织纤溶酶原激活物活性,减少渗出,保护、隔离、润滑组织创面及促进愈合的作用,是一种外用喷涂、湿敷、冲洗液[1]。该液具有黏性,动力黏度为1.2~3.0 mpa·s,且对生孢梭菌的作用较强,因此在建立无菌检查方法时必须采用适宜的方法处理样品液并消除其抗菌活性,以确保检验结果的准确性。为此,笔者根据《中国药典》2010年版二部附录无菌检查法[2],建立了该液的无菌检查方法并进行了验证。
1 仪器与材料
1.1 仪器
智能集菌仪HTY-2000A(杭州泰林生物技术设备有限公司);PY330一次性使用全封闭集菌过滤培养器(以下简称集菌器,常州市政政生化设备有限公司,批号:20100412)。
1.2 培养基
硫乙醇酸盐流体培养基(批号:090104)、改良马丁培养基(批号:090104)、营养琼脂培养基(批号:091124)、玫瑰红纳琼脂培养基(批号:0909215)、营养肉汤培养基(批号:090125)均为北京三药科技开发公司产品,试验时均按要求[2]制备及灭菌。
1.3 菌种
金黄色葡萄球菌(Staphylococcus aureus)[CMCC(B)26003]、大肠埃希菌(Escherichia coli)[CMCC(B)44102]、枯草芽孢杆菌(Bacillus subtilis)[CMCC(B)63501]、生孢梭菌(Clostridium sporogenes)[CMCC(B)64941]、白色念珠菌(Candida albicns)[CMCC(B)98001]、黑曲霉(Aspergillus niger)[CMCC(F)98003]均来源于中国食品药品检定研究院。
1.4 样品
羧氨基葡聚多糖钠生物胶体液(贵州扬生医用器械有限公司,批号:20100701,规格:每瓶50 mL,含量:以D-盐酸氨基葡萄糖计不低于1.3 mg·mL-1)。
2 方法与结果
2.1 样品无菌检查方法学验证试验
2.1.1 菌液的制备[2]。取经35℃培养20 h的金黄色葡萄球菌、大肠埃希菌、枯草芽孢杆菌营养肉汤培养物1 mL,生孢梭菌的硫乙醇酸盐流体培养物1 mL,分别用9 mL 0.9%无菌氯化钠溶液(以下简称溶剂)10倍逐级稀释,制成10~100 cfu·mL-1的菌液,备用。
取经25℃培养48 h的白色念珠菌改良马丁液体培养物1 mL,用9 mL溶剂10倍逐级稀释,制成10~100 cfu·mL-1的菌液,备用。
取经25℃培养7 d的黑曲霉改良马丁琼脂斜面培养物,加3~5 mL溶剂洗下霉菌孢子,吸取霉菌孢子悬液1 mL,用9 mL溶剂10倍逐级稀释,制成10~100 cfu·mL-1的菌液,备用。
对所制备的菌液进行计数,结果见表1。
2.1.2 灵敏度检查。取装量为12 mL硫乙醇酸盐流体培养基9份,分别接种金黄色葡萄球菌、大肠埃希菌、枯草芽孢杆菌、生孢梭菌各2份,另一份不接种,为阴性对照,置于30~35℃培养3 d;另取装量为12 mL改良马丁培养基5份,分别接种白色念珠菌、黑曲霉各2份,另一份不接种,为阴性对照,置于23~28℃培养5 d,逐日观察。结果培养基的灵敏度检查均符合规定,详见表2(“+”:表示有菌生长;“-”:表示无菌生长,下表同)。

表1 菌落计数结果Tab 1 Results of bacterial colony count
2.1.3 方法学验证Ⅰ[3]。取集菌器,第1个滤筒按薄膜过滤法滤过样品5瓶,然后将相应的培养基及试验菌加入滤筒中,作为试验管;第2个滤筒不滤样品,直接加入相应的培养基及试验菌,作为阳性对照管;第3个滤筒直接加入相应的培养基,作为阴性对照管。6种试验菌同法操作,置于规定温度培养3~5 d,逐日观察,各试验菌生长情况见表3。
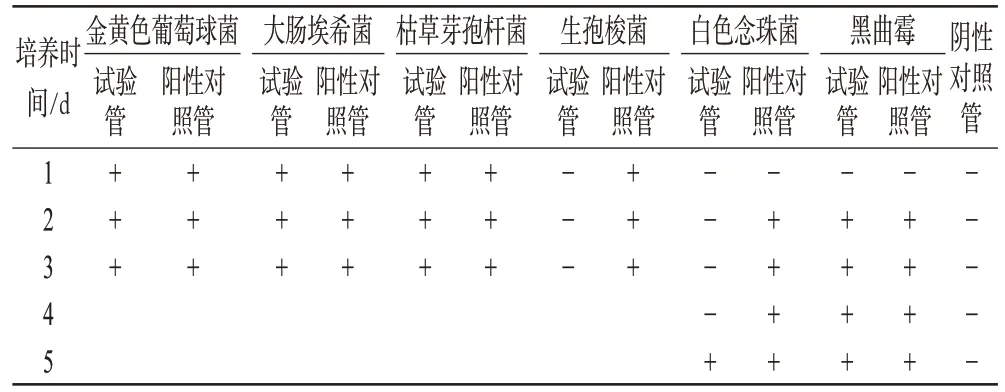
表3 方法学验证结果(Ⅰ)Tab 3 Results of methodology validation(Ⅰ)
表3结果显示,方法学验证Ⅰ中,直接薄膜过滤法验证6种菌,生孢梭菌试验管无菌生长,白色念珠菌试验管到第5天才有少量菌生长,而其他4种菌无论试验管还是阳性对照管都生长良好,说明样品对生孢梭菌、白色念珠菌有抑菌作用,因此需进一步作验证试验。
2.1.4 方法验证Ⅱ。针对被抑制试验菌的情况,采用冲洗方法消除样品对生孢梭菌、白色念珠菌的抑制作用。取集菌器,先用0.1%无菌蛋白胨水溶液浸湿滤筒,第1筒取样品5瓶滤过,然后用500 mL 0.1%无菌蛋白胨水溶液分5次冲洗,冲洗时充分振摇,在最后一次的冲洗液中加入生孢梭菌菌液1 mL,滤过,抽干,然后加入相应的培养基100 mL,作为试验管;同时第2筒、第3筒为阳性、阴性对照管。白色念珠菌同法操作。置于规定温度培养3~5 d,逐日观察。结果,生孢梭菌试验管仍未见菌生长,说明样品对其仍有抑菌作用。各试验菌生长情况见表4。
2.1.5 方法验证Ⅲ。针对被抑制生孢梭菌的情况,采用加热冲洗液冲洗的方法以消除样品对生孢梭菌的抑制作用,其中冲洗液取量分别为500、800 mL。
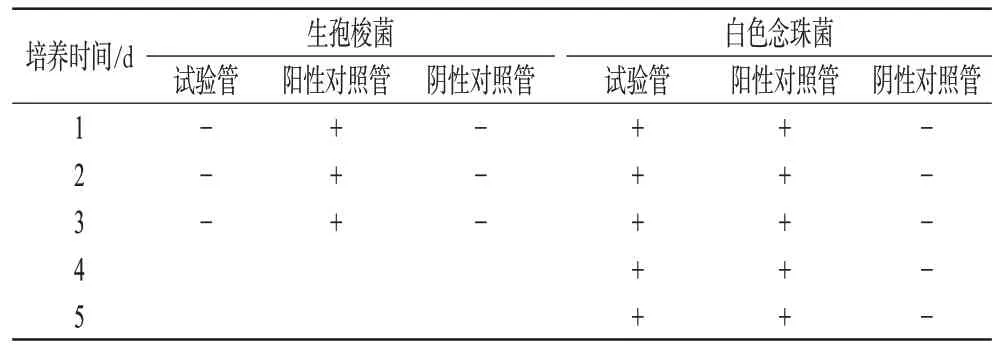
表4 方法学验证结果(Ⅱ)Tab 4 Results of methodology validation(Ⅱ)
取集菌器,先用加热至45℃的0.1%无菌蛋白胨水溶液浸湿滤筒,第1筒取样品5瓶滤过,用每膜500 mL、加热至45℃的0.1%无菌蛋白胨水溶液分5次冲洗,冲洗时充分振摇,在最后一次的冲洗液中加入生孢梭菌菌液1 mL,滤过,抽干,然后加入相应的培养基100 mL,作为试验管;第2、3筒为阳性、阴性对照管。另取集菌器同法进行试验,只是冲洗液取量为800 mL。置于规定温度培养1~3 d,逐日观察,试验菌生长情况见表5。
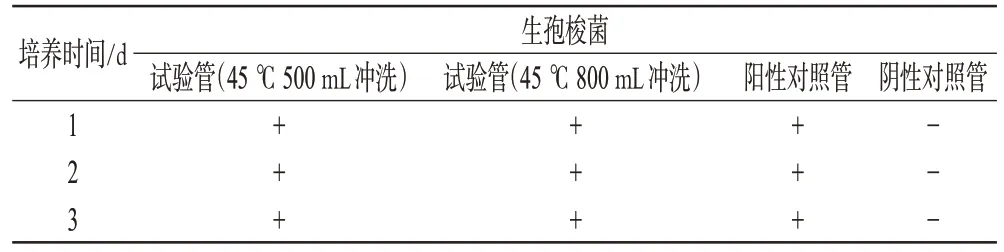
表5 方法学验证结果(Ⅲ)Tab 5 Results of methodology validation(Ⅲ)
方法验证Ⅲ结果说明,采用加热至45℃的0.1%无菌蛋白胨水溶液500、800 mL冲洗,均可消除样品对生孢梭菌的抑制作用。
2.2 样品无菌检查
确定羧氨基葡聚多糖钠生物胶体液无菌检查方法为:取集菌器,先用加热至45℃的0.1%无菌蛋白胨水溶液浸湿,取样品5瓶,滤过,用加热至45℃的0.1%无菌蛋白胨水溶液500 mL(每膜),分5次冲洗,再将相应的培养基100 mL加入滤筒内,以生孢梭菌为阳性对照菌,同时设立阴性对照,按规定温度培养14 d,逐日观察、记录。取样品按照上述方法进行验证试验,结果见表6。
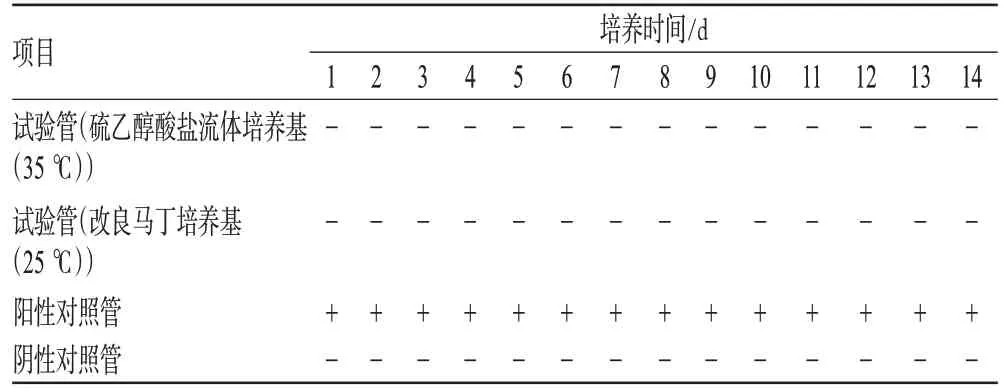
表6 样品无菌检查验证试验结果Tab 6 Sterility validation test results of sample
表6结果显示,羧氨基葡聚多糖钠生物胶体液采用加热至45℃的0.1%无菌蛋白胨水溶液500 mL冲洗(每膜),完全能消除其对生孢梭菌的抑制作用,试验管中各试验菌均生长良好,可作为羧氨基葡聚多糖钠生物胶体液的无菌检查方法。
羧氨基葡聚多糖钠生物胶体液为贵州扬生医用器械有限公司生产,报贵州省药品检验所注册检验,该样品为上市制剂。目前未见有关该类外用冲洗液无菌检查方法的报道。根据《中国药典》相关要求[2],羧氨基葡聚多糖钠生物胶体液属非注射产品,批产量>200,每种培养基最少检验数量为10个,因此取样品60瓶,按上法作6种菌的无菌检查试验,结果见表7。
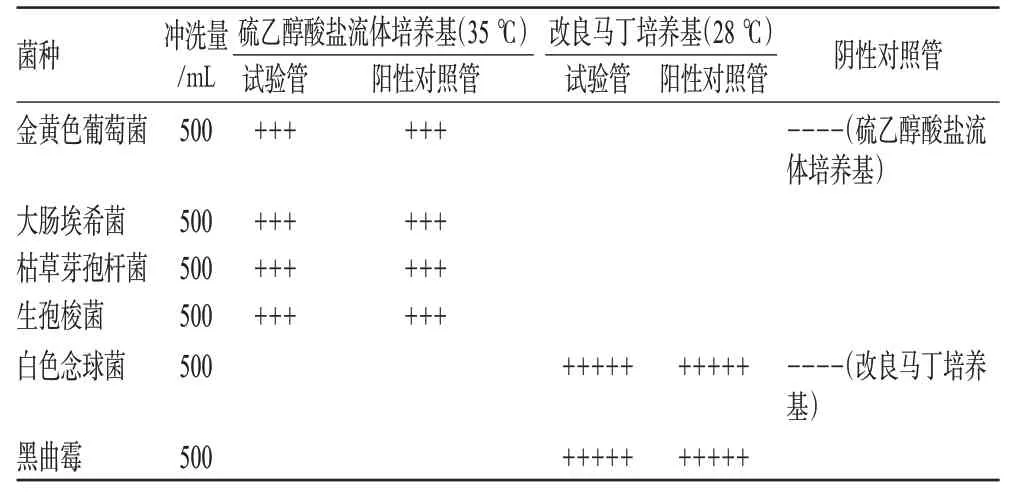
表7 批产量样品无菌检查法验证结果Tab 7 Results of sterility validation of batch production of samples
表7结果显示,按批出厂产品最少检验数量为10个,而上市抽验样品的最少检验数量为5个,虽然批出厂产品检验数量是上市样品检验数量的2倍,但在检验过程中使用加热后的冲洗液浸润滤膜,且冲洗分5次,冲洗时要充分振摇,同样能消除样品的抑菌作用。
3 讨论
根据《中国药典》2010年版二部附录无菌检查法的要求[2],薄膜过滤法为首选方法。薄膜过滤法采取封闭式集菌,供试品取量大,不易漏检,抽滤前的消毒及无菌操作也容易控制,故本试验选择薄膜过滤法。
羧氨基葡聚多糖钠生物胶体液具有一定的抗菌作用,且具黏性,无菌检查时,必须采用加热至45℃的冲洗液冲洗,此温度冲洗液冲洗样品,既不会使滤膜上的微生物受损伤,又能消除其抑菌作用。
[1]贵州扬生医用器材有限公司.羧氨基葡聚多糖钠生物胶体液说明书[S].2010.
[2]国家药典委员会.中华人民共和国药典(二部)[S].2010年版.北京:中国医药科技出版社,2010:附录103-107.
[3]郭朝晖,何晓英,欧阳晓玫.注射用夫西地酸钠无菌检查方法的建立及验证[J].中国药房,2011,22(5):453.
