适应性支持通气在体外循环下心脏手术患者脱机中的研究*
2012-01-24郑瑞强卢年芳於江泉窦英茹
邵 俊 郑瑞强 卢年芳 林 华 於江泉 窦英茹
江苏省苏北人民医院ICU 扬州大学临床医学院,江苏省扬州市 225001
目前临床常用脱机技术包括:T型管自主呼吸、压力支持通气(PSV)、同步间歇指令通气(SIMV)等[1]。以上几种脱机技术究竟哪一种更好,目前颇有争议,Brochard等[2]认为PSV要比T型管和SIMV好,其脱机失败率较低;而Esteban等[3]认为T型管的脱机时间要比SIMV和PSV短。但它们都有一个共同的缺点:即在脱机过程中,需多次观察患者临床表现、血气分析,调整呼吸机的参数决定患者是否开始脱机。这不仅费时费力,而且有可能延迟脱机,延迟脱机往往会造成呼吸机依赖和产生各种并发症,同时增加住院费用[4]。
SIMV是目前最常用的撤机模式之一,此模式既保留了患者的自主呼吸功能,又可逐渐降低呼吸机辅助支持的水平,有利于撤机。
随着计算机和呼吸监测技术的发展,使得实时监测患者自主呼吸能力和呼吸力学并据此自动调节呼吸机参数成为可能。闭合环路通气就是基于上述观念设计的一种新型通气模式。适应性支持通气(ASV)是一种新型的闭合环路通气模式,它通过O-tis运算法,为患者计算出最小呼吸做功的最佳通气频率和通气压力水平并进行通气,以实现良好的人机协调性。同时ASV从控制通气到自主呼吸完全由呼吸机自动切换,无需人工更动,患者始终处于最佳呼吸状态,所作呼吸功最小,并始终引导患者进入脱机状态,理论上ASV模式有利于早日脱机[5]。而ASV模式运用到心脏手术后患者脱机中的研究至今国内尚无相关报道。
本研究目的在于比较ASV和SIMV+PSV模式在心脏手术后患者的脱机,从而比较两种模式在机械通气时间、住ICU时间、气道峰值压力、呼吸机报警次数、人工操作次数等方面的区别,从而为临床寻找一个最合适的脱机模式。
1 材料与方法
1.1 病例选择 (1)入选标准:年龄>18岁,体外循环行非复杂心脏外科手术且可以行快通道拔管者(包括房间隔缺损、室间隔缺损、动脉导管未闭、二尖瓣置换术、主动脉瓣置换术等),术前无肺部感染征象、无肝肾功能不全等情况。(2)排除标准:术前排除标准:年龄≥80岁,术前心功能较差,通过超声心动图示左心射血分数<30%,有COPD病史需要行解痉治疗者(可能会耽误快速拔管);明显肝脏疾病(AST或AL>150IU/L),肾功能衰竭(CRE≥200μmol/L),有癫痫发作病史和中风病史者;术后排除标准:术后严重大出血,术后因外科并发症要再次手术,术后心功能衰竭而需要高剂量的收缩血管药物[多巴胺>20μg/(kg·min),多巴酚丁胺>20μg/(kg·min),去甲肾上腺素>20μg/min)或IABP进行治疗,术后顽固低氧血症(氧合指数 <200mmHg)],术后神经系统并发症而不能合作。
1.2 临床资料 依据上述标准,将2009年1月-2011年12月入住我院重症监护病房,体外循环行非复杂心脏外科手术患者共38例纳入研究。使用随机数字表随机分为ASV组和SIMV+PSV组,其中7例(ASV组3例,SIMV+PSV组4例)患者被排除,最后符合条件的患者ASV组16例,SIMV+PSV组15例,分别给予适应性支持通气和同步间歇指令通气-压力支持通气两种模式,并按标准的脱机程序脱机。
1.3 研究方法 (1)所有研究者手术后ICU的治疗方案相似,若患者入ICU时体温低于36℃,则使用静安持续静脉泵入直至患者体温大于36℃,当患者体温大于36℃后立即停用静安。输注浓缩红细胞使血色素提高到10g/dl以上,术后可以使用多巴胺或多巴酚丁胺使心排指数>2.5L/(min·m2)。若患者苏醒后烦躁不安,或诉明显疼痛,可适当使用镇静药静安20mg静脉推注或镇痛药吗啡1~2mg静脉推注,必要时以上药物可以重复使用。术后若患者存在寒战,可使用杜冷丁25mg静脉推注。入ICU后禁止使用肌松剂。(2)实验共分为三阶段:①ASV组:第一阶段:设置理想体重,分钟通气量设置到100%MV,PEEP 4cmH2O,气道峰压25mmHg(高压报警35cmH2O),吸氧浓度50%,流速促发2L/min,接上呼吸机10min后查血气分析。如果PaCO2<38mmHg或>50mmHg,则把分钟通气量降低或增加20%。10min后可再查血气,直到PCO2达标。当自主呼吸频率到6次或更大,则到第二阶段。查血气分析。第二阶段:将分钟通气量降低到50%MV(20min后查血气),若患者不能耐受,则到第一阶段。第三阶段:分钟通气量降低到25%MV,20min后查血气分析,血气分析符合拔管条件,则拔管。否则进入第二阶段。②SIMV+PSV组:第一阶段:潮气量7ml/kg,频率12次/min,高压报警设置到35cmH2O,吸氧浓度50%、PEEP 5cmH2O,流速促发2L/min,10min后查血气分析,如果PaCO2<38mmHg或>50mmHg,则呼吸频率分别降低或升高2次/min分去到达ASV时的PCO2标准。查血气调整参数(用呼吸频率调整PCO2)。自主呼吸频率到6次或更大有20min,则到第二阶段。第二阶段,PSV模式,PS设置10cmH2O,20min后查血气,窒息通气安全值20s,20min后查血气分析。若患者不能耐受,则到第一阶段。第三阶段,PSV模式,降低PS至5cmH2O,20min后查血气分析,血气分析符合拔管条件,则拔管。否则进入第二阶段。③拔管条件:患者清醒合作,吸氧浓度50%,PEEP=4cmH2O,氧合指数>150mmHg;尿量>0.5ml/(kg·h),引流量<100ml/h,血流动力学稳定,没有难以控制的心律失常发生,第三阶段下吸气压力5~10cmH2O持续20min;直肠温度>36℃。④撤机成功标准:指撤机48h内患者主观感觉舒适、循环稳定、血气分析显示无呼吸性酸中毒及低氧血症,而不需再插管者为撤机成功。
1.4 记录指标 术前记录两组患者的一般情况、疾病种类、APACHEⅡ评分(急性生理与慢性健康评分Ⅱ)、术中记录患者麻醉时间、体外循环时间、阻断时间、术中芬太尼用量、咪唑安定用量、静安用量。入ICU后记录患者静安、吗啡用量,机械通气时间、住ICU时间、每一阶段的血气分析结果、血流动力学指标、呼吸力学指标、呼吸机报警次数、人工操作次数、生命体征。
2 结果
2.1 38例患者符合研究条件被入选,其中7例患者因各种原因被排除,原因包括术后严重的低氧血症2例,术后大出血1例,术后低心排而需要大剂量的血管活性药物4例。最后,31例患者完成此研究。两组患者的一般情况、APACHEⅡ评分(急性生理与慢性健康评分Ⅱ)、麻醉时间、体外循环时间、阻断时间、术中芬太尼用量、咪唑安定用量以及术后静安、吗啡用量无统计学差异。两组患者的疾病种类(房间隔缺损、室间隔缺损、主动脉置换术、二尖瓣置换术病例)亦无统计学差异。
2.2 患者血流动力学和氧代谢动力学参数的比较见表1,从表1知ASV组和SIMV组之间心率、平均动脉压、心排、中心静脉压、肺动脉嵌顿压、血乳酸水平、血pH值、动脉血CO2、氧合指数(PO2/FiO2)之间无统计学差异。但术后0.5h、第一阶段、第二阶段、第三阶段相比,血乳酸水平先升高,后呈逐渐下降趋势,第一阶段血乳酸(Lac)水平较术后0.5h明显升高(P<0.05),第二、三阶段血乳酸水平较第一阶段有所下降,但无统计学差异。
2.3 从表2知,ASV组和SIMV+PSV组的统计学差异主要在第一阶段。第一阶段,ASV组的潮气量明显较SIMV+PSV组高(P<0.05),第二和第三阶段,ASV组潮气量较SIMV+PSV组高,但无统计学差异。第一阶段,ASV组的呼吸频率明显较SIMV+PSV组低(P<0.05);第一阶段ASV组的Pmean和Ppeak明显较SIMV+PSV组低,第二阶段,ASV组的Pmean和Ppeak虽然较SIMV+PSV组低,但无统计学差异。研究发现,ASV组总的机械通气时间比SIMV+PSV组短[(223.9±22.1)min VS(302.9±30.2)min],但主要在第一阶段ASV组比SIMV+PSV组机械通气时间短,而在第二和第三阶段两组机械通气时间无明显差异。

表1 两组患者血流动力学和氧代谢动力学参数的比较
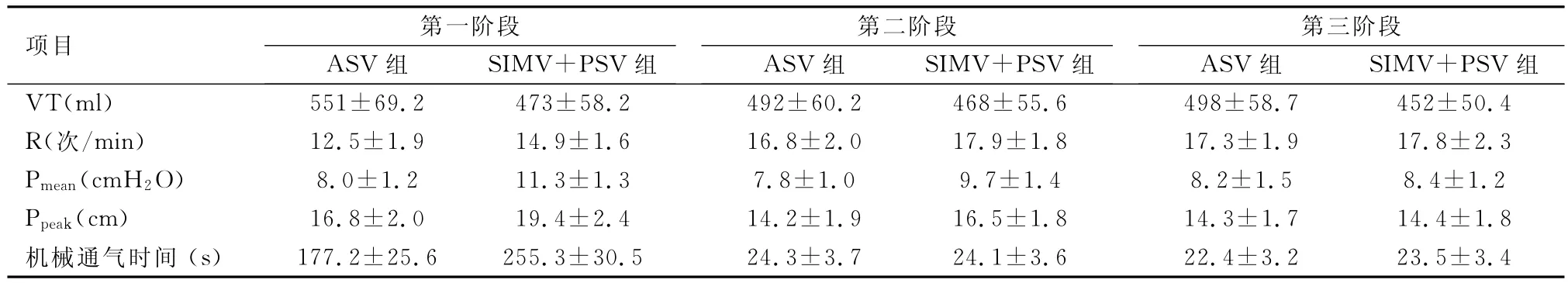
表2 不同组、不同阶段呼吸力学参数和机械通气时间的比较
2.4 从表3知,ASV组的人工操作次数、呼吸机报警次数、窒息通气次数明显比SIMV+PSV组低。
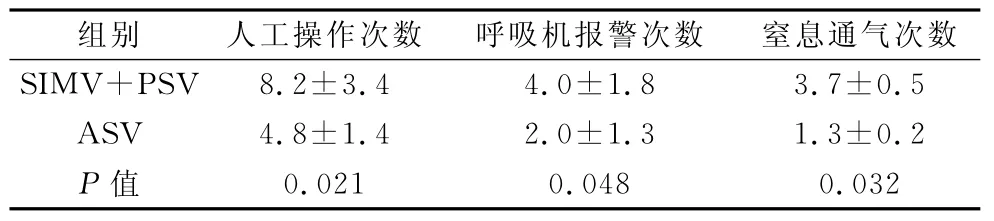
表3 两组之间人工操作次数、报警次数、窒息通气次数比较
3 讨论
适应性支持通气模式(ASV)是20世纪90年代夏美顿公司装备于伽利略呼吸机上的一种闭合环路通气模式,闭合环路模式可以同时监测多个输入参数和控制多个输出参数,这类呼吸模式模拟医生实施机械通气的全过程,获取患者的通气需求和各种相关资料,自动监测各种指标,分析监测结果并及时自动调整呼吸参数,从而使机械通气能适应患者的呼吸能力和通气需求,而且也有利于撤机过程。能参照监测到的肺功能指标来调整某些通气参数,同时避免通气并发症,减少人机对抗,增加患者的舒适度,同时可减少临床医生对呼吸参数的频繁调节和干涉[6]。
近年来,关于ASV模式运用到冠心病冠脉搭桥术后患者中的研究,研究表明ASV模式与常规的通气模式相比,ASV模式能减少脱机拔管时间,减少脱机期间人工操作次数,表明ASV模式在冠心病冠脉搭桥术后患者脱机中显示出巨大的优势[7~9]。但冠心病冠脉搭桥手术毕竟只占心脏手术患者中很小的一部分,至于ASV模式运用到其他心脏全麻术后脱机中的研究至今国内外相关报道甚少。
本研究表明,ASV模式运用到体外循环下非复杂心脏外科手术者,第一阶段,ASV组的潮气量明显较SIMV+PSV组高(P<0.05),ASV组的呼吸频率明显较SIMV+PSV组低(P<0.05);分析原因可能由于ASV测定的是气管插管近端的压力和流量,它们受气管插管阻力的影响较大,气管插管的阻力又是流速依赖型,流速越高插管阻力越大,为了减少由气管插管阻力引起的附加呼吸功,故ASV常会出现低吸气流速、低呼吸频率、大潮气量的呼吸。
同时本研究中,ASV组的平均气道压(Pmean)和气道内峰压(Ppeak)明显较SIMV+PSV组低,本研究结果与国外的研究结果一致[8]。可能与这两种模式的原理不同有关,ASV是建立在Otis等关于最小呼吸功的概念上,即一定的潮气量和呼吸频率总能在维持氧合和酸碱平衡的前提下,使弹性阻力最小,从而能降低气道压力,改善肺的顺应性有关。
本研究发现,ASV组总的机械通气时间比SIMV+PSV组短[(223.9±22.1)min VS(302.9 ±30.2)min],但主要在第一阶段,而在第二和第三阶段两组无明显差异,本研究结果与Dongelmans DA[9]研究结果一致。原因可能与机械通气期间患者自主呼吸的快速恢复有关,在ASV模式中患者恢复自主呼吸后,呼吸机能及时检测到,自动降低控制通气的成分,使患者始终处于最佳呼吸状态,所作呼吸功最小,并最终引导患者进入脱机状态,加快患者的脱机。
研究发现,ASV组与SIMV+PSV组相比,ASV组的人工操作次数、呼吸机报警次数以及窒息通气次数明显比SIMV+PSV组低。表明ASV的操作相对简单,使患者能够保持一个相对稳定的状态。可能与ASV模式本身可自动调节和设置呼吸机参数来适应患者的呼吸能力和通气需求有关,故可减少医务人员参数调节,减少呼吸机报警次数以及窒息通气次。
总之,ASV作为一种脱机模式,能缩短机械通气时间,加快气管插管的拔除,从而减少较长时间的机械通气相关并发症的发生。同时ASV模式需要设置的参数较少,应用过程中需要调节的参数亦较少,操作相对简单,对血流动力学影响小,是一种安全有效的脱机模式。
[1] 宋卫东,王春宝,熊剑飞,等.机械通气中不同脱机方法的比较〔J〕.中国危重病急救医学,2009,21(10):626-627.
[2] Brochard L,Rauss A,Benito S,et al.Comparison of three methods of gradual withdrawal from ventilatory support during weaning from mechanical ventilation〔J〕.Am J Respir Crit Care Med,1994,150(4):896-903.
[3] Esteban A,frutos F,Tobin MJ,et al.A comparison of four methods of weaning patients from mechanical ventilation.Spanish Lung Failure Collaborative Group〔J〕.N Engl J Med,1995,332(6):345-350.
[4] 张纳新,王平,秦英智.249例机械通气患者脱机失败原因分析〔J〕.中国危重病急救医学,2001,13(2):116-117.
[5] Gruber PC,Gomersall CD,Leung P,et al.Randomized controlled trial comparing adaptive-support ventilation with pressure-regulated volume-controlled ventilation with automode in weaning patients after cardiac surgery〔J〕.Anesthesiology,2008,109(1):81-87.
[6] Lellouche F,Brochard L.Advanced closed loops during mechanical ventilation(PAV,NAVA,ASV,Smart Care)〔J〕.Best Pract Res Clin Anaesthesiol,2009,23(1):81-93.
[7] Sulzer CF,Chioléro R,et al.Adaptive support ventilation for fast tracheal extubation after cardiac surgery:a randomized controlled study〔J〕.Anesthesiology,2001,95(6):1339-1345.
[8] Gruber PC,Gomersall CD,Leung P,et al.Randomized controlled trial comparing adaptive-support ventilation with pressure-regulated volume-controlled ventilation with automode in weaning patients after cardiac surgery〔J〕.Anesthesiology,2008,109(1):81-87.
[9] Dongelmans DA,Veelo DP,Paulus F,et al.Weaning automation with adaptive support ventilation:a randomized controlled trial in cardiothoracic surgery patients〔J〕.Anesth Analg,2009,108(2):565-571.
