钛氧化物熔盐电脱氧工艺用氯化物熔盐的选择
2012-01-19陈志远刘俊昊周国治
陈志远,刘俊昊,周国治,2
(1.北京科技大学钢铁冶金新技术国家重点实验室,北京100083)(2.上海大学材料科学与工程学院,上海200072)
钛氧化物熔盐电脱氧工艺用氯化物熔盐的选择
陈志远1,刘俊昊1,周国治1,2
(1.北京科技大学钢铁冶金新技术国家重点实验室,北京100083)(2.上海大学材料科学与工程学院,上海200072)
氧化钛熔盐电脱氧工艺所使用的熔盐电解质体系的选择是其走向工业化应用过程中必然需要解决的问题,然而现有文献中还没有较系统的研究。熔盐成分设计应该从熔盐的密度、粘度、表面性质、电导、离子迁移数及氧溶量等多方面考虑。因此在氯化物范围内从蒸汽压、熔点、分解电压及经济性等方面对氧化钛熔盐电脱氧工艺可以使用的各种熔盐做了考察,结果表明,可以使用的熔盐主要成分为CaCl2-KCl-NaCl三元系。BaCl2和LiCl及稀土氯化物等也可以适量加入电解质中。
熔盐;电脱氧;钛
1 前言
2000年以来,钛氧化物熔盐电脱氧工艺从FFCCambridge 法[1-2]发展到 OS 法[3-4]、SOM 法[5]、USTB法[6]及EMR/MSE法[7]等众多制备金属钛或钛合金的方法,并且有部分工艺已经向放大实验阶段发展。人们对熔盐电脱氧原理[8-10]、电解工艺参数[4]、阴极材料的制备和影响[10-12]、惰性阳极材料[13-14]等一系列的问题都已进行了大量的研究。众所周知,电解质性质对电解过程的影响十分重要,但在熔盐成分的选择优化方面,文献并没有给出系统和全面的考虑。现有工作中采用的电解质主要是氯化物体系,因为相对氟化物而言氯化物腐蚀性较弱,便于废弃物处理,其熔点也比氟化物和氧化物低,相对储量也较高。如表1所示,研究所用的电解质集中在单一的CaCl2,CaCl2配加一定量的NaCl以及KCl和NaCl混合物这几种熔盐体系上。也就是说,CaCl2,KCl和NaCl是现有研究考虑的基本体系,而且大多数研究采用纯CaCl2的电解质体系。但是在选择这些熔盐的必要性以及熔盐具体成分设计方面,文献中并没有详细的阐述,工艺路线是不完备的。如FFC-Cambridge工艺最开始采用CaCl2熔盐电解,但最终与OS法一样都采用了除CaCl2熔盐外还加入少量CaO。加入CaO对于OS法是工艺原理的要求,而FFC-Cambridge法是从动力学来考虑的。但是它们都没有对熔盐作用机理进行更深入地探讨。另外,随着工艺路线不断拓展,熔盐从单一的CaCl2向多种氯化物混合发展,虽然在这方面有一些评估和研究[15-18],然而却没有相关熔盐性质的详细论述,更多的研究工作是必要的。
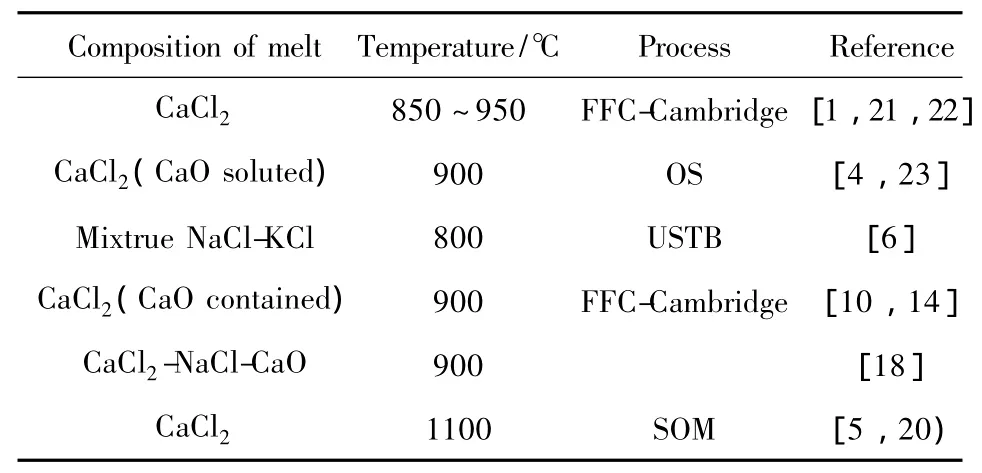
表1 文献中钛熔盐电脱氧生产方法研究采用的熔盐成分Table 1 The composition of melt using the electro-deoxidation process to produce Ti
使用氯化钙的原因在于氯化钙价格较低、熔点适宜、蒸气压低、氧溶量较高等。作为一项基础性的工作,本文将从以下几个因素来评价氯化物熔盐的可用性,并通过筛选得出合适的氯化物熔盐体系。在此基础上,通过对熔盐具体性能的评价和综合讨论,我们将进一步提出适合这一工艺体系的较优熔盐。
2 熔盐的选择
2.1 常见的氯化物熔盐
在进行物理化学性质的考量之前,首先从其价格因素来考虑。钛的生产需要向低成本的方向发展,因此成本过高、产量太少的氯化物不能做为主要成分使用。但稀土氯化物ReClx这一类熔盐可能对电解过程有所帮助,也可以做为微量添加剂加入。图1元素周期表中氯化物可作为本文研究的氯化物范围。表中给出了各元素对应的常见氯化物的熔点和相应阳离子价态[19]。其中有的元素有2种对应常见的氯化物。接近室温以液态形式存在、或直接从固态升华成气态的部分氯化物并未列出。

图1 氯化物对应阳离子价态及相应熔点(K)Fig.1 Melting point of chlorides(K)and valence state of corresponding cations
2.2 熔盐的熔点
大多数研究工作是在800~900℃范围进行的。这个温度的选择和熔融CaCl2的粘度、电导率变化及蒸汽压等有关。对于纯CaCl2来说,这样温度下的单位挥发量较少,同时由于比熔点高出一些,因此流动性和导电性都有较大提高。在一些文献中采用的实验温度更低一些,是因为加入了KCl等熔盐,使电解质的熔点下降。决定熔盐电脱氧温度的一个重要因素是高温时氧化钛阴极中氧的脱除速率比较快。温度较高可以使电脱氧的动力学有较明显的改善,但是温度升高也伴随着熔盐蒸气压升高、腐蚀性增强以及工艺成本增加。就以上温度考量,电脱氧工艺中熔盐的熔点比800~900℃这个范围低数十摄氏度较好。这样既保证了熔盐流动性,也避免温度相对熔点过高带来的弊端。因此熔盐主要成分的熔点须满足这一条件,而其它成分可以在这一范围上下浮动。一些熔点接近于室温的氯化物如AlCl3,ZnCl2,BiCl3等就不能做为熔盐的主要成分。大多数的稀土氯化物的熔点正好在电解温度附近。就熔点来说,Ca,K,Na,Mg,Zr,Co,Cr等元素的氯化物都适宜做电解质主要成分,Ba,Sc,Sr等元素的氯化物可适量加入。
2.3 熔盐的蒸气压
有些氯化物在熔点以上不多的温度下就能达到较大蒸气压值。蒸气压过高会使氯化物在电解过程中气相挥发,造成损失,影响电解进行。氯化物在电解槽的低温部位凝集,电解质成分波动等都对生产过程不利。研究中采用的CaCl2,NaCl,KCl都是蒸气压较低的熔盐。根据文献[19]计算,在800~900℃范围内接近这3种氯化物蒸气压的氯化物如图2所示。其中KCl,NaCl,MgCl2,LiCl等熔盐由于存在多种气相,图中只选取了其中气相分压较高的相。由图可见BaCl2,CaCl2,AgCl及图中ReClx的蒸气压较低,KCl,NaCl,LiCl和MgCl2等次之。可做电脱氧熔盐主要成分的除了稀土氯化物以外,以上氯化物都适宜。

图2 氯化物蒸气压与温度的关系Fig.2 Vapor pressure of chlorides
2.4 熔盐的分解电压
据Factsage计算,在钛熔盐电脱氧过程中发生的反应式为:

脱氧工艺电压以此为基础来设计。在不同工艺中,采用的脱氧电压有所不同。如FFC-Cambridge法和OS法等通常采用2.5~3.2 V操作电压[2,4];由于 SOM 法采用固体透氧膜防止了某些副反应的发生,所以采用的电压值可以更高[20]。这些电压值必须超过TiO2及其电解过程产生的中间生成物的分解电压。一般来说,熔盐的分解电压应该在工作电压之上。图3列出了除稀土元素以外的常见氯化物的分解电压以及电脱氧总反应式对应电压值。可以看出在碳作为阴极的情况下,相对于氯化物分解电压,TiO2电脱氧所需电压值不大。那么,结合其蒸气压值情况,从熔盐分解电压来考虑,Ba,K,Na,Ca,Li,Mg,Zr,Cr,Pb,Fe 等对应的氯化物都可以做为钛氧化物熔盐电脱氧所使用的电解质。但Zr,Cr,Fe,Pb均为变价元素,其氯化物做为电解质会产生电流空耗等问题。考虑到毒性和价格因素,BaCl2与LiCl不能做为主要成分使用。另外,如果对现有熔盐电解中常采用的电解电压来说,MgCl2仅有的2 V左右的分解电压是不太合适的。因此,KCl,NaCl,CaCl2是应考虑的基本氯化物电解质。
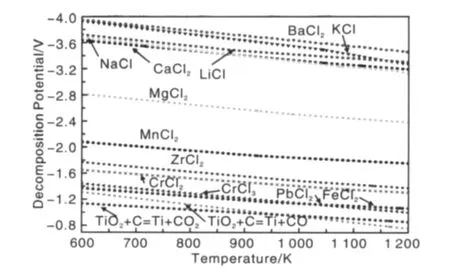
图3 氯化物熔盐分解电压与氧化钛电解电压值的比较Fig.3 Comparison of decomposition voltage of chlorides and electro-deoxidation voltage of titanium oxide
如果考虑电脱氧工艺中的阳极材料为惰性材料,那么反应过程就应该是以下方程:

这样一来,电脱氧所需电压值就大大上升了。如图3所示,KCl,NaCl,CaCl2,MgCl2,BaCl2与 LiCl可以满足要求。
钛有多种价态,相应也有许多氧化物形式存在,另外如果考虑在熔盐中电解,又可能与熔盐中的成分反应生成另外的复杂氧化物。这样使钛在电脱氧过程中的存在形式随电解时间的延长而会发生多次变化。由于动力学条件和观察手段等不同,不同文献检测到的反应中间产物中钛存在形式也不同。Fray及Bhagat等的研究观察到电解过程中钛的高价氧化物向低价氧化物方向依次出现,并且CaCl2作为电解质时会有钙钛氧化物的出现[10,21-22,24]。因此在这种多种氧化物存在的复杂情况下,避免不利于电脱氧过程的氧化物也是一项重要的研究内容。
就熔盐的选择来说,中间产物的分解电压也是需要考虑的影响因素之一。因为全部中间产物在施加的工作电压下均希望向有利于电脱氧过程的方向转变。图4根据文献中提及的常见的反应中间产物给出了可能发生的一些电化学反应对应电位值。其中,根据Suzuki的研究,电解质中对应最佳氧含量范围的是0.5% ~1.0%(物质的量)的 CaO[23]。因此,图4还给出了一组不同活度的CaO电解还原反应对应的电位值曲线。这一组曲线对应的电位值是最高的。从图4中可知,对于OS法,电脱氧无论是否使用惰性阳极,所选择氯化物电解质均是 KCl,NaCl,CaCl2,BaCl2与LiCl。FFC-Cambridge法的氯化物选择范围除此之外还有MgCl2。由于SOM法有固体电解质膜存在,所以电解质可选范围应该可以在FFC-Cambridge法的基础上适当增加。
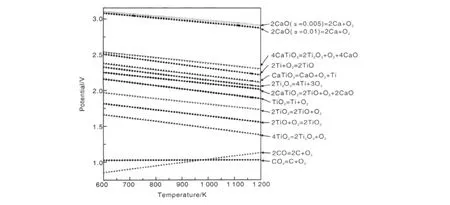
图4 电脱氧工艺中可能出现的部分电化学反应对应电位值Fig.4 The potential value of some electrichemical reaction in electro-deoxidation process
2.5 KCl-NaCl-CaCl2三元系的研究
从以上几个因素可以看出KCl-NaCl-CaCl2三元系作为电脱氧工艺生产金属钛或钛合金的基础三元系是较合适的。因此对以这个三元系为基础的多元系熔盐性质进行深入研究是必要的。
熔盐性质研究属于高温热力学范畴。通常,精确测定热力学数据对于实验设备、人员操作和经费要求是很高的。高温操作使实验更加困难,花费时间更长,还要保证数据具有足够的精确度。针对熔体的复杂性和测量上的困难,近年发展起来的半经验半理论的热力学模型,是解决上述困难的一种十分有效的方法。尤其以基于二元系计算多元系的“几何模型”,在相图计算和热力学性质的预测中,起到了重要的作用。其准确性和广泛的适用性已得到了检验。
几何模型是一类利用二元系热力学性质去计算三元系乃至多元系热力学性质的模型。我们已经将其成功应用到了四元系的计算中,并对多种热力学性质作了成功的预测。几何模型的发展经过了2个阶段。第一代模型有很多种,总体划分为对称模型和非对称模型。前者不能由三元系还原到二元系,而后者则会由于非对称造成了计算中选点的不唯一性。新一代几何模型打破了对称和非对称的界限,并克服了几何模型中的缺陷[25-28]。用这一模型预测熔盐性质,将有助于电脱氧电解质体系的优化工作。
新一代几何模型的核心在于提出了权重因子等相关概念,认为三元系计算所需的二元系点的选取与对应的体系有关。计算的基本思路是通过权重因子的分配,将三元系热力学超额量用边界上的二元系量求出。
三元系i-j-k的热力学性质超额量YE可用下式表示:


这里的xi和xj表示三元系中组元i和j各自占的量。它们与二元系i-j中组元i的量的关系如下所示::

这里,相似系数:
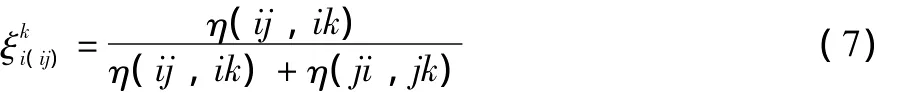
表示i-j和j-k两个二元系之间相偏离的偏差函数为:

在电脱氧熔盐性质研究中,我们利用几何模型初步进行了计算,根据 Janz的数据[29-30]得到在1 080 K温度时的KCl-NaCl-CaCl2三元系熔盐当量电导图如图5所示。由图5可知,NaCl的当量电导是最高的,而CaCl2-KCl的当量电导是最低的。除了这一体系电导的计算外,其它性质和体系也正在计算和评估中。

图5 KCl-NaCl-CaCl2三元系在1 080 K的当量电导值Fig.5 The equivalent conductance of KCl-NaCl-CaCl2at 1 080 K
3 结论
熔盐的成分设计应该还从熔盐的密度、粘度、表面性质、电导、离子迁移数及氧溶量等多方面考虑。研究结果表明,KCl-NaCl-CaCl2三元系可以作为电脱氧生产金属钛或钛合金的基础三元系。BaCl2,LiCl及稀土氯化物可少量加入。K,Na,Ca,Ba,Li对应的氯化物的分解电压绝对值都在3 V以上,因此电解时操作电压可大幅提升,有利于提高还原速率。实际上,多元系熔盐性质的信息还比较缺乏,需要大量的理论估算和实验测定。一些有关KCl-NaCl-CaCl2三元系性质的详细研究已经展开,我们对摩尔电导和熔盐密度等性质的计算及测定已经部分完成。其它性质的测定和优化,以及电脱氧熔盐体系的评定工作也正在计划中。
在电解过程中,由于碳、氧化物、氯化物等多种化学物质共存,副反应的发生在所难免。因此,减少副反应的发生和促进电脱氧反应的进行也是研究的重要内容,熔盐成分配比对这两者的影响十分显著。因此,探索熔盐成分、性质、结构与电脱氧过程中一些工艺参数之间的关系是非常必要的。
References
[1]Chen G Z,Fray D J,Farthing T W.Direct Electrochemical Reduction of Titanium Dioxide to Titanium in Molten Calcium Chloride[J].Nature,2000,407(6 802):361 -364.
[2]Schwandt C,Doughty G R,Fray D J.The FFC-Cambridge Process for Titanium Metal Winning[J].Key Engineering Materials,2010,436:13-25.
[3]Ono K,Suzuki R.A New Concept for Producing Ti Sponge:Calciothermic Reduction[J].JOM-Journal of the Minerals Metals &Materials Society,2002,54(2):59-61.
[4]Suzuki R O,Ono K,Teranuma K.Calciothermic Reduction of Titanium Oxide and In-Situ Electrolysis in Molten CaCl2[J].Metallurgical and Materials Transactions B—Process Metallurgy and Materials Processing Science,2003,34(3):287 -295.
[5]Ye X S,Lu X G,Li C H,etal.Preparation of Ti-Fe Based Hydrogen Storage Alloy by SOM Method[J].International Journal of Hydrogen Energy,2010,36(7):4 573-4 579.
[6]Jiao S,Zhu H.Electrolysis of Ti2CO Solid Solution Prepared by TiC and TiO2[J].J Alloys Compd,2007,438(1 -2):243 -246.
[7]Abiko T,Park I,Okabe T H.Reduction of Titanium Oxide in Molten Salt Medium[C]//Procedings of 10thWoild Conference on Titanium.Hamburg:10thWorld Conference on Titanium,2003:261-268.
[8]Fray D.Emerging Molten Salt Technologies for Metals Production[J].JOM—Journal of the Minerals Metals& Materials Society,2001,53(10):27-31.
[9]Suzuki R O.Direct Reduction Processes for Titanium Oxide in Molten Salt[J].JOM—Journal of the Minerals Metals& Materials Society,2007,59(1):68 -71.
[10]Alexander D T L,Schwandt C,Fray D J.The Electro-Deoxidation of Dense Titanium Dioxide Precursors in Molten Calcium Chloride Giving a New Reaction Pathway[J].Electrochimica Acta,2011,56(9):3 286-3 295.
[11]Ma M,Wang D,Wang W,etal.Extraction of Titanium from Different Titania Precursors by the FFC Cambridge Process[J].Journal of Alloys and Compounds,2006,420(1-2):37-45.
[12]Centeno-Sanchez R L,Fray D J,Chen G Z.Study on the Reduction of Highly Porous TiO2Precursors and Thin TiO2Layers by the FFC-Cambridge Process[J].Journal of Materials Science,2007,42(17):7 494-7 501.
[13]Jiao S,Fray D.Development of an Inert Anode for Electrowinning in Calcium Chloride-Calcium Oxide Melts[J].Metallurgical and Materials Transactions B,2010,41(1):74-79.
[14]Barnett R,Kilby K T,Fray D J.Reduction of Tantalum Pentoxide Using Graphite and Tin-Oxide-Based Anodes via the FFC-Cambridge Process[J].Metallurgical and Materials Transactions B—Process Metallurgy and Materials Processing Science,2009,40(2):150-157.
[15]Lebedev V A,Sal Nikov V I,Sizikov I A,etal.Mechanism and Kinetics of Processes Occurring at TiO2Cathode in CaCl2-CaO Melt[J].Russian Journal of Applied Chemistry,2007,80(9):1 503-1 508.
[16]Suzuki R O.Calciothermic Reduction of TiO2and in Situ Electrolysis of CaO in the Molten CaCl2[J].Journal of Physics and Chemistry of Solids,2005,66(2-4):461-465.
[17]Freidina E B,Fray D J.Study of the Ternary System CaCl2-NaCl-CaO by DSC[J].Thermochimica Acta,2000,356(1 -2):97-100.
[18]Wang S,Wang W,Li S,etal.Cathodic Behavior of Molten CaCl2-CaO and CaCl2-NaCl-CaO[J].International Journal of Minerals,Metallurgy and Matericals,2010,17(6):791 -794.
[19]Hesselmann K,Kubaschewski O,Knacke O.Thermochemical Properties of Inorganic Substances[M].Berlin:Springer,1991.
[20]Zou X L,Lu X G,Li C H,etal.A Direct Electrochemical Route from Oxides to Ti-Si Intermetallics[J].Electrochimica Acta,2010,55(18):5 173-5 179.
[21]Schwandt C,Fray D.Determination of the Kinetic Pathway in the Electrochemical Reduction of Titanium Dioxide in Molten Calcium Chloride[J].Electrochim Acta,2005,51(1):66 -76.
[22]Alexander D,Schwandt C,Fray D.Microstructural Kinetics of Phase Transformations during Electrochemical Reduction of Titanium Dioxide in Molten Calcium Chloride[J].Acta Materialia,2006,54(11):2 933-2 944.
[23]Suzuki R.Calciothermic Reduction of TiO and in Situ Electrolysis of CaO in the Molten CaCl2[J].Journal of Physics and Chemistry of Solids,2005,66(2-4):461-465.
[24]Bhagat R,Dye D,Raghunathan S L,etal.In Situ Synchrotron Diffraction of the Electrochemical Reduction Pathway of TiO2[J].Acta Mater,2010,58(15):5 057 -5 062.
[25]Zhang G H,Wang L J,Chou K C.A Comparison of Different Geometrical Models in Calculating Physicochemical Properties of Quaternary Systems[J].Calphad,2010,34(4):504 -509.
[26]Chou K C.A General Solution Model for Predicting Ternary Thermodynamic Properties[J].Calphad,1995,19(3):315 -325.
[27]Chou K C.A New Solution Model for Predicting Ternary Thermodynamic Properties[J].Calphad,1987,11(3):293 -300.
[28]Chou K C,Wei S K.A New Generation Solution Model for Predicting Thermodynamic Properties of a Multicomponent System from Binaries[J].Metallurgical and Materials Transactions B,1997,28(3):439-445.
[29]Janz G J,Allen C B,Bansal N P,etal.Physical Properties Data Compilations Relevant to Energy Storage.Ⅱ.Molten Salts:Data on Single and Multi-Component Salt Systems[R].NY:Rensselaer Polytechnic Inst,Cogswell Lab,1979.
[30]Janz G J.Physical Properties Data Compilations Relevant to Energy Storage[M].Washington:US Dept of Commerce,National Bureau of Standards,1981.
Selection of Chlorides Melt in Titanium Oxide Electro-Deoxidation Process
CHEN Zhiyuan1,LIU Junhao1,ZHOU Guozhi1,2
(1.State Key Laboratory of Advanced Metallurgy,University of Science and Technology of Beijing,Beijing 100083,China)(2.School of Materials Science and Engineering,Shanghai University,Shanghai 200072,China)
It is an important issue to be solved that how to select suitable electrolyte in the research of electro-deoxidation process to produce titanium from oxides.But there is no systemic study in literatures.A molten salt composition should be designed from the molten salt density,viscosity,surface properties,conductivity,ion migration number and dissolved oxygen etc..This paper discussed the proper chlorides which could be used in this process.Melting point,vapor tension,decomposition voltage,and other aspects have been investigated.CaCl2-KCl-NaCl tertiary was proposed to be the basis electrolyte system.BaCl2,LiCl and rare earth chlorides were important adjunct too.Some systematic study of these melts should be carried out with the consider of some phenomenon surveyed in previous research and properties of chlorides.
fused salt;electro-deoxidation;titanium

周国治
O645.5;TF823
A
1674-3962(2012)01-0044-06
2011-11-02
国家自然科学基金资助项目(50974084,51174022)
陈志远,男,1987年生,博士
周国治,男,1937年生,中国科学院院士
