早期药物干预能够预防2型糖尿病发生
2012-01-16德弗罗佐
德弗罗佐
早期药物干预能够预防2型糖尿病发生
德弗罗佐
在美国,大约有2.1千万例2型糖尿病患者,而糖耐量减低(IGT)的人数则是其两倍。接近40%~50%的糖耐量减低患者在一生之中会进展为2型糖尿病。因此,治疗患有IGT的高危人群,防止2型糖尿病发生,具有重要的医疗、经济和社会价值。虽然减轻体重能有效减少IGT转变为2型糖尿病,却理想的体重减轻常常难以达到和维持。而且,即使体重得到有效降低,仍然有40%~50%的IGT患者会进展为2型糖尿病。对比发现,IGT患者接受口服降糖药,改善胰岛素敏感性,且保护胰岛β细胞功能——IGT和2型糖尿病特征性的病理生理异常——都显示出可以阻止IGT转变为2型糖尿病。多个研究一致性地观察到噻唑烷二酮药物的2型糖尿病预防作用(Troglitazone in the Prevention of Diabetes [TRIPOD], Pioglitazone in the Prevention of Diabetes [PIPOD], Diabetes Reduction Assessment with Ramipril and Rosiglitazone Medication [DREAM], and Actos Now for the Prevention of Diabetes [ACT NOW]),可减少50%~70%的IGT转变为2型糖尿病。在美国糖尿病预防计划(DPP)中,二甲双胍使2型糖尿病发生风险减少了31%,同时被美国糖尿病协会(ADA)推荐用于治疗IGT高危人群。因为大部分IGT患者完全或几乎完全处于胰岛素抵抗状态,已丧失70%~80%的β细胞功能,有10%的几率发生糖尿病视网膜病变,所以,我们应该对其进行饮食、运动和药物的联合干预。
在美国,2型糖尿病患病率为7%,影响到2.1千万人。因为以下多种因素,过去几十年,2型糖尿病的患病率急剧增大。1)人群寿命增加;2)肥胖患病率增加;3)运动减少;4)2型糖尿病高危的少数族裔人口快速增长。2型糖尿病患者面临着严峻的微血管和大血管并发症高发病率和死亡率。美国糖尿病协会(ADA)评估2007年糖尿病及其相关并发症的花费是1,740亿美元,而且最近研究评估到了2050年糖尿病的相关费用将超过2倍。
来自糖尿病控制与并发症研究(DCCT)、英国前瞻性糖尿病研究(UKPDS)以及其他研究的结果已经明确了高血糖是微血管并发症的主要危险因素,以及大血管并发症的次要因素。因此,对于新诊断的2型糖尿病患者,更加强调在没有严重的副作用前提下,应尽可能获得正常的血糖控制。然而,美国糖尿病患者平均的血糖控制仍未达标。而且一旦空腹血糖明显增高,伴随而来的是持续的β细胞功能衰退。因为大部分2型糖尿病的致残率和死亡率升高源于长期并发症,早期发现和预防将对人文、社会、医疗和经济产生重大的有利影响。考虑到这些,我们有理由在2型糖尿病自然病程的早期即进行干预,采取针对逆转在糖尿病前期呈现且最终导致显性糖尿病的特异性病理生理缺陷的措施。这个方法需要具备:1)对于面临今后可能发展为2型糖尿病风险的糖尿病前期个体的识别能力;2)能够逆转导致2型糖尿病的病理性紊乱的干预手段。预防达到糖尿病诊断水平的高血糖有望阻止或减少微血管并发症的发生率。然而糖耐量减低(IGT)/空腹血糖受损(IFG)个体仅有中等升高的血糖水平,并且葡萄糖是心血管疾病相对较弱的危险因素。因此,可能是其它心血管因素导致了大血管疾病发生率的增加。降低A1C水平本身可能并不能减少心血管并发症,除非用于治疗IGT/ IFG的药物独立于血糖降低效应之外,能够纠正已知的心血管危险因素。
已知的2型糖尿病危险因素包括家族史、肥胖、胰岛素抵抗(代谢)综合征组分(血脂紊乱、高血压、内脏型肥胖、IGT、凝血异常、内皮功能紊乱)、胰岛素抵抗和高胰岛素血症、胰岛素分泌功能受损、妊娠期糖尿病、多囊卵巢综合征、IGT、IFG和高危种族。在已知的糖尿病危险因素中,β细胞衰退和胰岛素抵抗具有极大的2型糖尿病预测作用。IGT和IFG是2型糖尿病的强烈预测指标。大约50%的IGT个体在一生中会进展为2型糖尿病,每年进展为2型糖尿病的发生率波动在2.3%~11%(决定于特定的人群),而美国大约4.1千万人患有IGT。ADA认为A1C水平在5.7%~6.4%之间是糖尿病危险范围。然而,争论存在于在这一范围的A1C值如何预测将来的糖尿病风险。IGT进展为2型糖尿病的其他危险因素包括肥胖(尤其是内脏型肥胖)、空腹血糖>90~95mg/dL以及口服葡萄糖耐量试验血糖浓度总和处于IGT人群的前五十百分位数。年龄、炎症标志物(超敏C反应蛋白、肿瘤坏死因子-α、白介素-6)、脂联素和铁蛋白都被证实可预测糖尿病发生风险。通过选择具有一个或多个其他糖尿病危险因素的IGT人群,美国糖尿病预防项目(DPP)证实了一个IGT到2型糖尿病的年转变率约为11%。一项类似的高转化率呈现在DREAM研究中。在TRIPOD中,妊娠期糖尿病妇女糖尿病年转变率为12.4%。ACT NOW 研究中,安慰剂组IGT发展为2型糖尿病的年转变率略低,为6.0%。
界定了2型糖尿病的高危人群,我们有必要对其进行干预:1)逆转已知导致IGT/IFG个体葡萄糖稳态失衡的病理机制;2)可耐受地、安全地以及理想地减少IGT个体的心血管疾病危险。在接下来的部分,我们将简要评述2型糖尿病的病因,从而提供一个合理的药物干预策略。
2 型糖尿病的病因学
2 型糖尿病是遗传与环境因素共同作用的结果。空腹高血糖(≥126mg/dL)的糖尿病患者,尽管哪一种缺陷作为主要异常因素存在争议,胰岛素抵抗和胰岛素分泌功能受损都是特异性特征。目前证据支持2型糖尿病分两步发展。第一步,糖耐量正常(NGT)的个体进展到以胰岛素抵抗为主的IGT。第二步,随着β细胞功能进行性衰退,IGT恶化为2型糖尿病。IGT进展为2型糖尿病也与进一步的胰岛素敏感性减退有关。
胰岛素抵抗
胰岛功能受损是2型糖尿病的特异性特征,包括肝脏、肌肉和脂肪组织。胰岛素抵抗在2型糖尿病发生前就存在,并起到关键作用。因此,2型糖尿病个体的NGT一级亲属(糖尿病高危人群)明显对胰岛素抵抗。类似地,IGT人群也对胰岛素抵抗,同时表现出代偿性高胰岛素血症。高胰岛素血症,反映潜在的胰岛素抵抗,在2型糖尿病高发病率人群(高加索人、墨西哥裔美国人、瑙鲁人、日本裔美国人和皮马印第安人)中很常见,可预测IGT和2型糖尿病的发生。大量证据支持胰岛素抵抗的遗传因素,并因包括体重增加、运动减少和年龄增加在内的环境因素而恶化。
总之,胰岛素抵抗是2型糖尿病的共同特征,发生在IGT个体以及具有2型糖尿病遗传倾向的NGT个体病程早期。因此,旨在提高IGT个体胰岛素敏感性的干预可能有效阻止或延迟IGT进展为2型糖尿病。
胰岛素分泌受损
尽管胰岛素抵抗是导致NGT进展为IGT直至2型糖尿病的主要致病因素,直到β细胞功能不能代偿胰岛素抵抗时血糖控制才会恶化。最终,β细胞功能衰退导致IGT进展为2型糖尿病。在IGT人群中,OGTT 2小时较低的血清胰岛素浓度预示任何种族IGT人群进展为2型糖尿病。当空腹血糖超过100~110mg/dL,第一时相胰岛素分泌降低是IGT人群的共同点,受损的第一时相胰岛素分泌也意味着进展为糖尿病。β细胞功能不全是原发的还是继发于糖毒性或脂毒性或肠促胰岛素缺陷,这依然存在争论。值得注意的是,即使在NGT范围,β细胞功能是NGT进展为IGT,继而进展为2型糖尿病的最佳预测因子。一旦显性2型糖尿病发生,不论采用何种高血糖治疗方式(二甲双胍、磺脲类、胰岛素),β细胞功能都会日益衰退。包括遗传易感性、导致胰岛素分泌增多的胰岛素抵抗、糖毒性、脂毒性、受损的肠促胰素释放、胰岛胰淀素积累以及减少的β细胞数量在内的多种因素都被认为是导致β细胞损害的因素。理想情况下,旨在阻止IGT进展为2型糖尿病的干预措施应该能延迟或阻止β细胞功能衰退的发展。β细胞功能衰退的开始和严重程度在糖尿病病程的很早期就已存在,这比之前的认识要更为严重。在两项大型研究——圣安东尼奥代谢研究和退伍军人管理局遗传流行病学研究,259例IGT患者、201例2型糖尿病患者和318例NGT者接受OGTT胰岛素或C肽测量和正葡萄糖胰岛素钳夹试验。IGT患者按照OGTT 2h血糖值被分为三组(140~159、160~179和180~199mg/ dL)。伴随OGTT 2h血糖升高,血清胰岛素水平一开始升高,进而逐渐降低。然而血清胰岛素水平不能提供准确的β细胞功能。β细胞受血糖升高的刺激而引起血清胰岛素增加,这个反应受胰岛素抵抗严重程度的调节。胰岛素分泌/胰岛素抵抗指数(等于胰岛素×胰岛素敏感性)是β细胞功能定量的金标准。在NGT范围(2h血糖<100mg/dL vs. 2h血糖120~139mg/dL),类似于瘦者与肥胖或超重人群,β细胞功能减退50%~60%(图1)。IGT上三分位数组β细胞功能衰减70%~80%。Butler研究提示糖尿病前期个体β细胞功能衰退与严重的β细胞数量减少有关。
旨在预防2型糖尿病的干预
IGT代表NGT进展为2型糖尿病的第一步。ADA认为IFG和IGT是糖尿病前期状态。因为受损的β细胞功能和胰岛素抵抗是IGT/IFG特异性特征,保护β细胞功能和改善胰岛素抵抗的干预最可能阻止或减缓IGT进展为糖尿病。
饮食和运动
肥胖和不运动是2型糖尿病的主要危险因素。肥胖是导致过去20年2型糖尿病发病率和患病率显著增加最重要的因素。体重增加和不运动引起胰岛素抵抗。相反地,体重减轻和运动提高非糖尿病和糖尿病患者的胰岛素敏感性和改善其葡萄糖耐量。四项大型前瞻性研究证实,饮食控制和运动的治疗方案可减少IGT进展为2型糖尿病的风险。这样的行为干预项目最大的问题在于难以长期维持体重减轻和增加体力活动。在美国的DPP研究中,尽管启用了HELP计划,但体重减轻在项目结束后极大地反弹(图1A)。DPP项目生活方式干预的基本组成见表1。长期维持这种干预的困难不应该令人吃惊的。Look AHEAD研究,类似于DPP,显示第1年明显的体重减轻,然而尽管继续的强化干预和随访,随后的3年体重重新增加。体重再增加是大部分体重减轻项目的特异性特征,不论节食干预的类型如何。同样的,药物干预获得的体重减轻,一旦药物中止后大部分体重会重新回来。控制饮食使得体重减轻之后,受试者被随机分配到安慰剂组和西布曲明组,安慰机组个体在24月后重新获得曾经减轻的体重,然而分配到西布曲明组的个体维持减轻的体重(图1B)。我们在利莫那班中观察到了类似的结果(图1C)。
试图将DPP结果应用到临床实践是有困难的。最近芬兰的一个社区研究,2,797高风险人群入组糖尿病预防项目,设计目的是减轻5%~7%的体重。只有三分之一的参与者成功减轻体重>2.5%。最后,尽管体重减轻有效减低了IGT个体的糖尿病发病率,但糖尿病风险减低也仅为50%~60%。因此,尽管成功的减轻体重,仍有40%~50%的IGT个体将进展为2型糖尿病,这提示单独依靠生活方式干预不足以阻止大部分IGT个体进展到2型糖尿病。
总之,虽然初始体重减轻可以通过强化饮食干预获得,即便严密监督和频繁随访,一旦干预项目停止,体重再增加则是必然。而且,即使体重明显减轻,40%~50%的IGT个体仍会进展到糖尿病。这个问题不在于体重减轻是否有效阻止IGT进展为2型糖尿病,而在于结束干预项目后体重减轻是否能维持。
药物
与生活行为(饮食和运动)干预相比,IGT阶段药物治疗(噻唑烷二酮、二甲双胍、GLP-1受体激动剂)一致被证实能有效阻止IGT转变为2型
糖尿病(图2)
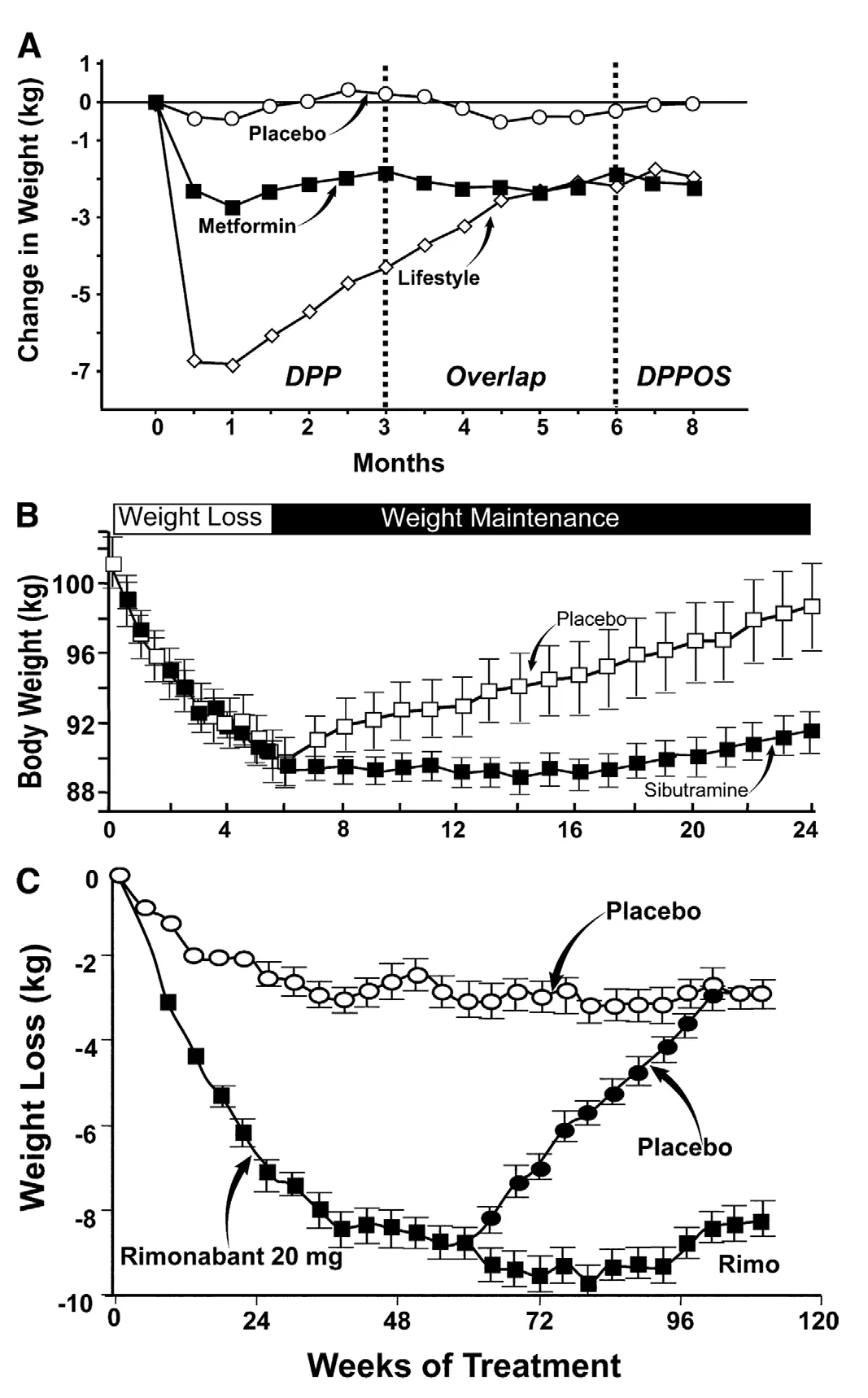
图1
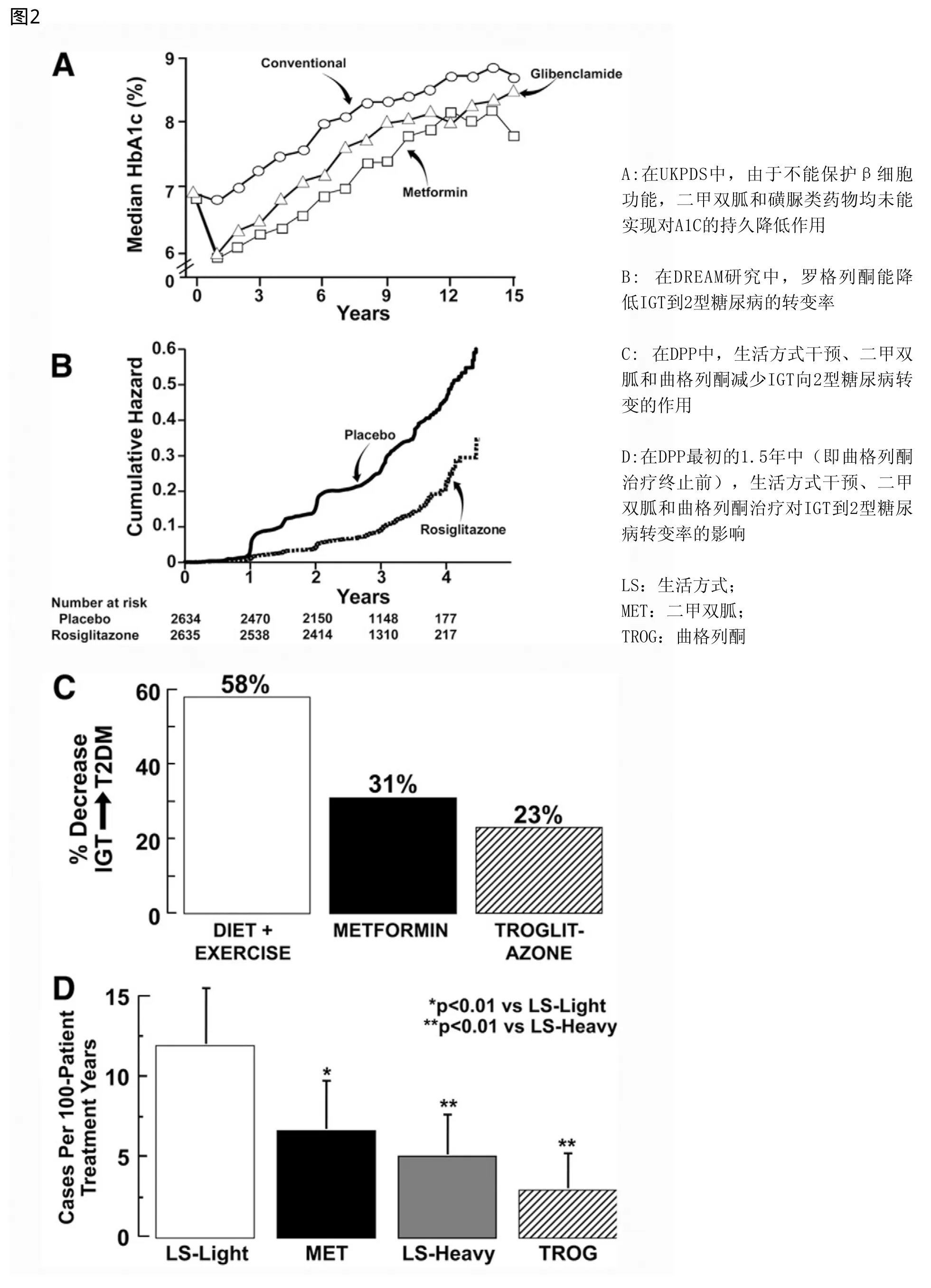
二甲双胍 二甲双胍通过抑制肝糖原生成、糖异生和改善外周肌肉组织胰岛素敏感性而改善2型糖尿病患者的血糖控制。二甲双胍不刺激胰岛素分泌或保护β细胞功能,与A1C进行性升高有关(图2A)。DPP显示,接受二甲双胍850mg Bid治疗,可减少31%的IGT个体转变为2型糖尿病(图2C);二甲双胍治疗也能改善胰岛素敏感性,减少代谢综合征发病率。印度DPP中,二甲双胍减少26%的IGT个体转变为2型糖尿病,ADA共识推荐IGT或IFG高危个体(HbA1c≥6.0%,BMI≥30kg/ ,年龄≤60岁)在饮食、运动基础上加用二甲双胍治疗。然而,二甲双胍,类似磺脲类,不能阻止2型糖尿病特征性的进行性的β细胞功能减退。
噻唑烷二酮 噻唑烷二酮是通过过氧化物酶体增殖物激活受体γ(PPAR-γ)途径介导的胰岛素增敏剂。PPAR-γ受体被发现在脂肪细胞中浓聚,也村在于肌肉、肝脏和β细胞。许多数据表明肌肉敏感性改善与血清脂肪酸或脂质水平减少及脂肪含量改变有关。曲格列酮、吡格列酮和罗格列酮能够改善2型糖尿病胰岛素敏感性和血糖控制。曲格列酮可提高胰岛素敏感性和改善肥胖/瘦的IGT个体及有妊娠期糖尿病史的IGT妇女的口服糖耐量。DPP显示曲格列酮减少23%的IGT个体进展为2型糖尿病,即便在应用10个月后因为肝毒性而停药(图2C)。然而IGT个体积极接受曲格列酮(最初的0.5~1.5年),糖尿病发病率是3/100人-年,而安慰剂组、二甲双胍组和生活方式干预组分别为12.0、6.7和5.1/100人-年(P<0.001,P=0.02,P=0.18)(图2D)。DREAM研究显示罗格列酮减少62%的IGT个体转变为2型糖尿病(图2B)。妊娠期糖尿病妇女的研究也提供强有力的支持噻唑烷二酮能阻止或延迟IGT个体转变为2型糖尿病。ACT NOW研究中,吡格列酮(45mg/天)减少72%的IGT个体转变为2型糖尿病。来自糖尿病人群和动物研究的证据表明曲格列酮、吡格列酮和罗格列酮也呈现出对β细胞功能有益的效应,这与包括逆转脂毒性和直接的β细胞保护效应有关。因为噻唑烷二酮可改善胰岛素敏感性和保护β细胞功能,从而有效阻止IGT进展为2型糖尿病。然而,由于体重增加、液体潴留和骨折等不良反应,ADA共识并不推荐噻唑烷二酮用于治疗IGT/IFG。尽管ACT NOW研究中吡格列酮剂量是45mg/天,更低剂量(15~30mg/天)也能改善2型糖尿病患者的胰岛素敏感性和胰岛素分泌,且能有效减少IGT转变为2型糖尿病,使IGT重新回到NGT。低剂量应用可带来较少的体重增加和液体潴留,我们在加拿大土著IGT人群中进行的低剂量罗格列酮研究中观察到了类似的结果。应该引起重视的是DREAM和ACT NOW研究中,TZD治疗停止后,糖尿病发病率回升,变得与安慰剂组类似。
GLP-1类似物 GLP-1是一种由末端大肠L-细胞对食物消化刺激所释放的强力的胰岛素促分泌剂,与葡萄糖依赖性促胰岛素肽一起,占到肠促胰素效应的90%。GLP-1通过食欲抑制效应也抑制胰高血糖素分泌,延迟胃排空和促进体重减轻。尽管这些特点使GLP-1成为理想的抗糖尿病药物,但它会很快被二肽基肽酶(DPP-4)分解(T1/2 =1~2min)。利拉鲁肽和艾塞拉肽是GLP-1受体激动剂,模拟GLP-1的效应,又能防止被DPP-4分解。利拉鲁肽和艾塞拉肽是有效的胰岛素促泌剂,能高效地降低血糖浓度。长期(3年)艾塞拉肽治疗产生持久的血糖控制、进行性体重减轻和β细胞功能改善。2型糖尿病患者以严重受损的β细胞功能为特征,减少了血浆GLP-1对进餐消化的反应,这与胰岛素分泌减少和对GLP-1的胰岛素分泌刺激作用严重抵抗有关。在IGT个体,对混合餐总的GLP-1反应降低或者正常。然而,在这些研究中的三项研究里,早期(0~10min)GLP-1水平缺陷,提示IGT个体反应性和总的GLP-1水平都是不足的。对GLP-1刺激胰岛素分泌的明显β细胞抵抗也被证实。由于进行性胰岛素缺乏主要导致NGT个体进展为IGT进而发展到2型糖尿病,GLP-1类似物适合用于IGT人群的干预治疗。而且,GLP-1和GLP-1类似物对胰岛素分泌的刺激性效应是葡萄糖依赖性的,这使低血糖风险降到最低。在啮齿类动物研究中,GLP-1类似物也刺激胰岛增生和β细胞复制和抑制胰岛凋亡。然而,最近Bunck等在2型糖尿病患者中进行的研究强烈质疑GLP-1增加人β细胞数量的效应,因为停止艾塞拉肽1月后,β细胞功能即恢复到治疗前水平。一天一次的利拉鲁肽也能降低肥胖的非糖尿病个体的体重,减少IGT转变为2型糖尿病。长效GLP-1类似物目前正在研究中。由于给药一周一次,而且能够增加β细胞功能和促进体重减轻,被证实是理想的阻止IGT进展为2型糖尿病的药物。尽管GLP-1类似物的心血管安全性尚未确定,但是GLP-1可以纠正许多已知的心血管危险因素(肥胖、脂质紊乱、高血压、炎症、胰岛素抵抗)。尽管GLP-1类似物导致胰腺炎的问题已引起关注,但多项大型医疗数据库回顾性分析并没有发现胰腺炎发病率的升高。
α-葡萄糖苷酶抑制剂 已证实阿卡波糖(STOP-NIDDM)和伏格列波糖可减少IGT转变为2型糖尿病。尽管这一预防性效应最初被认为来源于抑制碳水化合物的吸收,但α-葡萄糖苷酶能增加肠促胰素的分泌。因此,升高的β细胞功能可以部分解释它们对葡萄糖稳态的的作用。通过改变肠道微生物菌群,α-葡萄糖苷酶抑制剂对葡萄糖耐量呈现有益效应。
IGT加速进展为糖尿病的相关因素
2 型糖尿病是美国乃至全球的一个主要的健康医疗问题,它的发病率在迅速增加。由此,识别那些可能发展为2型糖尿病的高危个体,如糖尿病前期患者,具有重要的意义,因为他们代表一个合理的干预靶点。而且,多达10%的A1C在6%左右的IGT个体已经有糖尿病视网膜病变和糖尿病神经病变。胰岛素分泌受损和胰岛素抵抗是糖尿病的特征性因素。然而,筛查胰岛素功能或分泌缺陷的个体是不切实际的。前瞻性流行病学研究显示,接近50%的IGT个体最终进展为2型糖尿病。Stern等圣安东尼奥市心脏研究表明,包含人体测量指标(年龄、性别和BMI)和其他常见代谢综合征测量指标的预测指标在墨西哥裔美国人和高加索人的2型糖尿病预测上与IGT相当或更优。2型糖尿病家族史也增加IGT进展为2型糖尿病的可能性。OGTT血糖浓度总和在前五十百分位数的IGT个体或空腹血糖≥90~95mg/dL的给他更有可能发展为2型糖尿病。妊娠期糖尿病和PCOS也是2型糖尿病的高危因素。我们已经证实,Botnia和圣安东尼奥心脏研究都显示1h血糖≥155mg/dL是最佳的预测IGT或无IGT个体将来发生2型糖尿病的因子。Dresden研究,1h血糖≥155mg/dL以及A1C大于5.7%优于之前所有预测2型糖尿病的模型。包含A1C、空腹血糖、胰岛素、IL-2 RA、脂联素、铁蛋白和CRP的生物标记组能极高的预测将来的糖尿病。因此,通过选择有2型糖尿病额外危险因素的IGT个体,可以更好地选择最可能受益于药物干预的人,这已经在美国DPP和ACT NOW研究中得到证实。
药物干预的选择
虽然体重减轻能有效阻止2型糖尿病的发生,但难以获得和维持。即便体重减轻,仍不足以完全阻止IGT进展为2型糖尿病。基于前面对病理生理学的讨论、改善β细胞功能和提高胰岛素敏感性的药物干预(联合饮食和运动)是合理的IGT治疗之选。噻唑烷二酮研究(DREAM、美国DPP、ACT NOW 、TRIPOD、PIPOD)已经完成,并显示有效。美国DPP和印度DPP表明二甲双胍具有延迟IGT转变为2型糖尿病的效应,ADA专家共识推荐二甲双胍用于高危的IGT个体。二甲双胍已在全世界范围内长期使用,具有可靠的安全性。然而,二甲双胍阻止IGT转变为2型糖尿病的效应仅为吡格列酮和罗格列酮的一半(31% vs. 72%和62%)。近期一项小型研究显示,罗格列酮(2mg/天)加上二甲双胍(1000mg/天)联合治疗对减少加拿大土著人群从IGT转变为2型糖尿病尤为有效,且伴有很少的副作用。因为罗格列酮的心血管问题和对血脂谱的影响,我们认为低剂量吡格列酮(15~30mg/天)联合低剂量二甲双胍(1000mg/天)是治疗IGT个体更好的选择。
GLP-1类似物具有以下特点:1)有效治疗2型糖尿病;2)改善β细胞功能和对葡萄糖的敏感性;3)促进体重减轻;4)改善心血管危险因素;5)不引起低血糖;6)可以一天一次(利拉鲁肽)或一周一次(长效制剂)用药。所以,我们认为GLP-1类似物也很可能成为治疗IGT个体的理想药物。
10.3969/j.issn.1672-7851.2012.07.009
美国德州大学健康科学中心糖尿病学部
(邓超 编译中南大学糖尿病中心/中南大学湘雅二医院内分泌科)
热点评述
