胰岛移植临床预后的改善:1999~2010
2012-01-16巴顿
巴顿 等
胰岛移植临床预后的改善:1999~2010
巴顿 等
目的 描述1999至2010年在合作胰岛移植登记处(CITR)的伴有严重低血糖的1型糖尿病患者接受胰岛移植的主要疗效和安全性结果的趋势。研究设计与方法 CITR总共有677例胰岛单独移植或肾移植后胰岛移植的1型糖尿病患者用来分析五个主要的治疗结果和整体安全性,每年随访一次至移植后5年,以确定任何早期(1999-2002年)、中期(2003-2006年)或更近期(2007-2010年)的差异。结果 胰岛移植3年后,不依赖胰岛素的比例分别提高到早期(1999-2002年,n=214)27%,中期(2003-2006年中,n=255)的37%和更近期(2007-2010年,n=208)44%(P=0.006 各时期间年份比较;P=0.01,单独时期中年份比较)。提示胰岛移植功能的C-肽≥0.3ng/mL一直保留到更近期(P<0.001)。移植治疗在糖化血红蛋白减少和严重低血糖问题解决上表现出持久的长期效应。更近期的空腹血糖稳定性也呈现出改善。不良事件发生率也有轻度减少。胰岛再输注率更低:48%/年(2007-2010年)vs. 60%~65%/年(1999-2006年)(P<0.01)。曾经达到过不依赖胰岛素程度的患者的胰岛移植功能持续时间更长(P<0.001)。结论 由此得出CITR 2007-2010年间接受胰岛移植者的主要效应和安全性比在1999年至2006年的那些患者均得到改善,且伴随更少的胰岛再输注损伤和副反应。
介绍
同种异体胰岛移植为复杂的反复严重低血糖和/或显著的血糖不稳定的1型糖尿病患者β细胞替代提供了一种微创治疗方法。在1999年之前,只有不到10%的胰岛移植受者实现不依赖胰岛素。2000年,Edmonton胰岛移植方案在连续七例接受一个以上供体胰岛的受者中,达到了无需类固醇激素免疫抑制疗法而获得不依赖胰岛素的结果。在这个概念被证明成功后,胰岛移植方案在北美和其他地区的应用范围扩大。虽然资源很有限,但仍然无法阻止临床I /II期试验以达到规范流程、实现成功、稳定结果的目的,这些中心提供了胰岛移植和免疫抑制进一步优化的策略。
即使存在胰岛素依赖,只要残留胰岛移植功能得以维持(以C肽分泌的恢复来衡量),胰岛移植就可以保护1型糖尿病受者免受严重低血糖发作的折磨。尽管基本原理令人兴奋,但是临床上胰岛移植治疗1型糖尿病的预后差异很大,疗效持续性也难以预测,而且经常需要多个供体,同时不得不去平衡一种疾病负担(严重低血糖)与另一种负担(长期免疫抑制)。在美国以外的一些国家,胰岛移植在过去的十年中已被指定和资助作为非实验性治疗,在严重低血糖和免疫抑制的风险之间的权衡中合理的精心挑选患者。胰岛移植在美国仍然处于实验阶段,并等待正在进行的III期临床试验结果证明生物学许可和过渡到标准治疗。
研究者建立CITR,通过美国、加拿大、欧洲和澳大利亚青少年糖尿病研究基金会 (JDRF)支持的一些中心的数据监测胰岛移植进展和安全性。CITR代表过去十年中最完整的胰岛移植的信息。本次调查的目的是描述胰岛移植的主要成果和安全性的趋势,根据首次胰岛输注的年份定义的队列(早期:1999-2002;中期:2003-2006;或更近期:2007-2010)。分析包括截至2010年12月31日的异体胰岛单独移植和肾移植后胰岛移植(IAK)的数据,更新至2012年1月4日。
研究设计和方法
患者
CITR是一项综合性的胰岛移植登记项目,包含自1999年以来,国家糖尿病、消化和肾脏疾病研究所(NIDDK)资助的北美中心和JDRF资助的欧洲和澳大利亚中心共计27个,包括81%的异体胰岛移植无对照的I / II期临床试验或标准治疗。患者和方法在以往和当前的CITR年度报告进行了全面介绍,这是公开的。简单地说,异体胰岛移植受者通常是年龄在18岁至65岁之间。1型糖尿病病史>5年,>95%的患者检测不到空腹C-肽(<0.3ng/ mL)和糖尿病难以控制,包括未察觉低血糖、严重低血糖和/或显著血糖不稳,特点是血糖水平的大幅波动,往往糖化血红蛋白水平持续升高(>8%)。该报告没有包括全胰切除术后的胰岛移植病例。
登记处收集胰腺捐赠者、胰岛处理和测试、免疫抑制和药物治疗、严重低血糖事件、HbA1c、空腹血糖和C肽水平、每日胰岛素剂量、至关重要的生命状态、胰岛移植物功能障碍和损失,以及按照临床胰岛移植协会(CIT)不良事件分级的术语标准报告的以3,4,5级分类的不良事件和严重不良事件的信息。胰岛受者参加CIT协议,同意其数据和信息登记在CITR。
CIT协议包括一系列的II期和III期临床试验,目的是测试目前的免疫策略和管理方法,并寻求在美国开展临床胰岛移植的许可。CIT数据由爱荷华州立大学临床试验和数据管理中心的 William Clarke博士协调管理,通过共同的赞助商——美国NIDDK在合作协议下提供给CITR。CITR数据都经过严格监控的数据协调中心——马里兰州罗克维尔市EMMES公司,以符合美国食品药品监督管理局(FDA)第21号联邦法规要求。网站在注册表中,需要当地的研究伦理委员会的批准,严格保证病人的机密信息,胰岛供受者签署知情同意书。CITR出版物和报告委员会批准该研究。
在输注前和每次安排的后续随访,5个共同主要终点通过实验室测量或临床评价来评估:基础C-肽(进一步划分为≥0.3和<0.3ng/mL),包括报告完全的移植物无功能(定义始终检测不到空腹C肽与本地检测刺激C肽<0.3ng/mL,以后也无法恢复到≥0.3ng/mL或再灌注,也表示为“无功能”);不依赖外源性胰岛素≥连续14天;糖化血红蛋白(进一步划分为6.5%和/或下降两个百分点或更多);空腹血糖(进一步划分为60-140,<60,和>140mg/dL);以及没有严重的低血糖发作(需要他人协助)。每次输注预定的时间为移植前,移植后7天,1个月,6个月,及此后每年,在以后的每次输注时再按此程序执行。每个受者从最后的一个或多个注入后的年度时点结果用于本分析中。除了完全移植失败,虽然相对长时间的稳定状态,上述结果都可以发生,复发,然后再次出现在随访期间。因此,他们患病率(百分比)在最后输注的随访中进行分析。完全的移植失败定义为不能再恢复,因此,这一结果通过故障时间技术进行分析。当直接的数据丢失,但已知移植功能此前已丢失,无法恢复,胰岛素独立性设置为依赖,以及C-肽设置为0。否则,丢失的数据在计算和建模中忽略(即视为随机失踪)。
对于同一天接受两到三个不同的供者的胰岛输注,捐助者、获取、加工和隔离特征在多个捐助者中进行总结(例如,捐赠者平均年龄,总的输入胰岛当量等)。每个受者在发生超过两次到六次输注事件后信息将再次总结。植入的胰岛通过在准备中总胰岛计数的百分比来表达。免疫抑制剂在每次给予时记录。每个受者按照表1所示分为诱导和维持的组合分类。所有可用的受者,供者,胰岛和免疫抑制变量作为主要结果可能的预测因子用于多变量分析。
每个受者重复测量的广义估计方程被用来评估的不同时代的效应(1999-2003年,2003-2006年,2007-2010),第一次输注后随访时间,和其他变量关于各主要终点理想结果发生率。所有可用的受者、供者、胰岛和医疗管理因素的多变量分析也用于观察对各个时代观察到的变化存在影响的病人选择和管理办法是否发生改变。
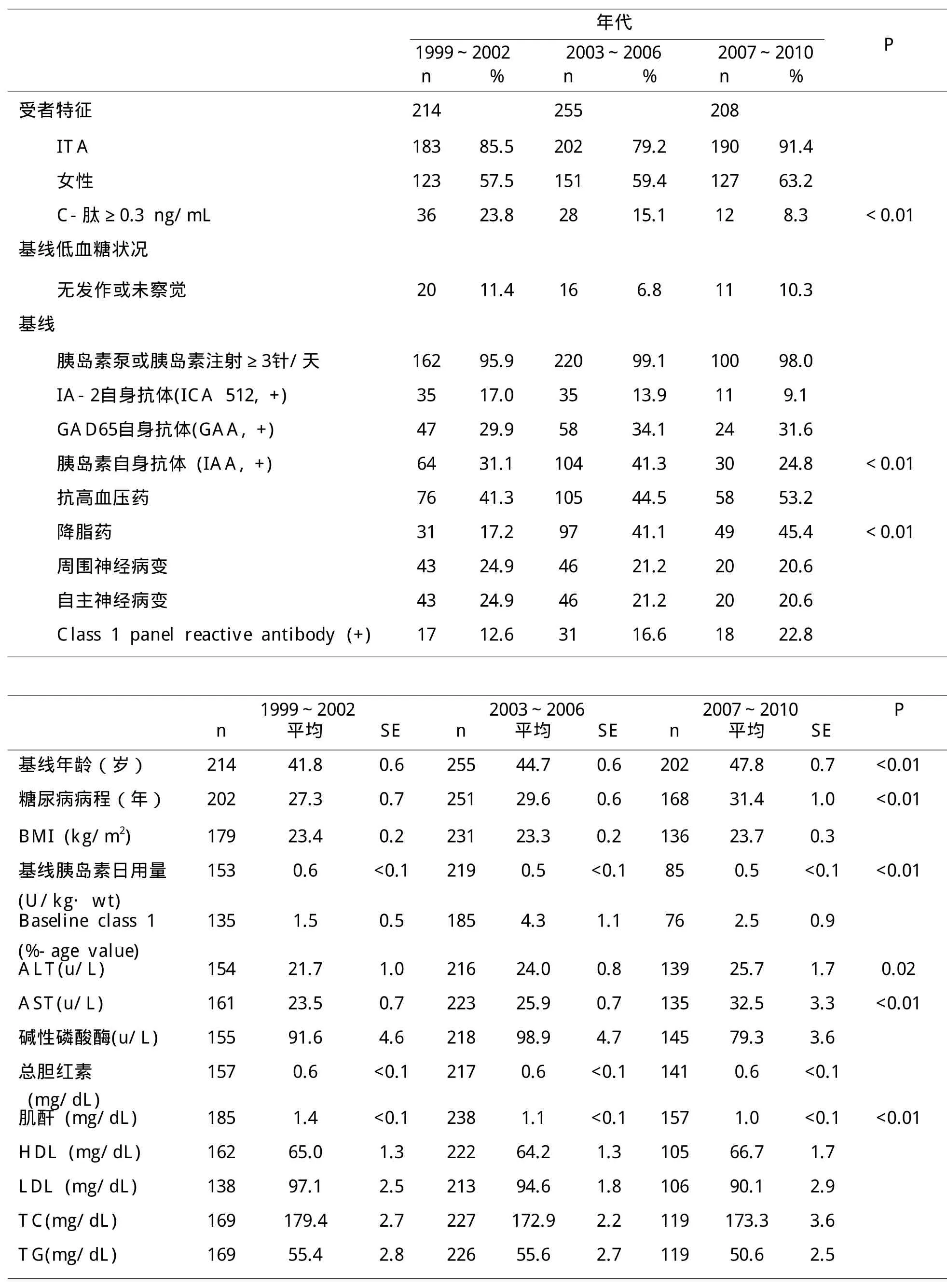
表1 受体、供体、胰岛和免疫抑制数据

表1 受体、供体、胰岛和免疫抑制数据(续)

表1 受体、供体、胰岛和免疫抑制数据(续)
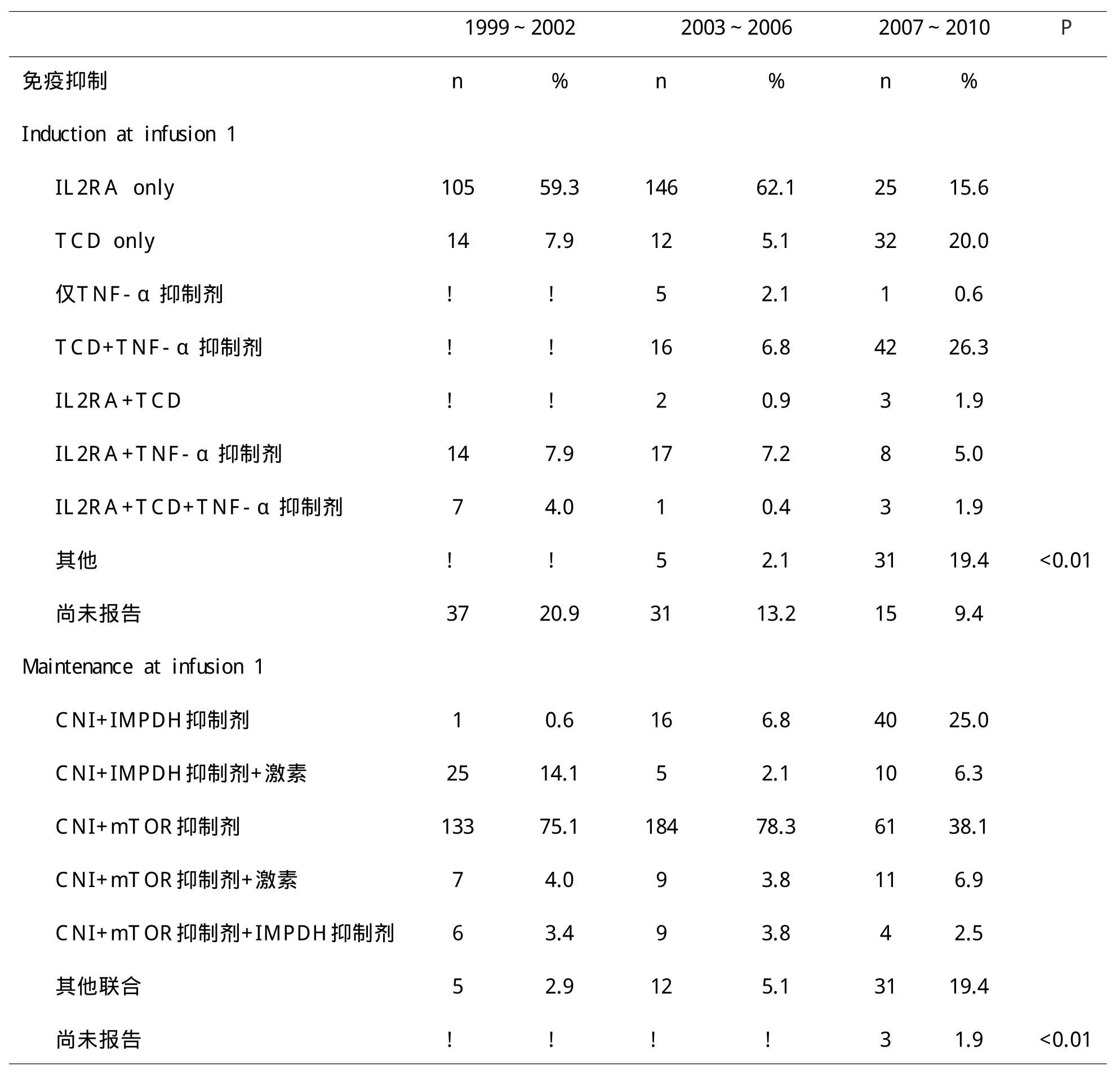
表1 受体、供体、胰岛和免疫抑制数据(续)
临床报告的不良事件(CRAEs)发生和结果,分为可能性不大,可能,或肯定与输注程序或免疫抑制方案有关的,根据各个时期进行分析。每个受者根据他或她的整个输注和随访期间相关的CRAEs和免疫抑制相关的最坏的结果,进行分类和制表。使用Mantel-Haenszelχ2进行比较。
跨时期的比较显然不是随机的,样本量并不通过实验确定。在该注册表数据,名义P值报告没有预先设定的I型错误率。
结果
本分析是基于对677例异体胰岛移植的受者同意的CITR报告的数据,在1999-2002年(早期)间214受者,在2003-2006年(中期)的255例,和2007-2010年(最近)208例;423(62%)来自北美,254(38%)来自欧洲和澳大利亚JDRF网站。包括移植胰岛单独移植575(85%)和102(15%)IAK或同时的胰岛移植(IAK/SIK)。CIT在2008-2010年登记46(7%)。他们收到1,3751胰岛输注,来自于1502捐助者,其中约10%为2~3个供者在同一天,这里被认为“多供者输注。”约36%的受者只获得了一次输注,44%的患者接受了两次输注,18%接受三次输注,1.3%接受四次输注,一个人接受六次输注。
在1999年和2010年间,CITR数据代表北美和JDRF欧洲和澳大利亚中心进行的胰岛移植的81%。新的胰岛移植受者的数量在1999年和2002年之间(图1)每年翻了一番。2002年至2003年数量有明显的下降,反映了当时的现有协议的登记饱和,加上一些中心报告在2-3年内逐渐减弱的胰岛素独立性后对这一方法缓和的热情。尽管北美各中心进行胰岛移植的数目在2005年继续增长,但每年的胰岛异体移植数量仍低于2002年水平。相比于2005年,由于常用的胶原酶释放酶Liberase不可再用,在2007年只有不到一半的北美中心进行胰岛移植,而且胰岛移植总数只有三分之一。伴随着胶原酶产品可供使用和CIT试验的开始,胰岛移植活动在2008年又出现了一个显著的回升。
随着更长的随访期数据丢失水平逐渐增加,这包括不可使用的医疗记录和仍有待进入注册表中的数据。对胰岛素独立性缺失的数据的百分比在1年、3年和5年分别为3%、5%和7%,其他主要终点在1-3年为10%至20%。
那些在1999-2002年接受器官移植者,在第一次输注后1年51%达到胰岛素独立,无论是否再回输,这一比例在第2年下降到36%,第3年降至27%。与之形成对比的是2007-2010年时期,1年、2年和3年的胰岛素独立分别在66%、55%和44%(P=0.01,图2A)。在各个时期5年随访期胰岛素独立下降率具有统计学差异(P<0.001)。在三个时期之间下降率的差异(P=0.006)表示下降的幅度平缓,在最近的时期呈现持续性的显著改善。胰岛移植物功能的持久性,即测量的空腹C肽≥0.3ng/mL,在各时期间显著改善(P<0.001,图2B左)。如果以前获得胰岛素独立性,移植功能丧失率显著减少,出现在各个时期的效果(图2B,右)。几乎所有的胰岛移植受者在胰岛移植后的HbA1c和空腹血糖均显著改善。从早期到中期,复合终点HbA1c<6.5%,或下降两个或更多个百分点(P =0.03)的改善,虽然在最近的时期没有进一步的改进,表现为2-5年成功率50%至60%(图2C,左)。空腹血糖从早期到中期表现出显著的改善(P<0.01,未显示)。
严重低血糖在第一次输注时是普遍的,在所有时期都>90%。严重低血糖事件的可用数据显示,无论以前的移植物是否丢失(C-肽<0.3ng/ mL,没有恢复),各个时期超过90%的受者可免于严重低血糖事件,而且这种关系一直持续到5年的随访(图2C右)。严重低血糖事件的分辨率在各时期的差异,既检测不出也不重要。如果严重低血糖事件的数据丢失,之前的完整的移植物丢失算作是严重的低血糖事件——一个极端的假设——与1999-2002年相比,在2003-2006年的2-4年内仍然有改进(P=0.03,未展示)。
当时的C肽与所有其他主要结果呈现强关联:C肽水平越高,HbA1c<6.5%或下降两个百分点的可能性就越大(P<0.001,图2D),严重低血糖事件的可能性越低(P<0.001,图2D),空腹血糖在60-140ng/mL范围内(P<0.001,图中未示出)的可能性就越大,以及更大的胰岛素独立可能(P<0.001,图中未示出)。
一个综合所有预测的因素的模型——标记患者的年龄和免疫抑制策略(表1)在各时期的转变——主要解释了造成各时期间胰岛素独立的差异。T细胞消耗(TCD)药物联合肿瘤坏死因子-α(TNF-α)抑制剂的作用显示了持久胰岛素的独立被证实:最后一次输注后3-5年50%~62%接受这种诱导治疗的受者获得胰岛素独立(图2A,右),相比与那些没有接受TCD+TNF-α抑制剂的只有34%~43%。
再次输注是在第一个移植完全失去功能或下降的功能经C肽水平下降证实后进行的。胰岛再输注在12年期间有较大幅度下降:在2007-2010年48%的受者1年内接受再回输,在1999年至2006年则为60%到65%(P<0.01)。


图2
本组1型糖尿病患者在12年期间死亡率低,有重大疾病负担,稳定的事件发生率(图3A)。危及生命的事件的发生率有所下降(P=0.002,图3B)。1年的任何CRAE的发生率从1999-2006年的50%~53%,下降至2007-2010年的38%(P=0.02,图3C)。腹膜腔出血或胆囊穿孔率从1999-2003年的5.4%下降到2007-2010年的3.1%。慢性肾脏病流行病学协作(CKD-EPI)计算肾小球滤过率(GFR)在胰岛移植后下降(图3D),但是,在类似组别的1型糖尿病没有公布的可供比较的随访数据。无主要疗效或安全性终点与受赠者或捐赠者的性别或种族相关联。
结论
在北美,进行临床胰岛移植的中心数量和胰岛移植总数在2006-2007年间下降,2008年有明显的复苏。下降的原因并不直接是注册登记引起的,可能反映了用于胰岛消化的胶原酶的生产和供应的变化,对于胰岛素独立的长期临床效果热情的消减,对单独胰岛移植受者肾功能的免疫抑制效果的关注,对受者的HLA致敏性风险的关注和不稳定1型糖尿病最严重的患者的参照数据饱和。然而,随着2008年CIT方案的开始,加上长期效果中更令人鼓舞的趋势,以及新方案诱导T细胞耗竭,接受新的胰岛细胞的数量在近期逐年增加。
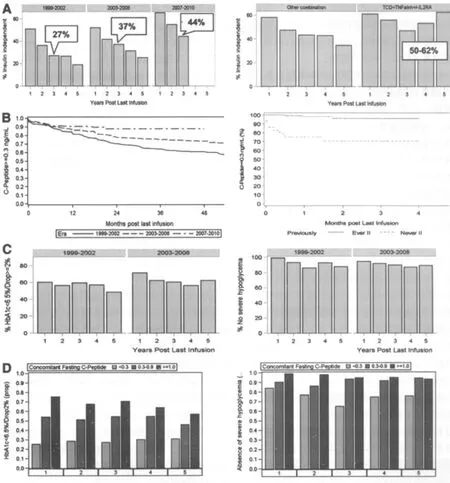
图3
直接证据是提出持久的胰岛移植功能对获得多种临床获益作为随后效应的重要性。阳性C肽与所有的其他主要临床结果紧密联系在一起的。因此,尽管额外的因素也可能有助于其他的好处,可维持阳性的C-肽水平的因素,必然导致其他临床益处。对这些主要终点发挥影响的所有因素综合分析表明,年长者、较低的初始胰岛素需要量以及尤其在联合TNF-α抑制剂时使用T细胞耗竭剂,与改善的临床结果显著相关。这些例数太低而无法准确地估计出霉酚酸替换mTOR抑制剂在维持免疫抑制方面改变的影响,这两种药物通常还是在钙调神经磷酸酶抑制剂(CNI)中联合应用。
值得注意的是,CITR数据并没有实时更新,而是,当网站已加入了12年的生活到注册表,大部分的数据,包括一些历史数据,已在近1-3年报告。因此,目前的结果可能会与包括CITR的年度报告在内先前报道的结果有些变化。目前的数据是最全面和1999-2010年间最新的信息。
在本次分析中,随着随访时间增加,丢失的数据水平的不断提高,造成一定的局限性。此次分析的优势是提供一套最完整的数据和可能性以跟踪在这12年期间不用类固醇激素的免疫抑制疗法的趋势。将CITR数据按移植时期分层分析显示一个引人注目的趋势(P≤0.01),即在最近几年存在更好的结果,尽管世界各地的胰岛移植受者的总人数还是比较低的。有迹象显示出选择年龄更大的糖尿病病程更长和C肽缺失的受者来颠覆风险利益比的趋势。选择体重较重的供者趋势可能是由于全球性的肥胖流行,供者重量较高与分离出的胰岛当量较高之间显然存在相关性。这必须权衡来自供者中未诊断的2型糖尿病患者移植胰岛细胞的不利影响,因为这个原因,在移植前确认肥胖的供者的糖化血红蛋白是否在正常范围内是非常重要的。
在过去,胰岛分离后迅速进行移植被认为是最佳的。近年来,倾向于短暂的培养期后进行胰岛移植,目前的假设是,培养删除了不能存活的胰岛,减少可导致非特异性炎症的组织因子表达和移植后的胰岛损失。经皮注射技术偶尔产生腹腔出血,早期门静脉分支静脉血栓形成,但这些并发症的发生率在当今时代较低。
全胰腺移植是1型糖尿病患者β细胞替代治疗经过批准的一种选项,虽然它大多局限于同时接受肾脏移植手术的糖尿病肾病患者,往往不包括老年患者和冠状动脉疾病患者,因其潜在有显著的手术风险。因此,胰岛移植可能会提供一个补充的选择给那些不适合或不愿意接受重大手术的潜在风险的患者,所以需要一些疗效比较的评估。在2007-2010年,胰岛移植物的存活率(C-肽≥0.3ng/ mL)1年为92%和3年为83%(图2B)优于全胰腺移植物的存活率(1年为80%和3年为61%)。在最近的时期,这些移植物存活率转变为3年内44%的胰岛素绝对独立(图2A),观察到目前为止最高的长期胰岛移植的成功率。虽然这仍少于已报道最成功的1型糖尿病的胰腺单独移植受者队列中的61%胰岛素独立,这种差异的原因可能是由整个胰腺移植时正常的胰岛β细胞团的100%移植与幸存于胰岛分离时可变化的胰岛β细胞团,从而减少β细胞分泌能力。此外,在整个12年的时间内,这些数据表明,HbA1c减少和空腹血糖稳定的长远收益。
更重要的是,胰岛素依赖的胰岛移植物的存活定义的C肽>0.3ng/mL的存在保护免受严重低血糖,这种效应甚至在胰岛移植物丢失后仍然存在。在各时代间胰岛移植物丢失的下降率表明,多变量分析确定的最近的免疫抑制策略,可以更好地保护胰岛同种免疫排斥反应和自身免疫性疾病复发。成功的策略包括已知在高剂量时表现出β细胞毒性的CNIs。但是,一项研究表明现代使用较低的剂量,CNI为基础的免疫抑制导致在全胰腺移植受者100%正常β细胞分泌能力,提示这些药物可以使用,甚至对于成功的胰岛移植可能是必要的。最后,研究结果表明,当胰岛素独立在先前获得时,移植功能丧失率显著降低。这一发现表明,足够的胰岛β细胞团移植以消除外源性胰岛素需求,可以减轻由于增加的β细胞需求而发生的非免疫性胰岛移植物丢失。目前改善胰岛移植存活比例的策略预计将导致胰岛受者的功能改善。
CITR显示了一致的趋势,在2007-2010年接受胰岛移植的队列,相比在1999至2006年那些人,呈现胰岛移植主要终点的改善。目前,胰岛移植避免许多严重低血糖的发生和以最小侵入性方式使得大量患者不依赖外源性胰岛素。在胰岛生产、加工、配送和免疫抑制保护方面新兴的创新,无疑将推动这一领域的发展。胰岛移植已经从临床I / II阶段发展到第三阶段的评估,从CIT期待已久的结果为胰岛分离和免疫抑制的标准化方案提供了疗效和安全性信息。
1.文稿:应具前沿性、新颖性、创新性、实用性,主题明确,中心突出,资料可靠,数据准确,文字精炼,层次清楚。
2.作者:文章应由一位作者负责。作者姓名及排序应在投稿时确定,并在文题下按序排列;作者单位名称及邮政编码注于首页左下方。
3.摘要:论著须附中文摘要,能体现出主要结果及数据,300字左右。
4.关键词:文稿需标引2~5个关键词。尽量使用美国国立医学图书馆编辑的《Index Medicus》主题词。
5.医学名词:应用全国科学技术名词审定委员会审定公布的医学名词,尚未公布者以人民卫生出版社编的《英汉医学词汇》为准。中文药物名称应用《中国药品通用名词》,英文药物名称采用国际非专利药名,不用商品名。
6.图表:采用三横线表,表内数据要求同一指标有效位数一致。
7.数字:公历世纪、年代、年、月、日、时刻均用阿拉伯数字。
10.3969/j.issn.1672-7851.2012.10.010
美国马里兰州EMMES公司
(邓超 编译中南大学糖尿病中心/中南大学湘雅二医院内分泌科)
