Np的环境化学研究进展
2012-01-04姜涛,姚军
姜 涛,姚 军
1.中国原子能科学研究院 放射化学研究所,北京 102413;2.中国国际工程咨询公司,北京 100048
Np是93号元素,是超铀元素的第一个。在Np的同位素中237Np是唯一既容易得到又最稳定的同位素,它的半衰期长达2.14×106a。Np在反应堆生成的超铀元素中生成量仅次于Pu[1]。Np的化学毒性与Pu相当,化学形态复杂,在环境中Np的最稳定价态是Np(Ⅴ),Np(Ⅴ)溶解度较大,在环境中的迁移能力很强,一旦进入环境将对生态环境构成严重的威胁。由于Np的高危险性和地质处置研究的需要,国际上对研究Np在环境中的化学行为给予了高度的重视。
Np的环境化学主要包括两个方面的研究内容:(1)溶解行为研究;(2)迁移行为研究。溶解行为研究的核心问题是溶解度和主要存在形态。迁移行为研究的核心问题是Np与环境介质之间的相互作用(以吸附作用和氧化还原作用为主)。由于Np是一种人造元素,自然界中并不存在。所以自然界中的Np主要来源于核设施,包括核电站、后处理厂、地下处置库。其中正常运行的核电站和后处理厂几乎不向环境中释放Np。这些核设施产生的Np几乎全部存在于乏燃料和高放玻璃固化体中,而世界上各有核国家都计划将乏燃料和高放玻璃固化体进行深地质处置。因此深地质处置库中的高放玻璃和乏燃料是Np可能向环境释放的主要源项。尽管237Np在高放废物中的含量并不高,但高放废物中241Am(T2/1=432.2 a)会衰变为237Np,因此其含量会随时间的推移而升高。另外由于237Np的半衰期很长,在处置库运行的100 000年后,237Np将成为主要的放射性核素之一[2]。在处置库失效后地下水可能进入处置库,乏燃料或高放玻璃固化体与地下水接触,乏燃料或高放玻璃固化体中的Np溶解进入到地下水中。地下水中的Np可能会在人工屏障材料和围岩中迁移并释放到环境中。所以目前国际上对Np的环境化学研究重点是研究Np在深地质处置库环境中的溶解和迁移行为。本文拟总结近年来Np的环境化学方面的研究成果,并对今后的研究方向提出建议。
1 溶解行为
溶解度和主要存在形态是Np溶解行为研究的核心问题。主要存在形态是进一步研究胶体和迁移问题的基础。从工程应用的角度,溶解度是高放废物地质处置安全和环境评价中的重要数据,它直接影响核素在地质介质中的迁移能力,可以用来预测若干年后放射性核素在处置场周围的地下水中的浓度和形态[3]。Np在环境中可以有+3~+7价五种价态,在天然水体的pH、Eh范围内的存在价态示于图1[4]。天然水体的pH、Eh多分布于图1中点密集的区域。这一区域内Np以Np(Ⅳ)和Np(Ⅴ)存在。世界各国都将Np(Ⅳ)和Np(Ⅴ)作为溶解行为研究的主要对象。
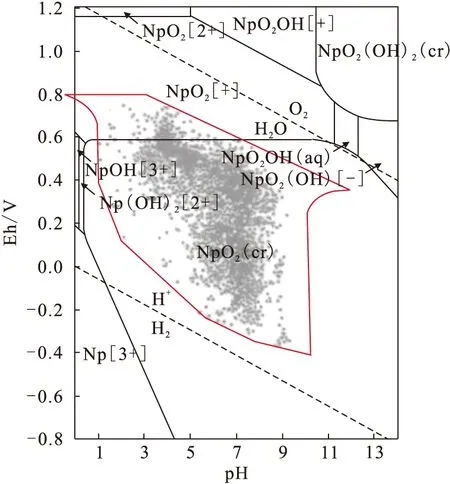
图1 Np-O-H系统的Eh/pH分布图[4]
1.1 溶解度
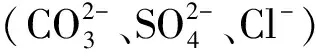
国内外针对Np的溶解度开展了很多工作。Np的溶解度主要受pH和Eh的影响。图2显示了Np的溶解度与pH和Eh的关系。
Np的溶解度依赖于水的Eh和pH值。图2(a)显示Np的浓度与pH值的函数关系。图中给出了不同Eh值下的溶解度的分界线。灰色区域中Np的主要形态是Np(Ⅴ),该区域上下的分界线分别是Np2O5(s)和Np(OH)4(s)的溶解度分界线。在溶液中Np的浓度高于这条线时,将会出现过饱和现象,在溶液中会出现Np(Ⅴ)和Np(Ⅳ)各自的沉淀。在氧化条件下,pH=4~12的范围内溶液中Np的总浓度可以相差6个数量级。
图2(b)显示了pH=7时溶解度与Eh值的关系,图2(b)中所示的溶解度线就是图2(a)中的pH=7时的不同Eh条件下的溶解度曲线。在还原条件下(Eh<-120 mV)Np(Ⅳ)是溶液中Np的主要形态。Np的溶解度受Np(OH)4(s)控制,浓度小于10-8mol/L。当Eh值逐渐升高,在氧化条件下更加稳定的Np(Ⅴ)将逐渐变为溶液中的主要形态。在过渡阶段Eh值决定Np(Ⅳ)/Np(Ⅴ)的比例。溶液中Np(Ⅳ)的总浓度受Np(OH)4(s)的控制。溶液中Np的浓度随氧化还原电位的升高而增加,当还原电位达到约250 mV时,Np的浓度达到约10-4mol/L。此时如果溶液中Np的浓度继续升高则会出现过饱和现象,将会出现Np2O5(s)沉淀。溶液中Np的浓度也会从此保持恒定。在阴影区域中Np的浓度由Eh和Np(Ⅳ)的溶解度控制。在这一区域之外Np的浓度受Np2O5(s)和Np(OH)4(s)的溶解度支配,与Eh无关。
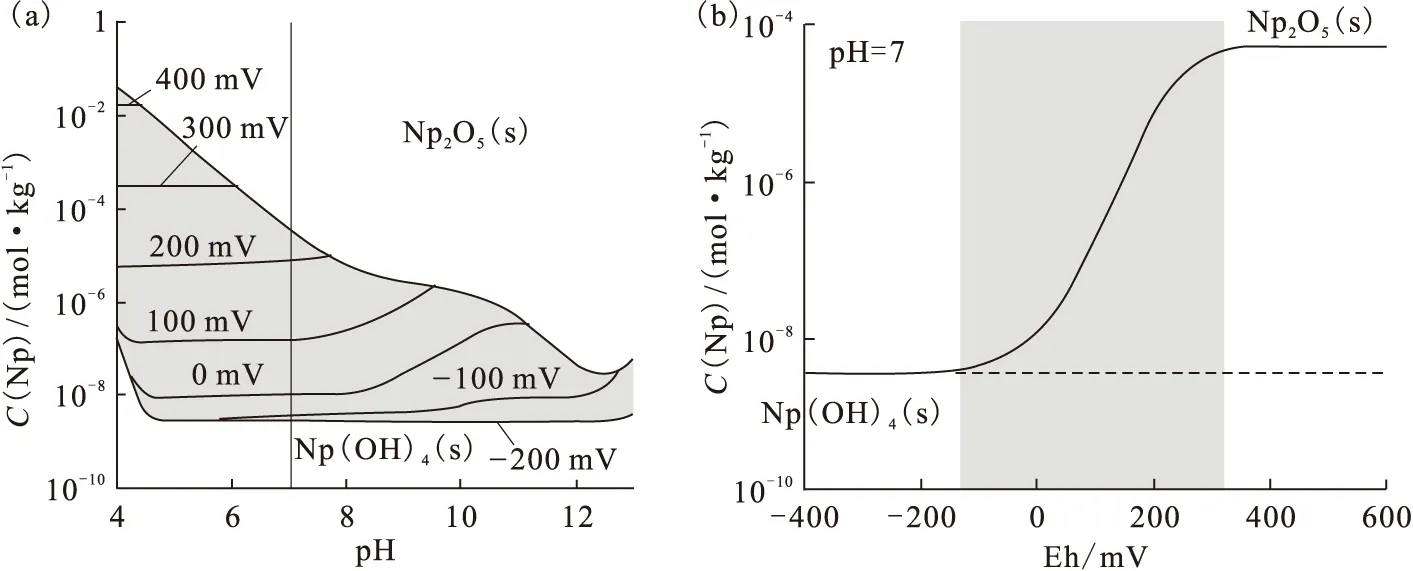
图2 Np的溶解度与pH(a)和Eh(b)的关系
世界各国研究Np的溶解度,多是为了高放废物地质处置提供数据支持。各国的处置库选址的情况不同,关心的问题也不同。美国的处置库位于非饱和带,则美国的研究主要关心Np(Ⅴ)的溶解问题,以及固相中Np(Ⅴ)/Np(Ⅳ)的转化动力学常数。包括我国在内的大多数国家处置库位于深部含水层中,是一个还原性环境,这些国家的研究者比较关心Np(Ⅳ)的溶解问题。
1)Np(Ⅴ)溶解度



表1 不同温度和pH下J-13地下水中Np(Ⅴ)的溶解度控制固相成分[5-9]
Silber等[11]研究了Np(Ⅴ)和Np(Ⅳ)在盐溶液中的形态和长期溶解行为,研究历时很长(>2 000 d)。平衡时的Np浓度为10-5~10-6mol/L之间,pH=8~13。由于放射性的自氧化作用,Np(Ⅳ)被氧化成Np(Ⅴ),造成了溶解度随时间的延长而增大。

Np(Ⅴ)较高的溶解度,对于高放废物的地质处置将是一个非常严重的问题[17]。在处置库安全评价过程中即使使用最保守的数据,即认为Na-NpO2-CO3·xH2O的固相控制着Np的长期溶解行为,那么计算值将大大超过安全允许值。在还原条件下Np的溶解度会受NpO2·xH2O或Np(OH)4控制,会比氧化条件下小几个数量级。因此如果Np的溶解度由NpO2·xH2O或Np(OH)4控制则会大大增加处置库的安全性。

在模拟地质处置条件下,还原态气氛中,在较短时间内(几个月到一年)Np的溶解行为是研究得比较清楚的,长期的溶解行为还要继续深入研究。急需研究Np(Ⅴ)/Np(Ⅳ)固体的溶解速度,以及固体中Np(Ⅴ)/Np(Ⅳ)的转化速度。有一些实验工作还在进行中。由于Np(Ⅴ)/Np(Ⅳ)转化问题的重要性,在这一领域有大量的工作要做。应该优先研究长期的辐解影响和用量热法研究Np(Ⅴ)固体的溶解热。
2)Np(Ⅳ)溶解度
目前国际上有关Np(Ⅳ)在近中性水溶液中的溶解行为研究较少。只有少数几篇报道了Np(Ⅳ)的溶解度[8,19-22],研究结果示于图3。

图3 Np(Ⅳ)的氢氧化物的溶解度
如图3中所示的研究结果,当pH>6时Np(Ⅳ)的溶解度都在10-7~10-10mol/L之间。但是遗憾的是这些报道中并没有对溶解度控制固相成分进行直接研究,只是通过间接分析认为溶解度控制固相应为Np(OH)4(am)。这也是国际上公认的结果。
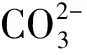
日本研究者[24]研究了NpO2在NaClO4溶液中,离子强度I=0.001~0.1 mol/L、pH=2~6、温度为30~90 ℃条件下的溶解行为。结果显示溶解速度随pH的增大而减小,随温度的升高而增大。在整个实验过程中溶解行为没有达到平衡。
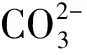

表2 NEA-TDB、EQ/36、JNC-TDB中的水解常数和络合常数[25-27]
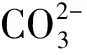
1.2 Np在环境中的主要存在形态
1)Np(Ⅴ)在环境中的主要存在形态

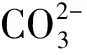
腐殖酸是自然水体中广泛存在的有机配体,各国的研究机构对Np(Ⅴ)与腐殖酸的络合和氧化还原反应进行了大量研究[31-41]。

日本研究者曾经用超滤和超离心法研究了Np(Ⅴ)的胶体行为[41]。发现当水溶液中的主要存在形态是NpO2OH(aq)时,有Np(Ⅴ)的假胶体生成。同时发现,在还原性地下水中Np(Ⅳ)形成不定型的NpO2·xH2O沉淀和胶体的反应是影响Np(Ⅳ)迁移的主要反应。
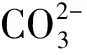
2)Np(Ⅳ)在环境中的主要存在形态
在还原性地下水中Np以Np(Ⅳ)的形态存在,会生成溶解度很小的氧化物或氢氧化物,所以Np(Ⅳ)不易迁移。在近中性地下水中一般认为Np(OH)4(aq)是主要存在形态[44]。但是这一结果来源于间接推断,缺乏直接实验证据。
1.3 小结
国际上经过多年的研究,对Np的溶解行为已经有了一定的了解。Np(Ⅴ)的溶解度和主要存在形态研究得比较清楚。Np(Ⅳ)的溶解行为研究取得了一些成果,但是Np(Ⅳ)的溶解度和主要存在形态还远远没有研究清楚。尤其是Np(Ⅳ)容易形成胶体,加大了研究的难度,在这方面各国还在进一步研究中。
实验方法方面,很多传统的测量方法已经不能满足环境水体条件下对Np的浓度和形态分析的要求。低浓Np的浓度分析方面传统的液闪谱仪无法满足要求。超低本底液闪谱仪虽然可以用于研究Np(Ⅳ)的溶解度,但是其探测下限与Np(Ⅳ)的溶解度在一个数量级上,测量误差较大。近年来国外分析低浓Np时多使用ICP-MS,中国原子能科学研究院将在“十二五”期间建立ICP-MS分析低浓锕系核素的装置和方法。
形态研究方面,溶剂萃取、共沉淀、近红外光谱法已经不能满足研究Np在环境水体中的存在形态的要求。近年来兴起的EXAFS、激光诱导分解光谱(LIBD)、激光诱导光声光谱(LIPAS)已经成为研究Np存在形态的主要手段。
溶解行为研究有向两个方向分化的趋势,其中一个方向是实验研究,另一个方向是模拟计算。从事实验研究的学者们通过改进实验方法、提高测量仪器的精度,降低实验数据的不确定度。实验研究的难度在于Np(OH)4(am)和NpO2(cr)的溶解度很低,一般都在测量下限附近,要准确测得水溶液中Np浓度有很大的难度,要用直接实验方法研究Np(Ⅳ)在水溶液中的存在形态难度会更大。
模拟计算是利用实验测定Np(Ⅳ)的水解和络合常数,再利用这些常数计算溶液中Np(Ⅳ)的总浓度即为Np(Ⅳ)的溶解度。计算的难度在于热力学数据的误差较大,计算结果的不确定度一般在两个数量级左右。并且对热力学数据进行离子强度还原有一定的难度。
2 迁移行为
Np的环境化学研究的另一个重要方面是Np在环境中的迁移行为研究。迁移行为研究的最终目的是要搞清楚Np在环境水-固体介质中的迁移行为,并预测迁移程度。国内外对Np在膨润土、粘土矿物中的扩散进行了大量研究。利用恒定源法、背靠背法、毛细管法等测定了Np(Ⅴ)在膨润土中的表观扩散系数,以及一些影响因素对扩散行为的影响。由于Np的不同形态与膨润土之间的相互作用(氧化还原作用、吸附作用)还远远没有研究清楚,因此测定的扩散系数只能称为表观扩散系数。
Np在水-固体介质中的迁移行为非常复杂,涉及到Np与固体介质之间一系列的相互作用,这种相互作用几乎决定了Np在环境中的迁移行为。因此Np的迁移行为研究的核心问题是研究Np与环境介质的相互作用。这种相互作用主要表现为吸附和氧化还原作用(往往这两种作用伴随在一起发生)。也就是说吸附行为研究是研究Np的迁移行为的核心问题。本文将重点介绍Np的吸附行为研究成果。前一部分已经阐述了Np(Ⅴ)和Np(Ⅳ)是Np在环境中的主要存在形态。在这两种存在形态中Np(Ⅴ)的溶解度大,迁移能力强,因此对Np(Ⅴ)的迁移行为研究比较充分。国际上普遍认为Np(Ⅳ)溶解度很低,在环境中迁移能力不强,所以对Np(Ⅳ)的迁移行为研究的不多。Np在环境中迁移的过程中可能遇到的介质有土壤、处置库基岩(花岗岩、粘土、凝灰岩等)、人工屏障材料(废物包装体、膨润土等),这些介质是研究吸附行为的主要对象。
2.1 Np在矿物上的吸附
作为一种氧化还原敏感元素,Np可以被含铁氧化物的矿物阻滞。这些含铁氧化物的矿物广泛存在于土壤颗粒的表面或是一些土壤颗粒的主要成分。矿物中的Fe(Ⅱ)可以将Np(Ⅴ)还原为Np(Ⅳ)。这些反应最近被给予了很大的关注。因为这些反应是影响Np在渗流区、水底沉积物和地下水中迁移行为的主要反应。同时还是选择处置库基岩和回填材料添加剂的基础。
美国的Nishita[46]比较了超铀元素在环境中的迁移能力,研究发现Np比Am、Pu、Cm更易迁移。还有一些研究比较了多种矿物对Np的吸附能力[47],发现在比表面积相同的情况下,吸附能力强弱顺序为:霰石、文石≥方解石>针铁矿>氧化锰≈粘土类矿物。
Combers等[48]利用EXAFS和近边X射线吸收精细结构技术(XANES)研究了Np(Ⅴ)在针铁矿上的吸附。试验中使用的是大表面积的针铁矿(goethite)固体。Np(Ⅴ)的初始浓度为1.3×10-5mol/L、pH=7.2、离子强度为0.08 mol/L。实验结果显示,Np(Ⅴ)吸附在针铁矿(goethite)上是一种表面络合反应。日本学者[49]研究了Np(Ⅴ)在天然含铁矿物:赤铁矿(α-Fe2O3)、磁铁矿(Fe3O4)、针铁矿(α-FeOOH)和黑云母上的吸附和解吸行为。研究发现在pH=4~11的范围内吸附是可逆的。并发现吸附量与pH值有关,针铁矿在pH>6时出现吸附量迅速增加的现象。其他3种则是在pH>9时出现了吸附量迅速增加现象。含铁矿物对Np(Ⅴ)的吸附伴随着氧化还原过程一起发生。在吸附过程中Np(Ⅴ)被还原成Np(Ⅳ)。美国Oak Ridge National Laboratory[50-51]研究发现含Fe(Ⅱ)的矿物可以将Np(Ⅴ)还原为Np(Ⅳ)。瑞典的研究者[52]证明在低氧条件下,溶液中的Np(Ⅴ)可以被金属铁还原为Np(Ⅳ)。并发现在金属铁表面有NpO2生成。并利用地下实验室研究了Np(Ⅴ)在裂隙花岗岩上的迁移行为,发现花岗岩裂隙填充物对Np(Ⅴ)有很强的吸附能力。
尽管一些报道称已经发现Np(Ⅴ)被含Fe(Ⅱ)的矿物还原为Np(Ⅳ),但是从日本的研究结果[49]中没有发现含Fe(Ⅱ)矿物黑云母(biotite)和磁铁矿(magnetite)与含Fe(Ⅲ)的矿物赤铁矿(hematite)对Np(Ⅴ)的吸附能力有所不同。这是因为含Fe(Ⅱ)矿物还原Np(Ⅴ)发生在吸附反应之后,也就是说Np(Ⅴ)先以表面络合的形式吸附在含Fe(Ⅱ)矿物的表面上然后被还原。很多研究结果[53-56]都证明Np(Ⅴ)还原为Np(Ⅳ)的反应发生在矿物表面而不是发生在液相中。
美国的研究者[57]应用EXAFS研究Np(Ⅴ)与含Mn矿物的相互作用,实验数据证明Np(Ⅴ)在含Mn矿物表面被还原为Np(Ⅳ),并生成了Np(Ⅳ)的氧化物沉淀。
Pacific Northwest Laboratory的研究人员发现,Np在高岭石(kaolinite)上的吸附与pH值密切相关,在pH<5时,吸附很弱;在pH=5~7.5之间时,pH增加吸附作用增强[58]。
20世纪80年代初曾有人研究了有氧条件下Np(Ⅴ)在花岗岩上吸附的Kd与pH的关系[59-60]。地下水中Np(Ⅴ)的初始浓度为10-7mol/L。实验结果显示:在高pH时Kd值比低pH时的Kd值有明显的提高;当pH=2附近时,Kd≈0;当pH=7.8时,Kd=50~100 mL/g;在更高的pH时,Kd=200~300 mL/g。并发现花岗岩表面对Np的吸附作用与花岗岩中含Fe矿物的存在有很大的关系。
还有一些学者[61-62]]研究了Np(Ⅴ)在羟基磷灰石上的吸附行为。研究发现在c(Np(Ⅴ))=1.0×10-7~1.0×10-6mol/L时,在3 h内有90%的Np(Ⅴ)被吸附。pH=6~11时对Kd的影响明显。当pH由6增大到8.5时,Kd从123 L/mol增大到69 200 L/mol,但是随着pH值进一步增大,Kd值有所减小。

Np(Ⅴ)可以被氧化物和粘土吸附,但不能被自然界存在的大多数矿物吸附。因为Np(Ⅴ)在与Ca2+等+2价金属阳离子竞争吸附点位时不占优势。Np(Ⅴ)在大多数矿物上吸附的Kd值很小,并且与pH有很大关系。当pH<5时Np(Ⅴ)的吸附很弱;当pH=5~7时,吸附作用随pH增大而增强。这种吸附与pH的关系说明在溶液中Np以阳离子的形态存在。pH=7~9的含碳酸根的溶液中,Np(Ⅴ)在氧化物上的吸附作用随pH的升高而减弱,这是因为形成了碳酸根络合物的缘故。Np在矿物上的吸附是一种表面络合过程。
2.2 Np在胶体上的吸附
在自然水体中,Np可能与天然存在的胶体发生吸附反应,这是影响Np的迁移的重要反应。20世纪80年代曾经有研究Np(Ⅴ)与天然存在的Al胶体的吸附作用[65-67]。其中Righetto[67]研究了Np(Ⅴ)在粒径为20 nm的Al氧化物胶体上的吸附,发现吸附量随pH的增大而增加,当pH>8时吸附量达到了100%。
Shepard等[68]研究了Np在土壤胶体颗粒上的吸附。这些胶体是把土壤溶解在水中形成的。他研究了14种不同的土壤形成的胶体,分别来自Muscatine、Illinois、Hanford、Washington、Barnwell、South Carolina、Idaho Falls、Idaho、Paradise、Placerville、California等不同地点。实验结果显示,有部分Np被胶体颗粒吸附;吸附反应在6个月时还没有达到平衡,并且吸附在胶体上的Np量随时间的增加而减少。实验结果很难用一般的物理化学理论解释,这是因为缺乏Np与腐殖酸发生离子交换和表面络合反应对吸附的贡献的有关数据。
基于这一结果,Shepard建议将Np在Clay胶体和腐殖酸胶体上的吸附行为作为研究Np在土壤中迁移的研究重点。
2.3 吸附机理
金属离子在矿物表面的吸附有4种类型:(1)静电吸附;(2)离子交换;(3)表面络合;(4)表面沉淀。经过多年研究发现,Np在矿物上的吸附实际上是一种表面络合的过程。使用表面络合模型解释Np的吸附行为,成为近年来的研究重点。已经有报道研究了Np在赤铁矿和不定形铁氢氧化物上的吸附和表面络合反应[69-71]。
俄罗斯的研究者[72]研究了低氧条件下Np(Ⅴ)在膨润土上的吸附,发现在pH较低时吸附机理是离子交换和表面络合;在近中性或弱碱性pH范围内吸附以表面络合为主。Np(Ⅴ)不但可以络合于方解石的表面,还可以进入方解石的晶体结构中[73]。


2.4 小 结
总结这些研究成果发现:粘土和含铁矿物对Np(Ⅴ)的吸附能力比较强,尤其是在低氧条件下,吸附能力更强。在近中性条件下,Np(Ⅴ)在环境介质上的吸附以表面络合为主,这是国际上公认的结果。表面络合的研究已经基本确定了Np在表面的形态。目前研究的重点是确定表面络合常数。

图4 用球-棍模型表示的Np(Ⅴ)的碳酸根络合物在赤铁矿上的吸附
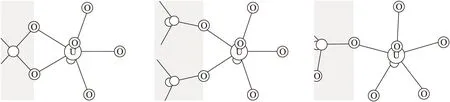
图5 用球-棍模型表示的Np(Ⅴ)在表面上的三种吸附一般形式
表3 与>FeOH、>SiOH、>AlOH的表面络合反应方程和平衡常数
这些研究成果已经在实践中有所应用。基于粘土和含铁矿物对Np的吸附能力较强,各国的处置库选址都选在粘土岩、花岗岩或凝灰岩中。回填材料多选择蒙脱土含量高的粘土矿物,如膨润土。
未来Np的迁移研究应该向2个方向发展:(1)完善吸附模型,主要是完善表面络合模型,获得Np与表面官能团的表面络合常数;(2)开展大尺度、多因素的迁移实验,并与模型预测的结果相比较。主要借助于地下实验室开展这一部分的工作。
3 有关研究工作的建议
Np的环境化学行为与一系列非常复杂的化学反应有关。虽经过多年的研究取得了一批相当有意义的成果,对Np的环境化学行为有了一定的了解。但是仅有这些成果还是远远不够的。现对进一步研究做如下建议。
(2)研究Np(Ⅴ)/Np(Ⅳ)的固体溶解动力学,重点研究晶体NpO2和不定型NpO2·xH2O的溶解反应热力学和动力学常数。以及固体中Np(Ⅴ)/Np(Ⅳ)的转化动力学。
(3)研究Np(Ⅳ)的胶体行为。应对腐殖酸胶体与Np的相互作用给予更大的关注。在胶体研究方法方面,重点进行胶体的非破坏性分离和分析表征研究。
(4)进一步研究Np与表面的相互作用机理。重点关注Np在含铁矿物表面和天然胶体表面的吸附和氧化还原反应。建立和完善表面络合模型。测定Np(Ⅴ)/Np(Ⅳ)与各种表面的表面络合常数和吉布斯自由能,完善表面络合数据库。建立Np的迁移模型。
(5)针对地质处置的需要,研究Np在大尺度地质介质和人工屏障材料中的迁移行为研究。当前和将来这一部分研究的主要方向是在地下实验室中开展处置环境下的热-湿-力-化学耦合迁移实验。验证Np的迁移模型,并根据验证结果校正和完善Np的迁移模型。
[1]克勒尔C.超铀元素化学[M].《超铀元素化学》编译组,译.北京:原子能出版社,1977:289-290.
[2]Kaszuba J P,Runde W H.The Aqueous Geochemistry of Neptunium: Dynamic Control of Soluble Concentrations With Applications to Nuclear Waste Disposal[J].Environ Sci Technol,1999,33: 4 427-4 433.
[3]姚军.237Np在模拟处置条件下的迁移行为研究[D].北京:中国原子能科学研究院,2006.
[4]Naturwissenschaften der D.Sorption and Direct Speciation of Neptunium(Ⅴ)on Aluminium Oxide and Montmorillonite[R].Mainz,Germany: Sonja Wendt Born in Langenhagen,2009.
[5]NItsche H.Solubility Studies of Transurznium Elements for Nuclear Waste Disposal: Principles and Overview[J].Radiochim Acta ,1991(52/53): 3-8.
[6]Nitsche H,Gatti R C,Standifer E M.Measured Solubility and Speciations of Neptunium,Plutonium,and Americium in a Typical Groundwater (J-13)From the Yucca Mountain Region: LA-12562-MS[R].Los Almos,NM: Los Alamos National Laboratory,1993.
[7]Nitsche H.Effect of Temperature on the Solubility and Speciation of Selected Actinides in Neat-Neutral Solutions[J].Inorg Chim Acta,1987(127): 121-126.
[8]Nitsche H,Roberts K,Prussin T,et al.Measured Solubilities and Speciations of Neptunium,Piutionium and Americium in UE-25p#1 Well Water From the Yucca Mountion Region: Milestone Report 33290-WBS1.2.3.4.1.3.1,LA-12562-MS[R].Los Almos,NM: Los Alamos National Laboratory,1994.
[9]Nitsche H,Roberts K,Prussin T,et al.Solubilities and Speciations Result From Over- and Undersaturation Experiments on Neptunium,Piutionium and Americium in Water From the Yucca Mountion Region Well UE-25p#1: LA-13017-MS[R].Los Almos,NM: Los Alamos National Laboratory,1995.
[10]Lemire R J,Boyer G D,Campbell A B.The Solubilities of Sodium and Potassium Dioxoneptunium(Ⅴ)Carbonate Hydrates at 30,50,and 75 ℃[J].Radiochimica Acta,1993( 61): 57-63.
[11]Silber H B,Nitsche H,Gatti R C,et al.The Effects of Radiolysis Upon Speciation and Solubility of Neptunium in Brine Solutions[J].Radiochim Acta,1994(66/67): 15-18.
[12]Runde W,Neu M P,Clark D L.Neptunium(Ⅴ)Hydrolysis and Carbonate Complexation: Experimental and Predicted Neptunyl Solubility in Concentrated NaCl Using the Pitzer Approach[J].Geochim Cosmochim Acta,1996(60): 2 065-2 073.
[13]Itagaki H,Nakayama S,Tanaka S,et al.Effect of Ionic Strength on the Solubility of Neptunium (Ⅴ)Hydroxide[J].Radiochim Acta,1992(58/59): 61-66.
[14]Roberts K E,Silber H B,Torretto P T,et al.The Experimental Determination of the Solubility Pro-duct for NpO2OH in NaCl Solutions[J].Radiochim Acta,1996(74): 27-30.
[15]Neck V,Kim J I,Kanellakopulos B.Solubility and Hydrolysis Behaviour of Neptunium(Ⅴ)[J].Radiochim Acta,1992(56): 25-30.
[16]Neck V,Runde W,Kim J I,et al.Solid-Liquid Equilibrium Reactions of Neptunium(Ⅴ)in Carbonate Solution at Different Ionic Strength[J].Radiochim Acta,1994(65): 29-37.
[17]Wolery T J,Palmer C E,Knauss K G.The Neptunium Solubility Problem in Repository Performance Assessment:A White Paper[R].Livermore,CA: Lawrence Livermore National Laboratory,1995.
[18]Roberts K E,Wolery T J,Atkins-Duffin C E,et al.Prussin.Precipitation of Crystalline Neptunium Dioxide From Near-Neutral Aqueous Solution[J].Radiochim Acta,2003(91): 87-92.
[19]Nakayama S,Yamaguchi T,Sekine K.Solubility ofNeptunium(Ⅳ)Hydrous Oxide in Aqueous Solutions[J].Radiochim Acta,1996(74): 15-19.
[20]Rai D R,Swanson J L.Solubility of NpO2·xH2O(s)in the Presence of Cu(Ⅰ)/Cu(Ⅱ)Redox Buffer[J].Radiochim Acta,1987(42): 35-41.
[21]Eriksen T E,Ndalamba P,Cui D,et al.Solubility of the Redox-Sensitive Radiouclides Tc and Np Under Reducing Conditinons in Neutral to Alkaline Solution Effect of Carbonate: TR 93-18[R].Stockholm: SKB,1993.
[22]Rai D,Ryan J L.Neptunium(Ⅳ)Hydrous Oxide Solubility Under Reducting and Carbonate Conditions[J].Inorg Chem,1985,24(3): 247-251.
[23]姜涛,姚军,王波,等.不同温度下Np(Ⅳ)在北山地下水中的溶解度[J].核化学与放射化学,2011,33(2):77-83.
[24]Nakayama S,Nagano T.Dission of Neptunium Dioxide in Aqueous Solutions[J].Radiochim Acta,1991(52/53): 9-11.
[25]Robert J.Chemical Thermodynamics Series Volume 4,Chemical Thermodynamics of Neptunium and Plutonium[M].OECD Nuclear Energy Agency Data Bank,Ed.Amsterdam,The Netherlands: North Holland Elsevier Science Publishers B.V.,2001.
[26]JNC.DATABASE Version: 011213c2.tdb,Waste Isolation Research Division[R].Tokai: Waste Management and Fuel Cycle Research Center,Tokai Works,Copyright 2003-2004.
[27]Wolery T J.1992.EQ/36,A Software Package for Gechemical Modeling of Aqueous Systems (Version 7.0): UCRL-MA-110662 PT Ⅰ-Ⅳ[R].Livermore,CA,USA: Lawrence Livermore National Laboratory,1992.
[28]Runde W,Neu M P,Clark D L.Neptunium(Ⅴ)Hydrolysis and Carbonate Complexation: Experimental and Predicted Neptunyl Solubility in Concentrated NaCl Using the Pitzer Approach[J].Geochim Cosmochim Acta,1996(60): 2 065-2 073.
[29]Fanghänel Th,Neck V,Kim J I.Thermodynamics of Neptunium(Ⅴ)in Concentrated Salt Solutions: I.Ion Interaction (Pitzer)parameters for Np(Ⅴ)Hydrolysis Species and Carbonate Complexes[J].Radiochim Acta,1995(69): 169-176.
[30]Neck V,Fanghänel Th,Kim J I.Mixed Hydroxo-Carbonate Complexes of Neptunium(Ⅴ)[J].Radiochim Acta,1997(77): 167-175.
[31]Moulin V,Tits J,Ouzounian G.Actinide Speciation in the Presence of Humic Substances in Natural Water Conditions[J].Radiochim Acta,1992(58/59): 179-190.
[32]Artinger R,Marquardt C M,Kim J I,et al.Humic Colloid-Borne Np Migration: Influence of the Oxidation State[J].Radiochim Acta,2000(88): 609-612.
[33]Sakamoto Y,Nagao S,Ogawa H,et al.The Migration Behavior of Np(Ⅴ)in Sandy Soil and Granite Media in the Presence of Humic Substances[J].Radiochim Acta,2000(88): 651-656.
[34]Marquardt C,Kim J I.Complexation of Np(Ⅴ)With Humic Acids at Very Low Metal Concentrations[J].Radiochim Acta,1996(73): 119-125.
[35]Marquardt C,Kim J I.Complexation of Np(Ⅴ)With Humic Acid: Intercomparison of Results From Different Laboratories[J].Radiochim Acta,1998(80): 129-137.
[36]Rancon D.Comparative Study of Radioactive Iodine Behavior in Soils Under Various Experimental and Natural Conditions[J].Radiochim Acta,1995(44/45): 187-193.
[37]Rao L,Choppin G R.Study of the Complexation of Neptunium(Ⅴ)With Humic Acids[J].Radiochim Acta,1988(69): 87-95.
[38]Choppin G R.The Role of Natural Organics in Radionuclide Migration in Natural Aquifer Systems[J].Radiochim Acta,1992(58/59): 113-120.
[39]Kim J I,Sekine T.Complexation of Neptunium(Ⅴ)With Humic Acid[J].Radiochim Acta,1991 (55): 187-192.
[40]Zeh P,Kim J I,Marquardt C M,et al.The Reduction of Np(Ⅴ)in Groundwater Rich in Humic Substances[J].Radiochim Acta,1999(87): 23-28.
[41]Itagaki,Tanaka H S,Yamawaki M.Neptunium Chemical Behavior in Underground Environments Using Ultrafiltration and Centrifugation[J].Radiochim Acta,1991(52/53): 91-94.
[42]Clark D L,Conradson S D,Ekberg S A,et al.EXAFS Studies of Pentavalent Neptunium Carbonato Complexes.Structural Elucidation of the Principal Constituents of Neptunium in Groundwater Environments[J].J Am Chem Soc,1996(118): 2 089-2 090.
[43]Sachs S,Schmeidel K,Reichl T,et al.EXAFS Study on the Neptunium(Ⅴ)Complexation by Various Humic Acids Under Neutral pH conditions[J].Radiochim Acta,2005 (93): 17-25.
[44]Neck V,Kim J I.Solubility and Hydrolysis of Tetravalent Actinudes[J].Radiochim Acta,2001 (89): 1-16.
[45]Kitamara A,Kohara Y.Carbonate Complexation of Neptunium(Ⅳ)in Highly Basic Solutions[J].Radiochim Acta,2004(92): 538-588.
[46]Nishita H,Wallace A,Romney E M,et al.Effect of Soil Type on the Extractability of Np-237,Pu-239,Am-241,and Cm-244 as a Function of pH[J].Soil Science,1981(132): 25-34.
[48]Combers J,Chisholm-Brause C J,Brown G E J,et al.EXAFS Spectroscopic Study of Neptunium(Ⅴ)Sorption at the R-FeOOH/Water Interface[J].Environ Sci Technol,1992,26: 376-382.
[49]Nakayama S,Sakamoto Y.Sorption of Neptunium on Naturally Occurring Iron Containing Mineral[J].Radiochim Acta,1991(52/53): 153-157.
[50]Meyer R E,Arnold W D,Case F I.Valence Effects on the Adsorption of Nuclides on Rocksand Minerals: NUREG/CR-3389 (ORNL-5978)[R].Oak Ridge,Tennessee: Commission by Oak Ridge National Laboratory,1984.
[51]Susak N J,Friedman A,Fried S,et al.The Reduction of Neptunium(Ⅵ)by Basalt and Olivine[J].Nucl Technol,1983(63): 266-270.
[52]Vejmelka P,Fanghaenel Th,Kienzler B,et al.Rartinger Sorption and Migration of Radionuclides in Granite: FZKA 6488[R].Karlsruhe: Institut fur Nukleara Entsurgent,2000.
[53]Nakata K,Nagasaki S.Sorption and Desorption Kinetics of Np(Ⅴ)on Magnetite and Hematite[J].Radiochim Acta,2000(88): 453-457.
[54]Grigorive M S,Fedoseev A M.Studay of Interaction of Pu(Ⅳ)and Np(Ⅳ,Ⅴ,Ⅵ)With Fe Hydroxides to Predict the Behavior of Actinides in Environmental Media[J].Radiochim Acta,2001(89): 95-100.
[55]Nakata K,Nagasaki S.Reduction Rate of Neptuni-um(Ⅴ)in Heterogeneous Solution With Magnetite[J].Radiochim Acta,2004(92): 145-149.
[56]Nakata K,Nagasaki S.Sorption and Reduction of Neptunium(Ⅴ)on the Surface of Iron Oxides[J].Radiochim Acta,2002(90): 665-669.
[57]Wilk P A,Shaughnessy D A,Wilson R E,et al.Interfacial Interactions Between Np(Ⅴ)and Manganese Oxide Minerals Manganite and Hausmannite[J].Environ Sci Technol,2005,39: 2 608-2 615.
[58]Relyea J F,Martin W J.Adsorption of Np-237 and Ra-228 on Kaolinite: PNL-4426[R].Richland,Washington: Pacific Northwest Laboratory,1982.
[59]Torstenfelt B,Rundberg R S,Mitchell A J.Actinide Sorption on Granites and Minerals as a Function of pH and Colloids/Pseudocolloids[J].Radiochim Acta,1988(44/45): 111-117.
[60]Beall G W,Allard B,Krajewski T,et al.Chemical Reactions in the Bedrock-Groundwater System of Importance for the Sorption of Actinides[J].Scientific Basis for Nuclear Waste Management,1980,2: 625-631.
[61]Moore R C,Holt K,Zhao H T,et al.Sorption of Np(Ⅴ)by Synthetic Hydroxyapatite[J].Radiochim Acta,2003(91): 721-727

[63]姚军,苏锡光,龙会遵,等.237Np(Ⅴ)在膨润土上的吸附行为研究[J].核化学与放射化学,2003,25(2):102-114.
[64]姜涛,姚军,周舵,等.温度对Np在北山花岗岩上吸附行为的影响[J].核化学与放射化学,2011,33(1):25-31.
[65]Kim J I,Buckau G,Baumgartner F,et al.Colloid Generation and the Actinide Migration in Gorleben Groundwaters[J].Mat Res Soc Symp Proc,1984(26): 31-40.
[66]Kim J I,Buckau G,Rommel H,et al.The Migration Behavior of Tramsuranium Elements in Gorleben Aquifer Systems: Colloid Generation and Retention Process[J].Mat Res Soc Symp Proc,1989(127): 849-854.
[67]Righetto L,Bigodlio G,Marcandalli B,et al.Surfece Interactions of Actinide With Alumina[J].Radiochim Acta,1988(44/45): 73-80.
[68]Sheppard J C,Campbell M J,Kittrick J A,et al.Retention of Neptunium,Americium,and Curium by Diffusible Soil Particles[J].Environ Sci Tech-nol,1979(13): 680-684.
[69]Kohler M,Honeyman B D,Leckie J O.Neptunium(Ⅴ)Sorption on Hematite (γ-Fe2O3)in Aqueous Suspension: The Effect of CO2[J].Radiochim Acta,1999(85): 33-48.
[70]Girvin D C,Ames L L,Schwab A P,et al.Neptunium Adsorption on Synthetic Amorphous Iron Oxyhydroxide[J].J Colloid Inter Sci,1991(141): 67-78.
[71]Fujita T,Tsukamoto M,Ohe T,et al.Modeling of Neptunium(Ⅴ)Sorption Behavior Onto Iron-Containing Minerals[J].Scientific Basis for Nuclear Waste Management XVII,1995,353: 965-972.
[72]Sadobina M N, Kalmykov S N.Neptunium,Plutonium and137Cs Sorption by Bentonite Clays and Their Speciation in Pore Waters[J].J Radioanal Nucl Chem,2006,270(2): 349-355.
[73]Heberling F,Demcke M,Dirkbosbach.Neptunium(Ⅴ)Coprecipitation With Calcite[J],Environ Sci Technol,2008,42: 471-476.
[74]Arai Y,Moran P B,Honeyman B D,et al.In Situ Spectroscopic Evidence for Neptunium(Ⅴ)-Carbonate Inner-Sphere and Outer-Sphere Ternary Surface Complexes on Hematite Surfaces[J].Environ Sci Technol,2007,41: 3 940-3 944.
[75]Zavarin M,Roberts S K,Rose T P,et al.Validating Mechanistic Sorption Model Parameters and Processes for Reactive Transport in Alluvium: UCRL-ID-149728[R].Livermore,CA: Lawrence Livermore National Laboratory,2002.
