猴头菌固体发酵基质的抗氧化活性成分研究
2011-12-27张新超郭丽琼林俊芳雷韵祺
张新超 郭丽琼 林俊芳 雷韵祺
(1.华南农业大学食品学院生物工程系,广东 广州 510640;2.华南农业大学生物质能研究所,广东 广州 510640;3.广东珠江桥生物科技股份有限公司,广东 中山 528415)
猴头菌固体发酵基质的抗氧化活性成分研究
张新超1,3郭丽琼1,2林俊芳1,2雷韵祺1
(1.华南农业大学食品学院生物工程系,广东 广州 510640;2.华南农业大学生物质能研究所,广东 广州 510640;3.广东珠江桥生物科技股份有限公司,广东 中山 528415)
选用燕麦、大豆、玉米、麸皮、大米、荞麦6种培养基质,对猴头菌进行固体发酵及抗氧化活性研究。结果表明:猴头菌最佳抗氧化发酵基质为荞麦大豆培养基(荞麦79.13%,大豆20.87%),最佳发酵条件为温度30℃,培养料粒度40目,培养基含水量70%,初始pH值4,接种量4.5%,发酵时间12d。猴头菌荞麦发酵基质抗氧化活性成分种类丰富,含量高,其中总黄酮物质87.13μg/g,总三萜2.58mg/g,多酚4.51mg/g,还原糖 21.53mg/g,花色苷68.96μg/g,VC14.07mg/g,VE205.85μg/g,GSH 853.65mg/g,SOD 酶活性293.57U/g。
猴头菌;固体发酵;发酵基质;抗氧化成分
人类和动物持续暴露在活性氧与促氧化剂中,很容易引起机体组织发生氧化应激,导致机体代谢性功能的紊乱以及一系列的慢性疾病,如癌症、血脂异常等[1]。食用一些富含具有抗氧化生物活性物质的功能性食品,可以延缓或预防机体组织氧化应激损伤。食药用菌以其较强的生理功能和较小的毒副作用的特性,被越来越广泛采用。
猴头菌是著名的食用、药用真菌,素称“蘑菇之王”,它与熊掌、燕窝、鱼翅并列为四大名菜,自古以来被誉为“山珍”。猴头菌富含多种有益菌多糖和人体必需氨基酸以及微量元素(如Fe、Cu、Zn、Se等),此外还含有多种抗氧化成分[2]。中国已经广泛用于医治消化不良、胃溃疡、食道癌、胃癌、十二指肠溃疡、肛门癌等消化系统的疾病与肿瘤的治疗[3]。
目前对猴头菌的抗氧化功能研究仅仅停留在其子实体或菌丝体成分分析阶段。本试验选用燕麦、大豆、玉米、麸皮、大米、荞麦6种培养基对猴头菌进行固体发酵研究,分析其发酵基质的抗氧化成分,为开发猴头菌功能性菌质食品提供帮助。
1 材料与方法
1.1 材料与试剂
猴头菌:购于山东寿光食用菌研究所;
燕麦、大豆:市售;
2,2-联氮-二(3-乙基-苯并噻唑-6-磺酸)(ABTS)、VE标准品(含量≥96%,以α-生育酚计)、芦丁标品、齐墩果酸标品、抗坏血酸标准品(L-抗坏血酸):Sigma Aldrich公司;
还原型谷胱甘肽 (GSH)试剂盒:南京建成生物工程研究所;
其余试剂:均为市售分析纯。
1.2 培养基与培养方法
PDA培养基:马铃薯(去皮)200g/L、葡萄糖20g/L、磷酸氢二钾3g/L、硫酸镁1.5g/L、葡萄糖 20g/L、琼脂20g/L,蒸馏水定容,高压灭菌后备用。
猴头菌母种经活化后接种于PDA平板并置于30℃培养7d,然后在无菌条件下转接入发酵培养基(玻璃组培瓶,高10cm,直径6.5cm)中,30℃培养。
1.3 试验方法
1.3.1 最优抗氧化培养基的确定 以大米、燕麦、大豆、麸皮、玉米、荞麦为基本培养料,按照猴头菌所需碳氮比(27∶1)。运用design expert 7.0软件选用 mixture design的单型格子设计,以生长速度和总自由基清除率为响应值确定最佳抗氧化培养基。
1.3.2 总自由基清除率测定
(1)浸提液的提取:参照文献[4]的方法并作改进。将发酵后的固体菌质60℃烘干,粉碎,过60目筛,精确称取1.000g,加入95%乙醇10mL,25℃以200r/min摇床旋转下萃取24h,离心(6 000g,5min),上清液即为醇提液。剩余残渣,加10mL水,25℃下以200r/min摇床旋转萃取24h,离心(6 000g,5min),取上清液即为水提液。
(2)自由基清除率测定:采用 ABTS法[5]。
1.3.3 最佳发酵条件的确定 在培养料未分粒度,培养料含水量为60%,接种量为1.5%,发酵温度为30℃,培养基初始pH值自然的基础上,对发酵温度(20,25,28,30,32,35℃)、培养料粒度(10,20,30,40,60目)、培养基含水量(50%,60%,65%,70%)、培养基初始pH 值(4,5,6,7,8,9)、接种量(1.5%,3%,4.5%,6%,7.5%)进行优化,确定最佳的发酵条件。
1.3.4 抗氧化成分测定 发酵结束后,将猴头菌发酵基质置于烘箱60℃下烘干,粉碎过60目筛,备用。未发酵基质灭菌(121℃,30min)后置于烘箱60℃下烘干,粉碎过60目筛,备用。
(1)总黄酮的测定:参照文献[6]的方法进行。以芦丁为标准品,标准曲线回归方程为y=5.112 5x+0.006 6,R2=0.999 6。
(2)总多酚的测定:参照文献[7]的方法进行。以没食子酸为标准品,标准曲线回归方程为y=0.025 1x+0.045 4,R2=0.996 2。
(3)总三萜的测定:总三萜的提取参考文献[8]的方法并有所改进。称取(0.250 0±0.000 2)g,加入三氯甲烷100mL回流提取1h,冷却,于45℃减压回收至干,加15mL饱和NaHCO3溶液洗至分液漏斗,再用6mol/L的HCl调节pH值至3~4,后用氯仿(CHCl3与NaHCO3体积比为1∶2)萃取,收取氯仿层(下层),减压蒸干氯仿,加甲醇定容至10mL的容量瓶刻度。
总三萜的测定参照文献[9]的方法进行。以齐墩果酸为标准品,标准曲线回归方程为y=4.822x-0.006 6,R2=0.992 8。
(4)还原糖的测定:采用 DNS法[10,11]。以葡萄糖为标准品,标准曲线回归方程为y=0.533 3x-0.009 6,R2=0.998。
(5)VC的测定:参照文献[12]的方法进行。以L-抗坏血酸为标准品,标准曲线回归方程为y=0.105 2x-0.110 7,R2=0.999。
(6)VE的测定:参照文献[13]的方法进行。以α-生育酚为标准品,标准曲线回归方程为y=2.900 5x-0.000 7,R2=0.999 2。
(7)花色苷的测定:参照文献[14]的方法进行。
(8)内源性抗氧化物质(GSH、SOD)的测定:谷胱甘肽(GSH)和超氧化物歧化酶(SOD)样品液的提取参照Chung等的方法[15]进行。还原型谷胱甘肽的测定严格按照试剂盒说明书操作,GSH含量的单位为 mg/g;SOD的测定参照Beyer等的方法[16]进行。
1.3.5 数据统计 样品测定采用6个重复。试验结果用SPSS 17.0软件进行统计分析,以平均值±标准差 (x±S)表示,运用Excel 2003软件作图。
2 结果与分析
2.1 最优培养基配方的确定
猴头菌在不同培养基质的生长速度及发酵后基质的总自由基清除率结果见表1。由表1可知,配方5生长速度与配方1、2、3、4、6、7差异均不显著(P<0.05),与其他配方差异显著(P<0.05);总自由基清除率与其他配方差异均显著(P<0.05),最终选定配方5为最优抗氧化培养基即荞麦大豆培养基。培养基组成成分为:荞麦79.13%,大豆20.87%。
2.2 最佳发酵条件的确定
2.2.1 温度对发酵的影响 猴头菌在不同发酵温度下发酵后基质的自由基清除率和生长速度见图1。
由图1可知,猴头菌30℃生长速度与其他温度差异均显著(P<0.05);自由基清除率与其他温度差异均显著(P<0.05),最终选定温度30℃为猴头菌最优发酵温度。
2.2.2 培养料粒度对发酵的影响 猴头菌在不同培养料粒度下发酵后基质的自由基清除率和生长速度见图2。
由图2可知,猴头菌40目,生长速度与20,30目呈现不显著差异(P<0.05),与10,60目差异显著(P<0.05);自由基清除率与其他均呈显著差异(P<0.05)。最终选定培养料粒度40目为猴头菌最优培养料粒度。

表1 培养基质对猴头菌生长速度及总自由基清除率的影响 Table 1 Influence of the mixture composition on the growth rate and the radical scavenging activity during solid cultivation of Hericium erinaceum
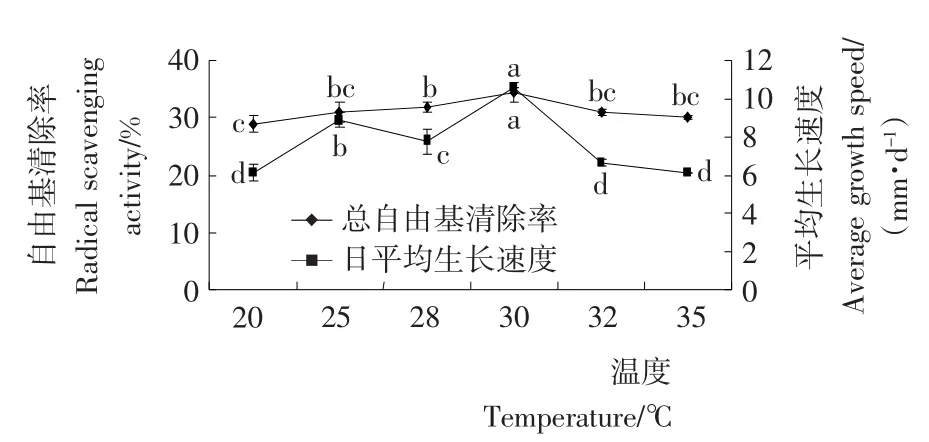
图1 发酵温度对猴头菌发酵后基质的自由基清除率和生长速度的影响Figure 1 Influence of fermentation temperature on the radical scavenging activity and the average growth speed during solid cultivation of Hericium erinaceum

图2 培养料粒度对猴头菌发酵后基质的自由基清除率和生长速度的影响Figure 2 Influence of material grain size on the radical scavenging activity and the average growth speed during solid cultivation of Hericium erinaceum
2.2.3 初始pH值对发酵的影响 猴头菌在不同初始pH值下发酵后基质的自由基清除率和生长速度结果见图3。由图3可知,猴头菌pH=5,生长速度与其他均呈现不显著差异(P<0.05);自由基清除率与pH=6、pH=7、pH=9均呈不显著差异(P<0.05),与pH=4、pH=8差异显著(P<0.05)。但由于pH=5时猴头菌发酵后基质的自由基清除率最高,故最终选定初始pH=5为猴头菌最优初始pH值。
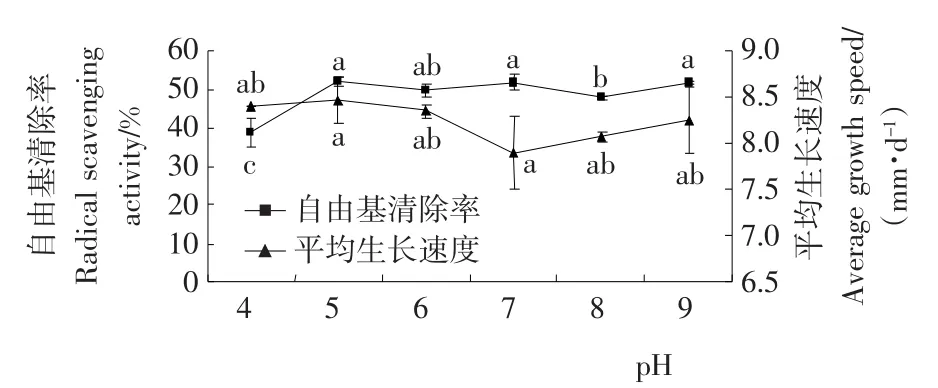
图3 初始pH值对猴头菌发酵后基质的自由基清除率和生长速度的影响Figure 3 Influence of initial pH on the radical scavenging activity and the average growth speed during solid cultivation of Hericium erinaceum
2.2.4 培养基含水量对发酵的影响 猴头菌在不同培养基含水量下发酵后基质的自由基清除率和生长速度见图4。
由图4可知,猴头菌培养基含水量60%,生长速度与80%呈不显著差异,与其他差异均显著(P<0.05);自由基清除率与其他差异均显著(P<0.05)。最终选定60%为猴头菌最适培养基含水量。
2.2.5 接种量对发酵的影响 猴头菌在不同接种量下发酵后基质的自由基清除率和生长速度见图5。

图4 培养基含水量对猴头菌发酵后基质的自由基清除率和生长速度的影响Figure 4 Influence of culture medium moisture on the radical scavenging activity and the average growth speed during solid cultivation of Hericium erinaceum
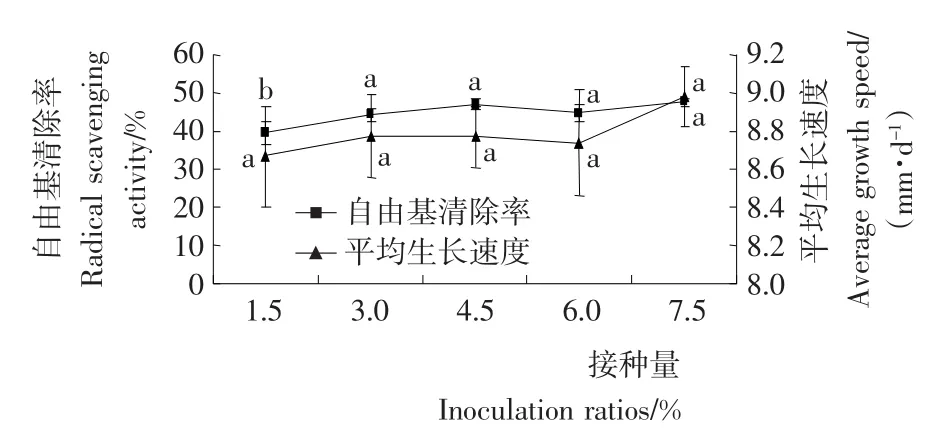
图5 接种量对猴头菌发酵后基质的自由基清除率和生长速度的影响Figure 5 Influence of inoculation on the radical scavenging activity and the average growth speed during solid cultivation of Hericium erinaceum
由图5可知,猴头菌接种量7.5%,生长速度与3%、4.5%、6%呈不显著差异,与1.5%差异显著(P<0.05);自由基清除率与其他差异均不显著(P<0.05)。但由于接种量为7.5%时猴头发酵后基质的总自由基清除率最高,最终选定7.5%为猴头菌最适接种量。
2.3 培养时间的确定
发酵时间对猴头菌自由基清除率的结果见图6。

图6 发酵时间对猴头菌基质自由基清除率的影响Figure 6 Influence of fermentation time on the radical scavenging activity during solid cultivation of Hericium erinaceum
由图6可知,猴头菌基质自由基清除率随着发酵时间的增长发生显著性变化(P<0.05),其中在12d出现最大,14,16d未出现显著性差异,但其他时间点出现显著性差异(P<0.05)。故选择12d作为猴头菌最佳培养时间。
2.4 猴头菌基质抗氧化活性成分分析
猴头菌发酵完全后,其基质的抗氧化活性成分测定结果见表2。由表2可知,猴头菌发酵基质中抗氧化活性成分,与未发酵的基质相比,总黄酮含量及还原糖含量下降明显,总三萜物质含量略有下降,花色苷及总多酚含量上升,VC略有下降,VE含量明显上升,SOD酶活性提高,GSH含量上升为原来的4倍左右。

表2 猴头菌发酵基质抗氧化活性成分分析Table 2 The antioxidant components analysis of full fermentation substrate of Hericium erinaceum
3 讨论
本试验在前期研究的基础上,对猴头菌在荞麦大豆培养基固体发酵得到的发酵基质进行抗氧化成分分析,发酵前后各抗氧化成分含量变化明显。总黄酮含量的下降可能是猴头菌生长代谢中利用黄酮醇物质(包括花色素)与还原糖发生反应生成苷元含量降低造成,这与Gert等[17]报道相符。总三萜物质含量略有下降的原因可能是发酵过程中猴头菌菌丝生长代谢过程中分解三萜皂苷,释放苷元以合成其他新的糖苷物质,这与Shashi等[18]报道相符。总多酚含量的上升可能是猴头菌生长过程中产生的酚类次生代谢产物聚合累积所致,这与Fulgencio等[19]报道基本相符。花色苷含量的升高可能是猴头菌生长代谢过程中利用糖类和色素物质合成了花色苷,这与Jin等[20]报道相一致。还原糖的含量显著降低与总黄酮含量的下降和花色苷含量的上升相吻合。维生素类物质中VC略有下降,VE含量明显上升的原因为发酵过程中通过分解VC并利用其他物质产生新的VE。内源性抗氧化物质中SOD酶活性和GSH含量的提高是发酵过程中猴头菌菌丝生长代谢过程自身产生的结果。本试验结果表明,猴头菌在荞麦大豆基质发酵后,基质中抗氧化物质含量整体提高明显,以猴头菌固体发酵后基质中的抗氧化物质开发新型抗氧化食品切实可行,为进一步开发功能性菌质食品提供了参考。
1 Diplock A T,Charleux J L,Crozier-Willy G Kok,et al.Functional food Science and defence against reactive oxidative species[J].British Journal of Nutrition,1998,80:77~112.
2 刘梅森,陈海晏.猴头菌的药用价值概述[J].中国食用菌,1998,18(1):24~25.
3 蒲昭和.猴头菇:山珍美味的抗癌食品[J].药膳食疗研究,2000(2):36.
4 Pellegrinin R R,Yang M.Screening of dietary carotenoids and carotenoid-rich fruit extracts for antioxidant activities applying 2,2-azinobis(3-ethylenebenzothiazoline-6-ulfonic acid radical cation decolonization assay[J].Methods Enzymol,1999(299):379~389.
5 Roberta R E,Pellegrini A,Proteggente A,et al.Antioxidant activity applying an improved ABTS radical cation decolorization assay[J].Free Radical Biology and Medicine,1999(26):1 231~1 237.
6 洪艳平,陈木森,上官新晨,等.枸骨叶总黄酮超声辅助提取与测定[J].食品与机械,2009,25(1):72~75.
7 李志洲.微波辅助提取石榴叶中多酚类物质的工艺[J].食品与机械,2009,25(4):72~75.
8 蔡辉,王芳生,王丽凤,等.赤芝中灵芝酸类生物活性成分含量的测定方法[J].中国兽医学报,2001,21(4):381~383.
9 刘海良,宋爱荣,黄芳.树舌灵芝发酵液中灵芝酸的提取及测定[J].食用菌学报,2008,15(3):68~71.
10 Bojana Boh,Marin Berovic,Zhang J S,et al.Ganoderma lucidum and its pharmaceutically active compounds[J].Biotechnology Annual Review,2007(13):265~301.
11 Miller G L.Use of dinitrosalicylic acid reagent for determination of reducing sugar[J].Analytical Chemistry,1959(31):426~428.
12 Saliha Erenturk,M Sahin Gulaboglu,Selahattin Gultekin.The effects of cutting and drying medium on the vitamin C content of rosehip during drying[J].Journal of Food Engineering,2005(68):513~518.
13 Magda S Taipina,LedaC A Lamardo,Maria A B Rodas,et al.The effects of gammair radiation on the vitamin E content and sensory qualities of pecan nuts(Caryaillinoensis)[J].Radiation Physics and Chemistry,2009(78):611~613.
14 Fuleki T,Francis F J.Quantitative methods for anthocyanin:1.Extraction and determination of total anthocyanins in cranberries[J].Journal of Food Science,1968(33):72~77.
15 Ill Min Chung,Jong Jin Kim,Jung Dae Lim,et al.Comparison of resveratrol,SOD activity,phenolic compounds and free amino acids in Rehmannia glutinosa under temperature and water stress[J].Environmental and Experimental Botany,2006(56):44~53.
16 Beyer W,Fridovich I.Assaying for superoxide dismutase activity:some large consequences of minor changes in conditions[J].Anal.Biochemistry,1987(161):559~566.
17 Gert Forkmann,Stefan Martens.Metabolic engineering and applications of flavonoids[J].Current Opinion in Biotechnology,2001(12):155~160.
18 Shashi B Mahato,Sudip K Sarkar,Gurudas Poddar.Triterpenoid saponins[J].Phytochemistry,1988(27):3 037~3 067.
19 Fulgencio Saura-Calixto,JoséSerrano,Isabel Go i.Intake and bioaccessibility of total polyphenols in a whole diet[J].Food Chemistry,2007(101):492~501.
20 Jin-Ming Kong,Lian-Sai Chia,Ngoh-Khang Goh,et al.Analysis and biological activities of anthocyanins[J].Phytochemistry,2003(64):923~933.
Analysis of antioxidant components of solid fermented substrates withHericium erin aceum
ZHANG Xin-chao1,3GUO Li-qiong1,2LIN Jun-fang1,2LEI Yun-qi1
(1.Department of Bioengineering,College of Food Science,South China Agricultural University,Guangzhou,Guangdong510640,China;2.Institute of Biomass Research,South China Agricultural University,Guangzhou,Guangdong510640,China;3.Guangdong Pearl River Bridge Bio-Tech CO.,LTD,Zhongshan,Guangdong528415,China)
Hericium erinaceumwas cultured on the medium including oat,wheat bran,soybeans,corn,rice and buckwheat with solid-state fermentation,and then was determined the best fermentation time and was analyzed antioxidant components of substrate.The results show that the best antioxidant fermentation substrate ofHericium erinaceumwas buckwheat and soybeans complex medium (79.13%buckwheat and 20.87%soy beans),the optimum fermentation temperature for 30℃,material grain size for 40mesh,medium moisture for 70%,initial pH for 4,inoculation for 4.5%,and the best fermentation time was 12d.The antioxidant components ofHericium erinaceumsubstrate with buckwheat were rich in varieties and high in contents,such as flavonoids 87.13μg/g,total triterpenoid 2.58mg/g,total polyphenols 4.51mg/g,reducing sugar 21.53mg/g,anthocyanins 68.96μg/g,VC14.07mg/g,VE205.85μg/g,GSH 853.65mg/g,SOD activity 293.57U/g.
Hericium erinaceum;solid fermentation;cultivation substrates;antioxidant components
10.3969/j.issn.1003-5788.2011.04.011
国家自然科学基金(编号:31071837);广东省科技计划(编号:2009B020201012)
张新超(1986-),男,华南农业大学在读硕士研究生。E-mail:selvan.zhang@gmail.com
林俊芳
2011-04-01
