饱和食盐水比热容的测量
2011-12-09武银兰张青兰
武银兰,张青兰
(太原理工大学山西太原 030024)
饱和食盐水比热容的测量
武银兰,张青兰
(太原理工大学山西太原 030024)
在室温下分别利用散热法、混合法对饱和食盐水的比热容进行测量,通过比较推知饱和食盐水比热容的值大约为3.212~3.243 J/(g.K)。所得结果的可靠性主要与实验的系统误差有关。
比热容;散热法;混合法
比热容反映了物质的热学性质,可通过混合法、散热法、电热法等方法进行测量[1]。对于饱和食盐水的比热容的测量未见报道,本文利用散热法、混合法分别测其比热容,并就测量误差进行分析。
1 散热法
1.1 牛顿冷却定律
一个系统的温度如果高于环境温度,它就会损失热量,如果低于环境温度,它就会吸收热量。实验证明,当系统与外界环境温度差较小(10~15℃以内)时,其单位时间内损失的热量与温度差成正比,这就是牛顿冷却定律:
其中:δq是系统在一个很小的时间段δt内散失的热量,δq/δt称为散热速率,k是散热系数,与物体的表面性质、表面积、物体周围介质的性质和状态以及物体的表面温度等许多因素有关。在T-θ很小时,k可看作是一个常数。
如果在实验中保持环境温度θ恒定,则δq=Csδ(T θ),式中Cs是系统的热容。对(1)式积分得到:


其中b是积分常数。可见ln(T-θ)与时间t成线性关系,通过测量可以求得直线斜率k/Cs。如果已知系统的热容Cs,可以求得其散热系数。反过来,如果已知系统的散热系数k,可以求得其热容Cs。
1.2 比较法进行散热修正
量热器是在物质的比热容测量中经常使用的仪器,尽管对它的设计已经采取了许多措施以减小系统与外界的热量交换,但仍然不能做到完全绝热。在精确的测量中,还必须对系统的散热进行修正。
利用(2)式,分别写出对标准液体(水)和待测液体(饱和食盐水)进行冷却的公式:

上式中Csw和Css分别是系统中盛水和饱和食盐水时的热容。如果在实验中用同一个容器分别盛水和饱和食盐水,并保持在这两种情况下系统的初始温度、表面积和环境温度等基本相同,则可以认为系统在分别盛水和饱和食盐水时的散热系数kw和ks相同,即:
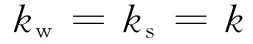

式中:Sw和Ss的数值可由作图法得出。
热容Csw和Css分别为:

其中mw、ms、c0、cs分别是水和盐水的质量及比热容;m1、c1是量热器内筒和搅拌器的质量及比热容;δC′和δC″是温度计浸入已知液体和待测液体

1.3 实验部分
测量量热器内筒和搅拌器的质量,及饱和食盐水、纯水质量,并将饱和食盐水、纯水分别加热部分的等效热容。这部分等效热容很小,可以忽略不计。所以待测盐水的比热容为:到高于环境温度约10~15℃,记录系统散热的环境温度(量热器外筒的水温),各数据见表1。
分别把加热到高于环境温度约10~15℃的盐水与普通水放入相同的量热器中,再把量热器放入温度恒定的凉水中,用搅拌器搅拌并每隔2 min记录其温度,其值见表2~3。

表1 饱和食盐水与纯水散热前各物理量的测量数据

表2 盐水测量所得数据

表3 水测量所得数据
利用表2、表3中数据,用Origin作图软件作出ln(T-TR)-t的关系曲线见图1,由图得直线的斜率分别为Sw=-0.010 93,Ss=-0.011 11。
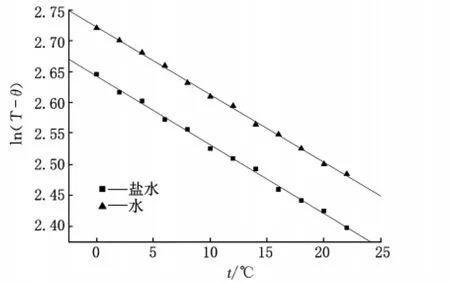
图1 ln(T-θ)~t l的关系曲线
将有关数据及黄铜的比热容c1=0.389 J/(g·K),水的比热容c0=4.182 J/(g·K)代入公式(6)与(8)得饱和食盐水的比热容为cx=3.243 J/(g·K)。
2 混合法
2.1 混合法测液体比热容原理
将温度不同的物体混合后,如果由这些物体组成的系统没有与外界交换热量,最后系统将达到均匀、稳定的平衡温度。在此过程中,高温物体放出的热量等于低温物体所吸收的热量。
本实验系统的高温部分为饱和热盐水,其温度高于室温约10~15℃,低温部分为量热器内筒、搅拌器和室温饱和盐水。设量热器内筒和搅拌器的质量为m,比热容为c0,冷盐水质量为m1,这二者初温为T1,热盐水质量为m2,初温为T2。将加热到一定温度的热盐水迅速倒入装有一定冷水的量热器内筒中,经过搅拌后,系统达到热平衡时的温度为T,假设系统与外界没有任何热交换,则根据热平衡原理,实验系统的热平衡方程为


2.2 实验部分
分别测量热、冷饱和食盐水在混合前的质量及初温。室温下,把热盐水加热到比冷盐水温度高约10~15℃后很快倒入量热器内筒中的冷盐水中,用搅拌器不断搅拌并观察温度计的示数,当两分钟内,温度计示数稳定时记录此时热平衡温度。数据见表4。
将以上数据代入(10)式得饱和食盐水的比热容为c=3.212 J/(g·K).
由此得出待测盐水的比热容为

表4 热、冷饱和食盐水在混合前、后的有关数据
3 结果分析
文献[2]分别测得不同浓度2%,6%,10%的食盐水在24℃时的比热容,并与20℃时的标准值[3]比较,见表5。文献[4]测得环境温度为5.5℃时,10%,20%的食盐水的比热容分别为4.153 8 J/(g·K),3.523 8 J/(g·K)。从上文两种方法得出的测量值看来,两种方法所得结果相近,且与文献[2,4]的结果比较可推知,食盐水浓度越大比热容越小,饱和食盐水比热容的大小约为3.212~3.243 J/(g·K)。

表5 食盐水的比热容
散热法测量中,待测盐水的比热容公式(8)得出的前提是:系统在分别盛水和饱和食盐水时的散热系数kw和ks相同。为此,在实验中需用同一个容器分别盛水和饱和食盐水,并保持在这两种情况下系统的初始温度、表面积和环境温度等基本相同。本实验中,系统所处的环境为可控的流动水,每次实验大约花费30 min,由于室内大环境温度不稳定,系统所处的环境温度也不十分稳定,当系统的热容一定时,对散热系数有较大影响。所以需严密监控环境温度,适时增减水流。对饱和食盐水与纯水的两次实验,散热系统周围环境即水槽中的水面高度要一致,否则散热系数差别较大。量热器内筒中饱和食盐水与纯水的体积要大致相等,约为内筒高度的2/3。高度不等,其散热系数自然不等。另外,纯水和盐水放入量热器后,应不断轻轻搅拌,以保证系统温度各处均匀,测量温度符合被测温度。测量系统的温度和时间应同步进行,使其一一对应。
混合法测量中,加热到一定温度的热盐水倒往冷盐水时,速度要快,但再快热盐水也会向周围环境散失少部分热量。冷热盐水混合过程中,量热器不可避免地会与周围环境进行热交换,这部分损失的热量并未考虑,参与吸收热量的部分减小,测量值偏小。另外,准确地判断热平衡温度也是非常必要的。冷热盐水热交换过程较快,热平衡后温度还高于周围环境,于是会发生整个量热器系统与周围环境的热交换,系统温度继续降低,随着与周围环境温度的接近,温度的降低逐渐减慢。热平衡温度为系统温度呈现有规律降低前的温度,因此冷热盐水混合后,需用搅拌器不断搅拌混合液体,适时关注并记录其温度变化,准确判断平衡温度。
4 结 论
饱和食盐水比热容的值未见文献报道,本文分别使用散热法、混合法对其测量,测量值相近,所得结果的可靠性与测量方法的系统误差有很大关系。由于各实验方法不同,系统误差也不相同,每一因素不到位都会使结果有较大偏离。
[1] 王云才.大学物理实验教程[M]3版.北京:科学出版社,2010:121-127.
[2] 蒋林华,徐佩珠.冷却法测定盐水比热容的讨论[J].湖州师专学报,1994(6):53-59.
[3] 龚镇雄,刘雪林.普通物理实验指导:力学、热学和分子物理学[M].北京:北京大学出版社,1990:167-179.
[4] 何晓明,利用牛顿冷却定律测定盐水的比热容[J].青海大学学报:自然科学版,2007,25(4):85-87.
Measuring of Specific Heat of Saturation Salt Solution
WU Yin-lan,ZHANG Qing-lan
(Taiyuan University of Technology,Shangxi Taiyuan 030024)
In this paper,the specific heat of saturation salt solution was measured by cooling method and mixing method.It is shown that,the specific heat value of saturation salt solution is approximately 3.212~3.243J/(g.K).The reliability of result depends mainly of the experiment system error.
specific heat;cooling method;mixing method
O 343
A
1007-2934(2011)05-0032-03
2011-05-10
