新疆曼陀罗子及其代表制剂艾比西帕丸的大鼠长期毒性试验
2011-12-08热比姑丽伊斯拉木尤力都孜买买提阿布都吉力力阿布都艾尼艾西木江热甫卡提凯赛尔阿不都克热木
热比姑丽·伊斯拉木,尤力都孜·买买提,阿布都吉力力·阿布都艾尼,艾西木江·热甫卡提,闫 明,凯赛尔·阿不都克热木
(1.新疆维吾尔自治区维吾尔医药研究所,2.新疆维吾尔医方剂学实验室,新疆乌鲁木齐 830049)
用药安全性评价是药物临床前研究和临床评价的重要内容,维吾尔医药针对一些特色制剂及有毒性药材的使用和控制,以及临床前安全评价的研究较为滞后,这影响了维吾尔医药的发展。本研究选择临床常用、具有代表性的特色维吾尔药毒性药材曼陀罗子及其代表制剂镇痛艾比西帕丸为研究对象,通过毒理学研究,探讨其毒性表现和毒性靶器官。
1 材料与方法
1.1 样品与试剂 新疆曼陀罗子(生品)由自治区维吾尔医医院药厂提供,批号:20090503;曼陀罗子提取物由新疆维阿堂药业有限公司提供,批号:20090719;镇痛艾比西帕丸(成品)由新疆喀什维吾尔医医院提供,新药准字Z04000972,批号:20091072;血生化学、血细胞、电解质及凝血酶原时间试剂盒均购自中生北控生物科技股份有限公司。
1.2 仪器 PM4000/3全自动生化分析仪,意大利罗马;BC300全血细胞分析仪,深圳迈瑞生物医疗电子股份有限公司;HK2003电解质分析仪,郑州市汇科电子有限公司;SZZ血凝分析仪,深圳市鹏瑞佳电子有限公司;DM2500生物显微镜,德国莱卡公司;H-600型透射电镜,日本HITACHI公司。
1.3 动物 SD大鼠,SPF级,200只,♀♂各半,体质量80~120 g,由新疆实验动物研究中心提供,许可证号:SCXK(新)2003-0002。动物合格证:2010-D3418
1.4 试验方法[1-3]大鼠检疫1周后,按体重、性别随机分为对照组(0.5%CMC-Na)、曼陀罗子提取物组(1.55、3.10、6.20 g生药/kg)、生品组(3.1 g生药/kg)、成品组(2 g生药/kg),每组30只,♀♂各半。每组以1 ml/100 g体积灌胃给予相应的药物,连续90 d。d 91,动物用乙醚麻醉,每组处死20只(♀♂各半);停药后15 d,每组处死10只(♀♂各半)。检测相关血液学指标。取肝、肾、脑进行电镜检查。再取脑、心、肝等32个脏器,进行光镜检查。
Tab 1 90 days medicine given(¯ ± s,n=10)
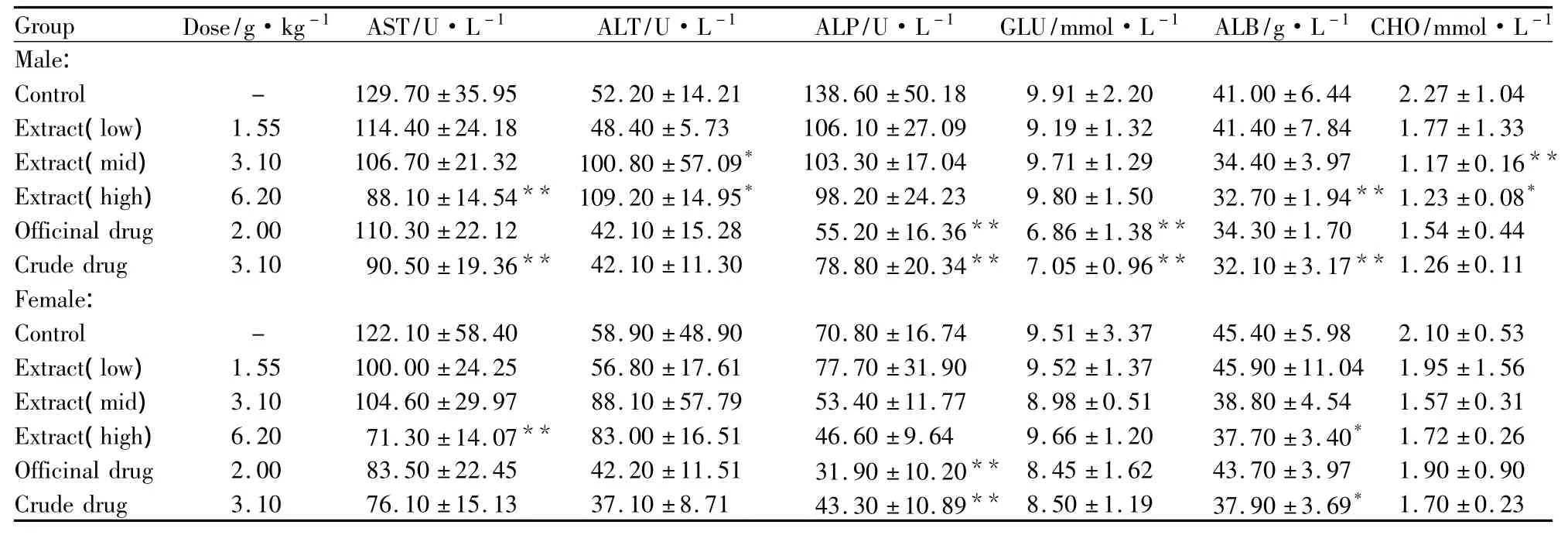
Tab 1 90 days medicine given(¯ ± s,n=10)
*P <0.05,**P <0.01 vs control group
Group Dose/g·kg-1 AST/U·L-1 ALT/U·L-1 ALP/U·L-1 GLU/mmol·L-1 ALB/g·L-1CHO/mmol·L -1 Male :1.70 ±0.23 Control - 129.70 ±35.95 52.20 ±14.21 138.60 ±50.18 9.91 ±2.20 41.00 ±6.44 2.27 ±1.04 Extract(low) 1.55 114.40 ±24.18 48.40 ±5.73 106.10 ±27.09 9.19 ±1.32 41.40 ±7.84 1.77 ±1.33 Extract(mid) 3.10 106.70 ±21.32 100.80 ±57.09* 103.30 ±17.04 9.71 ±1.29 34.40 ±3.97 1.17 ±0.16**Extract(high) 6.20 88.10 ±14.54** 109.20 ±14.95* 98.20 ±24.23 9.80 ±1.50 32.70 ±1.94** 1.23 ±0.08*Officinal drug 2.00 110.30 ±22.12 42.10 ±15.28 55.20 ±16.36** 6.86 ±1.38** 34.30 ±1.70 1.54 ±0.44 Crude drug 3.10 90.50 ±19.36** 42.10 ±11.30 78.80 ±20.34** 7.05 ±0.96** 32.10 ±3.17** 1.26 ±0.11 Female:Control - 122.10 ±58.40 58.90 ±48.90 70.80 ±16.74 9.51 ±3.37 45.40 ±5.98 2.10 ±0.53 Extract(low) 1.55 100.00 ±24.25 56.80 ±17.61 77.70 ±31.90 9.52 ±1.37 45.90 ±11.04 1.95 ±1.56 Extract(mid) 3.10 104.60 ±29.97 88.10 ±57.79 53.40 ±11.77 8.98 ±0.51 38.80 ±4.54 1.57 ±0.31 Extract(high) 6.20 71.30 ±14.07** 83.00 ±16.51 46.60 ±9.64 9.66 ±1.20 37.70 ±3.40* 1.72 ±0.26 Officinal drug 2.00 83.50 ±22.45 42.20 ±11.51 31.90 ±10.20** 8.45 ±1.62 43.70 ±3.97 1.90 ±0.90 Crude drug 3.10 76.10 ±15.13 37.10 ±8.71 43.30 ±10.89** 8.50 ±1.19 37.90 ±3.69*
Tab 215 days after the medicine withdraw(¯±s,n=5)
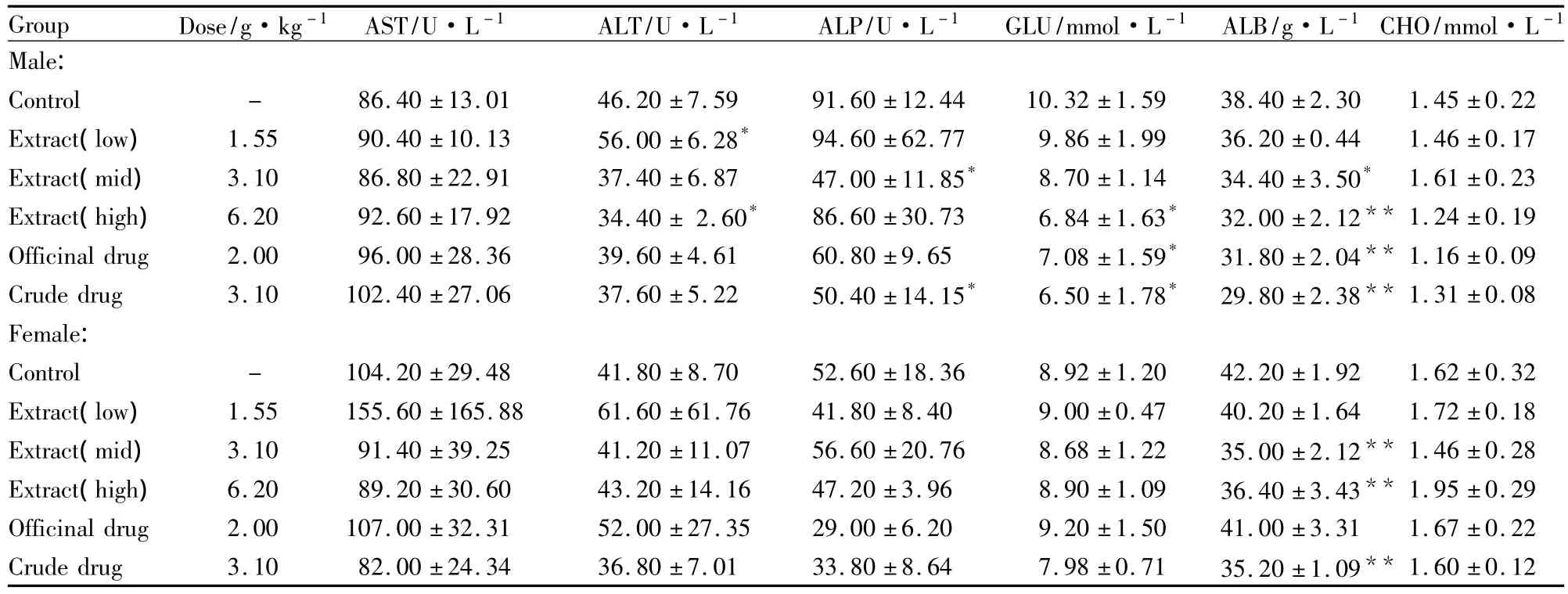
Tab 215 days after the medicine withdraw(¯±s,n=5)
*P <0.05,**P <0.01 vs control group
Group Dose/g·kg-1 AST/U·L-1 ALT/U·L-1 ALP/U·L-1 GLU/mmol·L-1 ALB/g·L-1CHO/mmol·L -1 Male :Control - 86.40 ±13.01 46.20 ±7.59 91.60 ±12.44 10.32 ±1.59 38.40 ±2.30 1.45 ±0.22 Extract(low) 1.55 90.40 ±10.13 56.00 ±6.28* 94.60 ±62.77 9.86 ±1.99 36.20 ±0.44 1.46 ±0.17 Extract(mid) 3.10 86.80 ±22.91 37.40 ±6.87 47.00 ±11.85* 8.70 ±1.14 34.40 ±3.50* 1.61 ±0.23 Extract(high) 6.20 92.60 ±17.92 34.40 ± 2.60* 86.60 ±30.73 6.84 ±1.63* 32.00 ±2.12** 1.24 ±0.19 Officinal drug 2.00 96.00 ±28.36 39.60 ±4.61 60.80 ±9.65 7.08 ±1.59* 31.80 ±2.04** 1.16 ±0.09 Crude drug 3.10 102.40 ±27.06 37.60 ±5.22 50.40 ±14.15* 6.50 ±1.78* 29.80 ±2.38** 1.31 ±0.08 Female:Control - 104.20 ±29.48 41.80 ±8.70 52.60 ±18.36 8.92 ±1.20 42.20 ±1.92 1.62 ±0.32 Extract(low) 1.55 155.60 ±165.88 61.60 ±61.76 41.80 ±8.40 9.00 ±0.47 40.20 ±1.64 1.72 ±0.18 Extract(mid) 3.10 91.40 ±39.25 41.20 ±11.07 56.60 ±20.76 8.68 ±1.22 35.00 ±2.12** 1.46 ±0.28 Extract(high) 6.20 89.20 ±30.60 43.20 ±14.16 47.20 ±3.96 8.90 ±1.09 36.40 ±3.43** 1.95 ±0.29 Officinal drug 2.00 107.00 ±32.31 52.00 ±27.35 29.00 ±6.20 9.20 ±1.50 41.00 ±3.31 1.67 ±0.22 Crude drug 3.10 82.00 ±24.34 36.80 ±7.01 33.80 ±8.64 7.98 ±0.71 35.20 ±1.09**1.60 ±0.12
2 结果
2.1 血生化结果 见Tab 1~2。
2.2 血细胞、电解质及凝血酶原时间结果 与对照组比较,未见明显异常。
2.3 组织病理学结果 与对照组比较,生品组全部动物、成品组和提取物组(6.20 g生药/kg)部分动物肝脏电镜检查发现脂滴略有增多、毛细胆管略有扩张,腔内有少量胆汁淤滞。
3 讨论
实验结果表明:提取物组(6.20 g生药/kg)降低ALB,生品组降低ALB、ALP,但不可逆。提取物组(3.10 g生药/kg)升高 ALT、HGB,提取物组(6.20 g生药/kg)升高 CK、TG、ALT,成品组降低ALP和升高HGB,生品组升高HGB有可逆性。电镜检查发现药物性肝损伤的病理改变。
曼陀罗子[4-5],维吾尔药物名衣提洋克欧如合,是茄科植物曼陀罗Datura stramonium L.的干燥成熟种子。药性4级干寒,有毒。维吾尔医学认为,人体各器官均有与自己功能相应的特有气质,如肝脏气质为湿热;因此,曼陀罗子以干寒气质来干预正常肝脏气质,从而影响肝脏正常功能,这与本实验结果相符。
[1] 袁伯俊,缪明阳,李 波.药物毒理学实验方法与技术[M].化学工业出版社,2007,1:200 -10.
[1] Yuan B J,Liao M Y,Li B.Drug Toxicological Method and Technic[M].Publishing House of Chemical Industry,2007,1:200 -10.
[2] 徐叔云,卞如濂,陈 修.药理实验方法学[M].第3版.北京:人民卫生出版社,2003:226-9.
[2] Xu S Y,Bian R L,Chen Xiu.Pharmacological Method(Third edition)[M].3rd ed.Beijing:Publishing House of Public Health,2003:226-9.
[3] 谢秀琼.中药新制剂开发与应用[M].北京:人民卫生出版社,2002:527 -35.
[3] Xie X Q.Chinese medicine for new agents in Development and application[M].Beijing:Publishing House of public health,2002:527-35.
[4] 易沙克江·马合穆德.中国医学百科全书-维吾尔医学[M].上海:上海科学技术出版社,2005:302-3.
[4] Iksakjan Mahmut.Encyclopedia of Chinese Medicine-Uyghur Medicine[M].Shanghai:Publishing House of Science Technology of Shanghai,2005:302 -3.
[5] 伊德力斯·巴克.中华人民共和国卫生部药品标准-维吾尔药分册[M].乌鲁木齐:新疆科技卫生出版社(W),1999:95.
[5] Idris Baki.Medical standard of the People’s Republic of China-Uyghur medicine[M].Urumqi:Technology Medical Publishing House of Xinjiang,1995:95.
