含氧燃料燃烧中燃料氧迁移路径及含氧中间体生成特性
2011-11-30张立志赵黛青蒋利桥杨玖重王占东金汉锋
张立志 高 健 赵黛青,* 蒋利桥 杨玖重 王占东 金汉锋
(1中国科学院广州能源研究所,广州510640;2中国科学技术大学国家同步辐射实验室,合肥230029;
3中国科学院可再生能源与天然气水合物院重点实验室,广州510640;4中国科学院研究生院,北京100049)
含氧燃料燃烧中燃料氧迁移路径及含氧中间体生成特性
张立志1,3,4高 健1,3赵黛青1,3,*蒋利桥1,3杨玖重2王占东2金汉锋2
(1中国科学院广州能源研究所,广州510640;2中国科学技术大学国家同步辐射实验室,合肥230029;
3中国科学院可再生能源与天然气水合物院重点实验室,广州510640;4中国科学院研究生院,北京100049)
与碳氢燃料相比,含氧燃料在燃烧过程中容易生成醛类等非常规污染物,这些含氧中间体的生成与燃料中氧的释放密切相关.本文从燃料氧迁移路径的角度来研究含氧中间体的生成特性及规律.并采用分子束质谱结合真空紫外同步辐射光电离技术(SVUV-PIMS)探测了丙烷、二甲醚、乙醇三种低压预混火焰中的主要含氧中间体,并获得了其摩尔分数分布.结果表明:与外部氧相比,燃料氧更易形成含氧中间体.生成的最主要的含氧中间体取决于燃料氧在分子中的结构.二甲醚火焰中甲醛为最主要的含氧中间体;乙醇火焰中乙醛为最主要的含氧中间体;丙烷火焰中,甲醛和乙醛的含量均很小,但碳氢中间体乙烯、乙炔和丙烯的含量较高.
含氧燃料; 非常规污染物;燃料氧;迁移路径;同步辐射
1 引言
柴油等传统的碳氢燃料在燃烧过程中容易生成碳黑.这些碳黑大部分属于直径小于2.5 μm的微细颗粒物,能够穿过人体呼吸系统进入体内而致病.在柴油发动机中添加含氧燃料成为减少碳黑排放的有效方法.1-5然而这又带来了新的问题,即这些含氧燃料在燃烧过程中会有非常规污染物生成,如甲醛、乙醛、甲酸、甲酸甲酯、丙酮等.6-11其中,醛类污染物属于高危化学物质,人体少量吸入足可以致命.此外,它们在大气中容易转化为硝酸过氧化乙脂(PAN)和硝酸过氧化丙脂(PPN)等二次污染物,导致光化学烟雾,还会导致大气中有机气溶胶浓度增加.12,13鉴于非常规污染物潜在的危害性,有必要给予足够的重视.
研究非常规污染物形成机理能够为降低其生成与排放提供理论指导.Xu等14采用分子束质谱结合真空紫外同步辐射光电离技术(SVUV-PIMS)探测了乙醇和二甲醚低压预混火焰中的C1-C3类主要中间体,含氧的主要中间体包括甲醛、甲醇、乙烯醇、乙醛、丙酮等.Wang15和Frassoldati16等也采用该燃烧诊断技术研究了在丙烯火焰中添加乙醇和二甲醚时,其甲醛、乙醛等含氧污染物的生成规律.他们的研究表明,二甲醚趋向于生成甲醛,而乙醇趋向于生成乙醛.我们注意到非常规污染物具有共同的特点,即其化学组成中都含有氧元素.因此,我们认为非常规污染物的形成与燃料中的氧元素密切相关.本文从燃料氧迁移路径的角度来研究燃料氧和非常规污染物形成的相互关系.含氧燃料种类很多,我们选择二甲醚(CH3OCH3)、乙醇(CH3CH2OH)以及碳氢燃料丙烷(CH3CH2CH3)作为研究对象,这主要基于以下考虑: (1)它们具有相似的化学结构.丙烷为C3类饱和碳氢燃料,在其分子结构中,中间CH2被O取代成为二甲醚,其侧翼的CH2被O取代成为乙醇,因此可以对比研究氧元素的作用.二甲醚和乙醇互为同分异构体,可以研究由于氧原子位置不同导致的差异.(2)目前丙烷、二甲醚、乙醇等含氧替代燃料的化学反应动力学机理发展已经比较完善,可以用来分析氧元素的迁移路径及非常规污染物形成过程.(3)丙烷为液化石油气(LPG)的主要成分,二甲醚和乙醇更是备受瞩目的含氧替代燃料,因此具有代表性.
首先,我们采用分子束质谱结合真空紫外同步辐射光电离技术17-19分别确认了丙烷、二甲醚、乙醇这三种燃料的低压预混火焰中的主要中间体构成.将实验获得的燃烧组分浓度分布和数值模拟的结果进行对比,在此基础上对燃料氧迁移路径及其对醛类非常规污染物形成的作用机制进行讨论.
2 实验方法
本文的实验部分是在中国科学技术大学国家同步辐射实验室燃烧火焰实验站进行.实验装置主要由燃烧室、差分室、电离室和反射式飞行时间质谱仪5部分组成.燃料、氧气、氩气通过质量流量控制器精确控制,混合后进入直径为60 mm的燃烧炉形成层流预混火焰.通过控制步进马达实现燃烧器在火焰传播方向上的移动,改变火焰与取样喷嘴的相对位置,从而探测火焰中物种的空间摩尔分布.燃烧室压力通过节流阀来调节,其压力稳定在4000 Pa.燃烧装置详细介绍见文献20.丙烷火焰中,丙烷、氧气、氩气流量分别0.463、1.278、0.75 L·min-1,冷气流速为37.44 cm·s-1.二甲醚或乙醇火焰中,二甲醚或乙醇、氧气、氩气流量分别0.429、1.286、1.286 L·min-1,冷气流速为44.67 cm·s-1.此外,火焰温度通过Pt/ Pt-13%Rh热电偶来测得.
实验主要分为两个部分:一是固定燃烧炉的位置,扫描光子能量,得到不同质荷比的离子信号强度随光子能量的变化曲线,即光电离效率谱(PIE),通过光电离效率谱得到分子的电离能,与文献21中电离能相比较以确定物种成分,详细方法介绍见文献.二是固定光子能量,扫描燃烧炉的位置,得到火焰中各物种成分的空间摩尔分数分布曲线.实验中测得火焰中各物种的光电离信号强度,应用文献22中的方法根据光电离信号强度计算出各物种在各位置的摩尔分数.
3 计算方法
在计算中,采用实验测得的火焰温度分布,因此不需要求解能量方程.为了补偿热电偶对流场的压缩效应以及石英喷嘴对火焰的冷却效应,23将火焰温度曲线朝远离炉子的方向移动了3 mm.通过求解组分方程可获得各组分浓度分布:
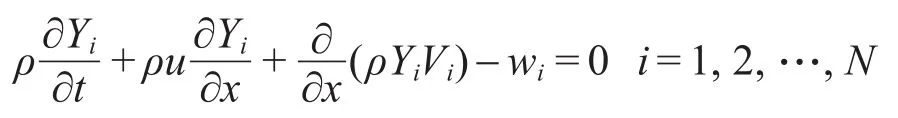
其中ρ为密度;u为沿x方向的速度;t为时间;Yi,Vi和wi分别为质量分数,扩散速度和质量生成率.本文采用时间推进法求解;微分方程组采用控制体积法进行离散;速度和压力的耦合采用SIMPLE方法;24扩散项采用中心差分格式;对流项采用QUICK格式;采用TDMA和低松弛因子进行迭代.计算长度选取为30 mm,沿流动方向划分为200个非均匀网格;计算的时间步长为1.0×10-5s;收敛准则为残差小于1.0×10-5.详细的计算方法描述可以参考文献25,26.
二甲醚采用美国劳伦斯国家实验室(LLNL) Curran等27-29提出的DME-2000化学反应动力学机理,包含79种组分,351步基元反应.乙醇采用LLNL实验室的Marinov等30提出的化学反应动力学机理,包括58种组分和383步基元反应.丙烷采用Qin等31提出的C3机理,包括70种组分和463步基元反应.热力学和输运参数等数据可以在LLNL实验室相关网站32上获得,其中输运参数采用多组分的Smooke简化模型33进行计算.
4 结果与讨论
4.1 火焰物种的浓度分布
通过高能扫描(16.64 eV),首先得到了火焰中的主要物种.主要物种是指反应物以及摩尔分数达到10-2量级的在燃后区仍然存在的产物,包括燃料、氧气、不参与反应的氩气以及主要产物(CO2、CO、H2O、H2).由于主要物种的浓度较高,关系到实验数据的元素平衡以及火焰中间体分布的精确度,因此对主要物种的测量影响到整个火焰物种的浓度分布精确性.图1给出了主要物种的实验测量以及数值模拟结果对比.可以看出,计算预测和实验测量吻合良好,其结果令人满意.
通过扫描PIE,我们探测到了主要的火焰中间体,包括甲基、甲烷、乙炔、乙烯、丙炔、丙烯、苯等碳氢中间体,以及甲醛、乙醛等含氧中间体,这与文献22,34中的结果一致.图2给出了丙烷火焰中C1-C4物种和苯的摩尔分数分布,并与模拟结果进行了对比.受到光电离截面误差的影响,实验测量的误差系数为2,即可信结果在实验结果50%到200%范围内.从图中可以看出,模拟的峰值基本在实验测量的误差范围之内,而出现峰值的位置也与实验的结果比较吻合,这表明数值计算所采用的动力学模型能够很好地反映火焰中间产物的形成规律.
4.2 燃料氧迁移路径
注意到含氧燃料燃烧过程中生成的非常规污染物的化学组成中含有氧元素,非常规污染物的形成可能与燃料中的氧元素相关.下面将从燃料氧迁移路径的角度来研究燃料氧和非常规污染物形成的相互关系.
4.2.1 二甲醚的燃料氧迁移路径
燃料氧源自燃料,因此分析燃料的消耗途径是获得燃料氧迁移路径的第一步.图3显示了二甲醚生成速率.根据二甲醚对称性的分子结构,二甲醚消耗通过两种方式进行,即C-O键断裂(R1)和C-H键断裂(R2、R3、R4).

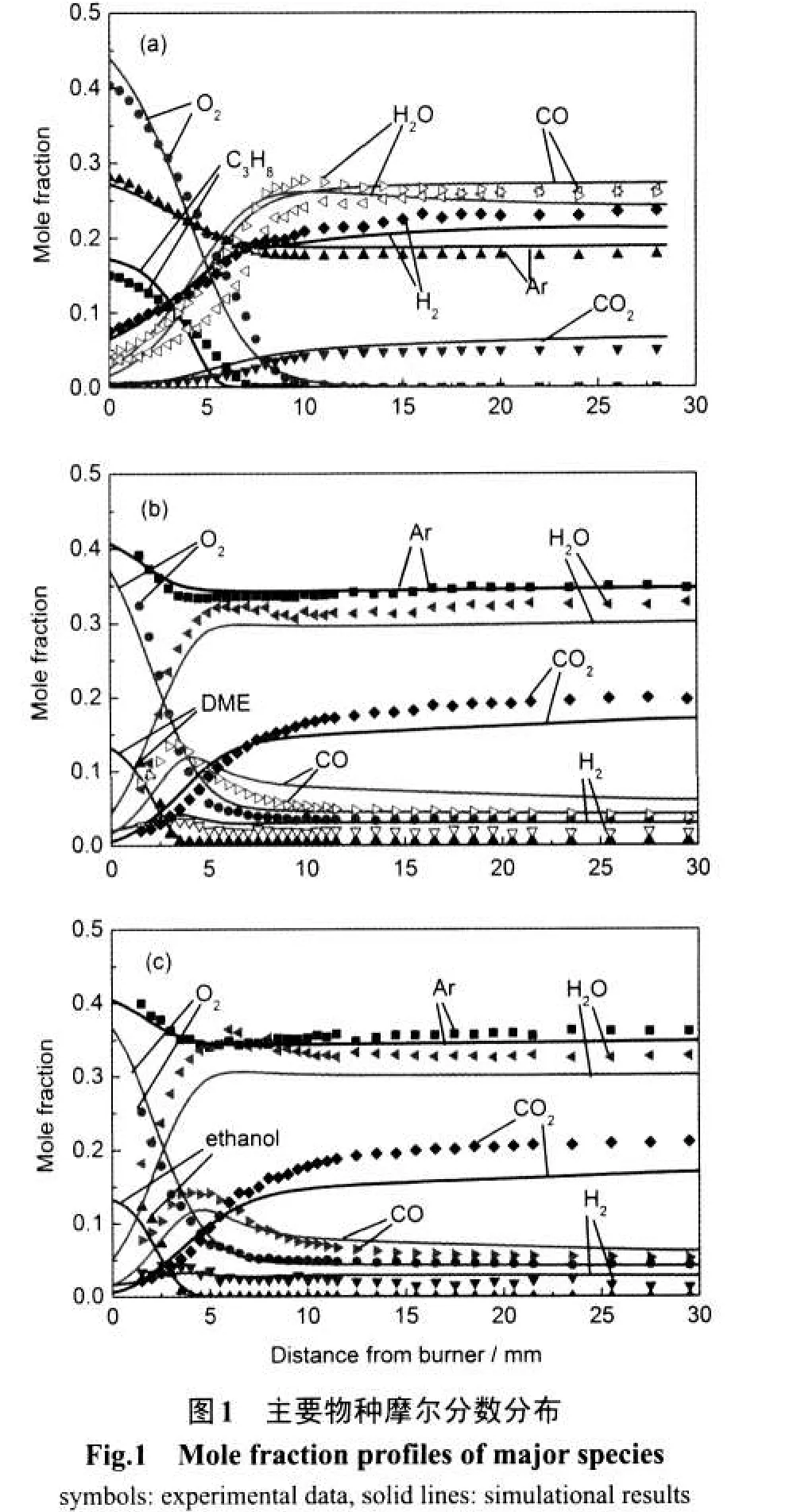

图2 丙烷火焰中主要中间体的摩尔分数分布Fig.2 Mole fraction profiles of intermediates in the premixed propane flamesymbols:experimental data,solid lines:simulated results
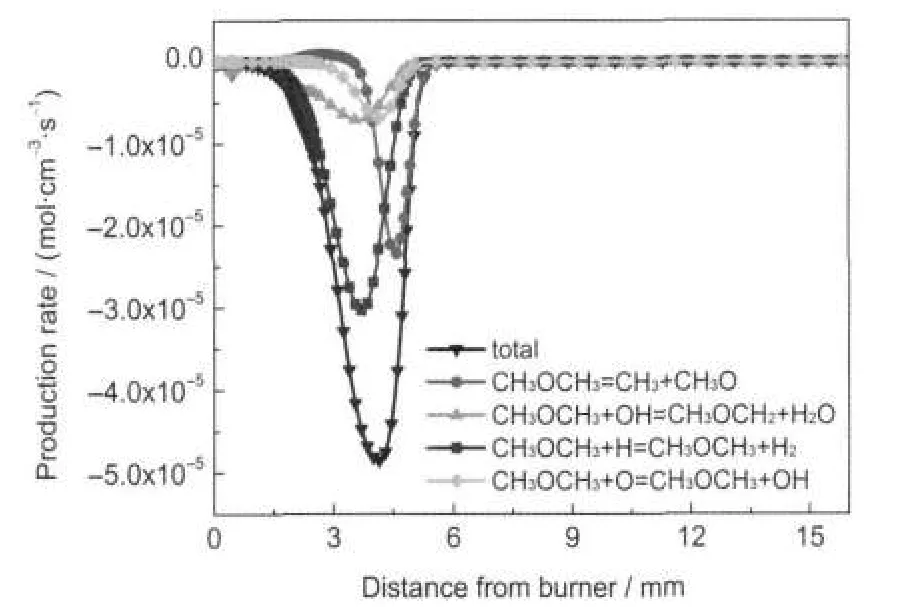
图3 二甲醚的生成速率Fig.3 Production rate of dimethyl ether


根据生成速率分析,其中19.8%的燃料氧进入了CH3O中,80.2%的燃料氧进入了CH3OCH2中.通过进一步跟踪CH3O和CH3OCH2的消耗途径,可以获得燃料氧的下一步走向,最后得到了燃料氧总的迁移路径如图4所示.燃料氧通过三种不同的路径汇集于甲醛(HCHO),然后连续两步脱氢转化为CO.可以看出,燃料氧和其中一个碳原子紧密结合直到生成CO,因此二甲醚燃烧的终产物H2O中不含有燃料氧.

图5 乙醇火焰中燃料氧迁移路径Fig.5 Migration pathway of oxygen from fuel in the premixed ethanol flame
4.2.2 乙醇的燃料氧迁移路径
乙醇与二甲醚互为同分异构体,具有非对称性分子结构,其消耗途径共有6种,如图5所示.一部分燃料氧进入H2O中,占总的燃料氧的47.4%;一部分进入乙醛(CH3CHO)中,占31.5%;一部分进入甲醛中,占21.1%.甲醛和乙醛中的燃料氧进一步转化到CO中.与二甲醚不同,乙醇燃烧的终产物H2O中含有燃料氧.
4.3 丙烷反应路径
丙烷本身不含氧,其燃烧过程是通过外部氧(来自氧化剂)的作用来进行的.因此分析丙烷的反应路径有助于理解外部氧和内部氧(即燃料氧)在燃烧过程中作用方式的异同.图6为丙烷的反应路径(碳反应流).可以看出,丙烷通过各级脱氢以及C-C键断裂形成CH3、C2H3和C2H2这三种碳氢中间体.这三种中间体可以通过外部氧的氧化转化为HCHO、HCO和HCCO等含氧中间体,并进一步生成CO.可以看出,通过外部氧的作用也能形成甲醛等含氧中间体.
4.4 燃料氧和外部氧的作用

图6 丙烷火焰中反应路径Fig.6 Reaction flux in the premixed propane flame

图7 甲醛和乙醛的摩尔分数分布Fig.7 Mole fraction profiles of formaldehyde and acetaldehyde
从以上分析可以看出,甲醛和乙醛等含氧中间体为反应路径的重要汇聚点,是燃料氧化生成CO的主要中间产物.图7给出了二甲醚、乙醇和丙烷三种火焰中甲醛和乙醛的摩尔分数分布.丙烷分子中CH2被O取代成为二甲醚或乙醇.相应地,乙烯(C2H4)和丙烯(C3H6)中的CH2被O取代成为甲醛和乙醛.因此图7中也给出了丙烷火焰中乙烯和丙烯的分布,其目的是对比性的研究燃料氧的作用.一般认为,乙炔(C2H2)在多环芳香烃(PAH)和碳烟(soot)的生长中起到关键性作用,是碳烟形成的前驱体.图8为乙炔的摩尔分数分布,用来对比考察含氧燃料和碳氢燃料中碳烟前驱体形成的难易程度.从图7、8中可以看出,二甲醚火焰中甲醛摩尔分数峰值明显高于其他两种火焰,乙醇火焰中乙醛摩尔分数峰值明显高于其他两种火焰.而丙烷火焰中,甲醛和乙醛的含量均很小,但其对应的碳氢中间组分如乙烯、乙炔和丙烯的含量极高.这表明含氧燃料较碳氢燃料不易形成碳烟,这与在碳氢燃料中添加含氧燃料能降低碳烟生成这一规律相一致.

图8 乙炔的摩尔分数分布Fig.8 Mole fraction profiles of ethyne

图9 甲醛、乙醛分子中来自燃料的氧和来自外部氧化剂的氧所占的百分比构成Fig.9 Percentages of oxygen from fuel and from oxidizerin formaldehyde and acetaldehyde(a)dimethyl ether flame;(b)ethanol flame
含氧燃料燃烧过程中含氧中间体的大量生成可以通过燃料氧和外部氧的贡献程度不同来理解.图9为甲醛和乙醛中氧元素的构成.在二甲醚火焰中,甲醛的燃料氧占75.8%,而外部氧只占24.2%.在乙醇火焰中,乙醛的燃料氧占98.31%,空气氧仅为1.7%.因此,与外部氧相比,燃料氧更易形成相应的含氧中间体.二甲醚没有C-C键,主要含氧中间体为甲醛;乙醇含有C-C键,主要含氧中间体为乙醛,这表明主要含氧中间体的形成还与燃料氧在分子中的结构有关.对于丙烷火焰,含氧中间体来源单一,即外部氧的氧化.而外部氧化生成含氧中间体的速率不及燃料氧脱氢或裂解生成含氧中间体的速率,待氧化的碳氢中间体在火焰中累积到较高的浓度,反应区域也较含氧燃料离炉子出口更远(见图7、8).
5 结论
通过实验和数值计算的手段研究了丙烷、二甲醚、乙醇三种燃料的预混火焰中的含氧中间体的形成规律,并从燃料氧迁移路径的角度阐明了燃料氧和非常规污染物形成的相互关系,得到了如下结论.
(1)火焰中主要的碳氢中间体包括甲基、甲烷、乙炔、乙烯、丙炔、丙烯、苯等;甲醛、乙醛为主要的含氧中间体.
(2)二甲醚火焰中,燃料氧通过三种不同的路径汇集于甲醛,最后转化为一氧化碳.乙醇火焰中,一部分燃料氧进入水中,一部分汇集于甲醛和乙醛,最后转化为一氧化碳.
(3)二甲醚火焰中甲醛摩尔分数明显高于其他两种火焰,乙醇火焰中乙醛摩尔分数明显高于其他两种火焰.而丙烷火焰中,甲醛和乙醛的含量均很小,但其对应的碳氢中间体乙烯、乙炔和丙烯的含量极高.
(4)与外部氧相比,燃料氧更易形成相应的含氧中间体.燃料氧也会降低碳氢中间体的生成.主要含氧中间体的种类与燃料氧在分子中的结构有关.
致谢: 本工作得到中国科学技术大学国家同步辐射实验室资助.感谢国家同步辐射实验室燃烧与火焰实验站齐飞教授、李玉阳博士对本实验工作的支持和指导.
(1)Natarajan,M.;Frame,E.A.;Naegeli,D.W.;Asmus,T.;Clark, W.;Garbak,J.;Manuel,A.;Gonzalez,D.;Liney,E.;Piel,W.; Wallace,J.P.Oxygenates forAdvanced Petroleum-Based Diesel Fuels:Part 1.Screening and Selection Methodology for the Oxygenates.In Oxygenated Fuels,SAE International Fall Fuels&Lubricants Meeting&Exhibition,SanAntonio,TX, USA,September,2001;SAE paper,2001-01-3631.
(2)Zannis,T.C.;Hountalas,D.T.;Kouremenos,D.A.Experimental Investigation to Specify the Effect of OxygenatedAdditive Content and Type on DI Diesel Engine Performance and Emissions.In CI Engine Performance for Use with Alternate Fuels,SAE 2004 World Congress&Exhibition,Detroit,MI, USA,March,2004;SAE paper,2004-01-0097.
(3)Manuel,A.;Gonzalez,D.;Piel,W.;Asmus,T.;Clark,W.; Garbak,J.;Liney,E.;Natarajan,M.;Naegeli,D.W.;Yost,D.; Frame,E.A.;Wallace,J.P.Oxygenates screening forAdvanced Petroleum-Based Diesel Fuels:Part 2.The Effect of Oxygenate Blending Compounds on Exhaust Emissions.In Oxygenated Fuels,SAE International Fall Fuels&Lubricants Meeting& Exhibition,SanAntonio,TX,USA,September,2001;SAE paper,2001-01-3632.
(4) McCormick,R.L.;Ross,J.D.;Graboski,M.S.Environ.Sci. Technol.1997,31,1144.
(5) Litzinger,T.Stoner,M.;Hess,H.Int.J.Engine.Res.2001,1,57.
(6)Chao,H.R.;Lin,T.C.;Chao,M.R.J.Hazard.Mater.2000,13, 39.
(7) Poulopoulos,S.G.;Samaras,D.P.;Philippopouos,C.J.Atmos. Environ.2001,35,4399.
(8)Zhang,Y.S.;Lang,J.;Mo,C.L.;Sun,H.Y.;Wu,H.W. Transactions of CSICE 2008,26,36.[张煜盛,郎 静,莫春兰,孙海英,吴宏伟.内燃机学报,2008,26,36.]
(9)Zhao,D.Q.;Zeng,T.;Jiang,L.Q.;Wang,X.H.;Yang,W.B.; Zeng,X.J.Chinese Journal of Environmental Engineering 2008,2,395.[赵黛青,曾 涛,蒋利桥,汪小憨,杨卫斌,曾小军.环境工程学报,2008,2,395.]
(10)Lang,J.;Zhang,Y.S.;Zhou,X.S.;Wu,H.W.Journal of Chongqing University 2008,7,284.
(11) Schifter,I.;Diaz,L.;Rodriguez,R.;Salazar,L.Fuel 2011,90, 779.
(12)Kalberer,M.;Paulsen,D.;Sax,M.;Steinbacher,M.;Dommen, J.;Prevot,A.S.H.;Fisseha,R.;Weingartner,E.;Frankevich,V.; Zenobi,R.;Baltensperger,U.Science 2004,303,1659.
(13) Grosjean,E.;Grosjean,D.;Woodhouse,L.F.;Yang,Y.J.Atmos. Environ.2002,36,2405.
(14)Xu,H.;Yao,C.D.;Yuan,T.;Zhang,K.W.;Guo,H.J.Combust. Flame.DOI:10.1016/j.combustflame.2011.01.004.
(15) Wang,J.;Struckmeier,U.;Yang,B.;Cool,T.A.;Osswald,P.; Kohse-Hoeinghaus,K.;Kasper,T.;Hansen,N.;Westmoreland, P.R.J.Phys.Chem.A 2008,112,9255.
(16) Frassoldati,A.;Faravelli,T.;Ranzi,E.;Kohse-Höinghaus,K.; Westmoreland,P.R.Combust.Flame DOI:10.1016/ j.combustflame.2010.12.015.
(17) Cool,T.A.;Nakajima,K.;Mostefaoui,T.A.;Qi,F.;Mcllroy, A.;Westmoreland,P.R.;Law,M.E.;Poisson,L.;Peterka,D. S.;Ahmed,M.J.Chem.Phys.2003,119,8356.
(18) Werner,J.H.;Cool,T.A.Proc.Combust.Inst.1998,27,413.
(19) McIlroy,A.;Hain,T.D.;Michelsen,H.A.;Cool,T.A.Proc. Combust.Inst.2000,28,1647.
(20)Qi,F.;Yang,R.;Yang,B.;Huang,C.Q.;Wei,L.X.;Wang,J.; Sheng,L.S.;Zhang,Y.W.Rev.Sci.Instrurr.2006,77,084101
(21) Li,Y.Y.;Yuan,T.;Zhang,K.W.;Yang,J.Z.;Qi,F.Journal of Engineering Thermophysics 2010,31,535.[李玉阳,袁 涛,张奎文,杨玖重,齐 飞.工程热物理学报,2010,31,535.]
(22) Cool,T.A.;Nakajima,K.;Taatjes,C.A.;McIlroy,A.; Westmoreland,P.R.;Law,M.E.;Morel,A.Proc.Combust. Inst.2005,30,1681.
(23)Hartlieb,A.T.;Atakan,B.;Hohse-Hoinghaus,K.Combust. Flame 2000,121,610.
(24) Patanker,S.V.;Spalding,D.B.Int.J.Heat Mass Transf.1972, 15,1787.
(25) Yamashita,H.JSME Int.J.Ser.B-Fluids Therm.Eng.2000,43, 97.
(26)Zhao,D.Q.;Yamashita,H.Combust.Flame 2002,130,352.
(27) Curran,H.J.;Pitz,W.J.;Westbrook,C.K.Int.J.Chem.Kinet. 1998,30,229.
(28) Fischer,S.L.;Dryer,F.L.;Curran,H.J.Int.J.Chem.Kinet. 2000,32,714.
(29) Curran,H.J.;Fischer,S.L.;Dryer,F.L.Int.J.Chem.Kinet. 2000,32,741.
(30) Marinov,N.M.Int.J.Chem.Kinet.1999,31,183.
(31) Qin,Z.W.;Lissianski,W.;Yang,H.X.;Gardiner,W.C.;Davis, S.G.;Wang,H.Proc.Combust.Inst.2000,28,1663.
(32) https://www-pls.llnl.gov/?url=science_and_technologychemistry-combustion
(33)Smooke,M.D.Reduced Kinetic Mechanisms and Asymptotic Approximations for Methane-Air Flames;SpringerVerlag: Berlin,Germany,1991;pp 1-28.
(34) Gao,J.;Zhao,D.Q.;Wang,X.H.;Jiang,L.Q.;Yang,H.L.; Yuan,T.;Yang,J.Z.Acta Phys.-Chim.Sin.2010,26,23. [高 健,赵黛青,汪小憨,蒋利桥,杨浩林,袁 涛,杨玖重.物理化学学报,2010,26,23.]
March 29,2011;Revised:May 4,2011;Published on Web:May 16,2011.
Migration Pathways of Oxygen and the Formation of Oxygenated Intermediates in Oxygenated Fuel Combustion
ZHANG Li-Zhi1,3,4GAO Jian1,3ZHAO Dai-Qing1,3,*JIANG Li-Qiao1,3YANG Jiu-Zhong2WANG Zhan-Dong2JIN Han-Feng2(1Guangzhou Institute of Energy Conversion,Chinese Academy of Sciences,Guangzhou 510640,P.R.China;2National Synchrotron Radiation Laboratory,University of Science and Technology of China,Hefei 230029,P.R.China;3Key Laboratory of Renewable Energy and Gas Hydrate,Chinese Academy of Sciences,Guangzhou 510640,P.R.China;4Graduate University of Chinese Academy of Sciences,Beijing 100049,P.R.China)
The combustion of oxygenated fuel produces more non-regulated pollutants which usually contain oxygen such as aldehydes than the combustion of hydrocarbon fuel.The formation of these oxygenated intermediates may be associated with the release of oxygen from the oxygenated fuel.In this paper,migration pathways of oxygen from several oxygenated fuels were investigated to obtain the formation characteristics of oxygenated intermediates.Major oxygenated intermediates and other intermediates were identified using synchrotron vacuum ultraviolet photoionization mass spectrometry in a dimethyl ether flame,an ethanol flame,and a propane flame.Their mole fractions were also evaluated. The results indicate that the oxygen from oxygenated fuel leads to an easier production of oxygenated intermediates,compared with oxygen from the oxidizer.The major oxygenated intermediate depends on the structure of the oxygenated fuel and was found to be formaldehyde in the dimethyl ether flame,and acetaldehyde in the ethanol flame.However,formaldehyde and acetaldehyde are present in low concentrations while hydrocarbon intermediates,such as ethene,ethyne,and propene,are present in high concentrations in the propane flame.
Oxygenated fuel;Non-regulated pollutant;Oxygen from oxygenated fuel; Migration pathway;Synchrotron photoionization
O643
*Corresponding author.Email:zhaodq@ms.giec.ac.cn;Tel:+86-20-87057765.
The project was supported by the National Natural Science Foundation of China(50806079)and Natural Science Foundation of Guangdong Province,China(8151007006000014).
国家自然科学基金(50806079)和广东省自然科学基金(8151007006000014)资助项目
