化香树果序总黄酮提取动力学研究
2011-11-30李稳宏廉媛媛李学坤朱骤海
李 冬,李稳宏*,廉媛媛,高 蓉,李学坤,朱骤海
1西北大学化工学院,西安710069;2陕西地矿医院药剂科,西安710014;3第四军医大学化学系,西安710032
化香树果序总黄酮提取动力学研究
李 冬1,李稳宏1*,廉媛媛2,高 蓉3,李学坤1,朱骤海1
1西北大学化工学院,西安710069;2陕西地矿医院药剂科,西安710014;3第四军医大学化学系,西安710032
以化香树果序为原料,60%的乙醇水溶液为溶剂提取黄酮类化合物,在不同温度下对总黄酮的传质动力学进行了研究。采用平板模型,以Fick第二定律为基础,建立了化香树果序总黄酮提取的动力学方程,求得了速率常数、活化能、相对萃余率等一系列动力学参数。研究结果可为化香树果序总黄酮提取工程放大和深入理论研究提供一定的依据。
化香树果序;总黄酮;提取;动力学
化香树果序是化香树的干燥果序,具有清热解毒、活血化瘀、清肿排脓、通窍止痛的功效[1]。黄酮类化合物具有抗菌、消炎、抗突变、降压、清热解毒、镇静、利尿、抗氧化、抗癌防癌、抑制脂肪氧化酶等多种生物活性。其显著的生物活性对于研究化香树果序治疗鼻炎鼻塞有较大的价值[2-5]。目前,尚无化香树果序黄酮提取动力学方面的报道。本文以Fick第二定律为基础,建立化香树果序总黄酮提取的动力学模型,并依此对速率常数和相对萃余率等一系列动力学参数进行求解,以求为化香树果序提取工业化放大和深入理论研究提供一定的依据。
1 提取动力学模型的建立
天然产物有效成分的提取过程中,往往同时伴随其它成分的浸出,机理较为复杂。但一般包括三个步骤,即:(1)溶剂向固体植物颗粒内部渗透,浸润颗粒并溶解有效成分;(2)被溶解的有效成分以分子形态从植物颗粒内部扩散迁移到固液界面上; (3)有效成分从固液界面向溶剂主体扩散[6]。其中内扩散常被认为是整个提取过程的速率控制步骤[7]。
化香树果序内部的总黄酮浓度随提取时间的增加不断降低,为不稳定扩散过程。为便于分析,本研究中采用平板模型,以单果序叶片为计算对象,现假设:(1)颗粒的厚度是均匀的;(2)有效成分的扩散方向是沿颗粒的厚度方向进行的;(3)萃取开始时刻颗粒内各成分是均匀分布的;(4)颗粒表面的传质阻力忽略不计且在任意取样时间间隔内,有效成分的扩散系数不变;(5)颗粒与溶剂的温度是相同的,且温度是均匀分布的。
由于平板中的扩散在中心面的两侧对称,因此,任意时刻浓度分布在两侧必然对称。将坐标原点取在平板中心,研究半个平板。则根据Fick扩散第二定律,有

将其简化建立控制方程,并确定初始条件和边界条件为

初始条件c(d,0)=c0
式中:t为提取时间,min;d为距平板中心的距离,m;c为提取过程中t时刻颗粒内距平板中心为d处的有效成分质量浓度,%;D为单片化香树果序厚度的一半,m;DS为内扩散系数,m2/min。
定义无量纲浓度c*=(c-c1)/(c0-c1)
将式(2)改写为

初始条件c*(d,0)=1
用分离变量法求解式(3),令无量纲浓度c*(d,t)=X(d)T(t),有
式(4)只有两侧均为常数时才能成立,令该常数为-f2,得到两个常微分方程

它们的通解分别为

代入边界条件式,得到常数C1=0,特征值为

由解的叠加原理,得到无量纲浓度的解
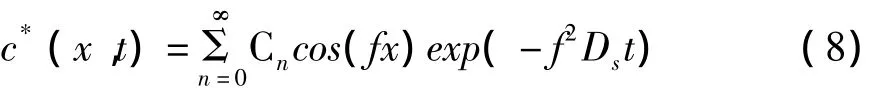
由初始条件,确定常数
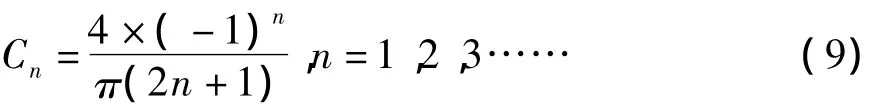
最后,得到无量纲浓度

式(10)表示了忽略表面传质阻力情况下,大平板内有效成分扩散浓度是时间和位置的函数。提取是内扩散控制,有效成分一经扩散到表面,即进入溶液主体,在d=D处,c=C,可把式(10)变为

式中:C0为提取液中溶质的初始质量浓度,%; C∞为提取平衡时提取液中溶质的初始质量浓度,%。非稳态传质的浓度分布式为一无穷级数,一般取第一项计算即可,故

式(13)便是根据Fick第二定律建立的动力学模型。该模型可表达化香树果序颗粒尺寸、提取时间、提取温度和料液比与有效成分提取液浓度之间的关系。
2 材料与方法
2.1 材料
化香树果序由陕西香菊药业集团有限公司提供;芦丁,中国医药(集团)上海化学试剂公司提供;乙醇、亚硝酸钠、硝酸铝、氢氧化钠等试剂均为分析纯。
紫外可见分光光度仪,UV-2501PC,日本岛津公司;电热恒温水浴锅,DK-98-1型,天津市泰斯特仪器有限公司;精密增力电动搅拌器,JJ-1型,常州国华电器有限公司;旋转蒸发仪,RE-52AA型,上海嘉鹏科技公司;分析天平,AL204型,瑞士梅特勒-托利多仪器有限公司。
2.2 试验方法
2.2.1 化香树果序饱和吸溶剂率的测定
精确称取不同质量化香树果序,用滴定管将60%乙醇水溶液滴加,每次滴加后充分振荡并浸润数分钟,使果序充分吸收溶剂,直至充分吸湿且无多余溶剂,记录消耗的溶液体积。则P=(V1-V2)/M,式中:P为饱和吸溶剂率,mL/g;V1为滴定管初读数,mL;V2为滴定管终读数,mL;M为化香树果序质量,g。
2.2.2 提取方法
将厚度为0.25 mm的化香树果序12 g加入500 mL的三口烧瓶中,根据果序的饱和吸溶剂率先用适量的60%乙醇水溶液室温浸润10 min,再立刻向三口烧瓶中加入己加热到设定温度的60%乙醇水溶液至总量200 mL,在此温度下进行常压恒温水浴回流提取,同时在100 rpm下进行搅拌并计时,按试验设计在不同时间间隔定时取样200 μL。
提取时间为:t1=10 min,t2=30 min,t3=60 min,t4=90 min,t5=120 min,t6=150 min,t7=180 min,t8=210 min,t9=240 min,t10=270 min,t11=300 min,t12=360 min;
提取温度为:T1=313 K,T2=323 K,T3=333 K,T4=343 K,T5=353 K。
2.2.3 标准曲线的绘制[8]
精密吸取0.1 mg/mL的芦丁标准品溶液0、1、2、3、4、5 mL置于10 mL容量瓶中,各加入30%乙醇补齐至5 mL,依次分别加入5%NaNO2溶液0.3 mL,静置6 min;10%Al(NO3)3溶液0.3 mL,静置6 min;4%NaOH溶液4 mL;最后用蒸馏水稀释到10 mL并静置20 min。用紫外可见分光光度仪在波长510 nm处测定吸光度,绘制标准曲线,得到回归方程为:C=0.0927A-0.000333,R2=0.9997。
2.2.4 样品浓度测定方法[9]
每次取样后浸提液总体积将减少200 μL,多次取样将导致提取液总体积的减少,同时也造成提取液中有效成分质量的减少。因而,必须对浸提稀释液所测得的浓度进行修正,修正式为:

式中:Cn为第n次取样的浓度修正值,μg/mL; C'n为第n次取样的浓度测定值,μg/mL;n为取样次数,n=l,2,3,……。C'n的测定方法采用2.2.3得到的标准曲线进行换算得到。
3 结果和讨论
3.1 化香树果序饱和吸溶剂率
根据2.2.1的方法得到化香树果序的吸溶剂率P=0.68 mL/g。
3.2 速率常数的求解
不同温度下提取液中总黄酮浓度实验结果见表1。

表1 不同温度下提取液中总黄酮浓度(%)Table 1 Concentration of total flavonoids at different temperature(%)
由表1可以看出,不同浸提温度条件下,总黄酮浓度差异较大,提取温度越高,提取速度越快,提取液浓度越大。当温度为333 K、343 K、353 K时,提取时间达到210 min时,基本达到平衡,温度越低,达到平衡时所需的时间越长。提取时间小于210 min时,达到相同浓度所需时间不同,温度越高,所需时间越短。在提取过程中,提取液浓度在较长时间内基本保持不变,可认为此时己基本达到浸提平衡,该浓度可作为平衡浓度。
利用表1的数据得到ln[C∞/(C∞-C)和提取时间t的关系结果见表2。

表2 不同温度下ln[C∞/(C∞-C)]与t的关系Table 2 Relationship between ln[C∞/(C∞-C)]and t at different temperature

323 ln[C∞/(C∞-C)=0.0125t+1.23390.9941 4.02 2.08 2.85 333 ln[C∞/(C∞-C)=0.015t+1.1431 0.9879 4.26 2.50 2.90 343 ln[C∞/(C∞-C)=0.0173t+1.109 0.9960 4.49 2.88 3.01 353 ln[C∞/(C∞-C)=0.0203t+1.124 0.9846 4.58 3.38 3.09
从表2可以看出,所建立的动力学方程式与实验结果能较好的吻合,ln[C∞/(C∞-C)与t之间线性关系良好,R2均在0.98以上。表观速率常数随着温度的升高较显著地增大,有效成分的提取速度越快,同时可以看出C0随温度的升高也略有升高。
3.3 相对萃余率的求解
设相对萃余率y=(C∞-C)/(C∞-C0),则式(12)变为y=(4/π)exp(-λt),分别利用实验数据作y对提取时间t的关系图,结果见图1。

图1 不同温度下y与t的关系Fig.1 Relationship between y and t at different temperature
由图1可知,拟合方程的复相关系数R2均在0.98以上,曲线的拟合精度较高,所以化香树果序中总黄酮的提取符合指数模型。由相对萃余率的定义可知,其值越小说明提取率越大,图中可以看出随着时间的增加或温度的升高相对萃余率不断的减小,提取率在不断增大,但是增长的幅度下降。所以,实际提取过程中并非时间越长越好,还需考虑提取的效率以及设备的利用率等因素。
3.4 活化能的求解

图2 –lnk与1000/T关系图Fig.2 Relationship between–lnk and 1000/T
由化学反应动力学可知,在低温下表观扩散速率常数是温度的函数。那么,在总黄酮的提取过程中其表观扩散速率常数与提取温度的关系应遵循Arrhenius公式,对-lnk和1/T作图,结果见图2。
由图2可知,lnk和1/T线性关系良好,其回归方程为:lnk=1776.4/T+2.9659。据此可以算出化香树果序提取总酚过程中的活化能,Ea=1367× 8.314=11365 J/mol。
3.5 有效扩散系数的求解
提取过程的内扩散系数可以通过速率常数计算。由λ=(π2Ds)/(4D2)可知,速率常数是内扩散系数Ds和颗粒尺寸的函数。由Ds对T作图得图3。得到回归方程为:104Ds=0.0056exp(0.0153T),由此可以计算出不同温度下化香树果序中总黄酮和总酚提取的内扩散系数。
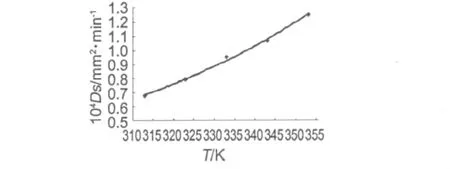
图3 Ds和T的关系图Fig.3 Relationship between Ds and T
4 结论
采用平板模型,根据Fick第二定律为基础,通过一些假定和简化,建立了化香树果序总黄酮提取的动力学模型,模型计算值与实验数据吻合良好。通过对化香树果序总黄酮的提取试验研究,结合所建立的动力学模型,求得了速率常数、相对萃余率、活化能以及有效扩散系数等一系列有价值的动力学参数。研究结果可为化香树果序有效成分的提取工艺条件优化以及工艺设计提供相应的理论依据和参考。
1 Northwesters Institute of Botany of Academia Sinica.Flora of Qin Ling,1st(秦岭植物志).Beijing:Science Press,1970.121-125.
2 Pei LP(裴凌鹏),Hui BL(惠伯棣),Jin ZL(金宗濂).Review on health function processing technology and market prospects of flavonoids.Food Sci,2005,25:203-207.
3 Peng F(彭芳),Chen ZH(陈植和).Biological Effects of Flavones.J Da Li Med Coll(大理医学院学报),1998,7 (4):52-54.
4 Huang HS(黄河胜),Ma CG(马传庚),et al.The advance of research on pharmacological effects of flavonoids.Chin J Chin Mat Med(中国中药杂志),2000,25:589-592.
5 Zhang AL(张安灵),Gao JM(高锦明),et al.The distribution,development and utilization of the flavonoids.J Northwest Forest Univ(西北林学院学报),2000,15:69-74.
6Chu MQ(储茂泉),Gu HC(古宏晨),Liu GJ(刘国杰).Kinetic model on medicinal herb extraction process.Chin Tradit Herb Drugs,2000,31:504-506.
7 Spiro M,Page CM.The kinetics and mechanism of caffeine infusion from coffee:hydrodynamic aspects.J Sci Food Agric,1984,35:925-930.
8 GaoR(高蓉),Li WH(李稳宏),Liu MX(刘明霞).Research on extraction of flavonoid infructescence of Platycarya strobilacea Sieb.et Zucc with diferent distilling methods.Food Sci,2007,28:230-232.
9 Liang Y(梁英).Study on Extraction Kinetics and Extraction Techniques of Flavonnoids from Scutellaria radix.Beijing: China Agricultural University,2005.24-26.
Kinetics on the Extraction of Total Flavonoids from Infructescence of Platycarya Strobilacea Sieb.et Zucc
LI Dong1,LI Wen-hong1*,LIAN Yuan-yuan2,GAO Rong3,LI Xue-kun1,ZHU Zhou-hai11School of Chemical Engineering,Northwest University,Xi’an 710069,China;2Department of Pharmacy,Shaanxi Dikuang Hospital,Xi’an 710014,China; 3Department of Chemistry,Fourth Military Medical University,Xi’an 710032,China
In this paper,60%ethanol was used as solvent to extract flavonoids from Platycarya Strobilacea Sieb.et Zucc.,and the mass transfer kinetics of polyphenol at different temperature was investigated.According to Fick’s second law of diffusion,the kinetic equation for Platycarya Strobilacea Sieb.et Zucc.extraction process was established with plate model,and the parameters,such as K(rate constant),Ea(activation energy),y(yield)were gained.The results could provide the valuable theory basis for the technical design and further research of total flavonoids extraction process.
Platycarya Strobilacea Sieb.et Zucc.;total flavonoids;extraction;dynamics
1001-6880(2011)04-0689-05
2009-10-10 接受日期:2010-02-04
陕西省教育厅重大产业化项目(2007JC18);西安市科技创新支撑计划(F07071)
*通讯作者 E-mail:liwenhong@nwu.edu.cn
TQ028.96;Q946.91
A
