苯并咪唑-镍(Ⅱ)-L-α-氨基酸配合物的合成及其SOD活性*
2011-11-27周晓华马卉芳吴海雷
周晓华,马卉芳,吴海雷
(华南农业大学 理学院 应用化学系,广东 广州 510642)

由于组氨酸残基、天冬氨酸残基和胱氨酸残基等在Ni-SOD的活性中心与Ni离子配位,Ni-SOD的抑制类型和生物活性与CuZn-SOD相似[4,10],在化学稳定性及空间结构上,苯并咪唑(bim)比咪唑更适合模拟组氨酸残基,L-氨基酸为金属酶蛋白的结构单元。
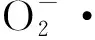
1 实验部分
1.1 仪器与试剂
UV-Vis 4000型紫外-可见分光光度计;ACATAR 360 FT-IR型红外光谱仪(KBr压片);Vario EL型元素分析仪;DDS-11A型数显电导仪。
天然CuZn-SOD酶(纯度98%,比活6 000 μ·mg-1);其余所用试剂均为分析纯或生化纯。
1.2 1~3的合成
在反应瓶中加入NiCl2·6H2O 1 mmol,L-氨基酸2 mmol和热水10 mL,搅拌使其完全溶解后加入bim(2.2 mmol)的乙醇(5 mL)溶液,用NaOH溶液调pH至中性,回流反应2 h~3 h。冷却至室温,过滤,滤液于室温放置几天后析出蓝色微晶。过滤,滤饼用乙醇洗涤,真空干燥得蓝色晶体1~3。
1.3 SOD活性测定[11,12]
用磷酸缓冲液(pH 7.8)配制c(NBT)=9.32×10-5mol·L-1,c(VB2)=6.80×10-6mol·L-1,c(四甲基乙二胺)=1.0×10-4mol·L-1和c(1~3)=0.01 μmol·L-1~0.8 μmol·L-1的各种试样溶液。恒温25 ℃下,用恒定光强的冷光灯(50 500±500 Lux)照射(首次60 s,以后30 s/次)待测溶液,测定560 nm处的吸光度(平行实验两次,取平均值),计算IC50。 IC50越小,SOD活性越强。
2 结果与讨论
2.1 配合物的表征
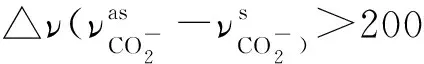
Λ值表明1~3均为非电解质类型[15]。从表1还以看出,1~3均有三个较强的吸收峰,归属于bim的π→π*跃迁。与bim相比,1~3的π→π*峰位基本未变,但由于bim的N与Ni(Ⅱ)配位,引起π电子云密度下降,使其强度减弱。另外,在可见光谱区,1~3在620 nm左右均出现了一个归属于Ni(Ⅱ)的d→d*跃迁的弱而宽的吸收峰。UV-Vis数据也表明bim与Ni(Ⅱ)配位成键。
综合UV-Vis, IR,Λ值和元素分析数据,并参考文献[12,14]方法,推测1~3的分子式分别为:Ni(bim)2(L-ala)2,Ni(bim)2(L-leu)2·H2O和Ni(bim)2(L-arg)2,其可能的结构如Chart 1所示。
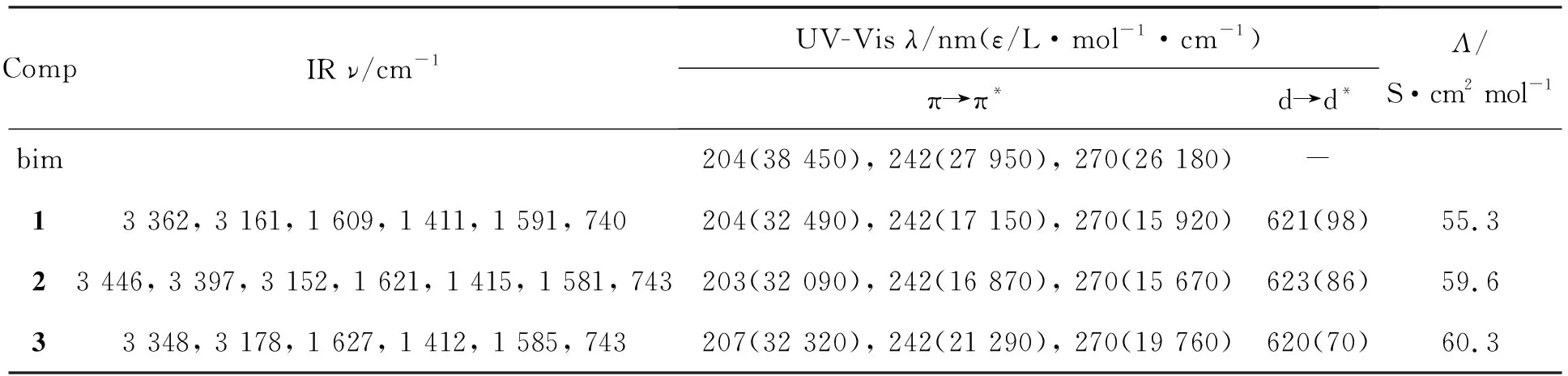
表1 配合物的IR,UV-Vis和Λ数据
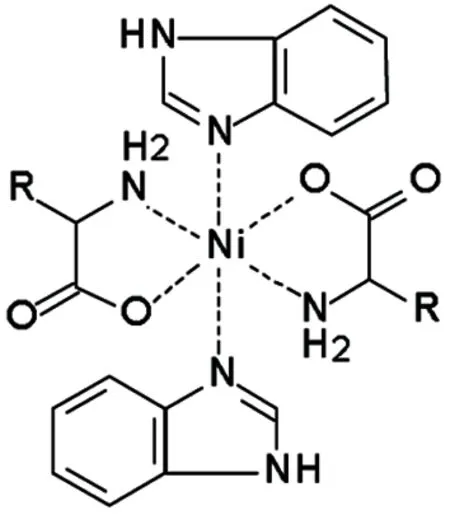
1~3

Chart1
2.2 配合物的SOD活性
1~3的相对分子量和IC50值列于表3。由表3可知,1~3的IC50接近于文献[8,12,16]值,优于文献[5,9]报道的类似配合物,说明三种配合物具有良好的清除超氧阴离子自由基的活性。其SOD活性顺序为:1⟩3⟩2。
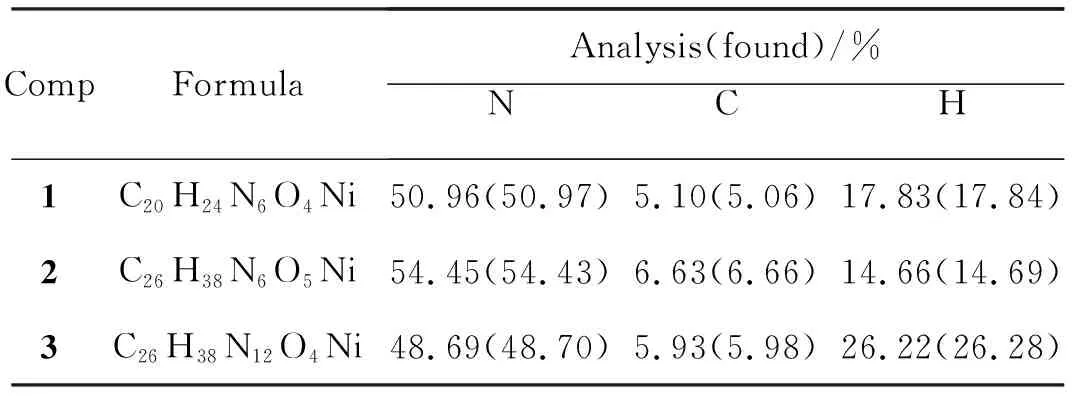
表2 配合物的元素分析数据

表3 配合物的相对分子量和IC50值
[1] H D Youn,E J Kim,J H Roe,etal.A novel nickel-containing superoxide dismutase from streptomyces spp[J].Biochem J,1996,318:889-896.
[2] Lee J W, Roe J H, Kang S O.Nickel-containing superoxide dismutase[J].Methods in Enzymology,2002,349:90-101.
[3] A E O Fisher, G Lau, D P Naughton.Lipophilic ionophore complexes as superoxide dismutase mimetics[J].Biochem and Biophy Resea Comm,2005,329(3):930-933.
[4] 张翘楚,曾锦萍,应惠芳,等.微量元素镍及镍超氧化物歧化酶的模拟化学[J].微量元素与健康研究,2006,23(1):57-60.
[5] 刘媛媛,岳俊杰,刘小兰.镍超氧化物歧化酶模拟化合物的合成、表征及活性[J].天津师范大学学报(自然科学版),2003,23(2):1-3.
[6] 岳俊杰,孙云,马燕等.镍超氧化物歧化酶模型化合物的合成、表征和量化计算[J].天津师范大学学报(自然科学版),2004,24(4):8-11.
[7] 姚克敏,鲁桂,朱丹.直链醚型Schiff碱与钴(Ⅱ),镍(Ⅱ)配合物的合成、表征及其活性的研究[J].波谱学杂志,1999,16(4):313-319.
[8] 祝心德,乐芝风,吴自慎,等.3,4-二羟基苯甲醛缩氨基脲及其铜、镍配合物的合成与抑制超氧阴离子自由基的研究[J].无机化学学报,1994,10(2):136-140.
[9] 吴辉禄,高忆慈.超氧化物歧化酶模型化合物的合成、表征及其SOD活性研究[J].化学通报,2003,(11):770-774.
[10] D P Barondeau,C J Kassman,C K Bruns,etal.Nickel superoxide dismutase structure and mechanism[J].Biochemistry,2004,43:8038-8047.
[11] 自俊青,邓希贤,金虬,等.氮蓝四唑光照法实验操作的改进及效果[J].北京师范大学学报(自然科学版),1998,34(1):101-104.
[12] 周晓华,马卉芳,赵盼.Ni-SOD模拟物的合成及其SOD活性测定[J].中国农学通报,2010,26(22):170-174.
[13] K Nakamoto.Infrared and Raman Spectra of Inorganic and Coordination Compounds[M].3rd Edn,John Wiley and Sons,Inc.:New York,1978.
[14] L Zhang,Z Y DAI.Synthesis and structure of L-aspartato-nickel(Ⅱ) complex with benzimidazole[J].Chin J Struct Chem,2004,23(4):386-390.
[15] W J Geary.The use of conducity measurements in organic solvents for the characterization of coordination compound[J].Coord Chem Rev,1971,7(1):81-12.
[16] H F Ma, X R Zeng, X H Zhou,etal.Synthesis,characterization and SOD-like activities of a ternary copper(Ⅱ) complex with 1,10-phenanthroline and L-arginine[J].J of Coord Chem,2008,61(23):3829-3838.
