硫酸中Q235钢缓蚀剂的电化学研究
2011-11-22余强魏昶陈阵司云森聂金艳
余强,魏昶,陈阵,司云森,聂金艳
(1.昆明理工大学理学院,云南 昆明 650093;2.昆明理工大学冶金与能源工程学院,云南 昆明 650093)
【腐蚀防护】
硫酸中Q235钢缓蚀剂的电化学研究
余强1,2,魏昶2,陈阵1,*,司云森1,聂金艳2
(1.昆明理工大学理学院,云南 昆明 650093;2.昆明理工大学冶金与能源工程学院,云南 昆明 650093)
采用塔菲尔极化曲线和电化学阻抗谱(EIS)测量方法,研究了5%(质量分数)硫酸溶液中N,N′–二苯基硫脲(DPH-TU)和十二烷基磺酸钠(SDS)对Q235钢的协同缓蚀效应及其机理。实验表明,添加十二烷基磺酸钠对 N,N′–二苯基硫脲的缓蚀效果有促进作用。当 N,N′–二苯基硫脲和十二烷基磺酸钠的浓度比为1∶1时,其协同缓蚀效应最为显著。
Q235钢;缓蚀剂;极化曲线;电化学阻抗谱;协同效应
1 前言
腐蚀是现代工业中一种极为严重的破坏因素[1],缓蚀已成为防腐蚀技术中应用最广泛的方法。在腐蚀介质中添加缓蚀剂是简单而有效地解决金属腐蚀问题的方法之一[2]。有机缓蚀剂具有用量少、高效、易降解等优点,具有广阔的应用发展前景[3]。Q235钢作为一种重要的常用金属材料,在工业环境中极易遭受腐蚀。研究 Q235钢在酸性介质中的腐蚀特点以及缓蚀剂对其腐蚀进程的影响具有重要意义,可为实际生产中选用缓蚀剂的可行性研究提供理论指导和依据。20世纪初期已有以硫脲类化合物作为金属酸洗缓蚀剂的专利出现;在20世纪40年代,硫脲已被用于金属酸洗缓蚀剂。近年来,硫脲及其衍生物成为了复合缓蚀剂的主要成分[4]。N,N′–二苯基硫脲(简称DPH-TU)是一种典型的在N原子上取代的硫脲衍生物。十二烷基磺酸钠(简称 SDS)是一种常见的阴离子表面活性剂,与阴离子及非离子表面活性剂的复配性好。研究发现,硫脲和SDS在硝酸溶液中对锌有优良的协同缓蚀作用[5]。本文研究 N,N′–二苯基硫脲与十二烷基磺酸钠在 5% H2SO4溶液中对Q235钢的协同缓蚀效应及相关机理,以期对实际生产中缓蚀剂的选用提供参考。
2 实验
腐蚀介质为 5%(质量分数)H2SO4溶液,材料为Q235钢,试验用所有化学试剂均为分析纯,试验温度30 °C。采用三电极体系进行动电位极化曲线扫描和电化学阻抗谱测试[6]。工作电极裸露面积为1 cm2,其余部分用环氧树脂密封,参比电极为饱和甘汞电极(SCE,饱和K2SO4溶液),辅助电极为Pt电极。动电位扫描极化曲线用CHI660B电化学工作站测试,扫描速率为2 mV/s。根据极化曲线得出电化学腐蚀参数Bc和Ba,缓蚀效率 其中是未添加缓蚀剂时金属的腐蚀电流,icorr是添加缓蚀剂后金属的腐蚀电流)。电化学阻抗谱用 PARSTAT 2263测定,测量频率为100 kHz ~ l0 mHz,幅值为5 mV,同时用ZSimpWin软件对阻抗谱进行模拟。
3 结果与讨论
3. 1 不同浓度的DPH-TU和SDS对Q235钢耐腐蚀性能的影响
30 °C时,在5% H2SO4溶液添加不同浓度的DPH-TU,测得塔菲尔曲线如图1所示,相应的腐蚀参数见表1。
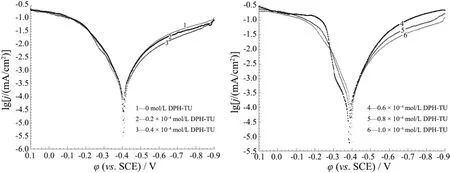
图1 Q235钢在含不同浓度的DPH-TU的5% H2SO4溶液中的塔菲尔曲线Figure 1 Tafel curves for Q235 steel in 5% H2SO4 solution containing different concentrations of DPH-TU
30 °C时,在5% H2SO4溶液中保持DPH-TU和SDS的总浓度为1.0 × 10−4mol/L,通过改变两者的浓度比,考察其协同缓蚀效率。实验测得的Tafel曲线如图2所示,相应的腐蚀参数见表2。

图2 Q235钢在含不同比例的DPH-TU和SDS的5% H2SO4溶液中的塔菲尔曲线Figure 2 Tafel curves for Q235 steel in 5% H2SO4 solution with different ratios of DPH-TU to SDS

表2 Q235钢在含不同浓度比的DPH-TU和SDS的5% H2SO4溶液中的腐蚀参数Table 2 Corrosion parameters of Q235 steel in 5% H2SO4 solution with different concentration ratios of DPH-TU to SDS
由图2可知,当DPH-TU和SDS的浓度比小于1∶1时,DPH-TU和SDS构成混合型缓蚀剂,对阴、阳极部分均有抑制作用,自腐蚀电位发生了变化。当添加的比例大于1∶1时,缓蚀体系表现为阳极型缓蚀剂,阴极极化曲线基本重合,斜率也基本相同。阳极极化曲线随着DPH-TU比例的增大而不断正移,对阳极金属的溶解表现出抑制作用[7]。
比较表1和表2可以看出,在DPH-TU缓蚀体系中添加SDS的缓蚀效率比单独使用DPH-TU高得多,说明添加SDS对DPH-TU的缓蚀效果有促进作用。当DPH-TU和SDS的浓度比为1∶1时,DPH-TU和SDS的协同缓蚀效应最为显著。SDS分子结构中,中心原子是O原子,带有两对孤对电子,电子云密度较高,电负性较氮族元素原子大,能与金属的空 d轨道形成配位键,在金属电极表面吸附更牢靠,增加了溶解的活化能[8]。在DPH-TU缓蚀剂体系中加入少量的SDS表面活性剂,可以提高DPH-TU在H2SO4溶液中的分散能力、渗透能力和润湿能力,起到了协同缓蚀的效果。
3. 2 DPH-TU/SDS复配缓蚀剂与DPH-TU的缓蚀效率对比
30 °C时,在5% H2SO4溶液中添加DPH-TU和SDS复配缓蚀剂,与单独的DPH-TU缓蚀体系的缓蚀效率进行对比,结果如图3所示,图中横坐标为DPH-TU的浓度,DPH-TU和SDS的总浓度为1 × 10−4mol/L。
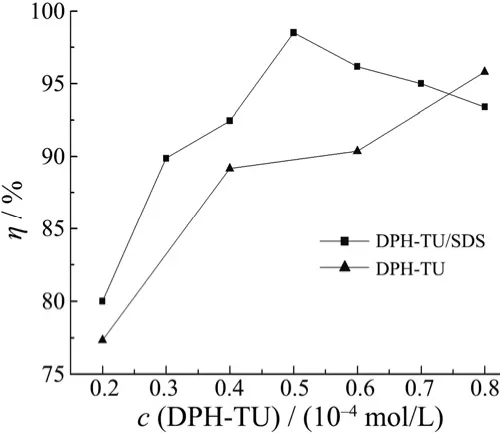
图3 DPH-TU/SDS复配体系与DPH-TU体系的缓蚀效率Figure 3 Corrosion efficiencies of combined DPH-TU/SDS and single DPH-TU
图3表明,DPH-TU/SDS体系的缓蚀效率比DPH-TU高出较多,当DPH-TU与SDS的浓度比为1∶1(即复配体系中DPH-TU的浓度为0.5 × 10−4mol/L)时,协同缓蚀效果最为显著。N,N′–二苯基硫脲能形成一种可镶嵌外来分子的螺旋状物,提供比自身还大的通道,因此可接受SDS中的十二烷基进入其中,形成致密的吸附膜,起到协同缓蚀作用[5]。
3. 3 Q235钢在含DPH-TU/SDS复配缓蚀剂的5% H2SO4溶液中的电化学阻抗谱
30 °C时,Q235钢在添加不同浓度的DPH-TU的5% H2SO4溶液中的电化学阻抗Nyquist图如图4所示,相应的动力学参数如表3所示。

图4 Q235钢在含不同浓度的DPH-TU的5%H2SO4溶液中的Nyquist图Figure 4 Nyquist plots for Q235 steel in 5% H2SO4 solution containing different concentrations of DPH-TU
30 °C时,Q235钢分别在5% H2SO4溶液和添加不同浓度的 DPH-TU/SDS复配缓蚀剂后的电化学阻抗Nyquist图如图5所示,相应的动力学参数如表4所示,等效电路图如图6所示。
由图5可知,复配体系下的Nyquist图在第一象限高频端出现了比较规则的压扁的半圆容抗弧,半圆直径即反应电阻增大,说明DPH-TU与SDS的加入有效地减缓了腐蚀的发生。缓蚀效率随着加入的 DPH-TU比例的变化而显著变化,这与极化曲线测得的数据相吻合。DPH-TU在第四象限低频端出现了感抗弧,且弧度随着DPH-TU的加入量增大而逐渐增大,这是由于DPH-TU的中间产物在电极表面的吸/脱附过程引起了感抗成分[9]。
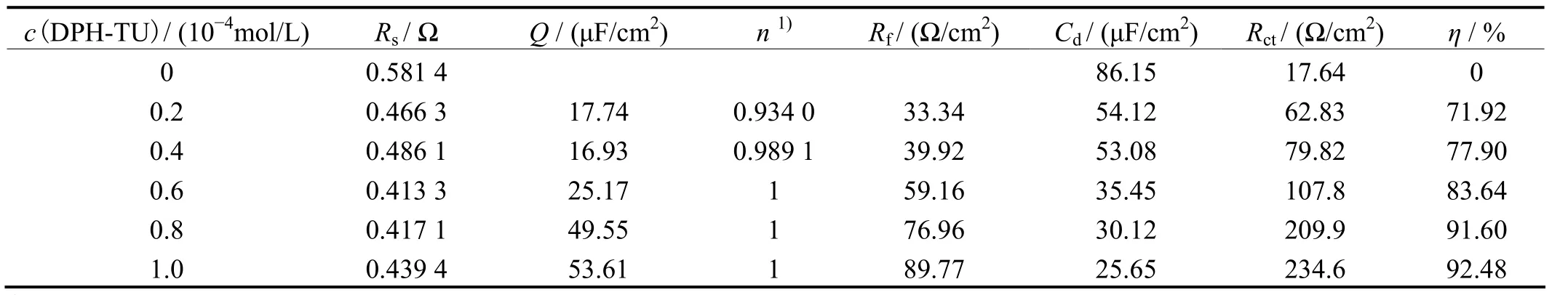
表3 添加不同浓度的DPH-TU时电化学阻抗谱图的拟合参数Table 3 Fitted parameters of electrochemical impedance spectra for different concentrations of DPH-TU
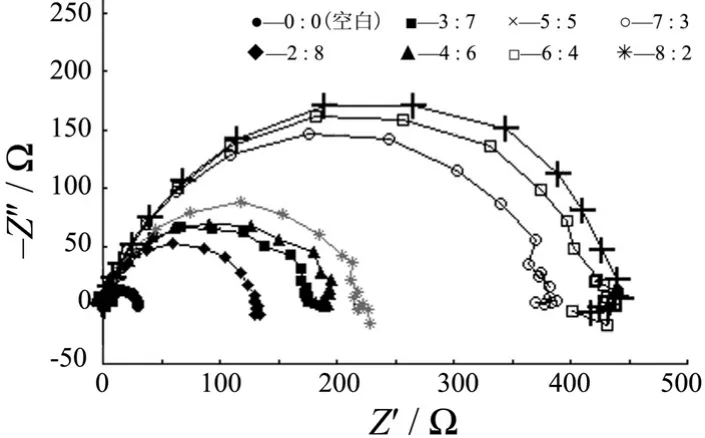
图5 Q235钢在含不同浓度比的DPH-TU和SDS的5% H2SO4溶液中的Nyquist图Figure 5 Nyquist plots for Q235 steel in 5% H2SO4 solution with different concentration ratios of DPH-TU to SDS

图6 Q235钢在DPH-TU/SDS体系中的等效电路Figure 6 Equivalent circuit for Q235 steel in DPH-TU/SDS system
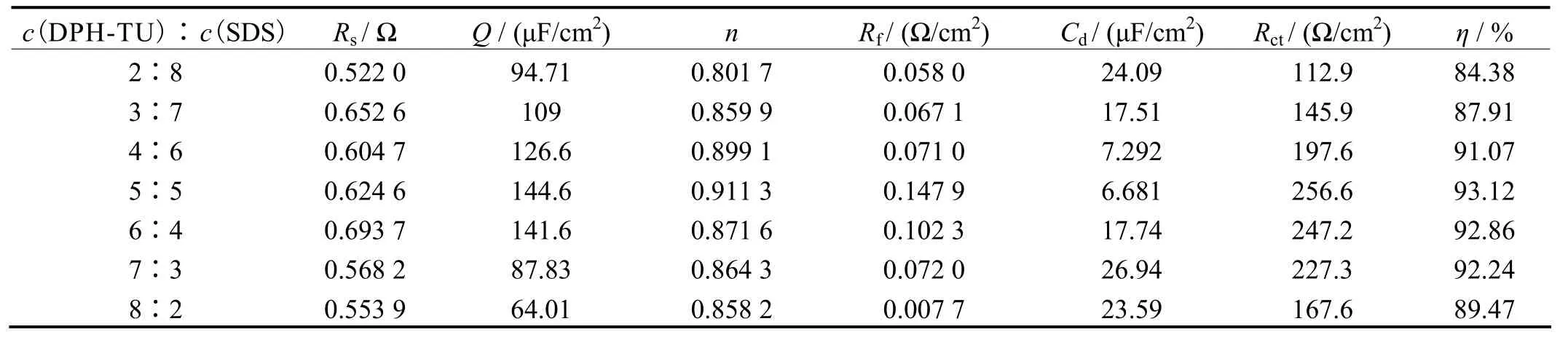
表4 添加不同浓度比的DPH-TU和SDS时电化学阻抗谱图的拟合参数Table 4 Fitted parameters of electrochemical impedance spectra for different concentration ratios of DPH-TU to SDS
由表4可知,DPH-TU与SDS加入后,相对于空白溶液[表3中c(DPH-TU)= 0 mol/L时]而言,随着DPH-TU加入量的增大,双电层电容降低,吸附膜电阻增大,这是由于DPH-TU与SDS发生了竞争吸附,导致复配缓蚀剂体系在 Q235钢表面的吸附层更加紧密。当DPH-TU与SDS的浓度比为1∶1时,吸附层最为紧密。弥散指数 n的增大也可以说明吸附膜的致密度提高,且吸附膜是逐渐均匀地覆盖在Q235钢的表面。与表3相比,表4的弥散指数偏小,说明加入SDS后复配缓蚀体系吸附膜的致密度和均匀性不及单独的DPH-TU体系。吸附导致的常相位角元件值越大,说明缓蚀剂的吸附量越大。DPH-TU/SDS复配体系中电荷转移电阻的变化规律与极化曲线中所测的数据相吻合,电荷转移电阻越大,缓蚀效果越显著。复配体系的弥散效应比单独 DPH-TU体系更大,可能是由于SDS的发泡作用导致了金属电极表面电荷的传递电阻不同[10]。
4 结论
(1) 在DPH-TU缓蚀体系中添加SDS后,缓蚀效率比单独使用DPH-TU时高得多,说明添加SDS对DPH-TU的缓蚀效果有促进作用。当DPH-TU和SDS的总浓度为1 × 10−4mol/L,而两者的浓度比为1∶1时,DPH-TU与SDS的协同缓蚀效应最为显著。
(2) 对于 DPH-TU/SDS复配缓蚀体系中,随着DPH-TU加入量的增大,溶液电阻增大,这是由于DPH-TU与SDS发生竞争吸附,导致复配缓蚀剂体系在Q235钢表面的吸附层更加紧密。当DPH-TU与SDS的浓度比为1∶1时,吸附层最为致密。
[1] 曹楚南. 腐蚀电化学[M]. 3版. 北京: 化学工业出版社, 2008: 1-2.
[2] 杨文治, 黄魁元, 王清, 等. 缓蚀剂[M]. 北京: 化学工业出版社, 1989: 136-140.
[3] 范洪波. 新型缓蚀剂的合成与应用[M]. 北京: 化学工业出版社, 2003: 24-33.
[4] 李广超, 路长青, 杨文忠, 等. 硫脲及其衍生物的缓蚀行为研究进展[J].腐蚀科学与防护技术, 2001, 13 (3): 169-172.
[5] 刘明婧, 焦庆祝. 十二烷基磺酸钠和硫脲对锌缓蚀协同作用[J]. 石油和化工设备, 2007, 10 (6): 50-53.
[6] 杨绮琴, 方北龙, 童叶翔. 应用电化学[M]. 广州: 中山大学出版社, 2005: 147-150.
[7] GILEADI E, KIROWA-EISNER E. Some observations concerning the Tafel equation and its relevance to charge transfer in corrosion [J]. Corrosion Science, 2005, 47 (12): 3068-3085.
[8] 高延敏, 陈家坚, 雷良才, 等. 有机缓蚀剂分子在金属表面的化学吸附过程和分子设计分析[J]. 中国腐蚀与防护学报, 2000, 20 (3): 142-148.
[9] VOSTA J, HACKERMAN N. The dependence of capacitance on time in an acid inhibition corrosion process [J]. Corrosion Science, 1990, 30 (8/9): 949-950.
[10] 刘明婧, 宋宏瑜, 杨婷. 硝酸溶液中十二烷基苯磺酸钠对锌缓蚀作用的电化学研究[J]. 清洗世界, 2008, 24 (2): 1-5.
Electrochemical study on corrosion inhibitors for Q235 steel in sulfuric acid //
YU Qiang, WEI Chang, CHEN Zhen*, SI Yun-sen, NIE Jin-yan
The synergistic inhibition effect of N,N′–diphenylthiourea (DPH-TU) and sodium dodecyl sulfonate (SDS) and related mechanism for Q235 steel in 5wt% H2SO4solution were studied by Tafel polarization curves and electrochemical impedance spectroscopy (EIS). The results showed that the corrosion inhibition effect of DPH-TU is promoted by the addition of SDS. The synergistic effect is most significant when the concentration ratio of DPH-TU to SDS is 1:1.
Q235 steel; corrosion inhibitor; polarization curve; electrochemical impedance spectroscopy; synergistic effect
Faculty of Science, Kunming University of Science and Technology, Kunming 650093, China
TG174.36; 174.42
A
1004 – 227X (2011) 02 – 0021 – 04
2010–08–24
2010–09–21
国家自然科学基金(50964008)。
余强(1980–),男,宁夏石嘴山市人,博士,工程师,主要研究方向电化学。
陈阵,副教授,(E-mail) chenzhen69@sina.com。
[ 编辑:温靖邦 ]
